Descargar PDF
Anuncio

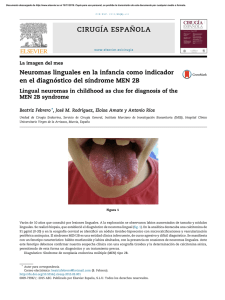
Documento descargado de http://www.elsevier.es el 19/11/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. Med Clin (Barc). 2012;138(1):41–45 www.elsevier.es/medicinaclinica Cartas al Editor Hematopoyesis extramedular presacra secundaria a cardiopatı́a congénita cianógena Presacral extramedullary hematopoiesis secondary to congenital heart disease Sr. Editor: La hematopoyesis extramedular (HE) se define como la presencia de elementos hematopoyéticos fuera de la médula ósea1. Es un proceso habitual en la vida fetal pero considerado anormal en la edad adulta2. La HE es un mecanismo compensador en diversas enfermedades hematológicas1–3. La localización presacra es poco frecuente y existen pocos casos descritos en la bibliografı́a médica. A continuación presentamos un caso de HE de localización presacra: mujer de 46 años que acude al servicio de urgencias por cuadro de 24 horas de evolución de dolor abdominal y vómitos. Como antecedentes personales presentaba cardiopatı́a congénita (atresia tricuspı́dea, comunicación interauricular, comunicación interventricular, y estenosis pulmonar) que fue intervenida quirúrgicamente en la infancia, y eritrocitosis secundaria en tratamiento con flebotomı́as periódicas y oxigenoterapia domiciliaria. Tres años antes del ingreso presentó un episodio de pancreatitis aguda biliar con colecistectomı́a posterior. La exploración fı́sica era normal. En la analı́tica de sangre destacaba amilasa 564 U/L, fosfatasa alcalina 141 U/L, gamma-glutamil transpeptidasa de 50 U/L, hemoglobina 19,9 g/dL y hematocrito 65,3%. La tomografı́a computarizada (TC) abdominopélvica mostró una leve dilatación de la vı́a biliar extrahepática y esplenomegalia; como hallazgo incidental se identificó una masa de partes blandas de morfologı́a lobulada y bordes bien delimitados localizada en la región presacra que no producı́a erosión ósea, ası́ como alteración difusa de la trabeculación ósea en la pelvis y en la columna vertebral (fig. 1). Se realizó una colangiografı́a por resonancia magnética (RM) que descartó obstrucción de la vı́a biliar. Con el diagnóstico inicial de pancreatitis aguda la paciente presentó buena evolución clı́nica con tratamiento conservador con fluidoterapia y analgesia. Ante los hallazgos de la TC se realizó una RM pélvica que confirmó la presencia de una masa presacra y alteración difusa de la señal de la médula ósea, planteándonos el diagnóstico diferencial entre sı́ndrome linfoproliferativo, tumor sólido, HE y leucemia. Dada la localización de la masa y la dificultad para acceder mediante cirugı́a, se realizó una biopsia guiada por ecografı́a transrectal, siendo el resultado anatomopatológico de tejido hematopoyético con elementos de las tres lı́neas germinales con importante predominio de los precursores eritroides dispuestos en densos agregados entre los que se identificaban elementos de la serie granulocı́tica y algunos megacariocitos, todo ello compatible con HE con notable hiperplasia de la serie eritroide. Los hallazgos de imagen en la columna vertebral y pelvis eran compatibles con hiperplasia difusa de la médula ósea roja. La paciente fue vista en consulta cuatro meses después manteniéndose asintomática, y actualmente está pendiente de nueva intervención cardiaca. La HE es un mecanismo compensatorio descrito en enfermedades con disminución de la producción de eritrocitos o aumento de la destrucción de los mismos1,2,4. Se asocia a talasemia, anemia de células falciformes, esferocitosis hereditaria, mielofibrosis con metaplasia mieloide, púrpura trombocitopénica inmune, leucemia mieloide crónica, linfoma de Hodgkin, policitemia vera, sı́ndromes mielodisplásicos y enfermedad de Paget. Tanto la anemia crónica como la hipoxia tisular producen una estimulación de la eritropoyesis celular tanto intramedular como extramedular1–5. La asociación de HE con cardiopatı́a congénita cianógena es infrecuente, y tras una revisión de la base de datos MEDLINE desde 1990 hasta 2010 con las palabra clave hematopoyesis extramedular, cardiopatı´a congénita y masa presacra, hemos encontrado sólo tres casos6,7. La localización más frecuente es hı́gado y bazo, aunque ha sido descrita con frecuencia en la columna vertebral, ganglios, pulmón, pericardio, timo y retroperitoneo, siendo la localización presacra poco común1,4,5. Clı́nicamente se presenta como un hallazgo incidental en la mayorı́a de los casos o sı́ntomas relacionados con la localización como dolor, estreñimiento o clı́nica compresiva neurológica3,5. El diagnóstico se basa en los [()TD$FIG]hallazgos de imagen (TC y RM) consistentes en una masa de Figura 1. Imagen sagital de TC que muestra una masa de partes blandas bilobulada (asteriscos) localizada en el espacio presacro y osteopenia difusa del sacro y de las vértebras lumbares. 0025-7753/$ – see front matter ß 2011 Elsevier España, S.L. Todos los derechos reservados. Documento descargado de http://www.elsevier.es el 19/11/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. 42 Cartas al Editor / Med Clin (Barc). 2012;138(1):41–45 partes blandas de similares caracterı́sticas al tejido hematopoyético intramedular, junto con la historia clı́nica y la biopsia. Histológicamente se caracteriza por la presencia de elementos de las tres lı́neas celulares con predominio de la serie eritroide en varios estadios de maduración1,3. El diagnóstico diferencial se plantea con lesiones congénitas, masas neurogénicas, linfoma, sarcoma y tumores de células gigantes3. Generalmente no es necesario tratamiento excepto en aquellos casos que presenten sintomatologı́a neurológica, siendo la radioterapia el tratamiento de elección ya que se trata de un tejido muy radiosensible. La cirugı́a queda reservada para cuando la descompresión de la médula espinal es necesaria para evitar daño neurológico permanente1–3. Bibliografı́a 1. Al-Abassi A, Murad BA. Presacral extramedullary hematopoiesis: a diagnostic confusion concerning a rare presentation. Med Princ Pract. 2005;14:358–62. 2. Rosada J, Bindi M, Pinelli M, Pandolfo C, Cassetti G. Hematopoyesis extramedular: mecanismo compensador o sı́ndrome clı́nico? Descripción de un caso y revisión bibliográfica. An Med Interna. 2007;24:77–80. 3. Babazadeh S, Broadhead ML, Slavin JL, Choong P. An interesting diagnosis for a presacral mass: case report. Int Semin Surg Oncol. 2009;8:18. 4. Gupta P, Eshaghi N, Ghole V, Ketkar M, Garcia-Morales F. Presacral extramedullary hematopoiesis: report of a case and review of the literature. Clin Imaging. 2008;32:487–9. 5. Koch CA, Li CY, Mesa RA, Tefferi A. Nonhepatosplenic extramedullary hematopoiesis: associated disease, pathology, clinical course, and treatment. Mayo Clin Proc. 2003;78:1223–33. 6. Luban NL, Kapur S, DePalma L. Pericardial extramedullary hematopoiesis in a neonate with congenital heart disease. A case report. Acta Cytol. 1993;37: 729–31. 7. Taylor CL, Maynard F, Liebman J, Hlavin ML. Extramedullary hematopoiesis causing paraparesia in congenital cyanotic heart disease. Neurology. 1998;51: 636–7. Laura Hurtado Carrilloa,*, José Alberto Merino Bonillab, Mariola Moreno Azofraa y Patricia Gil Armentiac a Servicio de Medicina Interna, Hospital Santiago Apóstol, Miranda de Ebro, Burgos, España b Servicio de Radiodiagnóstico, Hospital Santiago Apóstol, Miranda de Ebro, Burgos, España c Servicio de Cardiologı´a, Hospital Santiago Apóstol, Miranda de Ebro, Burgos, España * Autor para correspondencia. Correo electrónico: lhurcar@hotmail.com (L. Hurtado Carrillo). ? doi:10.1016/j.medcli.2011.04.003 Eficacia de tocilizumab en la enfermedad de Still del adulto Tocilizumab effectiveness in adult Still’s disease Sr. Editor: La enfermedad de Still (ES) del adulto es un desorden inflamatorio multisistémico de origen desconocido caracterizado por episodios diarios de fiebre, erupción cutánea, artritis y aumento de reactantes de fase aguda1. La patogenia de la enfermedad no está totalmente aclarada, pero la reacción inflamatoria mediada por citocinas jugarı́a un papel muy importante2,3. En el 80% de los pacientes, los corticoides controlan la sintomatologı́a4. En los casos refractarios o en aquellos en que los pacientes intoleran los inmunodepresores, los agentes biológicos pueden representar una opción terapéutica4. Presentamos el caso de un varón de 41 años con ES del adulto con buena respuesta a tocilizumab. Varón de 41 años diagnosticado en 2008 de ES del adulto a raı́z de cuadro de fiebre de dos meses de evolución, poliartritis, exantema maculopapuloso y leucocitosis junto a hepatomegalia con anticuerpos antinucleares y factor reumatoide negativos. En la analı́tica destacaba una PCR 28 mg/dl, VSG 80 mm/h y ferritina 1.527 ng/ml (N 20-400). Se inició tratamiento con antiinflamatorios no esteroideos y prednisona a dosis de 60 mg/dı́a con rápida mejorı́a y posterior pauta descendente. Cuando el paciente estaba en 15 mg/dı́a reaparecieron los sı́ntomas. Se añadió tratamiento con metotrexato 20 mg/semana que se retiró por astenia intensa y se sustituyó por azatioprina 100 mg/dı́a sin respuesta favorable y con intolerancia digestiva. El paciente decidió suspender el tratamiento y los controles médicos. Ocho meses después acudió de nuevo por empeoramiento progresivo con afectación del estado general, pérdida de 5 kg de peso, fiebre, poliartritis y exantema cutáneo. En los análisis destacaba una PCR 29 mg/dl, VSG 84 mm/h, hemoglobina 8,6 g/l, plaquetas 805 109/l y ferritina 3.847 ng/ml. En ese momento se decidió iniciar prednisona a dosis de 1 mg/kg/ dı́a junto a infliximab. Durante la segunda infusión de infliximab el paciente presentó un episodio de hipotensión, hipoperfusión periférica y edema lingual, por lo que se planteó el inicio de tocilizumab (8 mg/kg). Se administraron 6 infusiones de tocilizumab a intervalos de 4 semanas con buena tolerancia perinfusional y mejorı́a progresiva de su sintomatologı́a, lo que permitió reducir la dosis de prednisona hasta 5 mg/dı́a. Las alteraciones analı́ticas también mejoraron, con PCR 3 mg/dl, VSG 9 mm/h, hemoglobina 15 g/l, plaquetas 285 x 109/l y ferritina 268 ng/ml. Tres meses tras la última infusión el paciente refirió reaparición de las poliartralgias junto al rash macular por lo que se decidió reiniciar la administración de tocilizumab en régimen trimestral junto a prednisona 5 mg/dı́a. El tratamiento de primera lı́nea de la ES del adulto incluye los antiinflamatorios no esteroideos, pero en numerosas ocasiones, los glucocorticoides son necesarios para controlar la sintomatologı́a de la enfermedad. Con el fin de minimizar los efectos secundarios de éstos, se han usado otros tratamientos como metotrexato, azatioprina, talidomida, anti-TNF o anakinra, con resultados variables4. Tocilizumab es un anticuerpo monoclonal humanizado que se une al receptor celular de la interleucina-6 (IL-6), que interviene en la producción de inmunoglobulinas, en la diferenciación de linfocitos B, activa a los linfocitos T citotóxicos, células plasmáticas, modula la hematopoyesis y es la responsable, junto a la IL-1, de la sı́ntesis de proteı́nas de fase aguda en el hı́gado5. En pacientes con ES del adulto se han demostrado concentraciones plasmáticas elevadas de IL-6, que podrı́an explicar parte de la sintomatologı́a y de las alteraciones analı́ticas que presentan estos pacientes, como la elevación de los reactantes de fase aguda6. Además estos niveles se han relacionado con la actividad de la enfermedad7. En la literatura se han publicado varios casos de pacientes con ES refractarios a tratamiento convencional que han presentado respuesta satisfactoria al tratamiento con tocilizumab8,9. Puéchal et al10 han descrito las caracterı́sticas de una serie de 14 pacientes con ES del adulto tratados con tocilizumab. En todos los pacientes, metotrexato y anakinra habı́an fracasado o habı́an mostrado intolerancia. Además, 12 de ellos se habı́an tratado de forma previa con un anti-TNF. La dosis de tocilizumab fue de 5 a 8 mg/kg cada 4 a 8 semanas. En términos de eficacia, se observó una respuesta en el 64% a los 3 y 6 meses y una remisión en el 36% de los pacientes. Los