(período de comercialización)
Anuncio
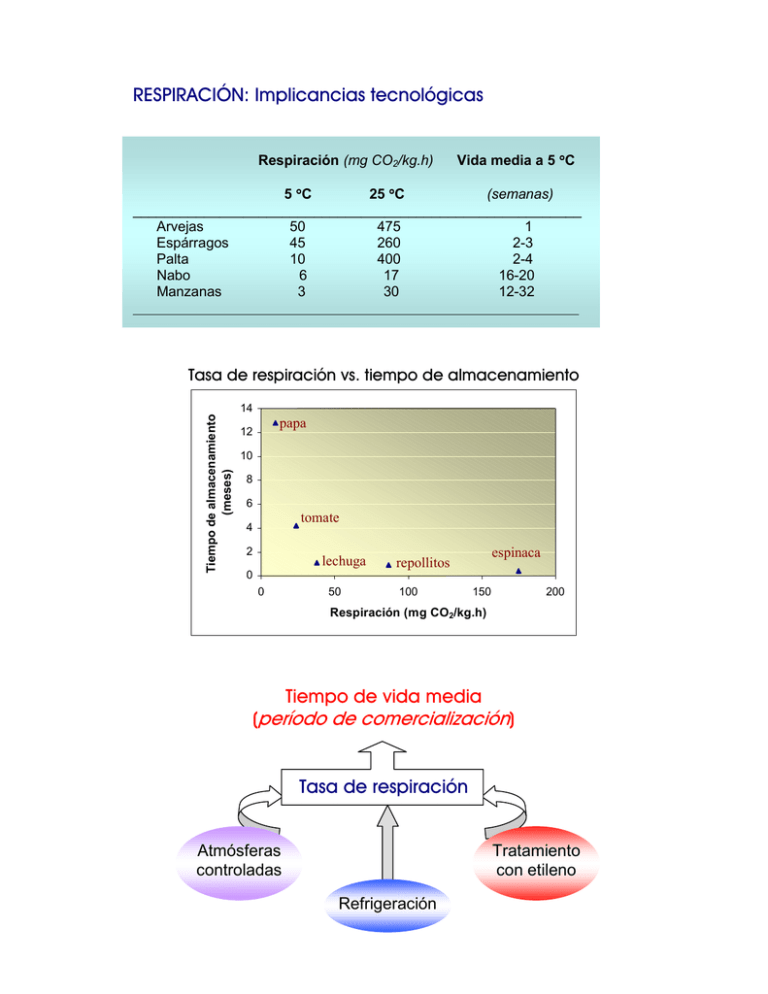
RESPIRACIÓN: Implicancias tecnológicas Respiración (mg CO2/kg.h) Vida media a 5 °C 5 °C 25 °C (semanas) _________________________________________________________ Arvejas 50 475 1 Espárragos 45 260 2-3 Palta 10 400 2-4 Nabo 6 17 16-20 Manzanas 3 30 12-32 _______________________________________________________________ Tasa de respiración vs. tiempo de almacenamiento Tiempo de almacenamiento (meses) 14 papa 12 10 8 6 tomate 4 2 lechuga espinaca repollitos 0 0 50 100 150 200 Respiración (mg CO2/kg.h) Tiempo de vida media (período de comercialización) Tasa de respiración Atmósferas controladas Tratamiento con etileno Refrigeración Cociente de respiración (CR) Oxidación completa del ácido málico: C4H6O5 + 3 O2 → 4 CO2 + 3 H2O Para glucosa: nO2 = nCO2 Definición: VCO2 (ml) CR = VO2 (ml) Ejs. Glucosa Õ CR = 1,0 Malato Õ CR = 1,3 Ácido esteárico Õ CR = 0,7 m Atmósferas controladas CO2 O2 [O2] min. crítica m Tratamiento con etileno Etileno endógeno → puede influenciar el tiempo de almacenamiento Etileno exógeno: frutas climatéricas → antes del climaterio frutas no climatéricas → en cualquier momento m Efecto de la temperatura Tasa de respiración α temperatura ( 5 °C<T<30°C) palta arvejas espárrago banana porotos tomate lechuga pomelo Valor Q10 (Tasa de respiración)T (Q10)T = (Tasa de respiración)-10 °C En general: 1< Q10<7 frutas climatéricas → T ↓ → retarda y disminuye el climaterio Tópt. → depende de la especie/variedad Control de la humedad CAMBIOS DE COLOR 4 Color → atributo determinante de la calidad 4 En general → pérdida del color verde (degradación de clorofilas) 4 Carotenoides → Síntesis (tomate) y/o revelación (banana) simultáneas 4 Degradación de clorofila y síntesis de carotenoides coordinadas e independientes (tomate green-flesh) 4 Antocianinas → presentes en algunas frutas y hortalizas \ CLOROFILAS Pigmentos verdes Intervienen en la fotosíntesis Presentes en membranas de cloroplastos Asociadas a fosfolípidos y proteínas Plantas superiores → clorofilas a y b (3:1) Clorofila a fitol Clorofila b fitol Estabilidad química de las clorofilas: aspectos tecnológicos Degradación enzimática Acción de ácidos y calor Oxidación H+ ( ∆ ) Feofitina Clorofila - Mg 2+ saponificación clorofilasa Clorofilina - fitol (MeOH) Feofórbido H+ - Mg 2+ - fitol O2 O2 O2 Clorinas Purpurinas Problema tecnológico: mantener el color verde de hortalizas en conserva r Adición de NaHCO3 (pH=8,0) → modifica textura, flavor indeseable, altera valor nutricional, disminuye eficacia de la esterilización r Uso de sales de Cu2+ → toxicidad r Uso de colorantes (tartrazina + verde S) → toxicidad r Uso de clorofilina de cobre sódica→ adecuado \ CAROTENOIDES Pigmentos amarillos - naranjas Son terpenoides (derivados de los terpenos -compuestos de unidades de isopreno con algunas alteraciones o reordenamientos-) C — C =C — C | C (con o sin doble enlace) Únicos tetraterpenoides conocidos (4 unidades de isopreno ⇒ 40 C) Presentes en cromoplastos Carotenos (hidrocarburos) Carotenoides Xantofilas (contienen O) Licopeno β-caroteno β-ionona Xantofilas → carotenos hidroxilados (mono, di) → epóxidos Solubles en solventes no polares Altamente estables en la planta Distribución en plantas ♦ Vegetales de hojas verdes: predomina β-caroteno (200-700 µg/g peso seco) y luteína, violaxantina y neoxantina. ♦ Frutas: mayor variedad ♣ papaya, mango (β-caroteno, criptoxantina, anteraxantina) ♣ tomate (licopeno) ♣ jugo de naranja (criptoxantina, luteína, anteraxantina, violaxantina) ♣ piminento rojo (capsantina) ♣ zanahoria (β-caroteno, α-caroteno) Carotenoides colorantes naturales o sintéticos: usados como Papel fisiológico en humanos no elucidado ♦β-caroteno puede tener acción antioxidante cooperativa con las vitaminas C y E ♦ Algunos carotenoides poseen actividad provitamina A (deben poseer el anillo β-inona) Formación de retinol (vitamina A) a partir de carotenoides precursores \ ANTOCIANINAS Pigmentos rosados, rojos, violetas, púrpura y azules Se encuentran glicosilados (antocianidinas: agliconas) ANTOCIANIDINA + AZÚCAR → ANTOCIANINA (aglicona) Son flavonoides (glicósido) Núcleo flavano Seis antocianidinas principales. Pueden presentar diferentes patrones de glicosilación ⇒ numerosas antocianinas Presentan azúcar (glucosa, galactosa, ramnosa, arabinosa, disacáridos raros) en posición 3, Glu en 5 (en general) Pueden estar aciladas Una o más moléculas de ácidos p-cumárico, ferúlico, cafeico, malónico, etc. esterificadas a los residuos glicosídicos Distribución en plantas Cianidina → ampliamente distribuída ♣ Uva: todas presentes, excepto pelargonidina. Presentan patrones de glicosilación y acetilación muy diversos Efecto del pH Cambios estructurales de la antocianina malvidina-3-glucósido con el pH Distribución de estructuras de antocianinas en función del pH CAMBIOS DE FLAVOR Ácidos orgánicos Compuestos fenólicos Substancias volátiles Azúcares FLAVOR Azúcares y ácidos orgánicos → de la fotosíntesis (frutas verdes), ácidos ↓, azúcares ↑ Frutas que acumulan carbohidratos antes de la maduración ♣ banana → almidón ♣ tomate → azúcares Frutas que dependen de la planta para asimilar substratos durante la maduración ♣ frutilla ♣ uva Compuestos fenólicos (adstringencia). Niveles bajos en frutas. Substratos de la PFO (polifenoloxidasa, polifenolasa o fenolasa) → importancia tecnológica Pardeamiento enzimático * * * diferentes clases de PFO Substratos fenólicos comunes: ácido catequinas, antocianinas y flavonoides clorogénico, Procesos para evitar el pardeamiento: ♦ Tratamiento térmico ♦ Agentes reductores (SO2, KHSO3) ♦ pH ácido ♦ Secuestradores de Cu II (ácidos cítrico y ascórbico) Compuestos volátiles → específicos para cada especie/variedad. Presentes en ppm. Perfil complejo (manzana:230, naranja: 330 compuestos identificados). Biosíntesis en fruta intacta o cuando el tejido es macerado. Estructuras de algunos componentes típicos de aroma de frutas CAMBIOS DE TEXTURA Textura → principal atributo de calidad Cambios estructurales de la pared celular Pérdida de turgencia Degradación de almidón TEXTURA Pérdida de turgencia → no fisiológico. Importante cuando la UR es baja Degradación de almidón → banana Cambios de la pared celular Bioquímica Componentes de la pared celular Pectinas pérdida de azúcares neutros (galactosa, arabinosa) aumento de solubilidad de poliurónidos (despolimerización) modificación del grado de esterificación (depende de la especie) Hemicelulosas despolimerización y "turn-over" Celulosa y proteínas estructurales cambios poco evidentes (menos estudiados) Enzimas Poligalacturonasa (PG): Agal (α 1→4) Agal (endo o exo) Pectinametilestearasa (PME): Retira grupos metil del C-6 del Agal Celulasa: Glu (β 1→ 4) Glu β-Galactosidasa: Substratos artificiales. Algunas no degradan galactanos nativos. Otras degradan polímeros de galactosa (βGalactanasas) Desarrollo Maduración PME.............................................................↑,↓, cte.............. β-Galactosidasa............................................↑..................... Celulasa.......................↑.. PG..................↑................ Principales componentes de frutas y sus implicancias tecnológicas AZÚCARES Fructosa Glucosa sacarosa ÁCIDOS Málico Cítrico COMPUESTOS FENÓLICOS Acidez. Bajan con la maduración. Ácido cafeico Adstringencia. Bajan con la maduración. Dan pardeamiento enzimático (fenolasas). Taninos POLISACÁRIDOS Almidón Pectinas AMINOÁCIDOS Varios Clorofila PIGMENTOS Dulzor. Valor calórico. Aumentan con la maduración. Con aminoácidos dan polímeros pardos (reacción de Maillard). Dan consistencia firme a las frutas Se hidrolizan con la maduración. Reaccionan con los azúcares. En frutas verdes. maduración. Se degrada con la Carotenoides En frutas amarillas o rojiizas. Se degradan por oxidación (productos deshidratados). Antocianinas En frutas rojo-azuladas. Inestables. Pardean por oxidación y polimerización (pulpas, mermeladas, jugos) Bajan con la madurez VITAMINAS Ácido Ascórbico Se oxida o disuelve en diferentes procesos. Provitaminas A Idem carotenoides AROMAS Diversas estructuras Aumentan con la madurez. Se pierden durante la concentración de jugos y se alteran por tratamientos térmicos. BIBLIOGRAFÍA TEXTOS GENERALES Química de los alimentos. Yúfera E. P., Ed. Síntesis, Madrid, 1998. Food. The chemistry of its components. Coultate T.P., 3rd. ed. RSC, Cambridge, 1996. Food Chemistry. Fennema O.R., Ed. 2nd. ed. Marcell Dekker, New York, 1985. TEXTOS ESPECÍFICOS Biochemistry of fruit ripening. Seymour G.B., Taylor J.E. & Tucker, G.A., eds. Chapman and Hall, London, 1996. Postharvest. An introduction to the physiology and handling of fruit and vegetables. Wills R.B.H., McGlasson W.B., Graham D., Lee T.H. & Hall E.G. Van Nostrand Reinhold, New York, 1982. ARTÍCULOS Fruit ripening. Brady C.J. Annual Reviews of Plant Physiology, 38:155178, 1987. Cell wall disassembly and fruit softening. Seymour G.B. & Gross K.C. Postharvest News and Information, 7:45N-52N, 1996. Postharvest changes in fruit cell wall. John M.A. & Dey P.M. Advances in food research, 30:139-193, 1986. Estructuras de algunos carotenoides con actividad de vitamina A Estructuras de algunos carotenoides encontrados en frutas y hortalizas Estructuras de algunos carotenoides encontrados en frutas y hortalizas (cont.) Carotenoides típicos del maíz Carotenoides típicos del pimiento