PROPIEDADES+DE+LA+SUSTANCIAS
Anuncio
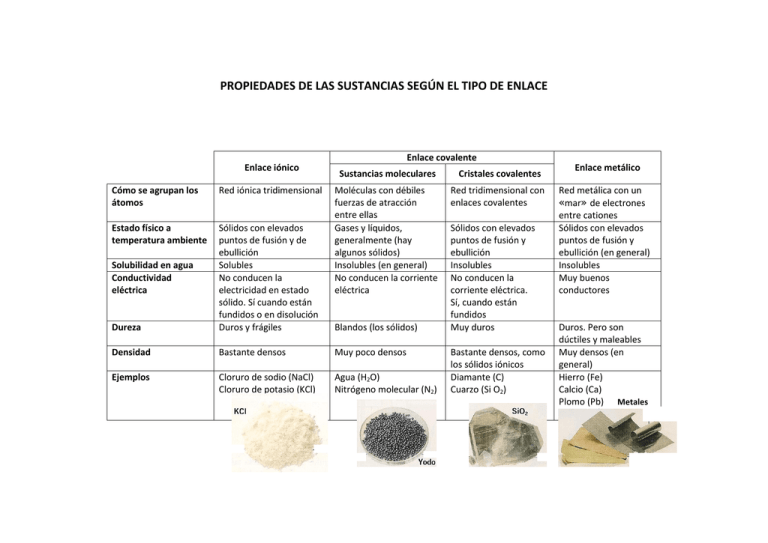
PROPIEDADES DE LAS SUSTANCIAS SEGÚN EL TIPO DE ENLACE Enlace iónico Enlace covalente Sustancias moleculares Cristales covalentes Moléculas con débiles fuerzas de atracción entre ellas Gases y líquidos, generalmente (hay algunos sólidos) Insolubles (en general) No conducen la corriente eléctrica Red tridimensional con enlaces covalentes Cómo se agrupan los átomos Red iónica tridimensional Estado físico a temperatura ambiente Dureza Sólidos con elevados puntos de fusión y de ebullición Solubles No conducen la electricidad en estado sólido. Sí cuando están fundidos o en disolución Duros y frágiles Densidad Bastante densos Muy poco densos Ejemplos Cloruro de sodio (NaCl) Cloruro de potasio (KCl) Agua (H2O) Nitrógeno molecular (N2) Solubilidad en agua Conductividad eléctrica Blandos (los sólidos) Sólidos con elevados puntos de fusión y ebullición Insolubles No conducen la corriente eléctrica. Sí, cuando están fundidos Muy duros Bastante densos, como los sólidos iónicos Diamante (C) Cuarzo (Si O2) Enlace metálico Red metálica con un «mar» de electrones entre cationes Sólidos con elevados puntos de fusión y ebullición (en general) Insolubles Muy buenos conductores Duros. Pero son dúctiles y maleables Muy densos (en general) Hierro (Fe) Calcio (Ca) Plomo (Pb) Metales