Teórica 12. Sistema Renal.pdf
Anuncio

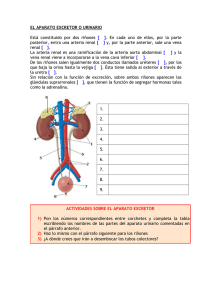
Sistema Excretor Vena cava inferior Aorta abdominal riñón arteria renal vena renal uréter vejiga uretra 1 Distribución del gasto cardíaco en reposo corazón derecho pulmón cerebro corazón RETORNO VENOSO sistema digestivo sistema excretor musculatura piel corazón izquierdo 20% 5% 25% GASTO CARDIACO 20% 5 litros /min 20% 10% El sistema renal ejerce control homeostático sobre: • concentración de electrolitos • osmolaridad • volumen del plasma (volemia) ⇒ Parterial • producción de renina ⇒ Angiotensina II • pH (bases y ácidos) • excreción de toxinas y residuos metabólicos 2 estructura del riñon corteza renal médula renal médula corteza nefrón 106/riñon estructura del nefrón cápsula de Bowman glomérulo arteriola eferente arteriola aferente túbulo contorneado proximal túbulo contorneado distal brazo descendente tubo colector asa de Henle brazo ascendente 3 Irrigación sanguínea del nefrón aparato yuxtaglomerular arteriola eferente mácula densa células epiteliales especializadas del tubo distal arteriola aferente células granulares células de músculo liso modificadas, productoras de renina 4 compartimentalización funcional del riñon componentes vascular y tubular 800 ml/min filtración reabsorción secreción excreción ULTRAFILTRACION GLOMERULAR arteriola aferente arteriola eferente capilares cápsula de Bowman 5 ULTRAFILTRACION GLOMERULAR capilares cápsula de Bowman endotelio fenestrado 200 nm lumen capilar . filtrado membrana basal . podocitos epiteliales espacio capsular Influencia del tamaño en la capacidad de atravesar la barrera de filtrado 2. Evaluation of kf (filtration coefficient) -- capillary permeability substance mw H2 O 18 1.0 1.0 urea 60 1.6 1.0 180 3.6 1.0 39 3.5 0.95 glucose K+ sucrose radius (Å) Filtrate/Filtrand 342 4.4 1.0 5,500 14.8 0.98 myoglobin 17,000 19.5 0.75 egg albumin 43,500 28.5 0.22 hemoglobin 64,000 32.5 serum albumin 70,000 35.5 inulin 0.03 “cutoff” point 50-60,000 mw <0.01 6 La filtración de solutos depende del tamaño y de la carga relative clearance aniónico neutra catiónico radio (A) La filtración de solutos depende del tamaño y de la carga filtrado relative clearance aniónico neutra catiónico radio (A) glicoproteinas polianiónicas revisten la superficie de filtración contituyendo una barrera eléctrica 7 ULTRAFILTRACION GLOMERULAR J = Kf (Pc – Po) - σd (πc-πo) Pc Po presión hidrostática filtración & absorción πc πo presión oncótica ultrafiltración renal (en la mayoría de los tejidos con excepción del cerebro) x 8 CONTROL DE LA ULTRAFILTRACION GLOMERULAR La filtración es altamente sensible a cambios en la presión arterial ⇑Paferente - ⇓Pfiltrado ⇑Peferente - ⇑Pfiltrado 9 CONTROL DE LA ULTRAFILTRACION GLOMERULAR J = Kfc (Pc - Pcb)-σd (πc-πcb) CONTROL DE LA ULTRAFILTRACION GLOMERULAR 10 La arteria renal presenta un robusto mecanismo de autorregulación J = Kfc (Pc - Pcb)-σd (πc-πcb) • reflejo miogénico • retroalimentación túbuloglomerular • cambios en la permeabilidad del filtro glomerular Regulación local del flujo sanguíneo renal 11 aparato yuxtaglomerular arteriola eferente mácula densa células epiteliales especializadas del tubo distal arteriola aferente células granulares células de músculo liso modificadas, productoras de renina Retroalimentación tubuloglomerular - flujo tubo contorneado distal cantidad de Na+, K+ y Cl- en el filtrado mácula densa libera vasoconstrictor vasoconstricción arteriola aferente filtración glomerular 12 lumen tubo Mecanismos de Reabsorción Selectiva espacio peritubular epitelio tubular membrana basal endotelio capilar • por vía pericelular • por transporte transepitelial Reabsorción a lo largo del nefrón tubo distal tubo colector tubo proximal brazo ascendente del asa de Henle 13 cara apical lúmen del tubo renal cara basolateral epitelio renal líquido intersticial vaso Regulación de [Na+] Boron 14 Reabsorción de Na+ tubo proximal 70% brazo ascendente del asa de Henle 20% Tubo colector % variable Transporte pericelular de Na+ tubo contorneado proximal H2O + electrolitos Na+ K+ X absorción mayoritariamente pericelular Na+ ATP Na+ X lúmen del tubo renal epitelio renal líquido intersticial vaso 15 Transporte transepitelial de Na+ Na+ ~15 mM ~120 mM K+ X tubo contorneado proximal ATP Na+ Na+ H+ brazo ascendente Asa Henle Na+ K+ 2Cl- K+ Na+ Na+ ATP H+ tubo colector Na+ aldosterona ATP Na+ K+ lúmen del tubo renal K+ epitelio renal líquido intersticial vaso Reabsorción de aminoácidos y glucosa tubo proximal 100% 16 Transporte transepitelial de glucosa y amino ácidos Na+ glucosa tubo contorneado proximal glucosa o aa aa lúmen del tubo renal ATP Na+ Na+ SGLUT-1 GLUT K+ epitelio renal líquido intersticial vaso transporte de glucosa trasporte tubular máximo 17 Regulación de [Ca++] Reabsorción de Ca++ tubo proximal 65% > pericelular < transmembranal Tubo colector 8% brazo ascendente del asa de Henle 25% > pericelular 18 Transporte transepitelial de Ca++ ~100 nM tubo contorneado proximal Ca++ ~2.5 mM Ca++ 3Na+ 2H+ ATP Ca++ brazo ascendente Asa Henle tubo contorneado distal Ca++ Ca++ lúmen del tubo renal Hormona paratiroidea & Calcitonina Hormona paratiroidea & Calcitonina epitelio renal Ca++ 3Na+ 2H+ ATP Ca++ Ca++ 3Na+ 2H+ ATP Ca++ líquido intersticial vaso Reabsorción de H2O tubo proximal reabsorción isosmótica 75% Tubo colector % variable brazo descendente del asa de Henle 20% 19 Transporte transepitelial de H20 Na+ tubo contorneado proximal K+ X Aqp1 H2O ATP Na+ Na+ H+ brazo descendente Asa Henle tubo colector K+ H2O Aqp1 ATP Na+ Na+ H2O vasopresina Aqp2 ATP Na+ K+ lúmen del tubo renal K+ epitelio renal líquido intersticial vaso Rol del asa de Henle en la dilución de la orina 20 La reabsorción de H2O solo puede hacerse generando un gradiente osmótico. La función principal del asa de Henle es generar el gradiente osmótico dentro de la médula renal. Esto se logra mediante la extrusión activa de NaCl en el asa ascendente. asa de Henle: mecanismo de multiplicación por contracorriente vasa recta: mecanismo de intercambio por contracorriente gradiente osmótico Rol del asa de Henle en la dilución de la orina brazo brazo acendente descendente 21 mecanismo de multiplicación por contracorriente asa descendente permeable al agua gradiente osmótico H2O asa acendente permeable a sales Na+ K+ Cl- Na+ X K+ X Cl- X X H2O Salida de sales que se acumulan en la médula renal desde el asa ascendente, fuerza la salida de agua en el asa descendente. La salida de sales produce, en principio, una orina diluída. Mecanismo de multiplicación por contracorriente La orina producida es hiposomótica 22 La arquitectura de la irrigación sanguínea del riñon evita la dilución del gradiente. Mecanismo de intercambio por contracorriente en la vasa recta La estructura de la vasa recta garantiza, que la sangre venosa conserve laosmolaridad normal. 23 A modo de ejemplo: intercambio de temperatura Intercambiador de temperatura a contracorriente Mecanismo de multiplicación e intercambio por contracorriente La orina producida es hiposomótica y la sangre vertida a las venas mantiene su osmolaridad transportando gran parte las sales y agua reabsorbidas! 24 Regulación de la osmolaridad de la orina tubo proximal reabsorción isosmótica 75% brazo descendente del asa de Henle 20% Tubo colector % variable Reabsorción de H2O En ausencia de vasopresina (hormona antidiurética), la baja permeabilidad al agua del tubo colector da como resultado una orina hipoosmótica. H2O regulado por vasopresina 25 Medidas de la función renal Para toda sustancia X que el riñon no produce ni metaboliza [X]a * Fa = ([X]v * Fv ) + ([X]o * V) mmol/ml ml/min a = arteria renal F = flujo v = vena renal o = orina V = velocidad de formación de orina [X]v * Fv [X]o * V [X]a * Fa Medidas de la función renal: caudal en la arteria renal Para un soluto X que no es reabsorbido y es completamente secretado: X [X]v * Fv [X]a * Fa [X]a * Fa = ([X]v * Fv ) + ([X]o * V) 26 Medidas de la función renal: caudal de la arteria renal El ácido para-aminohipúrico (AHP) es filtrado y secretado de tal manera que es eliminado completamente en la orina en una sola pasada por el riñon. El AHP no es reabsorbido. [X]a * Fa = ([X]v * Fv ) + ([X]o * V) [AHP]a * Fa = ( 0 * Fv ) + ([AHP]o * V) Fa = ([AHP]o / [AHP]a ) * V Medidas de la función renal: tasa de filtración glomerular [X]a * Fa = ([X]v * Fv ) + ([X]o * V) mmol/ml ml/min a = arteria renal F = flujo v = vena renal o = orina V = velocidad de formación de orina [X]v * Fv [X]o * V [X]a * Fa 27 Medidas de la función renal : tasa de filtración glomerular Para un soluto X que no es reabsorbido ni secretado, como la inulina : X X [X]o * V TFGa [X]a * Fa = ([X]v * Fv ) + ([X]o * V) [X]a * TFG = [X]o * V TFG = ([inulina]o / [inulina]a ) * V a = arteria renal TFG = tasa de filtración glomerular o = orina V = velocidad de formación de orina Medidas de la función renal : tasa de filtración glomerular La tasa de filtración glomerular depende de: • La presión neta en el glomérulo • Superficie del glomérulo disponible • Permeabilidad del glomérulo 28 Medidas de la función renal : aclaramiento El aclaramiento (clearance) de una sustancia se define como el volumen virtual de plasma que es limpiado o depurado de una sustancia X en una unidad de tiempo. El aclaramiento depende de: • tasa de filtración glomerular, • reabsorción • secreción El valor del aclaramiento puede variar desde cero (sustancias que no aparecen en orina) hasta 800 ml/min (valor del flujo plasmático renal). Para un soluto que no es excretado ni reabsorbido el aclaramiento es igual a la tasa de filtración Cinulina = TFG = ([inulina]o / [inulina]a ) * V Si el aclaramiento de X es < al de inulina: se reabsorbe. Si el aclaramiento de X es > al de inulina: se secreta. Si el aclaramiento de X es = al de inulina: solo se filtra. 29