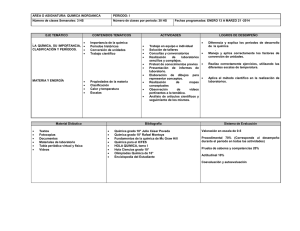
distribución del contenido programático
Anuncio

UNIVERSIDAD DE FALCÓN VICE-RECTORADO ACADÉMICO ESCUELA DE CIENCIAS DEL AGRO Y DEL MAR COORDINACIÓN DE CIENCIAS AMBIENTALES CARRERA: INGENIERÍA AMBIENTAL MENCIÓN: SEMESTRE: II CÓDIGO: A2EA ASIGNATURA: QUÍMICA GENERAL TEORÍA PRÁCTICAS LABORATORIO U.C HOR/SEM. HORAS/SEMANA 3 3 48 PRELACIONES: COMPONENTE: BÁSICO OBLIGATORIA: X ELECTIVA: - FECHA DE ELABORACIÓN DEL PROGRAMA: NOVIEMBRE 2004 PROGRAMA ELABORADO POR: Ing. Juan de Dios Colmenares. PROFESOR DE LA ASIGNATURA: Ing. Juan de Dios Colmenares. FECHA DE EVALUACIÓN DEL PROGRAMA: PROGRAMA ANALÍTICO FUNDAMENTACIÓN La asignatura QUÍMICA GENERAL está incorporada en los pensum de estudio de las carreras Ingeniería Electrónica e Ingeniería Ambiental, que son ofrecidas por la Universidad de Falcón (UDEFA) dentro de las áreas Ingeniería, Arquitectura y Tecnología y Ciencias del Agro y del Mar respectivamente. Esta asignatura, ubicada dentro del grupo de las que corresponden al componente básico, esta relacionada con otras que tendrán que cursar los estudiantes de la carrera Ingeniería Ambiental como lo son Química Inorgánica y Química Orgánica y que necesitan de ciertos aprendizajes previos o conductas de entrada que deben ser adquiridas en la asignatura Química General. De allí que su propósito es el de aplicar las fórmulas, los conceptos y el lenguaje básico de la química en el desarrollo de estas asignaturas posteriores, así como también proporcionar al estudiante herramientas de cálculo para resolver problemas de la vida diaria y del campo de la ingeniería. Dentro de sus contenidos, se contempla básicamente temas sobre la estructura y propiedades de la materia y las leyes y principios que rigen sus combinaciones y transformaciones. OBJETIVO GENERAL Aplicar las representaciones simbólicas, los conceptos y lenguaje básico de la Química en el desarrollo de cursos posteriores y en la resolución de problemas de la vida diaria y del campo de la ingeniería. 1 OBJETIVOS ESPECÍFICOS: Estudiar las características de los sistemas materiales, las transformaciones de la materia y el reconocimiento de sus propiedades macroscópicas, explicando dichas propiedades, mediante modelos microscópicos que incluyen: Leyes de combinaciones químicas, para expresar relaciones cuantitativas en los cambios químicos (conservación de la masa y energía, proporciones definidas), Teoría atómica – molecular de Dalton y algunos conceptos como el de mol y peso atómico relativo para la realización de cálculos estequiométricos. Estudiar la constitución de la materia a partir de la relación entre el modelo atómico (estructura electrónica y nuclear de los átomos de los elementos), la tabla periódica y los diferentes tipos de enlaces químicos. Estudiar los diferentes estados físicos o de agregación de la materia: gaseoso, liquido y sólido, a través de la caracterización de las propiedades generales de las sustancias en cada estado, y del conocimiento y aplicación práctica de las leyes y teorías que rigen el comportamiento de dichas sustancias. Estudiar la estructura y propiedades de las soluciones a partir del conocimiento y aplicación práctica de leyes y teorías que permiten describirlas en términos cuantitativos (composición) y cualitativos (diferencias en las propiedades físicas). SEMANA 1 2 3 4 DISTRIBUCIÓN DEL CONTENIDO PROGRAMÁTICO Introducción. Presentación del Programa Analítico. Presentación y discusión del Plan de Evaluación. Unidad I: Sistemas homogéneos y heterogéneos. Conceptos de material, fase, mezclas, soluciones, sustancias puras, átomos, elementos, compuestos, moléculas. Descripción de la tabla periódica. Interpretación de la información que suministra: número atómico, peso atómico relativo, grupo, período, valencia, metal, no metal, gas noble. Peso fórmula de un compuesto, composición porcentual de un compuesto. Unidad I: Nomenclatura y formulación de los compuestos inorgánicos: óxidos, ácidos, bases, sales e iones. Transformaciones físicas y químicas. Procesos químicos: representación a través de las ecuaciones químicas. Conceptos de reactantes, productos, sentido de una reacción, reversibilidad y estequiometría. Relaciones cuantitativas en los cambios químicos. Ley de la conservación de la masa y la energía. Leyes de las combinaciones químicas. Teoría atómica – molecular de Dalton. Ley de Avogadro. Balanceo de ecuaciones químicas por tanteo. Concepto de Mol. Unidad I: Concepto de proporción de reacción. Proporciones o relaciones: molares, másicas y mixtas. Conceptos de reactivo limitante y reactivo en exceso. Rendimiento teórico, rendimiento real y porcentaje de rendimiento de un proceso químico. Cálculos estequimétricos. 2 SEMANA 5 6 7 8 9 10 11 12 13 14 15 16 1. 2. 3. 4. 5. DISTRIBUCIÓN DEL CONTENIDO PROGRAMÁTICO Unidad II: Estructura electrónica y nuclear de los átomos, moléculas: Distribución de los electrones en los niveles de energía principales y en los subniveles. Cantidad máxima de electrones en los niveles de energía principales. Estructura atómica de los átomos. Relación entre la estructura atómica y la posición en la Tabla Periódica. Reglas para ubicar un elemento químico en la Tabla Periódica. Periodicidad en las propiedades de los elementos. Unidad II: El enlace químico. Tipos de enlace químico: iónicos, covalente, covalente coordinado. Tipos de reacciones químicas atendiendo al tipo de enlace que presentan las sustancias participantes en dichas reacciones. Ejercitación. Unidad III: Estados físicos o de agregación de la materia: gaseoso, líquido, y sólido. Sustancias gaseosas, conceptos de volumen, presión, temperatura, y condiciones normales para una sustancias gaseosa. Unidades de volumen, presión y temperatura. Concepto de gas ideal. Leyes que rigen el comportamiento de los gases ideales: Ley de Boyle, Ley de Charles, Ley Combinada, Ley de Dalton de las presiones parciales. Ecuación de estado de los gases ideales. Teoría cinética de los gases, Ley de difusión de Graham. Cálculos estequiométricos donde intervienen sustancias gaseosas. Unidad III: Capacidades caloríficas. Gases reales. Sustancias líquidas. Propiedades generales de los líquidos. Presión de vapor. Vaporización. Ebullición. Concepto de equilibrio. Equilibrio de fases en los cambios de estado. Curvas de equilibrio. Factores que afectan el equilibrio. Principio de Le Chatelier. Aplicación. Unidad III: El estado cristalino. Propiedades macroscópicas de los sólidos. Tipos de sólidos. Isomorfismo. Calor específico. Unidad IV: Conceptos de solución, soluto y solvente. Conceptos de Solubilidad, saturación y sobresaturación. Entalpia de Solubilidad. Unidades de concentración de las soluciones: unidades físicas y unidades químicas. Preparación de soluciones. Unidad IV: Ley de Henry. Teoría de las soluciones diluidas. Ley de Raoult. Soluciones ideales. Curvas de equilibrio líquido – vapor. Destilación. Grado de disociación en el equilibrio. Variación de la constante de equilibrio con la temperatura. Unidad IV: Propiedades coligativas de las soluciones: disminución de la presión de vapor, aumento ebullioscópico, descenso crioscópico, presión osmótica. Cálculos de soluciones (preparación, leyes y propiedades). ESTRATEGIAS DE ENSEÑANZA - APRENDIZAJE Lectura y discusión de materiales de apoyo sobre algunos contenidos de cada unidad del Programa Analítico. Resolución de Hojas de Trabajo por grupos de estudiantes con asesoría del profesor. Realización de trabajos bibliográficos por grupos de estudiantes, sobre algunos contenidos de las Unidades II y III. Lectura previa de contenidos del Programa Analítico. Asesoría docente sobre los contenidos programáticos en horarios pre-establecidos. 3 PLAN DE EVALUACIÓN SEMANAS UNIDADES 5 I 8 II 12 III 16 IV 4, 9, 11, 15 TIPO DE EVALUACIÓN CONTENIDO PONDERACIÓN % Sistemas materiales. Propiedades de Prueba escrita la materia Prueba escrita. Constitución de la materia. Trabajo bibliográfico Prueba escrita. Estados de agregación de la materia Trabajo bibliográfico Soluciones I, II, III, IV Los correspondientes a cada unidad 25 10 5 20 5 Prueba escrita. 25 Resolución de Hojas de Trabajo por grupos de estudiantes 10 BIBLIOGRAFÍA Babor, J., Ibarz, J. (1995) Química General. Editorial Marín S.A. 8va. Edición. Brady, J., Humiston, G. (1993) Química Básica. Editorial Limusa. 2da Edición. Burns (1996) Fundamentos de Química. Editorial Prentice Hall Hispanoamérica. Chang, R. (1992) Química. Mc Graw – Hill. 4ta. Edición. México. Colmenares, J. (2001) Química I. Procedimientos Metodológicos para la Resolución de Problemas. Trabajo de ascenso, libro texto. UNELLEZ – Apure. Garzón, G. (1986) Química General. Mc Graw – Hill. 2da. Edición. México. Masterton, W., Slowinski, E. Edición. México. (1984) Química General Superior. Editorial Interamericana. 5ta. Quiñoá, E., Riquera, R. (1996) Nomenclatura y Formulación de los Compuestos Inorgánicos. Mc Graw – Hill. España. Santos, E. (1991) Química General. Editorial UNED. 5ta. Edición. España. Seese, W., Daub, W. (1989) Editorial Prentice Hall. 5ta. Edición. México. Sherman, A. y otros México. (1999) Conceptos Básicos de Química. Editorial CEDSA. Sienko – Plane (1986) Química. Principios y Aplicaciones. Mc Graw – Hill. México. ____________ CZJ.- OCTUBRE 2004 Elaborado por: Ing. Colmenares Juan 4 1era. Edición.