Propiedades_de_la_materia_II_Conductividad_Termica_Emisionabsorcionluz.ppt
Anuncio

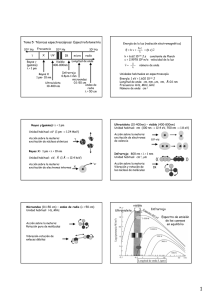
PROPIEDADES DE LA MATERIA A ESCALA ATÓMICA II Propiedades de la materia a escala atómica Electrización Conductividad Eléctrica Conductividad Térmica Emisión - Absorción de luz CONDUCTIVIDAD TÉRMICA Propiedad que consiste en la capacidad de conducir el calor. Los cuerpos que transmiten rápidamente el calor, son llamados CONDUCTORES TÉRMICOS. CONDUCTIVIDAD TÉRMICA CONDUCTIVIDAD TÉRMICA Si transfieren el calor más lentamente se llaman AISLADORES O AISLANTES TÉRMICOS. Un aislante, establece una barrera al paso del calor entre dos medios, impidiendo que entre o salga calor. Ejemplos: plumavit, cerámica. EMISIÓN Y ABSORCIÓN DE LUZ En condiciones normales (átomo en estado fundamental), los electrones ocupan los menores niveles de energía posibles (más cercanos al núcleo) Pero los electrones pueden absorber energía de una fuente externa. Cuando pasa esto, la energía absorbida puede hacer que los electrones pasen a mayores niveles de energía (estado excitado) El estado excitado es inestable, no se puede mantener en el tiempo y por lo tanto los electrones vuelven a niveles de energía mas bajos, emitiendo energía en forma de luz (fotones o cuantos) La luz blanca visible procedente del sol puede descomponerse en sus diferentes colores mediante un prisma. A la gama de colores en la que se descompone la luz se le denomina espectro visible, y es continuo (es decir, contiene todas las longitudes de onda del espectro visible, desde el rojo (400 nm) al violeta (700 nm)). Sin embargo, en los elementos químicos el espectro de la luz emitida es discontinuo, y consta de líneas o rayas localizadas a longitudes de onda específicas. Cada elemento posee un espectro característico y único, que puede utilizarse para identificarlo. Los saltos de los electrones desde niveles de mayor energía a otros de menor energía, y viceversa, suponen una emisión o una absorción de energía electromagnética (fotones de luz), respectivamente. Cuando una sustancia recibe energía, capta la necesaria para que sus electrones se muevan de un nivel de menor a uno de mayor energía (estado excitado). Esto se observa en su espectro de absorción. Ejemplo: Espectro de absorción del sodio(Na) Una sustancia en estado excitado emite espontáneamente la energía recibida, lo que provoca que el electrón regrese a su estado fundamental. Esto se observa en su espectro de emisión. Ej: Espectro de emisión del sodio (Na) Ello explica los espectros discontinuos de emisión y absorción de luz de los átomos, donde cada línea del espectro es un posible salto de un nivel energético a otro