LAB DE TERMODINAMICA
Anuncio

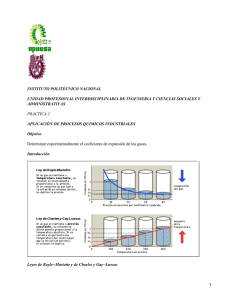
* DETERMINACIÓN DE LA CONSTANTE UNIVERSAL DE LOS GASES * Determinar experimentalmente la CONSTANTE UNIVERSAL de los gases R y el VOLUMEN MOLAR del hidrógeno. PROBLEMA Manteniendo constantes • Cantidad de materia (n), • Presión (P) • Temperatura (T) Obtener experimentalmente La constante universal de los gases R y el volumen molar a condiciones ambientales, a partir de la reacción Mg(s) + HCl(ac) MgCl2(ac) + H2(g) * Variables y modelos que describen el comportamiento de los gases Gas Hipotético Condiciones Normales y estándar IUPAC * Es una constante física que relaciona diversas FUNCIONES DE ESTADO TERMODINAMICO * Estableciendo esencialm Relación ENERGÍA-TEMP-mol * Proporcionalidad que combina LEYES AVOGADRO, LUSSAC y CHARLES * Figura 1 1. 3M Con el equipo armado, verificando que no existan fugas 2. Inyectando aire 3.-se trabaja en EL EXTREMO DE LA MESA para que NO SE EXTRANGULE LA MANGUERA LA BURETA DEBE DE ESTAR EN LA parte inferior de su soporte y el embudo en la PARTE mas arriba que se pueda de su soporte. Llena con agua, la bureta hasta el limite del vástago del embudo y el punto de referencia de la probeta 4.- Asegúrate que no existan burbujas de aire en la bureta y mangueras. MESA * 5.- Mide la T A (Tamb) y presión barométrica (Patm). * 6.- La tira de Magnesio dóblala en 4 partes y obtén la masa inicial m1 e introdúcela en el tubo de ensayo * m1 DETERMINACIÓN 6.- Mide el volumen inicial en la bureta (V1). 7.- Inyectar 0.5 mL de HCl 3M. 8.- Espera 15 minutos a que la reacción finalice y que el gas obtenido alcance el equilibrio con la T Amb. 9.- MUEVE el embudo para igualar el nivel del agua con el nivel de la bureta, como se muestra en la Figura 2. 10.- MIDE EL VOLUMEN V2 Desconecta el tubo del dispositivo y recuperar el Mg que no reacciono. 11.- Lava y seca perfectamente el Mg recuperado y obtener la masa final (m2). Si es necesario utiliza acetona o alcohol. 12.- Repite el experimento 2 veces y registra (nota: no necesitas secar el matraz o tubo, ni cambiar el agua en la bureta). * VOLUMEN Con el volumen inicial y final medido en la bureta, se obtiene el volumen del H2 recolect. V2-V1 =V H2 PRESIÓN El H2 no es el único gas en la bureta, existe Patm = PH20 + PH2 también vapor de agua, para poder determinar la presión parcial del H2 seco se necesita conocer la Pparcial del vapor de agua. En el experimento se ajusta el nivel de agua en el embudo con el de la bureta, esto significa que la presión total del sistema es igual a la presión atmosférica TEMP La temperatura será (Tamb). VOLUMEN MOLAR Se conoce el volumen y el número de moles generadas de H2 R Finalmente utilizando la ecuación del gas ideal se obtendrá R en (L Atm/mol K) V m H2= VH2 /nH2 *