Presentación de PowerPoint - Página Personal de Jose Luis Mesa
Anuncio

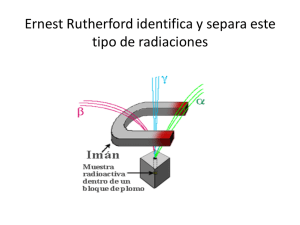
EL NÚCLEO ATÓMICO Los núcleos retienen sus identidades en los procesos químico, y las propiedades nucleares, con excepción de la carga, influyen en el comportamiento químico de modos tan sólo indirectos y sutiles La naturaleza del núcleo Los núcleos están compuestos de protones y neutrones, por lo cual se alude a estas partículas como nucleones. Se da la descripción de un núcleo particular en términos de su carga Z y de su número de masa A, que es la suma de sus neutrones y protones. Para representar a un núcleo, se escribe el símbolo químico con un subíndice igual a Z, y un superíndice igual a A Los núcleidos O816(8p, 8n) , O817 (8p, pn) y O818 (8p, 10n) representan a los tres isótopos del oxígeno: núcleos con cargas iguales pero diferentes números de masa. Nucleido es un término general utilizado para referirse a cualquier isótopo de cualquier elemento Isótopos son aquellos nucleidos que tienen el mismo número atómico Z, pero distinto número másico A Isótonos son aquellos nucleidos que tienen el mismo número de neutrones El tamaño nuclear La primera indicación del tamaño del núcleo fue el experimento de dispersión de las partículas a de Rutherford El resultado cualitativo de este experimento es que las partículas a pueden acercarse hasta dentro de 10-12 cm del centro de un átomo y todavía pueden ser dispersadas por una fuerza que está dada por la ley de Coulomb Un gran número de radios nucleares ha sido determinado y los resultados pueden resumirse por la ecuación: R = R0 A(1/3) siendo R0 = 1.33x10-13 cm, constante común a todos los núcleos La dependencia del radio nuclear respecto al número de masa indica que el volumen nuclear V debe, para una simetría esférica, ser proporcional a R3 R a R3 a A El volumen nuclear es directamente proporcional al número total de neutrones y protones que hay en el núcleo Este hecho sugiere que los protones y neutrones se empaquetan juntos como si fueran esferas rígidas, y hacen al volumen nuclear total igual a la suma de los volúmenes de los protones y neutrones individuales Forma nuclear Existen algunos núcleos como : H1 , O8 , Ca20, Ni28, Sn50, Pb82, que se ha comprobado que son esféricos Los núcleos que tienen números atómicos cercanos a uno de los de la lista precedente son esféricos o casi esféricos, mientras que la mayoría de los otros núcleos son esferoides ligeramente alargados (con forma de pelota de “football” americano) El alejamiento de la forma esférica no es nunca extremo: el cociente del semieje mayor al semieje menor es generalmente menos que 1.2 Masa y energía nuclear La unidad de masa nuclear es la unidad de masa atómica o “uma”, que se define exactamente como 1/12 de la masa de un átomo de C612 En esta escala, un neutrón tiene una masa de 1.00866544, mientras que la masa de un átomo de hidrógeno (protón más electrón) es de 1.00782522 Una comparación cuidadosa de la masa de cualquier átomo con la suma de las masas de los átomos de hidrógeno y de sus neutrones constituyentes, revela una interesante deficiencia de masa. Considérese, p. ej., el átomo O816 que tiene una masa de 15.994915 uma. En contraste con esto, la masa de ocho neutrones y ocho átomos de hidrógeno en conjunto es de 16.131925 uma [O816 = 8 masa del at H + 8 masa neutrón = 8.06260176 + 8.06932352 = 16.13192528 uma] Por eso, O816 es más liviano de lo que podríamos esperar en (16.131925 – 15.994915) ó 0.137010 uma De acuerdo con la equivalencia masa-energía expresada por la relación de Einstein: E = mc2 [g . cm . (cm/s2) ≡ dinas . cm = ergios] la deficiencia de masa del átomo de oxígeno puede ser atribuida a la energía emitida por el sistema cuando ocho neutrones, protones y electrones se unen para formar un átomo de O 816 En la secuencia anterior si se expresa “c”, la velocidad de la luz en cm/s, y la masa “m” en gramo las unidades de “E” son ergios. Así 1-g-masa es equivalente a cerca de 9x1020 ergios ó 2.1x1010 kcal Otra equivalencia de masa-energía que se emplea más comúnmente es la siguiente : 1 uma es equivalente a 931.4 millones de e.V de energía (931.4 MeV) La energía liberada cuando un átomo de oxígeno se forma de sus neutrones, protones y electrones es, por tanto, 0.137010 x 931.4 = 127.6 MeV por átomo Para apreciar cuán grande es esta cantidad de energía, compáresela con la energía de 5.2 eV que se libera cuando dos átomos de oxígeno forman entre ambos un fuerte enlace químico Fuerza y estabilidad nuclear Comparando la masa media de un átomo con la suma de las masas de sus neutrones, protones y electrones constituyentes, se puede calcular la energía total E b que une en conjunto a un núcleo. Más instructiva que la energía total de enlace es la energía de enlace por nucleón E b/A Después de una subida abrupta entre los núcleos más livianos, la energía de unión por partícula nuclear cambia solo ligeramente, oscilando entre 8 – 8.5 MeV, y tiene un valor de, aproximadamente, 8 MeV por nucleón Los núcleos de máxima estabilidad tienen números de masa cercanos a 60 o cargas de aproximadamente 25 Debido a que el máximo en la energía de enlace por partícula ocurre para núcleos de 60 [El máximo de estabilidad se observa para el Fe2656] la fisión de un núcleo muy pesado en un par de núcleos de masa próxima a 60 es un proceso que libera energía De igual manera, la fusión de dos núcleos más livianos, en otro de masa próxima a 60, va también acompañada por una liberación de energía Este hecho de la constancia a partir de un cierto umbral, indica que las interacciones fuertes son de corto alcance, puesto que basta que un nucleón esté rodeado por un número mínimo de nucleones al ir aumentando el número de nucleones la energía media no varía, puesto que aquéllos ya se encuentran rodeados por el número mínimo necesario Debido a que la energía de unión por nucleón para los elementos de número de masa mayor que 20 varía muy ligeramente, se puede decir, en primera aproximación Eb/A constante Eb cte x A Es decir que, la energía total de unión de un núcleo es aproximadamente proporcional al número de los nucleones Esta observación sugiere que las fuerzas que unen juntos a los nucleones son de corto alcance, es decir, que un nucleón ejerce fuerza atractiva solamente sobre sus vecinos más cercanos Si las fuerzas nucleares fueran de largo alcance, cada uno de los nucleones A sería atraído a otros A-1 nucleones, y la energía de enlace nuclear total sería proporcional a A(A – 1), en vez de serlo a A Además de ser de corto alcance, las fuerzas atractivas entre los nucleones son independientes de la carga Sin embargo, una repulsión culómbica entre protones; así, la energía de enlace neta entre dos protones es menor que entre dos neutrones. La energía nuclear atractiva de 14.1 MeV por partícula se reduce a un valor de 8 MeV, al tener en cuenta la repulsión culómbica entre protones Von Weizsäcker ideó una expresión semiempírica para la energía nuclear de enlace La energía total de enlace del núcleo, en MeV, está dada por: Eb = 14.1 A – 13 A(2/3) – [(0.6Z2) / A(1/3)] El primer término del lado derecho de la ecuación expresa que la energía de enlace atractiva es de 14.1 MeV por partícula Los nucleones en la superficie nuclear no tienen su complemento total de 12 vecinos más cercanos, y, por tanto, no contribuyen con los 14.1 MeV completos a la energía de unión nuclear, de ahí el término -13(A)(2/3) Existe la repulsión coulómbica entre los protones, que también constituye una pérdida de energía, y su efecto está representado por el término -0.6[(Z)2 / A(1/3) La relación entre la abundancia de los núcleos y el número de partículas de las que se compone el núcleo es también importante Los núcleos que tienen número par de neutrones y de protones parecen ser particularmente estables Mientras que, por el contrario, solamente ocho núcleos estables tienen número impar Estas observaciones sugieren que hay un apareamiento separado entre neutrones y protones que afecta la estabilidad nuclear Se conoce también que los núcleos con los números “mágicos” de neutrones igual a 2, 8, 20, 50, 82 y 126, y de protones igual a 2, 8, 20, 50 y 82, son particularmente estabables y abundantes en la naturaleza La existencia de estos números “mágicos” sugirió un “modelo de capa” del núcleo: es decir, un esquema de niveles de energía, semejante al esquema de niveles de energía orbital, que se emplea para los electrones atómicos Radiactividad El concepto de radiactividad hace referencia a los distintos procesos espontáneos mediante los cuales un núcleo emite algún tipo de radiación, alcanzando una situación más estable Una forma de radiactividad natural es la fisión espontánea de un núcleo muy pesado en dos fragmentos más estables de número de masa cercano a 60 La fisión espontánea es más bien poco común, y la mayoría de los núcleos espontáneamente radiactivos se desintegran por la emisión ya sea de una partícula a, una partícula b positiva o negativa, un rayo g o por la captura de un electrón orbital Haciendo una gráfica de la carga Z en función del número de neutrones N, para todos los núcleos no radiactivos, se encuentra a los núcleos estables dentro de una zona bien definida Entre los núcleos más livianos que Ca2040, los núcleos más estables tienen números iguales de neutrones y protones Entre los elementos más pesados, los núcleos más estables contienen más neutrones que protones. (Esto ocurre posiblemente debido a la necesidad de compensar las repulsiones entre protones, cada vez mayores, por la fuerza de atracción entre neutrones y protones) Procesos de desintegración Los núcleos que quedan fuera de la zona de estabilidad son radiactivos y se descomponen de manera que forman un núcleo que queda en la región estable Los núcleos que se encuentran por debajo de la zona de estabilidad son ricos en neutrones y alcanzan estabilidad emitiendo partículas b negativas o electrones. Este proceso se puede representar como una transformación de un neutrón del núcleo en un protón y en un electrón que es emitido. El núcleo que resulta tiene un protón más y un neutrón menos que su antecesor, y se encuentra más cerca de la zona de estabilidad C614 N714 + b-10 ; n p + b -10 Los núcleos que quedan por arriba de la zona de estabilidad tienen que disminuir su carga positiva para alcanzar la estabilidad. Son posibles dos procesos : Captura de un electrón orbital (captura K, porque un electrón de la capa K (n= 1) es capturado por el núcleo) seguida de la conversión de un protón a un neutrón O815 + e-10 N715 ; p + b -10 n Emisión por parte del núcleo de un psoitrón o electrón positivo, que acaba en la conversión de un protón nuclear a neutrón C611 B511 + b +10 ; p n + b +10 Proceso de desintegración a Con pocas excepciones, la desintegración por emisión de una partícula a ocurre solamente entre los elementos de número de masa mayor que 200 Un ejemplo típico de desintegración a es : U92238 Th90234 + He24 En este proceso, el número de masa nuclear disminuye en cuatro unidades y la carga nuclear en dos Proceso de desintegración g (radiación g ; l= 10-15 m) Con frecuencia, el núcleo hijo formado por la desintegración a ó b de su antecesor, es producido en un estado excitado El núcleo recién formado libera esta energía de excitación emitiendo un rayo g; esto es, una radiación electromagnética de longitud de onda extremadamente corta El núcleo U92238 emite partículas a que tienen energías ya sea de 4.18 MeV ó 4.13 MeV Cuando se emite una partícula a de 4.13 MeV el núcleo hijo, Th90234, queda en un estado de excitación cuya energía (4.18 -4.13) ó 0.05 MeV mayor que el estado alcanzado cuando se emite una partícula de 4.18 MeV En consecuencia, se podría esperar que el núcleo excitado debiera emitir un rayo g de 0.05 MeV, y esto es ciertamente lo que se encuentra experimentalmente Reacciones nucleares Es aquella en la que un núcleo se bombardea con una partícula dotada de gran energía, para conseguir la transmutación nuclear Rutherford obtuvo la primera transmutación artificial de un elemento por el bombardeo de una muestra de nitrógeno con partículas a procedentes del Ra N714 + He24 O817 + H11 Hay dos tipos de reacciones nucleares: Fisión, p. ej., U92235 + n Y3995 + I53138 + 3n Fusión, p. ej., H12 + H13 He24 + n01 Se cree que en el sol y en las estrellas se producen reacciones de fusión a temperaturas superiores a 107 K Debido a que las partículas a de que se dispone, procedentes de las fuentes naturales de radiactividad, tienen un ámbito limitado de energías, ellas pueden inducir relativamente pocas reacciones nucleares. El desarrollo de los aceleradores de partículas,como el ciclotrón y sus diversas modificaciones, ha hecho posible producir rayos relativamente intensos de partículas energéticas, y se ha estudiado un número muy grande de reacciones nucleares Uno de los hechos más conocidos en esta área ha sido la síntesis de los elementos transuránidos U92238 + H12 Np93238 + 2 n01 U92238 + He24 Pu94239 + 3 n01 U92238 + C612 Cf98246 + 4 n01 U92238 + N714 Es99247 + 5 n01 Una de las más famosas reacciones nucleares es la fisión del U92235, inducida por la captura de neutrón. No hay productos fijos en esta reacción; la fisión produce fragmentos cuyos números de masa varían desde aproximadamente 70 hasta 160. Un proceso de fisión es : U92235 + n01 Sr3890 + Xe54143 + 3 n01 Velocidades de desintegración radiactiva La desintegración espontánea de los núcleos radiactivos es un proceso cinético de primer orden El número de desintegraciones por segundo es proporcional al número de núcleos presentes De este modo, se puede escribir para la velocidad de desintegración : -(dN / dt) = l N siendo: l, la constante de desintegración del núcleo (lo que da idea de la mayor o menor velocidad con que se desintegra) y N el número de núcleos que hay en la muestra La expresión anterior se puede escribir de la forma: -(dN / N) = l dt La cual indica que la fracción de los núcleos, dN / N, que se desintegran en un intervalo de tiempo dt, es una constante. Integrando la expresión anterior, se tiene: N0N -(dN / N) =0t l dt Ln(N/N0) = - l t N/N0 = e-lt N = N0 e- l t siendo: N el número de núcleos que quedan al tiempo “t”, y N0 el número de núcleos al tiempo cero En general, la velocidad de una reacción se define como la desaparición de reactivo en la unidad de tiempo, o lo que es equivalente, el aumento de producto en la unidad de tiempo: v= -(dN / dt) = (dN’ / dt) si el proceso es : N N’ Al valor v= (dN / dt) se le denomina actividad y se mide en Becquerel (Bq) ó Curies (Ci); tal que, 1Ci = 3.7x1010 Bq En lugar de informar acerca de la velocidad de una desintegración nuclear mediante su constante de desintegración, es más conveniente dar la vida media del proceso. El tiempo que se requiere para que desaparezca la mitad de la muestra originalmente presente. t = t1/2 N = (1/2)N0 Ln (1/2)= - l t1/2 t1/2 = [ (Ln 2) / l] La estabilidad nuclear se mide mediante la vida media (si la transformación es espontánea) o por la facilidad de la conversión (si la transformación se debe a bombardeo). Cualquier núcleo con vida media igual o superior a 10 10 años se considera estable