2 - cideim
Anuncio

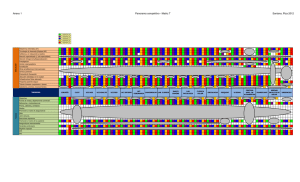
Algoritmo de decision para la escogencia empirica inicial basado en : La probabilidad de tener una Enterobacteriaceae productora de BLEE y la ausencia de P. aeruginosa Selección adecuada del antibiótico estará basada en: 1. 2. 3. 4. 5. Epidemiologia local Estratificación de la infección Mecanismos de resistencia De-escalonamiento Costo tratamiento/día Red de Resistencia Bacteriana CIDEIM MICROORGANISMOS MÁS FRECUENTES 2006 – 2010 (%): SALAS 100% 90% 80% 70% 60% 50% 40% 30% 3% 3% 3% 4% 3% 3% 4% 5% 8% 8% 9% 9% 13% 13% 20% 10% 27% 22% 3% 3% 4% 5% 2% 3% 4% 5% 3% 3% 5% 6% 7% 7% 7% 9% 10% 10% 11% 11% 10% 26% 24% 25% 0% 2006 (n=10748) E. coli S. aureus 2007 (n=14655) K. pneumoniae P. aeruginosa 2008 (n=20792) S. epidermidis 2009 (n=20250) E. faecalis E. cloacae 2010 (n=22525) A. baumannii P. mirabilis Red de Resistencia Bacteriana CIDEIM MICROORGANISMOS MÁS FRECUENTES 2006 – 2010 (%): UCI 100% 90% 80% 70% 5% 60% 50% 5% 6% 40% 7% 30% 7% 8% 20% 4% 9% 9% 6% 3% 11% 10% 12% 3% 4% 9% 9% 4% 7% 9% 9% 8% 11% 13% 12% 15% 14% 14% 6% 6% 4% 9% 10% 9% 12% 0% 2006 (n=5531) E. coli K. pneumoniae 2007 (n=7912) S. epidermidis S. aureus 2008 (n=8901) A. baumannii 2009 (9182) P. aeruginosa C. albicans 2010 (12429) E. cloacae E. faecalis Selección adecuada del antibiótico estará basada en: 1. 2. 3. 4. 5. Epidemiologia local Estratificación de la infección Mecanismos de resistencia De-escalonamiento Costo tratamiento/día Estratificación de la Infección 1. Permite correlacionar la severidad de la infección con las bacterias causantes. 2. Evita cubrimiento de amplio espectro cuando puede darse de espectro limitado. 3. Disminuye la presión selectiva innecesaria. Protocolizacion de Ertapenem basado en estratificación de la infección • Infecciones Intra-abdominales de la comunidad con peritonitis generalizada. • Neumonía de la comunidad severa III y nosocomial temprana < 4 días ( no asociada al Ventilador) • Infecciones de piel y tejidos blandos (mixtas, BLEE y AmpC ) • Pie diabético: categoría moderada. ▪ ITU: Pielonefritis en urgencias e ITU en pisos según epidemiologia. ▪ Infecciones por BLEEs y AmpC (excepto shock séptico o sepsis severa) Infecciones Intra-abdominales de la comunidad con peritonitis generalizada • Paciente con mayor inóculo bacteriano (más de un cuadrante y evento de íleon para abajo) y/o con peritonitis generalizada, y síntomas sistémicos (fiebre, leucocitosis) y/o que presenta además enfermedad de base como Diabetes Mellitus, Insuficiencia Renal , edad mayor 65 años, hospitalizaciones previas, historia de diverticulitis tratadas. • Tto de eleccion : Ertapenem • • • • Resistencia Quinolonas, posibilidad de BLEEs y de-represion AmpC Inoculo elevado Toxicidad Aminoglicosidos Bajo riesgo de Pseudomona o Enterococo ( no cobertura inicial ) Efectos de la exposición a carbapenems en el riesgo de portar en el tracto digestivo P. aeruginosa resistente a carbapenems endémica de la UCI en pacientes críticamente enfermos • Para determinar la epidemiologia y factores de riesgo para colonización del tracto digestivo P. aeruginosa resistente a carbapenems, semanalmente se obtuvieron isopados rectales y faríngeos en dos encuestas seriadas de incidencia (266 pacientes). • Análisis de regresión logística identificó: 1. Severidad de la enfermedad aguda (OR 1.0; IC 95% 1.0 a 1.1) 2. Uso previo de carbapenems (OR, 7.8; IC 95% 1.7 a 35.3) 3. Uso previo de fluoroquinolonas (OR, 11.0; IC 95% 1.7 a 67.9) como factores de riesgo independientes para colonización del tracto digestivo por PA resistente a carbapenems Peña C et al. Antimicrob Agents Chemother 2007; 51: 1967-1971 Estudio retrospectivo de 4 años Riesgo mínimo de P. aeruginosa resistente a imipenem con ertapenem Imipenem y Meropenem— 20% aumento de incidencia de IMP-R PA por cada 100DDD (P =0.0014) y un aumento anual de incidencia de IMP-R PA de 3.8%, (p< 0.001) Ertapenem— Sin correlación con P. aeruginosa resistente a Imipenem 95% CI Predicted imipenem resistance 95% CI Predicted imipenem resistance 7 P=0.2 P=0.001 6 Incidence Incidence 6 4 2 5 4 3 2 0 1 –2 0 0 20 40 DDD of Ertapenem 60 0 20 40 60 80 DDD of Group 2 Carbapenem Carmeli Y⁎, LidjiSK, ShabtaiE et al. Diagnostic Microbiology and Infectious Disease. 2011; Slide 10 70 : 367–372 Selección adecuada del antibiótico estará basada en: 1. 2. 3. 4. 5. Epidemiologia local Estratificación de la infección Mecanismos de resistencia De-escalonamiento Costo tratamiento/día FACTORES DE RIESGO PARA PACIENTE CON ENTEROBACTERIACEA PRODUCTORA DE BETA-LACTAMASAS DE ESPECTRO EXTENDIDO (BLEE) CATEGORÍA Uso previo de antibiótico Procedimientos/ dispositivos invasivos Ubicación del paciente Antecedentes médicos FACTOR DE RIESGO Piperaciclina/tazobactam en el último año OR 11,2 Combinación de quinolonas y cefalosporinas 5,5 Ref 5 3 Oxyimino-cefalosporinas 5,2 4 Cefalosporinas 4,7 5 Exposición reciente a quinolonas 4,4 3 Cefalosporinas de tercera o cuarta generación Aztreonam 3,5 3 3,3 1 Cefuroxime Hemodiálisis 2,6 1 13,6 2 Sonda urinaria a permanencia 6,2 4 Nutrición parenteral total 1,7 1 Vivir en hogares de cuidado 9,3 2 Admisión a UCI según epidemiología local 1,7 1 Infecciones recurrentes 2,9 3 Quemaduras 2,8 1 Insuficiencia renal 1,9 1 En resumen para BLEEs: • El Uso previo de Cefalosporinas (cualquiera), pero especialmente de 3ra generación, (por estar en mayor cantidad de estudios y con un OR mayor), seguido por el uso de quinolonas y Piperacilina/tazobactam , son los factores más importantes para considerar la presencia de BLEE y NO USAR ninguno de los antibióticos antes mencionados en forma empirica . • El haber estado hospitalizado y tener un procedimiento relacionado con hemodiálisis o sonda urinaria, seguido de hogares de cuidado, son los otros factores altamente asociados a tener una BLEE. Referencias • • • • • 1. Paterson DL, Ko WC, Von GA, Mohapatra S, Casellas JM, Goossens H et al. International prospective study of Klebsiella pneumoniae bacteremia: implications of extended-spectrum beta-lactamase production in nosocomial Infections. Ann Intern Med 2004; 140(1):26-32. 2. Saely S, Kaye KS, Fairfax MR, Chopra T, Pogue JM. Investigating the impact of the definition of previous antibiotic exposure related to isolation of extended spectrum beta-lactamase-producing Klebsiella pneumoniae. Am J Infect Control 2011; 39(5):390-395. 3. Cassier P, Lallechere S, Aho S, Astruc K, Neuwirth C, Piroth L et al. Cephalosporin and fluoroquinolone combinations are highly associated with CTX-M betalactamase-producing Escherichia coli: a case-control study in a French teaching hospital. Clin Microbiol Infect 2011; 17(11):1746-1751. 4. Wu UI, Yang CS, Chen WC, Chen YC, Chang SC. Risk factors for bloodstream infections due to extended-spectrum beta-lactamase-producing Escherichia coli. J Microbiol Immunol Infect 2010; 43(4):310-316. 5. Cohen-Nahum K, Saidel-Odes L, Riesenberg K, Schlaeffer F, Borer A. Urinary tract infections caused by multi-drug resistant Proteus mirabilis: Risk factors and clinical outcomes. Infection 2010; 38(1):41-46. Cual es la probabilidad de colonización con P. aeruginosa • P. aeruginosa rara vez es un miembro normal de la flora microbiana en humanos. • Sin embargo existen algunas tasas representativas de colonización por sitio especifico : – 0 a 2% para piel – 0 a 3.3% para mucosa nasal , – 0 a 6.6% para garganta y 2.6 a 24% para fecal. – Sin embargo las tasas de colonización pueden exceder 50% durante hospitalización !!! Pollack, M. 1995. Pseudomonas aeruginosa, p. 1820–2003. In G. L. Mandell,R. Dolan, and J. E. Bennett (ed.), Principles and practices of infectiousdiseases. Churchill Livingstone, New York, NY Factores de Riesgo para paciente con P. aeruginosa Categoria Factor de riesgo Fluoroquinolonas Carbapenems Terapia antimicrobiana en los últimos 30 días Uso previo de Penicilinas antibióticos Aminoglicosidos Beta Lactamicos Cefalosporinas de amplio espectro >90 años Edad >79 años Ventilacion mecanica Dispositivo urinario Dispositivos invasivos Sonda nasogastrica Cateter venoso central Estancia en UCI Ubicacion del paciente Traslado de otras unidades o instituciones Estar postrado en cama Inmunodeficiencias severas Antecedentes medicos Haber recivido tratamiento con vasoactivos OR Ref 11.0 7.8 3.7 3.1 2.7 2.5 2.1 5.4 4.5 27.0 6.8 5.3 3.8 17.0 11.1 3.4 * 4.0 6 6 9 8 8 7 8 9 7 8 9 7 8 8 8 8 9 8 * A los pacientes con inmunodeficiencias severas se les administra empíricamente tratamiento antipseudomonas por En resumen para P. aeruginosa: • El uso de antibióticos con actividad anti-Pseudomonas es un factor de riesgo elevado, junto con estar en la UCI y haber tenido algún procedimiento asociado al cuidado en UCI (Ventilación mecánica, sonda vesical, catéter venoso, sonda nasogástrica). • Si bien la edad, es un factor también asociado, se sugiere no tomarlo en forma aislada, sino que requiera la edad más alguno de los otros factores antes mencionados. Referencias • 6. Pena C, Guzman A, Suarez C, Dominguez MA, Tubau F, Pujol M et al. Effects of carbapenem exposure on the risk for digestive tract carriage of intensive care unit-endemic carbapenem-resistant Pseudomonas aeruginosa strains in critically ill patients. Antimicrob Agents Chemother 2007; 51(6):1967-1971. • 7. Defez C, Fabbro-Peray P, Bouziges N, Gouby A, Mahamat A, Daures JP et al. Risk factors for multidrug-resistant Pseudomonas aeruginosa nosocomial infection. J Hosp Infect 2004; 57(3):209-216. • 8. Aloush V, Navon-Venezia S, Seigman-Igra Y, Cabili S, Carmeli Y. Multidrug-resistant Pseudomonas aeruginosa: risk factors and clinical impact. Antimicrob Agents Chemother 2006; 50(1):43-48. • 9. Schechner V, Nobre V, Kaye KS, Leshno M, Giladi M, Rohner P et al. Gram-negative bacteremia upon hospital admission: when should Pseudomonas aeruginosa be suspected? Clin Infect Dis 2009; 48(5):580-586. Selección adecuada del antibiótico estará basada en: 1. 2. 3. 4. 5. Epidemiologia local Estratificación de la infección Mecanismos de resistencia De-escalonamiento Costo tratamiento/día Fiebre, escalofríos, Signos y sintomas de ITU complicada con/sin dolor en flancos Pielonefritis no complicada aguda NO Alteraciones funcionales o anatómicas Urocultivo Definir si requiere hospitalizar e Iniciar tto de acuerdo a esquema para ITU no complicada Si Urocultivo Hemograma, Creatinina, Bun Electrolitos, PCR Hemocultivos ITU Complicada No FR FR BLEE FR P. aeruginosa Shock Ceftriaxona Ertapenem Cefepime o Pip/taz Carbapenem antiPseudomonas •Mayor 65 años + uno de los siguientes FR para BLEE ( ver tabla ) : •Antec. de tratamientos con quinolonas y/o cefalosporinas. •Hospitalización en los últimos tres meses. •Hemodialisis, sonda urinaria. •Antec. de nutrición parenteral. •Residencia en hogar geriátrico. •Mayor 90 años + uno de los siguientes FR para P.aeruginosa ( ver tabla ) : •Haber recibido ttos. antipseudomona en los últimos 30 días. • Ingreso a UCI • Haber tenido uno de los sgtes dispositivos : V. mecánica, sonda urinaria o catéter venoso central . •Inmunodeficiencias severas. De-escalar con resultado de urocultivo Porque y cuando de-escalonar ? 1)Iniciar con carbapenem en shock séptico o UCI y de- escalonar con estabilidad hemodinámica/ mejoría cuando cultivo sea (+) para Enterobacteriaceae. 2)Iniciar tratamiento antipseudomonas en patologías donde se sospecha P. aeruginosa y con cultivo (+) para Enterobacteriaceae deescalonar a otro antibiótico sin actividad antipseudomonas. De-Escalar (DE), una nueva estrategia en el tratamiento de infecciones por Enterobacteriaceae multiresistente (MDRE) en la unidad de cuidados intensivos (ICU) • Métodos: • Estudio prospectivo descriptivo de 2 años de DE a ETP en la UCI de un hospital de tercer nivel. • Se incluyeron todos los pacientes adultos que recibieron antibióticos antipseudomonas empíricamente y que fueron DE a ETP después de un cultivo positivo para una MDRE. Poster at the 51sth Interscience Conference on Antimicrobial Agents and Chemotherapy, Chicago 2011. De-Escalar (DE), una nueva estrategia en el tratamiento de infecciones por Enterobacteriaceae multiresistente (MDRE) en la unidad de cuidados intensivos (ICU) • Resultados: – 39 adultos cumplían los criterios de inclusión – Edad promedio 64 años (26-89) – Estancia promedio en UCI 13 días (2-32) – 49% con APACHE II > 15. De-Escalar (DE), una nueva estrategia en el tratamiento de infecciones por Enterobacteriaceae multiresistente (MDRE) en la unidad de cuidados intensivos (ICU) • Diagnósticos incluían: – – – – – IIA (23%) ITU (33%) bacteremia (28%) infección de tejidos blandos (8% otros (8%). • Terapia empírica variaba entre los pacientes e incluía: – – – – Meropenem (36%) Cefepime (33%) Piperacilina/Tazobactam (21%) Doripenem (10%) De-Escalar (DE), una nueva estrategia en el tratamiento de infecciones por Enterobacteriaceae multiresistente (MDRE) en la unidad de cuidados intensivos (ICU) • Resultados: Todos los pacientes a excepción de 2, tuvieron desenlaces exitosos después de 7 días de terapia con ETP, evidenciado por el criterio medico y por una reducción en los niveles de PCR (p<0.001). • Los dos paciente que murieron se encontraban inmunosuprimidos y tenían un APACHE II > 20 antes del inicio del tratamiento. Koomanachai P, Bulik CC, Kuti JL, Nicolau DP. Pharmacodynamic modeling of intravenous antibiotics against gram-negative bacteria collected in the United States Clin Ther. 2010 Apr;32(4):766-79. Selección adecuada del antibiótico estará basada en: 1. 2. 3. 4. 5. Epidemiologia local Estratificación de la infección Mecanismos de resistencia De-escalonamiento Costo tratamiento/día Costos • La implementación de una terapia de deescalar a Ertapenem representó una reducción en los costos asociados a terapia antibiótica en promedio de US $1287 (58.5%) por paciente (p<0.001) Poster at the 51sth Interscience Conference on Antimicrobial Agents and Chemotherapy, Chicago 2011.