Epidemiologia: De acuerdo con recientes investigaciones el
Anuncio

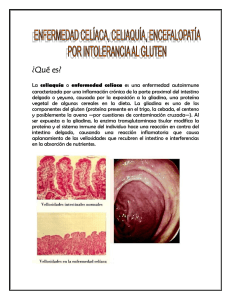
Facultad de Medicina y Enfermería Escuela de Medicina Sede Puerto Montt Integrantes: Andrea Aránguiz Yamilet Oliva Iván Vergara Curso: BCM II Docente: Dr. Leonardo Maggi Fecha Entrega: 31/08/2010 Vocabulario Anticuerpo Anti-Endomisio: Representados por IgA endomisial. En el 100% de pacientes que presenten atrofia intestinal, poseen anticuerpos anti-endomisio positivos. Es positivo un titulo superior a 1:5 con técnica de inmunofluorescencia indirecta (IFI). Anticuerpo Anti-Transglutaminasa tisular: Pertenece a una familia dependiente de calcio, catalizan la formación de enlaces cruzados, las proteínas se encuentra distribuidas por todo el organismo asociadas a fibras del músculo liso y células endoteliales del tejido conectivo. Interviene en mecanismos de ensamblaje de la matriz extracelular y de reparación de los tejidos. Caracterizada como el principal autoantígenos endomisial en los pacientes celiacos. Biopsia: extracción de una pequeña pieza de tejido vivo de un órgano u otro parte del cuerpo, mediante el examen microscópico, confirmar o establecer un dg, estimar un pronostico, o seguir el curso de una enfermedad. 2. El tejido cortado para examen. Carotinemia: presencia de concentraciones elevadas de caroteno en la sangre que dan lugar a un aspecto amarillento anómalo del plasma y de la piel. Hemograma: Es el examen que mas datos nos puede aportar y su utilidad estará en relación directa con los conocimientos hematológicos de quien lo interpreta, pues ofrece complejos y variados datos. Usualmente comprende el estudio de los siguientes parámetros, por medios manuales, automáticos y automatizado. - Numero de eritrocitos por mm3: La cifra es elevada (5 millones por mm3 en promedio). - Hematocrito: Hombre: 40-52% Mujer: 38-48% - Hemoglobina: Hombre: 13.5-17.0 g/d Mujer: - Indices hematológicos: Sirven para clasificar las anemias. El volumen 12.0-15.0 g/dL corpuscular representa el tamaño del glóbulo rojo, promedio es 92 micras cúbicas. - Leucocitos por µl: La cifra normal fluctúa entre 5.000 y 10.000 por µl. - Formula leucocitaria: Leucocito Neutrófilos que se encuentran en el adulto en una proporción de 63% y solamente un 2% máximo de neutrófilos falciformes. Leucocitos Eosinófilos con una proporción normal 1 a 3% Leucocitos Basófilos en proporción de 1x200. Linfocitos abundan en lactantes en proporción de 60 a 65%, en adultos es un 28% Monocitos en un 3a5%. Test de grasa en deposiciones: Examen para detectar concentraciones elevadas de grasa en las deposiciones. Empleando el método de dosificación húmedo los valores normales son: Grasa normal: 17,5 Grasa neutra: 7,3 Acidos graso libres: 5,6 Acidos grasos combinados: 4,6 Síndrome Intestino Irritable: Trastorno digestivo caracterizado por alteración de los hábitos intestinales y dolor abdominal en ausencia de anormalidades estructurales detectables. No existen marcadores diagnósticos para esta enfermedad, por lo que su diagnostico se basa en la presencia clínica. Predominio en mujeres. Los síntomas aparecen y desaparecen con el paso del tiempo. La gravedad de los síntomas varía y puede alterar de manera significativa la calidad de vida. Criterios diagnósticos para SII: Dolor o molestias abdominales recurrentes por al menos 3 días por mes, en los últimos 3 meses, relacionados con dos o más de los siguientes datos: 1.- Mejoría con la defecación 2.- Inicio relacionado con cambios en la frecuencia de las evacuaciones 3.- Inicio relacionado con cambio en la forma de las heces (aspecto) El estrés, la ansiedad emocional o la depresión suelen empeorar los síntomas. Cada paciente, a su vez, puede presentar hipersensibilidad a alimentos variados dependiendo del sujeto. Aunque se ha establecido que los principales grupos de alimentos a los que los pacientes de intestino irritable son hipersensibles son el gluten del trigo, cebada, centeno, levaduras, leche, grasas y alcohol. Blastocystis Hominis: protozoo que causa cuadros diarreicos. Para su diagnóstico en materia fecal se reconocen las formas vacuolar, avacuolar, granular y quística Blastocystis Clasificación científica Familia: Blastocystidae Género: Blastocystis Nombre binomial Blastocystis hominis Epidemiologia: De acuerdo con recientes investigaciones el Blastocystis se transmite entre animales y humanos por la ingestión de quistes, presentes en aguas o alimentos contaminados con materia fecal procedente de un portador. El parásito puede proliferar en el organismo humano por años sin causar síntomas, pero debido a que segrega proteasas, puede provocar como reacción, la producción de anticuerpos y el consecuente desencadenamiento de diarreas, náuseas, anorexia y espasmos abdominales. No es capaz de invadir la mucosa intestinal. Actualmente se trata con metronidazol u otros nitroimidazoles (tinidazol). Además de infectar a los humanos, pueden infestar animales de granja, aves, roedores, reptiles, peces, cerdos, monos e incluso cucarachas Enfermedad celiaca. Conocida también como esprúe celíaco y enteropatía por hipersensibilidad al gluten, es un proceso crónico en el que existe una lesión característica de la mucosa del intestino delgado, con afectación de la absorción de nutrientes, que mejora al eliminar de la dieta las gliadinas del trigo y proteínas similares de los cereales. La enfermedad celiaca afecta sobre todo a individuos de raza blanca, y es rara o inexistente entre los africanos, los japoneses y los chinos. Patogenia. El trastorno fundamental es la sensibilidad al gluten, un componente proteínico soluble en alcohol e insoluble en agua, del trigo y de los cereales íntimamente relacionados (avena, cebada y centeno). El dato característico de esta enfermedad es una reacción inflamatoria crónica mediada por las células T, con un componente autoinmune, que probablemente se desarrolla a consecuencia de la pérdida de tolerancia al gluten. La interrelación de factores genéticos predisponentes, respuesta inmune del huésped y factores medio ambientales, ocupa un lugar central en la patogenia de la enfermedad. La mucosa del intestino delgado, cuando es expuesta al gluten acumula células T CD8+ intraepiteliales y gran número de células T CD4+ en a lamina propia, que están sensibilizadas a la gliadina. Los epítopos reconocidos se limitan a los residuos 57-77 de la gliadina. Se sabe desde hace tiempo que los antecedentes familiares tienen importancia en la celiaquía. Casi todos los individuos con enfermedad comparten el complejo mayor de histocompatibilidad clase II HLA-DQ2 o el haplotipo HLA-DQ8. Se ha propuesto que la gliadina es desaminada por la enzima trasglutaminasa, y que los péptidos de la gliadina desaminada se unen a DQ2 o DQ8. El reconocimiento de esos péptidos por las células T CD4+ conduce a secreción d interferón gamma, que daña a la pared intestinal. Aunque esta hipótesis es atractiva, sus elementos claves aun no se han demostrado. Tampoco esta claro el modo como las células T CD8+ se acumulan en el epitelio. Esas células no reconocen la gliadina, pero parecen responder a las moléculas inducidas por el estrés en las células epiteliales. Las células epiteliales segregan grandes cantidades de IL-15, que activa a las células T CD8+ y aumenta el riesgo del desarrollo de un linfoma. Síntomas. Forma típica: Forma Atípica: - Diarrea. - Diarrea. - Debilidad. - Debilidad. - Perdida de peso. - Perdida de peso. - Flatulencia. - Flatulencia. - Distensión abdominal. - Anemia por deficiencia de hierro. - Esteatorrea. - Osteopenia. - Anemia (por deficiencia de vitaminas). - Artralgias. - Deficiencia de vitaminas. - Intolerancia a la lactosa. Síntomas extraintestinales Dermatitis herpetiforme (lesión cutánea vesicante). Trastornos neurológicos (ejemplo: depresión). Detección de anticuerpos (antitransglutaminasa, antiendomisio y antigliadina). Diagnóstico. Documentación clínica de la mala absorción. Biopsia del intestino delgado. Pruebas serológicas incluyen detección de anticuerpos. contra la transglutaminasa tisular, gliadina y endomisio. Tratamiento. Eliminación del gluten de la dieta. Helicobacter Pylori El Helicobacter Pylori (HP) es una bacteria microaerófila, espiroidea, catalasa, ureasa y oxidasa positiva, que coloniza primariamente la mucosa gástrica antral, donde produce una inflamación aguda y crónica, denominada gastritis crónica activa. La infección se ha asociado también a úlcera péptica, adenocarcinoma y linfoma gástrico. La asociación entre úlcera duodenal (UD) y HP ha sido repetidamente confirmada en estudios provenientes de todo el mundo. Aunque en un nivel un poco menor, la misma asociación existe en el caso de la úlcera gástrica (UG). Diagnóstico de infección por H. Pylori. a) Exámenes no invasivos Serología: Mediante ELISA se detectan IgG o IgA dirigidas contra varios antígenos específicos del HP. La sensibilidad y especificidad superan el 90% (8,22). Pruebas en aire espirado (Breath Tests): Utilizando 13C, no radiactivo pero mucho más caro, o 14C, que puede ser leído en un contador de centelleo, se detecta la descomposición, por la ureasa del HP, de la urea marcada ingerida por el paciente. b) Exámenes invasivos Prueba de ureasa en biopsia antral. Constituye el método más rápido y práctico para detectar el HP en pacientes sometidos a endoscopia. La ureasa producida por el HP convierte la urea a amonio y CO2, lo que modifica el pH del medio y provoca el cambio de color que define la reacción como positiva. Histopatología. Aún constituye el goldstandard para definir la presencia o ausencia de HP, tiñendo la muestra con Giemsa. Debe tomarse la muestra en mucosa antral sana, evitando la región prepilórica y la parte más baja de la curva menor. Dentro de estos exámenes se puede ver el rol que cumple la ureasa por parte de H. Pylori para el diagnóstico. En el caso clínico, el médico general supuso que al dar ureasa positiva en los exámenes pedidos por el médico internista, administró fármacos para erradicar H. Pylori, los cuales consisten en: Erradicación de H. Pylori: - Antibióticos: Amoxicilina Claritromicina Metronidazol, tinidazol - Antiulcerosos: - Bismuto - Inhibidor de la bomba de protones (Ej. Omeprazol). - Antagonista H2 Colitis Seudomembranosa Por otra parte, en forma post mortem se recibe del laboratorio un test de toxina A de Clostridium difficile positivo. Las especies de Clostridium son bacilos grampositivos que crecen en condiciones anaerobias, siendo C. difficile un comensal normal del intestino, el cual desplaza a la otra flora intestinal en pacientes tratados con antibióticos, libera toxinas y produce colitis seudomembranosa. La toxina A es una enterotoxina que estimula la producción de quimiocinas y atrae así a los leucocitos, destacando que las toxinas A y B no están presentes en las cepas de C. difficile no patógenas. Esta forma de colitis se caracteriza por la formación de una capa adherente de células inflamatorias y detritos sobre los sitios de lesión de la mucosa, lo que se conoce como seudomembranosa. La enfermedad es más frecuente en pacientes sin un fondo de enfermedad intestinal crónica que están recibiendo un ciclo de antibióticos de amplio espectro, dentro de los cuales se han implicado casi todos los fármacos antibacterianos. Macroscópicamente: Placas de fibrina amarilla y restos inflamatorios adheridos a una mucosa del colon. Microscópicamente: Erosión superficial de la mucosa y una seudomembrana adherida de fibrina, moco y restos inflamatorios. La lámina propia posee un infiltrado denso de neutrófilos. Por lo tanto, y en conclusión, luego de la explicación de ambas patologías, surge la hipótesis de que el esquema de tratamiento que el médico general utilizó pudo haber influido en la flora comensal del intestino y facilitar la acción de desplazamiento de la misma por C. difficile, ya que se presume que las cepas formadoras de toxina proliferan después de la alteración de la flora intestinal normal, y finalmente dar paso a la colitis seudomembranosa.