CAPITULO 1. PROPIEDADES DE LAS SOLUCIONES DILUIDAS
Anuncio
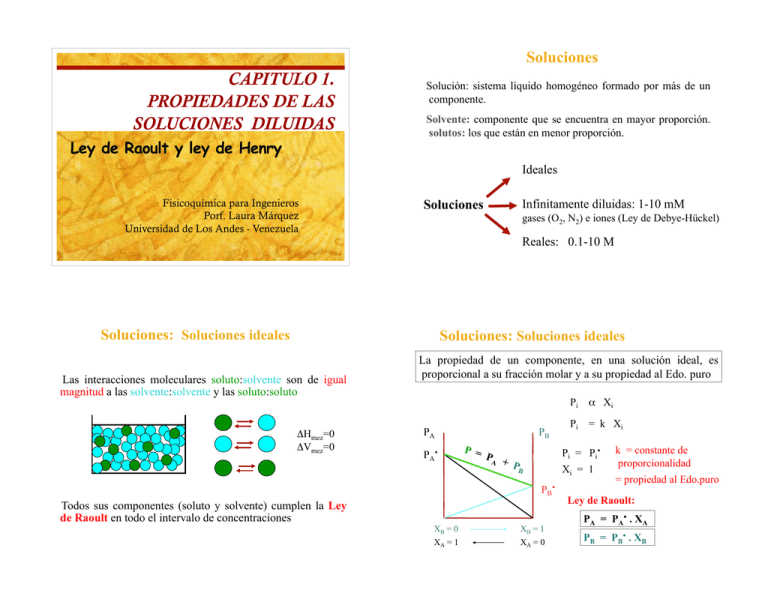
Soluciones CAPITULO 1. PROPIEDADES DE LAS SOLUCIONES DILUIDAS Solución: sistema líquido homogéneo formado por más de un componente. Solvente: componente que se encuentra en mayor proporción. solutos: los que están en menor proporción. Ideales Fisicoquímica para Ingenieros Porf. Laura Márquez Universidad de Los Andes - Venezuela Soluciones Infinitamente diluidas: 1-10 mM gases (O2, N2) e iones (Ley de Debye-Hückel) Reales: 0.1-10 M Soluciones: Soluciones ideales Soluciones: Soluciones ideales Las interacciones moleculares soluto:solvente son de igual magnitud a las solvente:solvente y las soluto:soluto !Hmez=0 !Vmez=0 La propiedad de un componente, en una solución ideal, es proporcional a su fracción molar y a su propiedad al Edo. puro Pi " Xi PA P A• PB P = PA + PB Pi = Pi• Xi = 1 PB• Todos sus componentes (soluto y solvente) cumplen la Ley de Raoult en todo el intervalo de concentraciones XB = 0 XA = 1 Pi = k Xi XB = 1 XA = 0 k = constante de proporcionalidad = propiedad al Edo.puro Ley de Raoult: PA = PA• . XA PB = PB• . XB Soluciones Cálculo de µ para soluto y solvente de soluciones ideales A (v) µi (solución) = µi µi (solución) = µº + RT ln Pi Según Raoult A (l) (vapor) Pi = Pi• Soluciones Reales y Soluciones infinitamente diluidas PA . Xi PA PB (solución) = µº + RT ln (Pi• . Xi) µi (solución) = µº + RT ln Pi• + RT ln Xi A una P y T, la Pi• es un valor definido µi (solución) = µi• + RT ln Xi XB = 0 XB = 1 XA = 1 XA = 0 PA PB P = PA + PB Exotérnica PA • XB = 1 XA = 0 PB PA PB ! PB• . XB P A• PB m = kH P = PA + PB Solvente # Ley de Raoult PB• PB• PB• XB = 0 XA = 1 PA ! PA• . XA Soluciones infinitamente diluidas > Endotérnica ! propiedad del puro Soluciones < • Pi = k Xi PB• Soluciones Reales PA P = PA + PB • Pi " Xi k = constante de proporcionalidad µi Permite calcular el µsoluto y el µsolvente, si la solución se comporta como solución ideal Soluciones XB = 0 XB = 1 XA = 1 XA = 0 XB = 0 XB = 1 XA = 1 XA = 0 A: solvente B: soluto XA 1 PA = PA• . XA Soluto Volátil # Ley de Henry XB 1 PB = kH . XB Solubilidad de Gases en líquidos Equivalencia entre HHenry - " Soluciones infinitamente diluidas – Ley de Henry Solubilidad en líquidos de Gases poco solubles Coeficiente Volgas (cm 3 ) " = de Bunsen VolSTE (cm 3 ) Soluto Volátil # Ley de Henry XB 1 PB = kH . XB Volgas = n gas * 3 "= Volgas (cm ) VolSTE (cm 3 ) Solubilizado a condiciones de: Pgas= 1atm y Temperatura de 25ºC El volumen del gas es medido a condiciones estandar P = 1 atm y T = 0ºC ! VolSTE = "= ! Xgas=Ppas / kH_gas R * T0 P0 (medidos _1atm _ 0ºC ) Vol! gas = n gas(mol Coeficiente de BUNSEN (")$ Ley de Henry gas ) * 22413,8(cm 3 gas X gas = n gas n gas = (n gas + n STE ) n STE / mol gas ) ngas/nSTE=Ppas / kH_gas n STE (mol STE ) * PM STE (g STE / molSTE ) " STE (g STE / cmSTE 3 ) ! n gas 22413,8 * # STE * n STE PM STE "= P( parcial _ gas) # STE * * 22413,8 K( Henry _ gas) PM STE ! ! Solubilidad de Gases en líquidos Solubilidad de Gases - Influencia de la Presión Equivalencia entre HHenry - " Presiones Moderadas coportamiento Lineal P( parcial _ gas) # STE "= * * 22413,8 K( Henry _ gas) PM STE ! α (cm3gas/cm3STE*atm) GAS KH (atm) KH (Torr) CO2 1644,7 1,25 * 106 CH4 41348,1 3,14 * 107 0,0300 O2 43421,1 3,30 * 107 0,0283 H2 70263,1 5,43 * 107 0,0175 N2 85657,9 6,51 * 107 0,0143 He 142579,5 1,08 * 108 0,0087 Solubilidad de diversos gases en agua (Atkins) Solubilidad = Xgas=Pgas/KHenry Presiones Altas coportamiento NO Lineal Xgas Xgas H2 O2 N2 N2 He Pparcial del gas 50 100 atm Solubilidad de diversos gases en agua (Atkins) Pparcial del gas 200 400 atm Solubilidad en agua (Levine Vol.1) Solubilidad de Gases _ Influencia de la Temperatura KHenrry_gas (GPa) en Agua Bajas Temperaturas ( 0 - 50ºC ) O2 Relación MUY simplificada Aumento lineal de KH-gas (disminución de Xgas) para algunos gases en Agua 1/KHenrry_gasҫXgas O2 K H (T1) T1 " T 2 = = K H (T 2) T2 " T1 N2 T (ºC) 200 300 Constantes de la Ley de Henry en agua (Levine Vol.1) Solubilidad de Gases _ Influencia de la Temperatura Bajas Temperaturas ( 0 - 100ºC ) Relación más ajustada Sander, (1999) K H (gas _ agua ) = K º H (gas _ agua ) *exp[" "d lnK H (gas _ agua ) #H solu = d(1/T) R #H solu 1 1 ( " )] R T Tº KH en (Molar/atm) T en (ºK) Una recopilación de "d lnK H (gas _ agua ) = #H solu R Puede encontrarse en: d(1/T) http://www.mpch-mainz.mpg.de/~sander/res/henry.html ! ! "=36,885 KH (bar) T (ºC) Solutos τgas αgas Helio 131,42 41,824 Neón 142,50 41,667 Nitrógeno 162,02 41,712 Oxígeno 168,87 40,622 Argón 168,87 40,404 Variación de la Constantes de la Ley de Henry en agua (Prausnitz) ! ! Relación más ajustada Benson y Krause (1976) $ gas $ gas 2 lnK H (gas _ agua ) = " gas (1 # ) # %(1 # ) + ln1,01325 T T Bajas Temperaturas ( 0 - 50ºC ) N2 100 Solubilidad de Gases _ Influencia de la Temperatura Sander, R. Modeling atmospheric chemistry: Interactions between gas-phase species and liquid cloud/aerosol particles. Surv. Geophys., 1999.