Constantes de acidez y basicidad
Anuncio
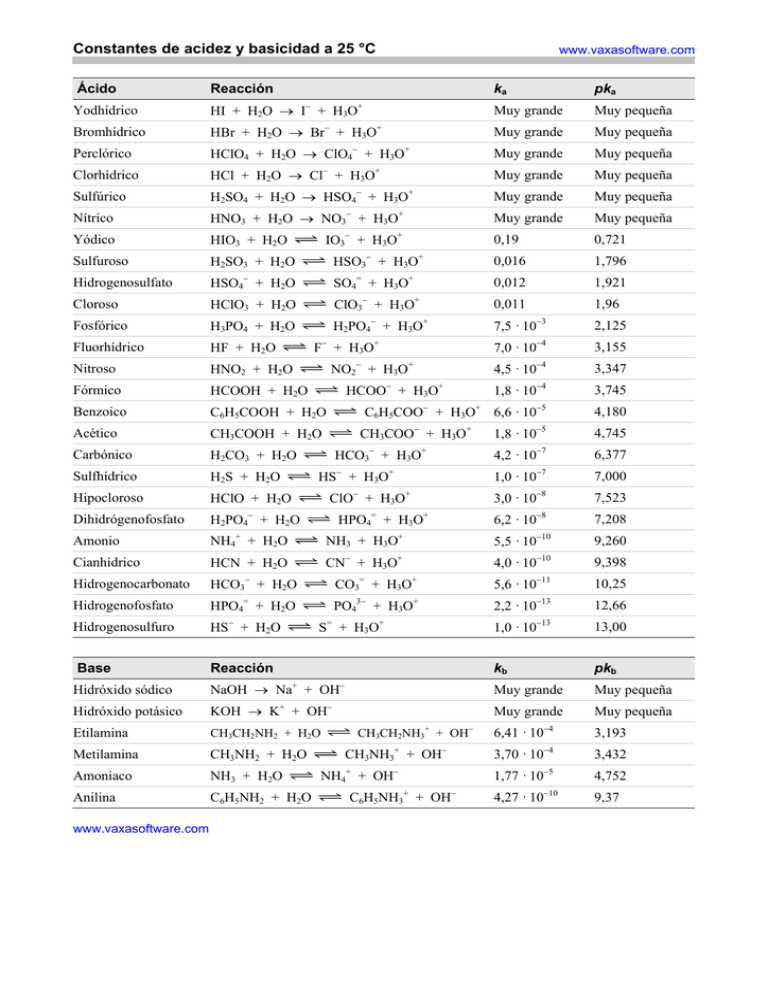
Constantes de acidez y basicidad a 25 °C Ácido Reacción Yodhídrico HI + H2O → I− + H3O+ − www.vaxasoftware.com ka pka Muy grande Muy pequeña Bromhídrico HBr + H2O → Br + H3O Muy grande Muy pequeña Perclórico HClO4 + H2O → ClO4− + H3O+ Muy grande Muy pequeña Muy grande Muy pequeña + − Clorhídrico HCl + H2O → Cl + H3O Sulfúrico H2SO4 + H2O → HSO4− + H3O+ Nítrico + Muy grande Muy pequeña − + Muy grande Muy pequeña − + 0,19 0,721 0,016 1,796 0,012 1,921 HNO3 + H2O → NO3 + H3O Yódico HIO3 + H2O Sulfuroso H2SO3 + H2O IO3 + H3O HSO3− + H3O+ − = + Hidrogenosulfato HSO4 + H2O SO4 + H3O Cloroso HClO3 + H2O ClO3− + H3O+ Fosfórico H3PO4 + H2O Fluorhídrico HF + H2O Nitroso Fórmico Benzoico − H2PO4 + H3O 7,5 · 10 F− + H3O+ HNO2 + H2O Carbónico H2CO3 + H2O Hipocloroso HClO + H2O + HCOO + H3O CH3COOH + H2O H2S + H2O 4,5 · 10 − 1,8 · 10 − C6H5COOH + H2O Sulfhídrico + NO2 + H3O HCOOH + H2O + C6H5COO + H3O − + CH3COO + H3O HCO3− + H3O+ − + H2PO4 + H2O Amonio NH4+ + H2O + HPO4 + H3O 6,2 · 10 + CN + H3O − = −5 −5 −7 −8 5,5 · 10−10 NH3 + H3O+ HCN + H2O −4 3,0 · 10−8 = − 1,8 · 10 1,0 · 10 ClO− + H3O+ Dihidrógenofosfato 6,6 · 10 −4 4,2 · 10−7 HS + H3O − 1,96 −3 7,0 · 10−4 − Acético Cianhídrico 0,011 + 4,0 · 10 + −10 −11 Hidrogenocarbonato HCO3 + H2O CO3 + H3O 5,6 · 10 Hidrogenofosfato HPO4= + H2O PO43− + H3O+ 2,2 · 10−13 − = + Hidrogenosulfuro HS + H2O Base Reacción Hidróxido sódico NaOH → Na + OH Hidróxido potásico KOH → K + OH Etilamina S + H3O CH3CH2NH2 + H2O Amoniaco NH3 + H2O www.vaxasoftware.com − + CH3NH2 + H2O Anilina − + Metilamina C6H5NH2 + H2O 1,0 · 10 CH3CH2NH3+ + OH− − + CH3NH3 + OH −13 − C6H5NH3 + OH 3,347 3,745 4,180 4,745 6,377 7,000 7,523 7,208 9,260 9,398 10,25 12,66 13,00 pkb Muy grande Muy pequeña Muy grande Muy pequeña 6,41 · 10 −4 −4 1,77 · 10−5 + 3,155 kb 3,70 · 10 NH4+ + OH− 2,125 4,27 · 10 −10 3,193 3,432 4,752 9,37