FICHA DE TRABAJO: El movimiento molecular
Anuncio
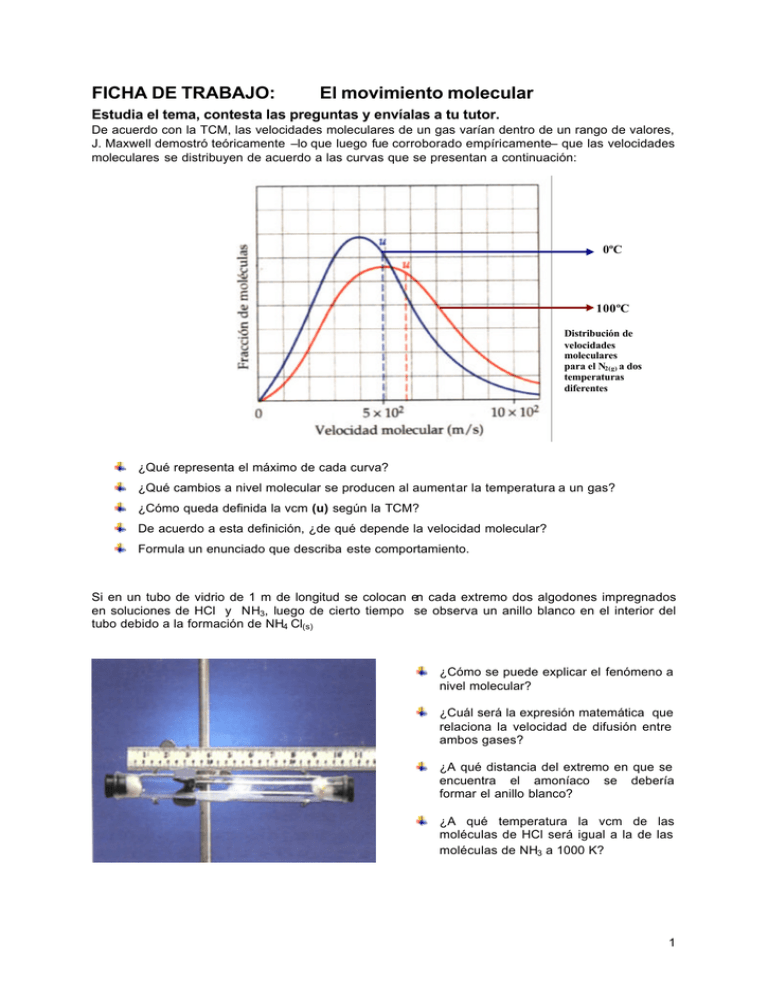
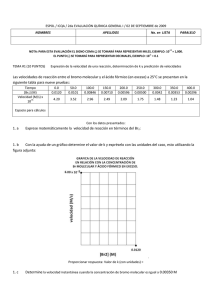
FICHA DE TRABAJO: El movimiento molecular Estudia el tema, contesta las preguntas y envíalas a tu tutor. De acuerdo con la TCM, las velocidades moleculares de un gas varían dentro de un rango de valores, J. Maxwell demostró teóricamente –lo que luego fue corroborado empíricamente– que las velocidades moleculares se distribuyen de acuerdo a las curvas que se presentan a continuación: 0ºC 100ºC Distribución de velocidades moleculares para el N2(g) a dos temperaturas diferentes ¿Qué representa el máximo de cada curva? ¿Qué cambios a nivel molecular se producen al aumentar la temperatura a un gas? ¿Cómo queda definida la vcm (u) según la TCM? De acuerdo a esta definición, ¿de qué depende la velocidad molecular? Formula un enunciado que describa este comportamiento. Si en un tubo de vidrio de 1 m de longitud se colocan en cada extremo dos algodones impregnados en soluciones de HCl y NH3, luego de cierto tiempo se observa un anillo blanco en el interior del tubo debido a la formación de NH4 Cl(s) ¿Cómo se puede explicar el fenómeno a nivel molecular? ¿Cuál será la expresión matemática que relaciona la velocidad de difusión entre ambos gases? ¿A qué distancia del extremo en que se encuentra el amoníaco se debería formar el anillo blanco? ¿A qué temperatura la vcm de las moléculas de HCl será igual a la de las moléculas de NH3 a 1000 K? 1