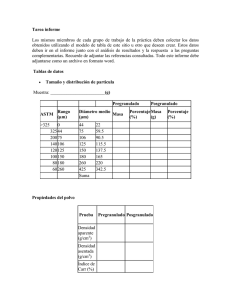
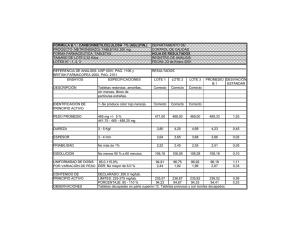
FORMAS FARMACÉUTICAS SÓLIDAS TABLETAS PARTE IV
Anuncio

FORMAS FARMACÉUTICAS SÓLIDAS TABLETAS PARTE IV QFB. Oscar Arturo Manzano Yescas QFB. Marco Tulio Morales Delgado Grupo Gylsa, S.A. de C.V. Tel 56114565 INTRODUCCIÓN Las tabletas son formas farmacéuticas sólidas de dosificación unitaria, obtenidas por compresión mecánica de granulados o de mezclas de polvos con uno o varios principios activos, con la adición, en la mayoría de los casos, de diversos excipientes. Las tabletas constituyen en la actualidad la forma farmacéutica sólida más administrada por vía oral. Contienen uno o más principios activos y diversos excipientes, llamados en ocasiones coadyuvantes, y se obtienen por compresión de la mezcla resultante de unos y otros. La forma, el tamaño y el peso de los comprimidos pueden variar sensiblemente de unos a otros. Por lo general, el tamaño se sitúa entre 5 y 17 mm; el peso, entre 0.1 y 1.5 g, y la forma puede ser redonda, oblonga, biconvexa, ovoide, etc. (Fig.1) Sobre la superficie pueden llevar una inscripción y una ranura para fraccionarlos y facilitar así el ajuste posológico a las necesidades individuales. 1 Figura 1. Diversas Formas y Tamaños de Tabletas CLASIFICACIÓN Podemos clasificar a las tabletas de administración oral en tres grupos: 1. Tabletas no recubiertas. 2. Tabletas recubiertas a) Con recubrimiento de azúcar. b) Con recubrimiento de película fina. 3. Tabletas especiales a) Efervescentes b) De disolución en la cavidad bucal: tabletas bucales y sublinguales c) Con recubrimiento gastrorresistente o entérico d) De capas múltiples e) De liberación controlada o modificada, que puede ser sostenida, retardada o prolongada , lenta, rápida o acelerada, o pulsátil f) Masticables. CARACTERÍSTICAS DE LAS TABLETAS En la tabla 1, se enlistan algunas de las ventajas y desventajas de esta forma farmacéutica Tabla 1. Ventajas y Desventajas de las Tabletas 2 Ventajas Desventajas Dosificación Exacta Pueden ser confundidas con dulces. Fácil de Administrar Formulación limitada en algunas ocasiones: Grandes dosis no pueden ser formuladas en tabletas. Aceptado por los pacientes (Conformidad) No pueden ser administradas en pacientes que presenten vomito o que se encuentren inconscientes. Pueden controlar la actividad del activo. Algunos pacientes pueden tener dificultad de deglución. Estabilidad Problemas en la uniformidad de contenido (exactitud y precisión en la uniformidad de contenido) para dosis bajas del fármaco. Manufactura económica Biodisponibilidad comprometida (baja solubilidad del fármaco; mal formulación). OBJETIVOS DE LA FORMULACIÓN DE TABLETAS Preformulación El objetivo de los estudios de preformulación es desarrollar un portafolio de información detallada sobre el fármaco que sirva como un sistema de parámetros contra los cuales la formulación pueda ser realizada. En las investigaciones de la preformulación se diseñan e identifican las propiedades fisicoquímicas del principio activo y excipientes y como estos, pueden influir en el diseño de la formulación, método de manufactura, y propiedades farmacocinéticas y biofarmacéuticas. Identidad y Pureza El estudio de cualquier activo debe comenzar con la determinación de identidad y pureza. Tales pruebas son necesarias para identificar degradantes, contaminantes y pueden incluirse pruebas organolépticas como color, olor y sabor. Otras pruebas aparte de la valoración que pueden ayudar a determinar la pureza de los compuestos, son: Punto de fusión, rotación especifica, pH, metales pesados, residuo de ignición, etc. Las impurezas pueden ocasionalmente afectar la estabilidad 3 Propiedades del Cristal y Polimorfismo Muchas sustancias activas aparecen en más de un forma polimorfa. La forma es determinada por ciertas condiciones durante el paso de cristalización (Fig. 2). Ocasionalmente los principios activos son precipitados de una manera tal que las moléculas no se organizan en ningún patrón de sistema, dando por resultado un polvo amorfo. Es también posible que los sólidos encierren solventes estequiometricamente para formar solvatos. Aunque son químicamente idénticos, las diferentes formas polimorficas de los compuestos están asociadas con diferentes energías libres y por lo tanto poseen diferentes propiedades físicas que pueden impactar significativamente en el funcionamiento del producto. Estas incluyen diferencias en la solubilidad y la velocidad de disolución (afectando la biodisponibilidad), estabilidad del estado sólido (afectando la potencia), características de deformación (afectando la compactibilidad), y el tamaño de partícula y forma (afectando la densidad del polvo y las propiedades de flujo). La forma con la energía más baja es la más estable. La transformación polimórfica puede ocurrir durante el proceso farmacéutico, por ejemplo en la reducción del tamaño de partícula, en la granulación húmeda, en el secado e igualmente durante el proceso de compactación. Diferentes pruebas son empleadas para determinar las propiedades del cristal incluyendo el análisis térmico diferencial, calorimetría diferencial de barrido, y difracción de rayos X. Figura 2. Cristal de Carbamazepina Obtenida de una Solución Supersaturada. Obtención de polimorfos La obtención de los polimorfos es afectada por los siguientes parámetros. 1. Manipulando adecuadamente los índices de cristalización 2. Naturaleza del disolvente 4 3. Temperatura 4. Velocidad de enfriamiento 5. Agitación 6. Cantidad de disolvente usado 7. Pureza del disolvente Desde el punto de vista biofarmacéutico la importancia del polimorfismo reside en que las distintas formas van a diferir entre si con relación a la solubilidad, forma cristalina, compactación de los polvos, propiedades de flujo, estabilidad, hay que conocer el polimorfismo porque puede ser necesario recurrir a las diferentes formas polimórficas en relación a la estabilidad y biodisponibilidad del medicamento (Fig. 3) Figura 3. Diferentes Formas Polimórficas de la Carbamazepina. Las formas polimórficas metaestables que son más solubles, son más biodisponibles. Al trabajar con una forma polimórfica metaestable hay que tener en cuenta su falta de estabilidad, hay que añadir sustancias a la formulación que aseguren la estabilidad, conocer el origen de la inestabilidad, origen del polimorfo en su forma metaestable para 5 que no se produzcan variaciones durante la formulación, sustancias como la Polivinilpirrolidona (PVP), el ácido algínico o la Carboximetil celulosa (CMC) confieren estabilidad. Si el origen de la inestabilidad es la oxidación habrá que añadir un antioxidante, si es el crecimiento bacteriano un bacteriostático. En los medicamentos distinguiremos entre la apariencia externa y la estructura interna. Según la estructura interna la sustancia puede ser amorfa o cristalina. El aducto molecular se forma en el proceso de cristalización de un medicamento a partir de una disolución. Químicamente son iguales (clatratos, capas y estrías), en los aductos no hay unión estequiométrica con el disolvente, en los aductos se producen variaciones en las propiedades físico químicas. Los polimorfos aparecen con frecuencia en esteroides y barbitúricos. La presencia de aductos influye en la biodisponibilidad y en la estabilidad con comportamientos farmacológicos diferentes. Hábito cristalino; indica la apariencia externa de los cristales que depende de la nucleación del cristal y de el crecimiento cristalino. La cristalización puede ser lenta o rápida; si es rápida y a partir de un gran número de núcleos los cristales que se forman no tienen apariencia externa reconocible; pocos núcleos y crecimiento lento producen cristales perfectamente reconocibles y formas bastante regulares. En la formación de los hábitos intervienen: sobresaturación, condiciones de cristalización (grado de enfriamiento, agitación, presencia de cosolutos o codisolventes), variaciones en las condiciones de cristalización. Las formas cristalinas irregulares también se llaman alotriomorficas. Normalmente los hábitos cristalinos se reconocen visualmente o por microscopía óptica según el tamaño del cristal, hay cristales tubulares, planos, aciculares, en forma de aguja, prismáticos. El no reconocer el hábito cristalino puede llevar a que aparezcan cambios en la biodisponibilidad, solubilidad y velocidad de disolución sin una explicación. Técnicas para la identificación de formas cristalinas. 1.- Microscopía, para manejar esta técnica es necesario tener conocimientos de cristalografía, los polimorfos tienen estructura interna diferente, lo cual influye en las propiedades ópticas. Los cristales tienen formas isotrópicas y anisotrópicas. La termomicroscopía consiste en usar un microscopio polarizante dotado de una platina caliente o fría que permita visualizar la solubilidad de polimorfos, solvatos o clatratos, ya que trabajamos con puntos de fusión diferentes. También pueden identificarse por las diferencias de color frente a los núcleos cruzados. 2.- Infrarojos; proporcionan información sobre la estructura y en particular de las uniones intermoleculares por puentes de hidrógeno. 3.- Rayos X; los difractogramas de rayos X son propios de cada especie cristalina, es uno de los mejores métodos para identificar estructuras cristalinas, se emplea también para ver la cristabilidad; no se obtiene información referente a la estructura química. hay que tener en cuenta que es necesario llevar a cabo un pulverizado previo, y esto puede dar lugar a cambios polimórficos. 6 4.- Métodos térmicos; análisis térmico diferencial, calorimetría diferencial de barrido, análisis gravimétrico térmico. Análisis térmico diferencial. Compara entre la temperatura de la muestra y la del material de referencia, cuando ambas se calientan en un mismo horno común a una velocidad de calentamiento controlada. Los cambios de temperatura se deben a transiciones de entalpía y pueden ser endotérmicos o exotérmicos y suceden durante los cambios físicos o químicos de la sustancia que son detectadas por un método diferencial, desfase entre la muestra y la sustancia de referencia plasmado en un termograma. El método se aplica en fenómenos de solvatación, transiciones polimorficas, observación de mezclas eutecticas, análisis de pureza de sustancias medicamentosas y para conocer estudios de estabilidad del medicamento. Calorimetría diferencial de barrido . Mide la energía necesaria para que la sustancia estudiada y la de referencia se mantengan a la misma temperatura, determinando así la entalpía de fusión. Se detectan polimorfos, pureza de la sustancia y de los posibles polimorfos. Análisis gravimétrico térmico. Determina la perdida de peso en función de la temperatura a velocidad de calentamiento controlado, básicamente cuantitativo. Tamaño de Partícula, Forma y Área superficial. No hay característica quizá más importante en un fármaco que el tamaño de partícula en la determinación funcional de una formulación. Esto es particularmente cierto en los casos donde el fármaco es pobremente soluble. La reducción del tamaño de partícula (micronización) es a menudo utilizada para incrementar la velocidad de disolución. Las partículas pequeñas presentan una gran área superficial por unidad de peso a la disolución media y por lo tanto se disuelve más rápido que las partículas grandes. El tamaño de partícula y el área superficial, son dos de las más importantes propiedades determinantes en la velocidad de solubilidad del fármaco así como la potencia y la biodisponibilidad. Son numerosos los ejemplos de problemas de biodisponibilidad y bioequivalencia debido a un inapropiado tamaño de partícula del fármaco. El tamaño de partícula y la forma del cristal juegan un papel importante en la homogeneidad en la mezcla de polvos y la fuerza del mezclado. La segregación durante el proceso de compactación tiene un efecto significativo en el contenido de uniformidad en el producto final. El tamaño de partícula puede también afectar la estabilidad del principio activo. El área superficial es crítica para la interacción de los excipientes en las tabletas y pueden afectar grandemente la estabilidad. Los métodos para determinar el tamaño de partícula y la forma incluyen la microscopia óptica, la microscopia electrónica de barrido, análisis de malla, y varios equipos electrónicos de contadores de partículas. Otros métodos están disponibles para medir el área superficial incluyendo permeabilidad del aire y varias técnicas de adsorción de gases. 7 Características Reologicas del Polvo Las características reologicas del polvo son extremadamente importantes en los procesos farmacéuticos El conocimiento real de la densidad del polvo del principio activo así como de los excipientes es extremadamente útil: • Proveen perspectivas en cuanto al tamaño final de la tableta y el tamaño y tipo de equipo necesario para el proceso. • Anticipan problemas en la mezcla física del polvo y de la homogenidad del granel y producto final por que las diferencias significativas en la densidad real pueden resultar en segregación. • Anticipan problemas en las propiedades de flujo, como las propiedades que son afectadas por la densidad. • Identifican diferencias en lotes y materias primas de diferentes proveedores por las diferentes formas polimorficas al exhibir diferentes densidades reales. Una comparación de la densidad real y densidad aparente y pueden dar información de la porosidad total, porosidad interparticular e intraparticular. El contenido de humedad y la higroscopicidad de los excipientes es particularmente importante, durante el proceso del producto así como del producto final, la estabilidad puede ser afectada. La higroscopicidad, los isotermas de humedad, el contenido de humedad en equilibrio pueden ser determinados por análisis termogravimetricos y métodos de titulación por Kart-Fischer Para la evaluación de las propiedades de flujo son utilizados los siguientes métodos. • • • • • Angulo de Reposo. Densidad Aparente y Relativa. Índice de Carr. Velocidad de flujo. Observación directa de variación de peso durante la corrida de tableteado. La última meta del análisis de flujo es identificar el polvo y la mezcla de polvos para proveer la menor variación de peso en el producto final Solubilidad y Permeabilidad En algunos casos, la velocidad de disolución en el fluido gastrointestinal es el paso límite en la absorción. Los requerimientos de bioequivalencia establecidos por la FDA 8 define la baja solubilidad como “ …<5mg/mL en agua, y la lenta velocidad de disolución debe ser <50% en 30 minutos”. Sin embargo la solubilidad del fármaco debe ser considerada junto con la dosis; es decir, incluso un fármaco poco soluble que tiene una dosis terapéutica suficientemente pequeña puede disolverse totalmente bajo condiciones fisiológicas El Sistema de Clasificación Biofarmacéutica (SCB) es un marco científico para clasificar los principios activos en base a su solubilidad acuosa y su permeabilidad intestinal. Cuando se combina con la disolución del producto, el SCB toma en cuenta tres factores principales que gobiernan la velocidad y el alcance de la absorción del fármaco a partir de formas posológicas orales sólidas de Liberación Inmediata (LI): disolución, solubilidad y permeabilidad intestinal. Según el SCB, los principios activos se clasifican de la siguiente manera: Clase 1: Alta solubilidad - Alta permeabilidad Clase 2: Baja solubilidad - Alta permeabilidad Clase 3: Alta solubilidad - Baja permeabilidad Clase 4: Baja solubilidad - Baja permeabilidad Además, se clasifican las formas posológicas orales sólidas de LI por su disolución rápida o lenta. Dentro de este marco, cuando se cumplen ciertos criterios, se puede usar el SCB como herramienta de desarrollo del fármaco. Es posible que las diferencias observadas in vivo entre la velocidad y el alcance de la absorción de un fármaco en dos productos orales sólidos farmacéuticamente equivalentes se deban a diferencias en la disolución del fármaco in vivo. Sin embargo, cuando la disolución in vivo de una forma posológica oral sólida de LI es rápida en relación con el vaciamiento gástrico y el fármaco tiene alta permeabilidad, es poco probable que la velocidad y el alcance de la absorción del fármaco dependan de la disolución y/o el tiempo de tránsito gastrointestinal del fármaco. Estudios de Compatibilidad Fármaco- Excipiente El conocimiento de la interacción del fármaco con los excipientes es esencial para la formulación inicial del producto. Puede también ser necesario más adelante durante el proceso de escalamiento, cuando se presentan los problemas, para determinar las incompatibilidades existentes cuales afectan la fabricación o la estabilidad. Las interacciones fármaco-.excipiente son a menudo directamente relacionadas con la humedad presente en uno u otro de los componentes o de la humedad a la cual la formulación esta expuesta durante el proceso de almacenamiento. Estos estudios son siempre realizados a condiciones aceleradas de humedad y temperatura. La evaluación incluye. 1. Inspección visual de los cambios en color y textura 9 2. Cromatografía de Líquidos de Alta Resolución (CLAR) y Cromatografía en Capa Fina (CCF) son comúnmente utilizados con muestras de control inicial 3. Análisis térmico diferencial Los estudios de compatibilidad son esenciales para la caracterización de las materias primas y la formulación final. PARTES Y PROPIEDADES DE LAS TABLETAS La parte central de una tableta es el núcleo. Las tabletas sin recubrimiento constan únicamente de núcleo. El principio de fabricación de los núcleos es simple, pero su aplicación plantea bastantes problemas habitualmente. No basta con colocar la cantidad necesaria de polvo o granulado en la matriz de una tableteadora y compactarlo entre dos punzones. Es preciso que ese polvo o granulado reúna una serie de condiciones: por un lado, las partículas han de aglutinarse suficientemente para resistir a golpes y manipulaciones tras la compresión, y, a la vez, deben deslizarse sin resistencia por la máquina y no adherirse a los punzones ni a otras partes; por otro lado, los comprimidos tienen que disgregarse dentro del organismo para liberar el principio activo y disolverse en los líquidos biológicos para su absorción. Además, es muy importante que las tabletas permanezcan estables física y químicamente durante un determinado periodo de exposición al aire y a la luz, así como a ciertas temperaturas y grados de humedad. Por último, la aceptabilidad de las tabletas por el consumidor tiene igualmente una relevancia nada desdeñable. Esta es, de hecho, una razón fundamental para el recubrimiento del núcleo con sustancias que, por ejemplo, oculten al paladar su sabor amargo. Por todos estos motivos, los principios activos requieren prácticamente siempre el acompañamiento de excipientes y un tratamiento especial, la granulación, para su transformación en tabletas mediante la compresión. Excipientes Diluentes Los diluentes son sustancias con función de relleno, sin actividad farmacológica, utilizadas para alcanzar el tamaño deseado de las tabletas. Se seleccionan en función de las propiedades de compresión, la solubilidad, la capacidad absorbente, la alcalinidad o 10 acidez, etc. Uno de los diluentes más utilizados es la lactosa, por su rapidez de disolución en agua y agradable sabor, pero sus propiedades de deslizamiento o flujo son desfavorables. Otros excipientes de uso frecuente como diluentes son el almidón y la celulosa microcristalina. Tabla 2. Diluentes Diluente Comentarios Carbonato de Calcio Insoluble en agua (Cal-Carb, Millicarb, PharmaCarb,Sturcal) Fosfato de Calcio Dibásico Insoluble en agua, buenas propiedades de flujo, disponible en forma anhidra (Cyfos, Calstar, Calipharm, Emcompress) Fosfato de Calcio Tribásico Insoluble en agua (Tricafos, Tri-Cal, Tri-Tab) Sulfato de Calcio Insoluble en agua (Cal-tab, Compactrol) Celulosa Microcristalina Buenas propiedades de compresión, puede no necesitar lubricantes, puede actuar como desintegrante (Flocel, Microcel, Avicel, Emcocel, Compactrol) Celulosa Microcristalina Silificada Combinación de celulosa macrocristalina y dióxido de silicio. (Prosolv) Celulosa Micronizada (Elcema, Solka-Floc) Dextratos (Emdex) 11 Dextrosa Azúcar reductor, Higroscopico (Tebfine) Fructosa (Fluctofin) Lactitol (Finlac) Lactosa Monohidratada Diluente comúnmente usado, Económico, participa en la reacción de Millard (Fast-Flo, Lactochem, Microtose, Pharmatose, Tablettose, Zeparox.) Carbonato de magnesio Maltitol (Maltisorb, Maltit) Maltodextrina (Glycidex, Lycatab,Maltrin) Maltosa (Advantose) Manitol Fácilmente soluble en agua, sabor fresco, uso en tabletas masticables, (Pearlitol) Cloruro de Sodio Fácilmente soluble en agua Sorbitol (Parteck SI 400, Parteck SI 450) Almidón Utilizado también como agente desintegrante. Almidón Pregelatinizado Utilizado también como agente desintegrante. (Lycatab, Pharma-Gel, Pre-Jel, Sepistab, Starch 1500, Stara 1500) Azúcar Fácilmente soluble en agua, sabor dulce, higroscópico, usado en conjunción con lactosa Azúcar Compresible (DINAC, Nutab) Talco Xilitol Sabor Fresco (Xylifin, Xylitab) Aglutinantes Estas sustancias unen las partículas entre sí cuando la sola presión no basta para mantenerlas agrupadas en gránulos. Además aumentan la resistencia a la ruptura de las 12 tabletas, pero reducen su velocidad de disolución. Aunque pueden utilizarse en seco, en general se agregan a la formulación en solución o dispersión para garantizar una distribución más homogénea. De entre los aglutinantes más utilizados cabe destacar la goma arábiga (acacia) y la gelatina como aglutinantes naturales, y de los sintéticos, la polivinilpirrolidona y ciertos derivados de la celulosa (metilcelulosa y carboximetilcelulosa sódica y hidroxipropilmetilcelulosa). Tabla 3. Aglutinantes Aglutinantes Concentración en el fluido de granulación (%p/v) Comentarios Goma Arábiga Hasta 20 Produce gránulos muy duros. Acido alginico 1-5 Carbomero 5-10 (Carbopol) Carboximetilcelulosa Ca 5-15 (Nymcel) Carboximetilcelulosa Na 5-15 (Nymcel) (Gelycel) Celulosa Microcristalina ( F l o c e l , M i c r o c e l , Av i c e l , Emcocel, Vivacel) Celulosa Micronizada (Elcema, Solka Floc) Etil Celulosa 1-3 (Aquacoat) Gelatina 5-20 Forma geles con agua fría, por lo tanto se usa en solución tibia, fuerte adhesivo. Glucosa Liquida Hasta 50 Goma Guar 1-10 Hidroxietil celulosa 2-6 (Cellosize) Hidroxipropil celulosa 2-6 (Klucel, Methocel) Hidroxipropil celulosa-baja sustitución 5-25 13 Hidroxipropilmetil celulosa 2-5 (Methocel, Pharmacoat) Silicato de Aluminio y Magnesio 2-10 (Pharmasorb, Veegum) Maltodextrina 2-10 (Glucidex, Lycatab, Maltrin) Metilcelulosa 1-5 (Celacol, Methocel) Polidextrosa Oxido de Polietileno Povidona (Litesse) 5 0.5-5 (Polyox) También conocida como PVP o polivinilpirrolidona. Soluble en agua y algunos solventes orgánicos como el alcohol, puede ser usado en granulaciones no acuosas, muy comúnmente usado, material sintético ( Povidona K29/32 USP 26, FEUM 8a , Kollidon, Plasdone) Alginato de Sodio 1-3 (Manucol) Pasta de Almidón 5-25 Muy comúnmente usado Almidón Pregelatinizado 5-10 (Lycatab C, Pharma- Gel, Pre-Jel, Sepistab, Starch 1500, Starx 1500) Azúcar Higroscopico, las tabletas pueden endurecer durante el almacenamiento. Agua Apto para sólidos que son fácilmente solubles en agua. Lubricantes y deslizantes A veces se les denomina, de manera global, agentes antifricción, pues una de sus funciones principales consiste en reducir o eliminar la fricción entre la mezcla para comprimir. También actúan como reguladores de flujo de la mezcla en la cámara de compresión, lo que constituye propiamente su efecto deslizante. La acción lubricante radica en la disminución de la fricción entre las partículas durante la compresión, 14 mejorando así la transmisión de la fuerza de compresión en la masa de polvo o granulado. El lubricante más usado es el estearato de magnesio. Tabla 4. Deslizantes Deslizantes Silicato de Calcio Concentración en la Tableta (%p) 0.5-2 Celulosa Micronizada 1-2 Carbonato de Magnesio 1-3 Oxido de Magnesio 1-3 Silicato de Magnesio 0.5-2 Dióxido de Silicio Coloidal Comentarios 0.005-0.5 Almidón 2-10 Talco 1-10 (Elcema, Solka Floc) Excelente deslizante (HDKN20, Aerosil, Cab-o-sil) Insoluble en agua pero no hidrofobico. Tabla 5. Lubricantes Lubricantes Estearato de Calcio Acido Fumarico Concentración en la Tableta (%p) 0.5 – 2.0 5.0 Comentarios Insoluble en agua Soluble en agua Behenato de Glicerol 0.5 – 4.0 Insoluble en agua Palmitoestearato de Glicerol 0.5 – 5.0 Insoluble en agua (Precirol) 15 Aceite Vegetal Hidrogenado 1.0-6.0 Insoluble en agua, puede ser usado en conjunción con talco (Lubritab, Sterotex) Luaril Sulfato de Magnesio 1.0 – 2.0 Soluble en agua tibia Estearato de Magnesio 0.25 – 5.0 Insoluble en agua, excelente lubricante, reduce la fuerza de la tableta, prolonga los tiempos de desintegración y disolución. Polietilenglicol 4000 o 6000 2.0 – 5.0 Soluble en agua, moderadamente efectivo, también conocido como macrogol (Carbowax) Lauril Sulfato de Sodio 1.0 – 2.0 Soluble en agua, lubricante moderado, a menudo empleado en conjunción con estearatos (Empicol, Stearowet) Estearil Fumarato de Sodio 0.5 – 2.0 Poco soluble en agua fría, soluble en agua caliente (Pruv) Almidón 2.0 – 10.0 Lubricante moderado Acido esteárico 1.0 – 3.0 Insoluble en agua Talco 1.0 – 10.0 Insoluble en agua pero no hidrofobico. Lubricante moderado. Estearato de Zinc 0.5 – 2.0 Insoluble en agua . Desintegrantes Los desintegrantes se utilizan para acelerar la disgregación del principio activo en el agua y en los jugos gástricos, facilitando así su disolución y absorción. Esta función la pueden ejercer en virtud de su solubilidad, mayor que la del principio activo; por ejemplo, cuando este es un poco hidrosoluble. También actúan por su capacidad de hinchamiento, favoreciendo la penetración de los líquidos en el comprimido y la separación de los gránulos. Por último, cuando los comprimidos son efervescentes, el mecanismo de acción consiste en fomentar la liberación de los gases –previamente incorporados- al contacto del comprimido con el agua, lo que conduce a su 16 disgregación. Desintegrantes de uso frecuente son el almidón de maíz o de papa, la croscarmelosa, la crospovidona y el glicolato sódico de almidón. Tabla 6. Desintegrantes. Agente Desintegrante Acido Alginico Concentración en la Tableta (%p) Comentarios 2-10 Dióxido de Carbono Creado in situ en las tabletas efervescentes Carboximetilcelulosa Calcica 1-15 (Nymcel) Carboximetilcelulosa Sódica 1 -5 (Nymcel) (Gelycel) Celulosa Microcristalina Hasta 10 Para compresión directa, posee algunas características de lubricante ( Flocel, Microcel, Avicel, Emcocel, Vivacel) Celulosa Micronizada 5 – 15 (Solka Floc) Croscaramelosa Sódica 0.5 – 5.0 (Ac-di-Sol, Solutab, Primellose) Crospovidona 2.0 – 5.0 (Kolidon CL, Poliplasdone XL) Docusato Sódico 0.5 – 1.0 Actúa sobre todo como agente de adherencia. Goma Guar 2.0 – 8.0 Hidroxipropil celulosa –bajasustitución. 5-0 – 25.0 Silicato de Aluminio y Magnesio Metilcelulosa 2.0 – 10.0 Polacrilin Potasico 2.0 – 10.0 (Veegum) 2.0 – 10.0 Resina de Intercambio Cationico (Amberlite IRP88) 17 Poloxamer 5.0 – 10.0 Povidona 0.5 – 5.0 (Povidona K29/32 USP 29 FEUM 8a , Kollidon, Plasdone) Alginato de Sodio 2.5 – 10 (Manucol) Glicina carbonato de sodio Fuente de Dioxido de carbono en las tabletas efervescentes. Lauril sulfato de sodio 0.5 – 2.0 Principalmente como agente de adherencia, pero ayuda a la desintegración (Empicol) Glicolato Sódico de Almidón 2.0 – 8.0 (Explotab, Primojel, Glycolis) Almidón 2.0 – 10.0 Almidones de papa y maíz, son más frecuentemente usados. Almidón Pregelatinizado 5.0 – 10.0 (Lycatab, Pharma-Gel, Pre-Jel, Sepistab, Starch 1500, Starx 1500) Tabla 7.Diluentes para Compresión Directa Diluente Nombre Comercial Comentarios 18 Fosfato de Calcio Dibásico Emcompress, Di-Tab Fosfato de Calcio Tribásico Tri-Tab Insoluble en agua Compactrol Insoluble en agua Sulfato de Calcio Celulosa Microcristalina Avicel, Emcocel, Vivacel, Alta compresibilidad, actúa Flocel, Microcel, Ciclocel como desintegrante. Celulosa Micronizada Elcema Dextrosa Emdex Lactitol Finlac DC Lactosa Anhidra Alfa Anhidra Beta Spray-Dried Buenas propiedades de flujo, alta densidad, insoluble en agua. Pharmatose DCL15 Pharmatose DCL21 Fast-Flow, Zeparox, Pharmatose DC11 Cellactose Buenas propiedades de flujo. Lycatab, Maltrin Soluble en agua, leve efecto lubricante Manitol Pearlitol Fácilmente soluble en agua Sorbitol Neosorb, Parteck SI 400, Parteck SI 450 Almidón de Maíz Pregelatinizado Starch 1500, Starx 1500 Desintegrante Azúcar-maltodextrina coprecipitada Des-Tab, Dipac, Un-Tab Buenas propiedades de flujo, sensible a la humedad. Xylitab Fácilmente soluble en agua. Mezcla coprocesada de Lactosa- Celulosa Maltodextrina Xylitol Métodos de Manufactura La selección del proceso adecuado para fabricar tabletas será determinado por las propiedades reologicas del fármaco, por el nivel de dosis y la economía de la operación. 19 • • • Compresión Directa Granulación Húmeda Granulación Seca Compresión Directa Este método consiste en comprimir la mezcla del fármaco y excipientes, los cuales tienen propiedades de fluidez y compresibilidad, esto es mediante la velocidad de flujo y la compresibilidad. (Fig.4) Ingrediente (s) Activo (s) Deslizante Diluente Mezclado Lubricante Agente Desintegrante Compresión Figura 4. Compresión Directa Tabla 8. Ventajas y Desventajas de la Compresión Directa Ventajas Desventajas 20 Menor costo en instalaciones, tiempo, equipos, energía y espacio. Es crítico el origen de las materias primas: exigencias de control de calidad. Elimina problemas en el proceso de granulación debido a la humedad y temperatura (vía húmeda) y presión (vía seca) Dificultad en alcanzar dureza en comprimidos con alto contenido de principio activo. Facilita la desintegración del comprimido en las partículas originales del principio activo. Distribución no homogénea del principio activo, en bajas dosis debido al mal mezclado( es necesario el uso de mezclas ordenadas). Disminuye la disparidad de tamaño de partícula en la formulación. Aumento de tamaño de partícula para aumentar la fluidez del principio activo en dosis altas (disminuye la velocidad de disolución) (necesidad de aglutinantes) Proporciona mayor estabilidad física y química frente al envejecimiento. Sobrelubricación por exceso de mezclado (disminución de la velocidad de disolución) Necesidad de precomprensión para comprimidos con alto contenido de principio activo. Limitaciones para preparar comprimidos coloreados. Granulación por Vía Húmeda Este método consiste en humectar la mezcla de polvos con una solución del aglutinante, proporcionando cohesividad a los componentes de la formulación, obteniendo una masa húmeda que se pasa a través de una malla para obtener un granulado húmedo, se seca en un horno y se tamiza para después mezclar con el lubricante y comprimirlo finalmente. (Fig. 5). 21 Ingrediente (s) Activo (s) Aglutinante Mezclado Diluente Solución Aglutinante Agua Granulación Secado Tamizado Mezclado Deslizante Lubricante Compresión Agente Desintegrante Fig. 5. Granulación por Vía Húmeda Tabla 9. Ventajas y Desventajas de la Granulación Vía Húmeda. 22 Ventajas Desventajas Permite el manejo mecánico sin perder laTamaño de partícula y solubilidad del calidad de la mezcla. principio activo (Afectando la Disolución) Mejora características de flujo de losDistribución no uniforme de agentes polvos: aumento de tamaño y esfericidad deaglutinantes o desintegrantes (Se afecta la las partículas. Disolución y la Dureza) Mejora la cohesión durante y después de laSegregación del principio activo inducida compactación por amasado y secado (Afectando uniformidad de contenido) Reduce el polvo fino y por lo tanto laExposición del principio activo a altas contaminación cruzada. temperaturas y humedad (Afectando la Estabilidad). Permite la incorporación de líquidos aS o b r e l u b r i c a c i ó n ( A f e c t a n d o l a polvos. Disolución). Hace de superficies hidrofóbicas más hidrofílicas. Permite el control de la forma y distribución de tamaño de partícula. Permite el recubrimiento de gránulos del principio activo, por lo tanto mejora la estabilidad o modifica la cesión. Granulación Vía Seca (Doble Compresión) El método consiste en compactar una mezcla de polvos en unidades de peso mayor que las tabletas finales, posteriormente son trituradas y tamizadas para dar el tamaño de gránulo, se adiciona el lubricante y desintegrante, se mezcla y se comprime para obtener las tabletas deseadas. (Fig. 6) 23 Ingrediente Activo (Aglutinante) Diluente Mezclado Lubricante Primera Compresión Mezclado Molienda Tamizado Deslizante Lubricante Mezclado Agente Desintegrante Segunda Compresión Fig. 6. Granulación por Vía Seca (Doble Compresión) Tabla 10. Ventajas y Desventajas Granulación por Vía Seca (Doble Compresión) 24 Ventajas Permite la manipulación mecánica sin perdida de los atributos de la mezcla. Desventajas Tamaño de partícula variable y problemas en la solubilidad de los principios activos, afectando la disolución. Mejora el flujo de los polvos por aumento Sobrecompactación de los tabletones de tamaño de partícula. iniciales (Disolución) Mejora la cohesión durante la compactación. Posible sobrelubricación debido al empleo de agentes lubricantes pre y post compresión inicial. Permite la granulación sin adición de líquidos o uso de calor. Erosión y segregación de partículas. Útil para fármacos sensibles al calor y la humedad. Gran nivel de reprocesamiento. No útil para tabletas con principios activos en bajas dosis. EQUIPOS Para producciones en gran escala, las máquinas rotativas ofrecen muchas ventajas. Un cabezal con una cantidad de juego de punzones y matrices que giran en forma continua, mientras la mezcla de polvos o granulado se desliza desde la tolva a través de un bastidor de alimentación para llegar a las matrices colocadas sobre un placa de acero que gira debajo. Este método proporciona un llenado uniforme en la matriz y, por esta razón, un peso exacto de la tableta. La compresión tiene lugar cuando los punzones superior e inferior pasan entre un par de rodillos. Esta acción produce un efecto lento de compresión sobre la cavidad matriz desde arriba y abajo, lo cual posibilita el escape del aire atrapado. El punzón se eleva y eyecta el comprimido. Las correcciones del peso y la dureza de los comprimidos se pueden realizar sin el uso de herramientas mientras la maquina este funcionando. (Fig.7) 25 Figura 7. Tableteadora Fette Perfecta 2000 ETAPAS DE COMPROBACIÓN DE LA CALIDAD DE LAS TABLETAS En cada uno de las etapas del proceso, se acostumbra a hacer ciertos controles o inspecciones de calidad que pueden dividirse en varios tipos. • Materias primas y excipientes: Se les hacen los controles respectivos que estipula la farmacopea oficial que sigue el laboratorio fabricante. • Etapa intermedia de producción: Se deben controlar los procesos de molienda, mezclado, granulación, y secado, para verificar la buena marcha de las operaciones, y si es preciso haciendo correcciones en los procesos. Los factores claves en estas etapas son la frecuencia granulométrica, cantidad de fármaco, humedad, ángulo de reposo etc. • Fase final de producción: Durante la compresión de un lote, se debe verificar permanentemente el peso, dureza y friabilidad de los comprimidos, los datos se deben pasar a gráficos de control. • Control producto terminado: Cuando termina la producción, se hace un muestreo de este para hacer un análisis detallado. Con base en estos resultados, se decide si se aprueba, rechaza o se reprocesa el lote. A las tabletas se les evalúan sus propiedades físicas, químicas y farmacopeicas. Estas propiedades en conjunto, describen la calidad total de cualquier formulación dada según su método de manufactura y condiciones de almacenamiento. Todas estas tres propiedades pueden cambiar el perfil de estabilidad y por tanto se beben realizar. Tabla. 11 Parámetros de comprobación de la calidad de las tabletas. 26 Caracteres organolépticos Apariencia visual, olor, textura, sabor Caracteres geométricos Forma, grabados, y dimensiones Caracteres químicos Contenido del fármaco, productos de degradación, contaminantes, y humedad. Caracteres posológicos Variación de peso y uniformidad de contenido. Caracteres de estabilidad Estabilidad del fármaco a la luz, humedad, calor. Caracteres de biodisponibilidad Tiempo de desintegración y velocidad de disolución Nota: Los ensayos críticos son los de contenido de fármaco y biodisponibilidad. Un cambio en las propiedades físicas de las tabletas puede provocar un cambio bajo las condiciones de estabilidad ambiental o acelerada que influye rotundamente en su biodisponibilidad. En general las farmacopeas exigen los mismos tipos de pruebas pero difieren en los equipos, y condiciones que exigen en cada una de ellas. TIPOS DE DEFECTOS EN LAS TABLETAS Durante el proceso de compresión suelen presentarse muchos problemas que pueden agruparse en dos categorías: los relacionados con la formulación (ingredientes, granulometría del producto, contenido de agua, etc.) y la otra relacionada con el equipo y condiciones ambientales de producción (Humedad Relativa y tipo de equipo utilizado). Los defectos de las tabletas son. Laminación y decapado (capping): Ocurre cuando en la eyección desde el punzón superior se arranca la parte superior de la tableta. Este defecto puede ocurrir en el momento del tableteado u horas después. Las causas son: • Gránulos frágiles y porosos que hacen que se atrape aire durante la compresión, y que no exista una deformación plástica. • El exceso de finos que se genera al aplicar la presión de compresión. • Gránulos excesivamente secos o excesivamente húmedos. • Gránulos con fuerzas de adhesión muy fuertes. • Punzones no bien lubricados y excesiva velocidad de compresión. • Matrices con superficies de expansión que hacen que la tableta se parta cuando asciende el punzón inferior al no haber espacio para desalojar el aire. 27 Pegado (sticking): De vez en cuando todo o parte del comprimido se pega a los punzones o a la matriz. La causa es la excesiva humedad del granulado o de los punzones, también pude ocurrir por lubricantes de bajo punto de fusión, punzones rayados y uso de una muy baja presión de compactación. Ruidos en la tableteadora: Se producen por el rozamiento por la adhesión de la masa de las tabletas a la pared de la matriz o a la cabeza del punzón inferior. Esto ocurre en granulados muy húmedos, o muy poco lubricados o por el uso de punzones desgastados. Fragilidad: Ocurre cuando la forma y tamaño de los gránulos es muy irregular, también por granulados muy porosos y falta de aglutinantes e insuficiente presión de compactación. Excesiva dureza: Se produce por el exceso de aglutinantes, poca porosidad y humectación del granulado, forma y tamaño irregular de este y excesiva presión de compactación. BIBLIOGRAFIA. 1. Chowhan, Z.T. Excipients and Their Functionality in Drug Product Devepment. Pharm. 1993, 17 (9), 72 2. Czeisler, J.L.; Penman, K.P. Diluents, Enciclopedia of Pharmaceutical Technology, 1st Ed.; Swarbrick, J., Boylan, J.C., Eds.; Marcel Dekker, Inc.:New Cork, 1991; 4, 40-43. 28 3. Augsburger, L.L.;Shangraw, R.F. Effect of Glidants in Tableting. J. Pharm. Sci. 1966, 55, 418. 4. Amidon, G.L.; Lennernas, H.; Shah, V.P.; Crisol, J.R. A Theorical Basis for a Biopharmaceutic Drug Classification: The Correlation of In Vitro Drug Product Dissolution and In Vivo Bioavailability. Pharm. Res. 1995, 12, 413. 5. American Pharmaceutical Association and the Royal Pharmaceutical Society of Great Britain. Handbook of Pharmaceutical Excipients, 3 rd Ed.; American Pharmaceutical Association and Pharmaceutical Press: Washington, 2000. 6. Armstrong, A.M.; James, K.C. Understanding Experimetal Desing and Interpretation in Pharmaceutics; Ellis Horwood Ltd: Chichester, UK, 1990. 7. Franz, R.M.; Browne, J.; Lewis, A. Experimental Desing, Modeling, and Optimization Strategies for Product and Process Development, Pharmaceutical Dosege Forms: Disperse Systems, 2nd Ed.; Lieberman, H.L.,Rieger, M., Banker, G., Eds.; Marcel Dekker, Inc.: New Cork, 1996; 1, 427-514. 8. Peck, G.E.; Mc Curdy, V. E.; Banker, G.S. Tablet Formulation and Desing, Pharmaceutical Dosege Forms: Tablets, 2nd Ed.; Lieberman, H.L., Lachman, L., Schwartz, J., Eds.; Marcel Dekker, Inc.: New York, 1989; 1, 75-130. 9. Polderman, J. Formulation and Preparation of Dosege Forms; Elsevier/NorthHolland: New York, 1977; 3-28. 10. Specifications and control tests on the finished products. 1992. Pp 1-11. http:// pharmacos.eudra.org/F2/eudralex/vol-3/pdfs-en/3aq11aen.pdf. 11. New technologies forum 4: Process measurenet and control. R. Alexander, J.A. Clements, R. Guest. Pp. 1-18 http://www.rpsgb.org.uk/pdfs/ntf4.pdf. 12. Dennis cooper and simon carter. (2004) Una cierta información sobre la dureza de la tableta. http://www.engsys.co.uk/spanish/testing.htm 13. Swarbrick, James. 1997. Encyclopedia of pharmaceutical Technology. Boylan, James. Marcel dekker Inc.Tomo XIV. Pg. 407. 29 14. United States Pharmacopoeia 26- National formulary 21, The United States Pharmacopoeial Convention,Inc. Rockville, MD, 2003. Chapter <905>pp. 1-8. 15. Egermann, H. (1980). Power Technol., 26:235; 27:203 16. United States Pharmacopoeia 26- National formulary 21, The United States Pharmacopoeial Convention,Inc. Rockville, MD, 2003. Chapter <1216>pp. 1-3. 17. Fonner, Anderson and Banker. Characterization of granulations. Pp. 246-247. 18. United States Pharmacopoeia 26- National formulary 21, The United States Pharmacopoeial Convention,Inc. Rockville, MD, 2003. Chapter <711>pp. 1-6. 19. Voigh, Rudolf. 1982. Tratado de tecnología Farmacéutica. Editorial Acribia. Zaragoza. 3ra. Edición. Zaragoza. pp. 212-213. 30