1) Contesta por qué son verdaderas o falsas las siguientes
Anuncio

EXAMEN DE DICIEMBRE DE QUÍMICA FÍSICA (3º Curso de Químicas): 3/12/2009.
1) Contesta por qué son verdaderas o falsas las siguientes afirmaciones:
a) La medida del momento lineal, px = −i ⋅ =
d
, puede dar como resultado una magnitud
dx
imaginaria.
b) En las proximidades del equilibrio un enlace químico se comporta como un oscilador
armónico cuántico.
c) Un átomo de hidrógeno solo posee energía electrónica.
d) Una configuración 1s1 solo posee un microestado.
e) Las configuraciones electrónicas de un átomo polielectrónico nos permite determinar de
forma cualitativa los niveles de energía del átomo.
+
2) Dada la función de onda del estado fundamental del He , calcula:
a) La distancia más probable de encontrar el electrón.
b) La posición media del electrón.
Compara los resultados obtenidos con los que se obtienen para el hidrógeno.
1 ⎛Z⎞
ψ 1s =
⎜ ⎟
π ⎝ a0 ⎠
3/ 2
e
− Zr / a 0
⎛Z⎞
R1s = 2 ⎜ ⎟
⎝ a0 ⎠
3/ 2
e − Zr / a 0
∞
∫x e
0
n − ax
dx =
n!
a n +1
3) a) Supónganse dos átomos A y B diferentes, unidos a lo largo del eje z. Indicar que tipos de orbitales
moleculares, σ, π ó δ, se forman con las siguientes combinaciones lineales de orbitales atómicos:
I) s(A) + s(B)
II) s(A) + pz (B)
III) px(A) + px (B)
IV) s(A) + px(B)
V) dz2(A) + dz2(B)
VI) dxy(A) + dxy(B)
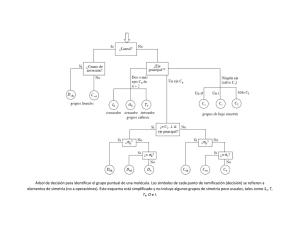
b) Para la molécula de la figura contigua, identifique el mayor número posible de
elementos de simetría que posee.
Nota: no es necesario indicar el grupo de simetría al que pertenece.
c) ¿Por qué los orbitales moleculares se clasifican en función de los elementos de simetría que posee una
molécula?
4) Determina el tanto de por ciento de carácter s y p que poseen los híbridos sp3 del oxígeno en la molécula
de agua. El ángulo de enlace del agua es de 104º30’.
5) Utilizando el método de Hückel, comprobar si en la molécula de alcohol vinílico,
H2C=CH-OH, el oxígeno presenta hibridación sp3 o sp2.
Datos: αO = α + 2β, βCO = β. Una de las raíces del determinante secular de orden tres que aparece en el
problema es x = +1.17.
1) Contesta por qué son verdaderas o falsas las siguientes afirmaciones:
a) La medida del momento lineal, px = −i ⋅ =
d
, puede dar como resultado una magnitud
dx
imaginaria.
b) En las proximidades del equilibrio un enlace químico se comporta como un oscilador
armónico cuántico.
c) Un átomo de hidrógeno solo posee energía electrónica.
d) Una configuración 1s1 solo posee un microestado.
e) Las configuraciones electrónicas de un átomo polielectrónico nos permite determinar de
forma cualitativa los niveles de energía del átomo.
Respuesta:
a) Falso. El momento lineal es un operador hermítico y como tal sus autovalores son siempre
reales. Además, según el 4º postulado la medida de una observable con sentido físico solo
puede dar como resultado uno de sus autovalores.
b) Verdadero. La energía electrónica en función de la distancia entre núcleos se asemeja a una
curva de tipo Morse, V ( x) = D ⎡⎣1 − exp ( −a ( r − re ) ) ⎤⎦ , curva que cuando r → re , tiene forma
2
cuadrática, V ( x) ≈ Da 2 [ r − re ] = k [ r − re ] / 2 , que es la forma de la energía potencial de un
oscilador armónico.
c) Falso. El operador energía del átomo de hidrogeno puede dividirse en dos H=Ht+He, uno
que da cuenta de la energía cinética del átomo y otro que da cuenta de la energía electrónica.
d) Falso. La configuración 1s1 posee dos microestados correspondientes a los dos valores de ms
= ±1/2.
e) Verdadero. Para obtener los niveles de energía de un átomo se van construyendo todas las
configuraciones electrónicas del átomo y a partir de ellas se construyen los términos
espectroscópicos, que nos dan los niveles de energía del átomo. Esta forma de trabajar es
cualitativa, ya que para obtener los valores de energía de cada estado hay que recurrir a
métodos aproximados de cálculo.
2
2
2) Dada la función de onda del estado fundamental del He+, calcula:
a) La distancia más probable de encontrar el electrón.
b) La posición media del electrón.
Compara los resultados obtenidos con los que se obtienen para el hidrógeno.
1 ⎛Z⎞
ψ 1s =
⎜ ⎟
π ⎝ a0 ⎠
3/ 2
e
⎛Z⎞
R1s = 2 ⎜ ⎟
⎝ a0 ⎠
− Zr / a 0
3/ 2
∞
∫x e
e − Zr / a 0
n − ax
0
dx =
n!
a n +1
Respuesta:
a) La función de distribución radial es:
3
⎛Z⎞
16π Z3 2 −2Zr / a 0
D(r)1s = 4π r R = 4π r 4 ⎜ ⎟ e −2Zr / a 0 =
r e
a 30
⎝ a0 ⎠
2
2
1s
2
la distancia más probable es aquella que:
dD(r)
16π Z3 ⎛
2 2Z ⎞ −2Zr / a
dr
=0=
a 30
⎜ 2r − r
⎟e
a0 ⎠
⎝
0
por lo tanto el máximo tiene lugar a:
r
a
a
Z
+
= 1⇒ r = 0 , luego para el He , r = 0 , mientras que para el hidrógeno r = a 0
2
a0
Z
b)
r = ∫ψ rψ dτ =
∞
π
2π
∞
Z3 3 −2Zr / a 0
Z3 4π 3 −2Zr / a 0
r
e
dr
sen
d
d
re
dr
θ
θ
φ
=
∫0 ( ) ∫0
π a 30 ∫0
π a 30 ∫0
∞
4Z3 3 −2Zr / a 0
4Z3 ⎛ a 0 ⎞
3 a0
=
=
r
e
dr
3!⎜
⎟
3 ∫
3
a0 0
a 0 ⎝ 2Z ⎠
2 Z
3
3
luego para He+; r = a 0 , mientras que para hidrógeno r = a 0
4
2
4
r=
3) a) Supónganse dos átomos A y B diferentes, unidos a lo largo del eje z. Indicar que tipos de orbitales
moleculares, σ, π ó δ, se forman con las siguientes combinaciones lineales de orbitales atómicos:
III) px(A) + px (B)
I) s(A) + s(B)
II) s(A) + pz (B)
IV) s(A) + px(B)
V) dz2(A) + dz2(B)
VI) dxy(A) + dxy(B)
Respuesta: I) σ,
δ,
II) σ,
III) π,
IV) no es posible formar OM, solapamiento cero, V) σ, VI)
b) Para la molécula de la figura contigua, identifique el mayor número posible de
elementos de simetría que posee.
Nota: no es necesario indicar el grupo de simetría al que pertenece.
Respuesta:
La molécula posee 4 elementos de simetría. La identidad E, centro de simetría i, un plano de simetría que
coincide con el plano de la molécula, σh y un eje de rotación C2, perpendicular a dicho plano y que pasa por
i. La molécula pertenece al grupo C2h.
En realidad, la molécula posee un elemento adicional, aunque no es independiente de los anteriores. Consiste
en un eje S2 = C2×σh
c) ¿Por qué los orbitales moleculares se clasifican en función de los elementos de simetría que posee una
molécula?
Respuesta:
Las propiedades de una molécula, perteneciente a un grupo de simetría determinado, deben
permanecer invariantes cuando se aplica cualquier operación de simetría de dicho grupo. De las propiedades
moleculares nos interesa la probabilidad de encontrar al electrón o densidad de carga, representada por el
cuadrado de la función de onda ψ 2 ( x, y , z ) . Así, por ejemplo, si nuestra molécula es el agua y se efectúa una
rotación con respecto al eje C2 = y, puede escribirse que: ψ 2 ( x, y , z ) = ψ 2 ( − x, y , − z ) . Si ahora tomamos raíz
cuadrada, tendremos dos soluciones: ψ ( x, y, z ) = ±ψ ( − x, y , − z ) . La solución de signo +, se denomina a, y la
de signo menos, b. Como no disponemos de números cuánticos, los orbitales moleculares se clasifican en
función de estas propiedades.
Otra forma de razonar lo anterior es la siguiente; Los operadores correspondientes a los elementos de
simetría de una molécula conmutan con su Hamiltoniano, lo que significa que las funciones de onda son
funciones propias de dichos operadores, siendo los valores propios ±1 , propiedad que se utiliza para
clasificar los orbitales moleculares.
4) Determina el tanto de por ciento de carácter s y p que poseen los híbridos sp3 del oxígeno en la molécula
de agua. El ángulo de enlace del agua es de 104º30’.
Respuesta:
La forma general de cada híbrido es:
φi = aiφs + biφ px + ciφ py + diφ pz
Suponiendo que los híbridos 1 y 2 son los que enlazan con los hidrógenos (equivalentes) y situándolos en el
plano x-y de forma que el eje x coincida con la bisectriz del ángulo, tendremos que:
a1 = a2 = a, b1 = b2, c1 = -c2 y d1 = d2 = 0.
Normalizando cualquiera de estos dos híbridos y aplicvando la condición de que deben ser ortogonales se
obtiene que:
a 2 + b12 + c12 = 1 (normalizar)
a 2 + b12 − c12 = 0 (ortogonales).
La suma y recta de estas ecuaciones nos permiten obtener que:
2a 2 + 2b12 = 1⇒ b1 = b2 =
1 − 2a 2
2
1
2
Definiendo los vectores asociados a cada híbrido se obtiene que:
JG
JG
1 − 2a 2 G 1 G
1 − 2a 2 G 1 G
y
t1 =
i+
j
t2 =
i−
j
2
2
2
2
Teniendo en cuenta que el módulo de estos vectores es:
JG JG
1 − 2a 2 1
+ = 1 − a2
t1 = t2 =
2
2
Tenemos que:
JG JG 1 − 2a 2 1
JG JG
− = −a 2 = t1 ⋅ t2 cos (θ ) = (1 − a 2 ) cos (θ )
t1 ⋅ t1 =
2
2
Por lo tanto
cos (θ )
a2 =
= 0.2
cos (θ ) − 1
Por lo tanto, los híbridos que enlazan con los hidrógenos tienen un 20% de carácter s y un 80% de carácter p
cada uno.
Los híbridos no enlazantes tienen un 30% de carácter s y un 70% de carácter p.
Téngase en cuenta que en una hibridación sp3 equivalente los híbridos poseen un 25% de carácter s y un 75%
de carácter p.
2c12 = 1⇒ c1 = −c2 =
5) Utilizando el método de Hückel, comprobar si en la molécula de alcohol vinílico,
H2C=CH-OH, el oxígeno presenta hibridación sp3 o sp2.
Datos: αO = α + 2β, βCO = β. Una de las raíces del determinante secular de orden tres que aparece en el
problema es x = +1.17.
Respuesta:
Si el oxígeno tiene hibridación sp2, la molécula será plana y podrán formarse orbitales π
deslocalizados con los 3 orbitales pz de los C y del O. La energía de estos orbitales deslocalizados
puede obtenerse resolviendo el determinante secular:
x+2 1 0
x 1 = x 2 ( x + 2 ) − x − ( x + 2 ) = x3 + 2 x 2 − 2 x − 2 = 0
1
0
1 x
Como el enunciado nos da una de las soluciones:
x 3 + 2 x 2 − 2 x − 2 = 0 = ( x 2 + bx + c ) ( x − 1.17 ) = x3 + (b − 1.17) x 2 + (c − 1.17b) x − 1.17c
Igualando los coeficientes:
2 = b − 1.17 ⇒ b = 3.17
−2 = −1.17c ⇒ c = 1.709
Por lo tanto:
x 2 + bx + c = x 2 + 3.17 x + 1.709 = 0 ⇒ x = {−2.481, −0.689}
La molécula tendría 4 electrones π, siendo su energía de ET = 4α + 2(2.481+0.689)β
= 4α + 6.34β.
Si la hibridación fuera sp3, se formaría un doble enlace C=C y el oxígeno en
lugar de participar con un orbital pz en la formación de orbitales deslocalizados,
poseería un híbrido sp3 no enlazante. La energía de los 4 electrones anteriores sería
por lo tanto: EL = 2α + 2β + 2(α + 2β) = 4α + 6β. Por lo tanto:
ED = ET - EL = 0.34 β, la molécula se estabiliza mediante la deslocalización
de electrones π, por lo que el oxígeno posee hibridación sp2.
" - 1.17$
¼¿
" + 0.689$
¼¿
" + 2.481$
ET = 4" + 6.34$
"-$
¼¿
"+$
" + 2$ (sp3 del O)
EL = 4" + 6$
¼¿