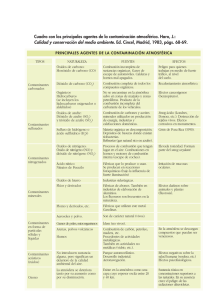
módulo: contaminación atmosférica
Anuncio

MASTER PROFESIONAL EN INGENIERIA Y GESTIÓN MEDIOAMBIENTAL 2007 MÓDULO: CONTAMINACIÓN ATMOSFÉRICA CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS JOSÉ ACOSTA LLINARES JULIO 2007 ©: Quedan reservados todos los derechos. (Ley de Propiedad Intelectual del 17 de noviembre de 1987 y Reales Decretos). Documentación elaborada por la EOI. SUMARIO 1. INTRODUCCIÓN .........................................................................................5 2. PARTÍCULAS .............................................................................................17 3. COMPUESTOS AZUFRADOS ...................................................................23 4. COMPUESTOS INORGÁNICOS DE CARBONO.......................................29 5. COMPUESTOS NITROGENADOS ............................................................37 6. HIDROCARBUROS....................................................................................43 7. COMPUESTOS ORGANOHALOGENADOS SIMPLES .............................49 8. DIOXINAS Y FURANOS ............................................................................57 9. METALES PESADOS ................................................................................65 10. OTROS CONTAMINANTES.....................................................................69 11. CONTAMINANTES SECUNDARIOS .......................................................71 12. GLOSARIO...............................................................................................77 13. BIBLIOGRAFÍA.........................................................................................91 14. PÁGINAS WEB ........................................................................................93 3 4 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS 1 INTRODUCCIÓN La degradación del medio ambiente constituye, sin duda alguna, uno de los problemas más importantes que el hombre tiene planteados en esta segunda mitad del siglo. La explotación intensiva de los recursos naturales, el desarrollo tecnológico, la industrialización y el lógico proceso de urbanización de grandes áreas territoriales son fenómenos que, incontrolados, han llegado a amenazar en determinadas regiones la capacidad asimiladora y regeneradora de la Naturaleza, y que de no ser adecuadamente planificados, pueden abocar a una perturbación irreversible del equilibrio ecológico general, cuyas consecuencias no son fácilmente previsibles. El aire es un bien común limitado y un elemento indispensable para la vida, por tanto, su utilización debe estar sujeta a unas normas que eviten el deterioro de su calidad por abuso o uso indebido del mismo, de tal modo que se preserve su pureza dentro de unos límites que no perturben el normal desarrollo del hombre y otros seres vivos ni atenten contra el patrimonio natural y artístico de la Humanidad, que esta generación tiene el deber de proteger para legar un mundo habitable a las generaciones futuras. 1.1. LA ATMÓSFERA La atmósfera es la capa gaseosa que envuelve la tierra. La necesidad de la atmósfera se debe a múltiples razones, desde ser el medio gaseoso que proporciona a los seres vivos sustancias imprescindibles para su desarrollo y evolución en la superficie de la Tierra, hasta el hecho de que constituye una pantalla protectora ante las radiaciones ultravioleta que proceden del Sol. Los componentes de la misma esenciales para estas funciones son el oxígeno y el ozono, los cuales, en su función de protección, actúan absorbiendo parte de la radiación ultravioleta que llega. El conocimiento exhaustivo de la atmósfera es de gran importancia cuando se aborda el estudio de su contaminación, puesto que su composición química implica la modificación de los contaminantes que son introducidos y su dinámica tiene como resultado el desplazamiento físico de los contaminantes, dando lugar los procesos de dispersión y transporte de éstos en su seno. Los 200 Km., aproximadamente, de grosor de atmósfera que posee la Tierra no son totalmente homogéneos, sino que los componentes de la misma se disponen en diferentes capas, las cuales se han tratado de clasificar de muy 5 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS diversas formas atendiendo a criterios diferentes como: variaciones de la temperatura con la altura, composición química, propiedades magnéticas o eléctricas, etc. La clasificación más adecuada al estudio de la contaminación es la basada en las variaciones de temperatura con la altura, según la cual tenemos: Troposfera: 12 Km. de espesor1 Estratosfera: 10 a 45 Km. por término medio Mesosfera: 40 a 90 Km. Termosfera. Por ser las dos primeras capas aquellas en las que se producen las emisiones de contaminantes y sus efectos se describirán alguna de sus características. TROPOSFERA Comenzando desde la superficie terrestre es la primera capa de la atmósfera que nos encontramos. Presenta tres características esenciales que la distinguen de las demás capas de la atmósfera: Es una capa sometida a perturbaciones. Su composición química es relativamente homogénea (debida a la agitación). Esta agitación permite una composición muy igualada en todo el espesor de la capa. La temperatura desciende regularmente con la altitud, siguiendo un gradiente de 0.6º C cada 100 m, por término medio, hasta alcanzar los –55º C. En la tabla 1 puede verse un análisis químico del aire atmosférico seco en la troposfera, en un punto localizado sobre el océano y alejado de las masas de terreno2. A esta composición es necesario añadir del orden del l% al 3% en volumen de agua (en estado de vapor, aunque se puede encontrar en estado 1 Estos valores de espesor dados para las diferentes capas de la atmósfera son siempre valores medios. El espesor de una determinada capa suele presentar los valores más divergentes cuando se comparan los correspondientes a los polos y el ecuador. 2 Aunque la composición quimica de la atmósfera varía de un lugar a otro, a lo largo del tiempo y con la altura, en esta capa es donde más homogeneidad se ha observado. 6 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS líquido o sólido) y presencia de otros componentes, en general, minoritarios como otros óxidos de nitrógeno, dióxido de azufre, formaldehído, yodo, cloruro de sodio, amoniaco, monóxido de carbono, ozono, polvo, etc. TABLA 1 COMPOSICIÓN QUÍMICA DEL AIRE SECO CONTENIDO VOLUMÉTRICO EN EL AIRE (%) CONCENTRACIÓN (ppmv)* Nitrógeno (N2) 78,084 780,084 Oxígeno (02) 20,946 209,460 Argón (Ar) 0,934 9,334 Bióxido de carbono (CO2) 0,0350 350 MOLÉCULA Neón (Ne) 20 Helio (He) 5,2 Metano (CH4) 1,2 Criptón (Kr) 1 Hidrógeno (H2) 0,5 Xenón (Xe) 0,08 Dióxido de Nitrógeno (N02) 0,03 Ozono (03) 0,005-0,02 * ppmv = partes por millón en volumen ESTRATOSFERA Es la capa que sigue a la troposfera, extendiéndose desde los 10 Km. de altura media hasta los 45 Km. Está caracterizada por corrientes horizontales y temperatura constante en sentido vertical en el transcurso de una misma estación climática. No obstante, en la zona superior de esta capa se da un gradiente positivo de temperatura de modo que ésta aumenta con la altura hasta alcanzar los 0º C en la zona inferior de la mesosfera. Hacia los 25 Km. de altura se localiza una zona con una concentración de ozono muy superior al resto de la atmósfera (4 ppmv). Se ha calculado que prácticamente la totalidad del ozono atmosférico de origen natural se encuentra concentrado aquí. 7 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS 1.2. CONTAMINACIÓN ATMOSFÉRICA Todos tenemos una idea más o menos clara de lo que significan las palabras contaminación atmosférica. Los habitantes de las grandes ciudades quizás entiendan mejor el término, pues en ciertos días la contaminación se ve, huele, y casi hasta se palpa. Según la Ley 38/1972, de 22 de diciembre, de Protección del Ambiente Atmosférico, actualmente en vigor: Artículo 1º.1: Se entiende por contaminación atmosférica, a los efectos de la citada ley, la presencia en el aire de materias o formas de energía que impliquen riesgo, daño o molestia grave para las personas y bienes de cualquier naturaleza. Cuando algunas sustancias, compuestos o formas de energía se encuentran en el aire en concentraciones o niveles tales que pueden causar daños o molestias a personas, animales, vegetación o materiales se denomina contaminación atmosférica. Esta idea de contaminación enriquece el concepto, ya superado de entender que un contaminante es cualquier sustancia o forma de energía que se encuentra en la atmósfera en cuantía superior a lo normal. Es necesario ligar esto a los efectos del mismo. De estos conceptos se desprende que lo que hoy en día no tiene la consideración de contaminante puede ser calificado como tal a la luz de resultados de estudios científicos, epidemiológicos o de otro tipo actuales y futuros. En el estudio de la contaminación atmosférica es importante, por lo tanto, tener en cuenta que existe un determinado grupo de sustancias que forman parte de la atmósfera de forma natural, las cuales juegan un importante papel en muchos aspectos de la dinámica atmosférica. Las mayoritarias de entre este grupo de sustancias se encuentran implicadas en los denominados ciclos biogeoquímicos. Estos ciclos nos muestran los movimientos de estas sustancias en el seno de los ecosistemas, reflejando las rutas que siguen desde el medio (sea éste aire, agua o suelo) a los organismos y de los organismos al medio. Muchas de estas sustancias y elementos que son componentes habituales de la atmósfera son los que, en concentraciones superiores a las que se reflejan en la tabla 1, consideraremos contaminantes cuando esto pueda suponer daños o riesgos para los seres vivos y bienes. Por lo tanto, la presencia de muchas sustancias en la atmósfera que se pueden considerar contaminantes tienen su origen en fuentes naturales y su evolución está gobernadas por los ciclos biogeoquímicos. 8 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS De los anteriores conceptos se desprende que la contaminación atmosférica y sus efectos nocivos no son un hecho reciente, pues aparte de la debida a fenómenos naturales (fuentes naturales), se tienen datos antiguos sobre la generada por el hombre (fuentes antropogénicas). En el año 1272 el Rey Eduardo I de Inglaterra trató de reducir los efectos del humo en Londres prohibiendo el uso de un tipo de carbón bituminoso, generador de gran cantidad de humos. En esta época y siglos posteriores, también en Inglaterra, se establecieron cánones a actividades generadoras de humos. Napoleón en 1.810, decretó la necesidad de autorización administrativas de las industrias generadoras de malos olores. Posteriormente, el desarrollo industrial, urbano y de los transportes hasta nuestros días, así como los episodios de contaminación urbana o industrial grave (Londres, 1952; Nueva York, 1953/1963; Los Angeles, varios años; Valle de Mosa -Belgica- 1.930; Donora (USA) 1.949, ..) y accidentes industriales (Poza Rica (Méjico) 1.950; Seveso (Italia), 1.976; Bhopal (India) 1.984;...) han aumentado la preocupación y atención mundial por la contaminación atmosférica. En los últimos tiempos esta preocupación se ha centrado más que en episodios de contaminación puntuales, en problemas globales cuyas consecuencias en la actualidad, en gran medida, están en fase de estudio como son el calentamiento de la baja atmósfera y la alteración de la capa de ozono estratosférico. La contaminación atmosférica parece acompañar al hombre y sus actividades, proviniendo la mayor parte de ella de la combustión, la cual es esencial para la vida humana, tal y como la conocemos, y para el nivel de desarrollo de nuestra sociedad, ya que permite la obtención de energía mecánica, luz y calor. Una estimación que proviene de Estados Unidos sitúa en alrededor de 133 millones de toneladas la cantidad de contaminantes de todos los orígenes (exceptuando el dióxido de carbono) emitidos en un año sobre el territorio federal. Alrededor de dos tercios (es decir 90 millones de toneladas) proceden de todos los medios de transporte, que se basan en procesos de combustión. La presencia de los contaminantes en el aire puede ser debida a una liberación singular intensa que desaparece con el tiempo por las corrientes de aire, por reacción química, por precipitación al suelo o por absorción del mar o del suelo, en definitiva, por la acción de los ciclos biogeoquímicos de los elementos que ya hemos visto. Tal puede ser el caso de un incendio, una erupción volcánica, tormentas de polvo, descomposición accidental de materia orgánica, percance industrial, etc., todo lo cual posee el carácter de accidental, pero que no origina una variación apreciable de la contaminación general de la atmósfera, salvo casos singularísimos (se especula sobre la desaparición de los dinosaurios a causa de la contaminación debida al impacto de un meteorito con la Tierra). 9 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS Otro caso diferente lo constituye la generación continua de contaminantes, que pueden originar un efecto local apreciable, como es el caso de concentraciones industriales, ciudades, etc., pero que aisladamente no puede generar una contaminación general apreciable. Por otro lado, la atmósfera, el mar o el suelo, tienen una cierta capacidad de eliminar los contaminantes (regida, en general, por los ciclos biogeoquímicos). Finalmente, se puede dar la circunstancia de acumulación por emisiones continuas o discontinuas en periodos prolongados de tiempo. Esta situación puede dar lugar a contaminaciones apreciables a gran escala, tal es el caso del efecto invernadero o el agujero de ozono. En este caso, aunque localmente no se detecte contaminación apreciable (aunque esto puede ocurrir), se excede la capacidad global de eliminación, detectándose en consecuencia un aumento paulatino del contaminante. El efecto de la meteorología resulta importante y en algunos casos decisivo, pues tanto el viento como la lluvia, la radiación solar o la presencia de vapor de agua pueden afectar directamente la generación, dispersión y eliminación de los contaminantes. Así, con una emisión estacionaria, en una ciudad por ejemplo, en un día lluvioso y ventoso se puede disfrutar de una atmósfera limpia, mientras que tras una temporada de calma anticiclónica y con inversión térmica, la acumulación local puede resultar en una atmósfera altamente contaminada. 1.3. EFECTOS DE LA CONTAMINACIÓN Los efectos nocivos de la contaminación pueden ejercerse directamente (afección por respiración, por ingestión de alimentos contaminados, corrosión de la piedra de monumentos, etc.), o puede originar efectos nocivos de forma indirecta, alterando alguna de las características físicas o químicas de la atmósfera (aumento de rayos ultravioleta por falta de ozono en la estratosfera debido a la presencia de CFC’s, cambio climático por efecto invernadero debido al incremento en la concentración de CO2, etc.). Los efectos de la contaminación pueden tener como consecuencia: Alteración en la salud y confort humano Daños en la vegetación Alteración en la salud animal Desequilibrios en los ecosistemas 10 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS Daños en los materiales Reducción de la visibilidad Cambio climático Por otra parte, todos estos efectos dependerán de: Tipo de contaminante Concentración del contaminante y evolución de ésta Periodo de exposición Sensibilidad de los receptores Sinergias y antagonismos Esta amplitud de factores de los que depende la degradación ambiental nos puede dar una idea de la complejidad en la definición de los diferentes efectos producidos por la contaminación ambiental. En general el estudio para la definición de los efectos provocados por la contaminación atmosférica se encuentran con una serie de dificultades; Los datos epidemiológicos presentan una alta dificultad de interpretación por la variabilidad de situaciones de exposición (Tipo, tiempo, sinergias, receptor,..). Los ensayos en condiciones controladas son costosos y complejos. En muchas ocasiones los datos de estudio provienen de episodios de contaminación accidental o ensayos a altas concentraciones de contaminante (efectos agudos), no contando con información de los efectos crónicos. Por último, las vías de entrada de los contaminantes en el organismo receptor son diversas, siendo muy difícil la diferenciación entre el efecto de la dosis de un contaminante inhalado y la dosis recibida por otras vias (alimento, agua, contacto dérmico,..). Los efectos generales de la contaminación atmosférica sobre el hombre, animales y plantas pueden ser somáticos (alteración de la salud, bioacumulación/biomagnificación) y genéticos (malformaciones, reducción o inhibición fertilidad). No obstante, mayoritariamente, los efectos de los contaminantes atmosféricos en el hombre se manifiestan en problemas en el sistema cardiorrespiratorio y en el caso de animales y plantas, en alteraciones que pueden tener como consecuencia la reducción de la productividad agrícola y ganade- 11 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS ra. Por otra parte, los efectos sobre los materiales van desde el ataque químico (corrosión metálica, mal de la piedra,..) hasta la alteración estética por deposición de partículas. 1.4. CONTAMINANTES Según su naturaleza podemos clasificar los contaminantes atmosféricos como: Físicos: Formas de energía. Por ejemplo: radiactividad, calor, ruido, etc. Biológicos: Entidades biológicas. Por ejemplo:microorganismos, pólenes, etc. Químicos: Sustancias o elementos químicos en forma: ¾ Particulada: Sólidos, líquidos o mixtos ¾ Gaseosa: Gases permanentes a presión y temperatura atmosférica. ¾ Vapor: Fase gaseosa de una sustancia que puede estar simultáneamente en forma de gas y líquido (punto de ebullición < 200º C). En el presente módulo se tratarán los contaminantes químicos. Estos pueden tener diferente origen: Natural: ¾ Actividad biológica ¾ Volcanes ¾ Incendios ¾ Procesos meteorológicos (por ejemplo: rayos) Antropogénico: ¾ Producción de energía ¾ Procesos industriales ¾ Tratamiento de residuos ¾ Actividad agrícola y ganadera. Los contaminantes químicos se pueden dividir, en función del punto de generación, en: 12 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS Contaminantes primarios: Son aquellos que son liberados directamente por el foco emisor. Los más representativos son: ¾ Partículas ¾ Contaminantes azufrados (principalmente SO2 ) ¾ Compuestos inorgánicos de carbono ¾ Contaminantes nitrogenados (principalmente NO y NO2 ) ¾ Hidrocarburos ¾ Compuestos organohalogenados simples ¾ Dioxinas y furanos ¾ Metales ¾ Compuestos halogenados inorgánicos Contaminantes secundarios: Son aquellos que se forman por la interacción química entre contaminantes primarios o éstos y compuestos habituales de la atmósfera, en procesos que puede intervenir la radiación solar. Los más importantes son: ¾ Contaminantes ácidos (ácido sulfúrico y ácido nítrico) ¾ Ozono troposférico (O3 ) ¾ Peroxiacetilnitrato (PAN) y otros contaminantes fotoquímicos. Por otra parte, la vida media estimada de los contaminantes puede darnos una idea de lo reactivo o inerte de los mismos. En el caso de contaminantes gaseosos, cuanto mayor sea su vida media mayor será el tiempo de permanencia en la atmósfera, más lejos podrán ser transportados y a más tiempo de exposición estarán sometidos los organismos y elementos afectados. 1.5. UNIDADES Las unidades más utilizadas en los países europeos para medir contaminantes gaseosos y partículas, son el microgramo o el miligramo por metro cúbico, que indican la masa de contaminante por unidad de volumen. En el caso de los contaminantes gaseosos también se emplean las unidades ppb (partes por billón o milmillonésimas, normalmente referidas a metro cúbico) y ppm (parte por millón o millonésimas, normalmente referidas a metro cúbico) que indican el volumen de contaminante por unidad de volumen. 13 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS La relación entre unas unidades y otras en condiciones de presión y temperatura de 0º C y 760 torr (condiciones reflejadas en la legislación sobre contaminación atmosférica) es la siguiente: mg/m3 de contaminante = ppm de contaminante x peso molecular del contaminante sustancia/22.4 en donde 22,4 es el volumen molar del contaminante en litros en las condiciones referidas. RESUMEN: INTRODUCCIÓN Capas de la atmósfera de interés Troposfera: Desarrollo de la vida y procesos de contaminación Estratosfera: Capa de ozono Contaminación Definición: Según la Ley 38/1972, de 22 de diciembre, de Protección del Ambiente Atmosférico, actualmente en vigor:.Artículo 1º.1: Se entiende por contaminación atmosférica, a los efectos de la citada ley, la presencia en el aire de materias o formas de energía que impliquen riesgo, daño o molestia grave para las personas y bienes de cualquier naturaleza. Combustión: Principal proceso contaminante Efectos de la contaminación Directos o indirectos sobre: ¾ Hombre ¾ Vegetación ¾ Fauna ¾ Materiales Grandes repercusiones sanitarias y económicas 14 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS Tipos de contaminantes Contaminantes primarios: Son aquellos que son liberados directamente por el foco emisor. Contaminantes secundarios: Son aquellos que se forman por la interacción química entre contaminantes primarios o éstos y compuestos habituales de la atmósfera. Unidades empleadas ppm: partes por millón ppb: partes por billón (americano) Mg/m3:miligramo por metro cúbico. µg/m3: microgramo por metro cúbico 15 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS 16 2 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS PARTÍCULAS La presencia de material partículado en la atmósfera se debe a una gran cantidad de procesos naturales o actividades antropogénicas. Estas se consideran como uno de los contaminantes principales de la atmósfera, estando muy reguladas legalmente tanto su emisiones como inmisiones. La gran mayoría de las medidas correctoras respecto a la emisión de contaminantes a la atmósfera tanto en actividades industriales como a producción de energía van encaminadas a la minimización o eliminación de este tipo de contaminación. 2.1 CARACTERÍSTICAS AMBIENTALES Las podemos denominar como una pequeña parte de materia sólida, líquida o mixta. Se forman por procesos de: Rotura Coagulación Condensación Las características fundamentales que van a condicionar sus efectos son: Forma: Puede ser muy variable: ¾ Esférica: líquidos ¾ Fibrilar: por ejemplo. Amianto ¾ Astillada: Polvo de cemento. Composición: ¾ Orgánica: por ejemplo: Hollín, hidrocarburos de quemador de gasoil mal regulado,.. ¾ Inorgánica: por ejemplo: Polvo del viento (silicatos, carbonatos, óxidos, principalmente), cenizas sin resto alguno que no haya sido quemado, aerosoles de ácido sulfúrico,.. ¾ Mixta: por ejemplo: Partículas derivadas de la contaminación urbana. Estas pueden contener: • Material carbonáceo, mayoritariamente grafito. • Oxidos (silicio, aluminio y hierro, principalmente) • Otros compuestos minoritarios como, ozono, H2O2, compuestos orgánicos parcial o totalmente oxidados. 17 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS Tamaño: Las partículas que actúan como contaminante atmosférico suelen presentar un tamaño comprendido entre 10-1 y 103 µm, si bien por encima de las 100 µm la velocidad de sedimentación se hace ya elevada, alcanzando un tiempo de residencia en la atmósfera muy bajo: ¾ Las partículas comprendidas entre 10-1 y 10 µm tienden a formar suspensiones mecánicamente estables, por lo que se conocen como “materia en suspensión”, y son las que, de modo general y especialmente las más pequeñas, constituyen los aerosoles (dispersiones de sustancias sólidas o líquidas en el aire). Los aerosoles en cuya composición predominan las sustancias líquidas se conocen específicamente como nieblas: fina (<1 µm de diámetro) o gruesa (1 - 10 µm de diámetro). Las partículas de menos de 10-1 µm experimentan un movimiento browniano, el cual se debe al desequilibrio de presión en una partícula pequeña por colisiones de moléculas del fluido en el que está inmersa y una difusión molecular apreciable, lo que da lugar a una velocidad de sedimentación muy baja. Cuando las condiciones son favorables, los movimientos al azar que se producen implican choques entre ellas, los cuales pueden generar agregados en un proceso que se denomina coagulación. ¾ Las partículas de tamaño superior a 10 µm, permanecen en el aire suspendidas mucho menos tiempo, por lo que se han catalogado como “partículas sedimentables”. Por esta razón, los efectos de estas partículas se dejan sentir con mucha mayor incidencia en las proximidades del punto donde se producen. En la tabla 1 se recogen las velocidades de sedimentación de las partículas en función de sus distintos diámetros aerodinámicos. TABLA 1. VELOCIDAD DE SEDIMENTACIÓN DE PARTÍCULAS DIÁMETRO AERODINÁMICO (µm) VELOCIDAD DE SEDIMENTACIÓN (cm/s) 0,1 4,0 · 10-5 1 4,0 · 10-3 10 0,3 100 30 Su origen condicionará características fundamentales respecto a sus efectos ambientales como son la forma, composición y tamaño. 18 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS 2.2 FUENTES Se estima que la presencia de partículas en el medio ambiente atmosférico es de origen natural en un 80/90% y antropogénico en un 10/20%, siendo los siguientes procesos y actividades los responsables. Naturales: ¾ Polvo del viento ¾ Aerosol marino ¾ Volcanes ¾ Incendios... Antropogénicas: ¾ Industria: principalmente siderurgia y fabricación de cemento. ¾ Producción de energía (móvil y fija) ¾ Aerosoles como contaminantes secundarios. 2.3 EVOLUCIÓN Y DESTINO Las partículas permanecerán en la atmósfera durante periodos más o menos prolongados en función de características internas (forma, tamaño, peso,..) y externas (condiciones meteorológicas). Su destino posterior será la deposición en el suelo en las proximidades del foco o a largas distancias. Esta deposición puede ser seca o húmeda. La deposición seca, mediante procesos de : ¾ Sedimentación: por gravedad ¾ Impactación sobre objetos y caída ¾ Difusión. La deposición húmeda (más eficaz) por: ¾ Incorporación a las nubes y posterior caída. ¾ Arrastre por lluvia 19 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS 2.4 EFECTOS En lo que se refiere a los efectos que pueden producir, hay algunas de sus características físicas muy determinantes. Uno de los primeros factores a considerar es su TAMAÑO, pues del mismo dependerá su facilidad de penetración en las vías respiratorias. Otro factor es la FORMA, la cual es muy constante en el caso de las sustancias líquidas y bastante más variable en el caso de las sólidas. La COMPOSICION QUIMICA es también muy crítica para los efectos que va a producir cierto aerosol, pero es un parámetro mucho más variable y depende en gran medida de su origen. La composición química de las partículas puede darles carácter de inerte, toxicidad propia o, incluso, a veces los componentes de las partículas pueden actuar de catalizadores en la transformación de unos contaminantes a otros (por ejemplo: paso de S02 a H2SO4). Efectos sobre el hombre. Las partículas que forman los aerosoles penetran en el cuerpo humano a través de las vías respiratorias, dependiendo los efectos que ejerzan de su tamaño y composición química. Las partículas superiores a 5 µm de diámetro quedan retenidas en la cavidad nasal (pelo y mucosas) o en la mucosa de la tráquea. Las comprendidas entre 0.5 y 5 µm de diámetro pueden penetrar hasta las vías inferiores, depositándose en los bronquios y bronquiolos. De este punto son eliminadas a las pocas horas mediante expectoración tras la acción del epitelio vibrátil cuyos cilios ayudan a este proceso o envían a estas partículas a la laringe y de ahí pueden acabar en el estómago. Las partículas de diámetro inferior a 0.5 µm son las que representan un riesgo mayor, puesto que se depositan en los alvéolos pulmonares de donde es difícil eliminarlas al carecer éstos de cilios y mucosas. De esta forma, pueden permanecer durante largos períodos de tiempo ejerciendo su acción tóxica provocando cuadros de bronquitis crónica caracterizados por flemas, exacerbación de catarros y dificultades respiratorias. En los alvéolos también pueden ser atrapados por fagocitos y terminar en el torrente sanguíneo. La concentración de este tipo de contaminantes a partir de la cual se producen efectos sobre la salud humana no es constante, puesto que las características físicas y químicas de las partículas, la presencia de otros contaminantes que puedan dar lugar a efectos sinérgicos, o las características del receptor (edad, fisiología, etc.) pueden hacer variar significativamente estos límites. 20 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS Efectos sobre la flora. Las partículas provocan una reducción de la actividad fotosintética en las plantas, pues reducen la cantidad de energía luminosa disponible al provocar el ennegrecimiento de las hojas sobre las que se depositan. Además de este efecto, pueden obturar los orificios de los estomas, a través de los cuales las plantas intercambian gases con la atmósfera, esencial para desarrollar procesos como fotosíntesis y respiración. Efectos sobre la fauna. En principio, los principales efectos conocidos vendrán afectados por los mismos factores de tamaño y composición que en el caso del hombre. Efectos sobre los materiales. Además de provocar alteraciones estéticas a causa de su deposición sobre los materiales, en muchos casos la composición química de las partículas depositadas acelera los procesos de corrosión, debido a que favorecen la presencia de humedad en los materiales, facilitan la formación de ácidos y otros procesos físicos. Efecto global. Uno de los efectos más importantes de las partículas es la disminución de la visibilidad. Se calcula entre un 15 y un 20% de disminución de radiación solar recibida en los núcleos urbanos frente a los rurales. Esta reducción de la visibilidad es debida a procesos de extinción y dispersión de la luz. Por otra parte, el aumento de partículas en la atmósfera puede ocasionar un descenso térmico de la atmósfera inferior 21 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS RESUMEN: PARTÍCULAS Características de interés Estado: Liquidas, sólidas o mixtas Composición: Orgánicas o inorgánicas Tamaño: En suspensión (0.1-10 µm: aerosoles) o sedimentables (>10µm) Fuentes mas importantes Naturales: 80/90% Antropogénicas: 20/10% ¾ Siderurgia y cementeras ¾ Producción de Energía Evolución y destino Permanencia en la atmósfera según características externas (meteorología) e intrínsecas (forma, tamaño y peso) Caída al suelo mediante deposición seca o húmeda (más eficaz) Efectos mas importantes Hombre: Patologías respiratorias. Flora: Inhibición de la fotosíntesis Materiales: Degradación estética y y facilita la corrosión Global: Disminución de la visibilidad 22 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS 3 COMPUESTOS AZUFRADOS El principal contaminante azufrado es el dióxido de azufre (SO2). Este gas se origina mayoritariamente por procesos antropogénicos relacionados con la combustión de combustibles fósiles, principalmente para la producción de energía en las grandes instalaciones fijas de combustión. Este gas contribuye de una manera importante a la generación de la lluvia ácida. 3.1 CARACTERÍSTICAS ÓXIDOS DE AZUFRE El SO2 es un gas incoloro, más pesado que el aire (2.2 veces) a pesar de lo cual se desplaza rápidamente en la atmósfera a grandes distancias. Es, así mismo, muy estable y reductor, oxidándose a SO3. El SO3, sin embargo, es un gas muy reactivo que condensa fácilmente, características que explican su baja presencia en la atmósfera. Las cantidades de SO3 que se forman cuando las condiciones son adecuadas, reaccionan fácilmente con el agua presente dando como resultado SO4H2. SULFURO DE HIDRÓGENO Este es un gas de olor desagradable, presente en la atmósfera de forma natural en una concentración muy baja. Su origen natural se debe a degradaciones por tiobacterias de materia orgánica, volcanes, incendios, etc. 3.2 FUENTES ÓXIDOS DE AZUFRE La mayor parte de las fuentes energéticas de la actualidad están basadas en combustibles fósiles (carbones de distintas calidades, petróleo, aceites minerales, etc.) los cuales tienen en su composición una determinada cantidad de azufre (hasta un 6% en peso). Este azufre es liberado a la atmósfera en forma de óxido, primordialmente como SO2 y SO3, en cantidades anuales del 23 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS orden de millones de toneladas. Existen otras fuentes generadoras de estos compuestos, tanto de origen antropogénico, como natural (volcanes, incendios, océanos y zonas pantanosas). Los principales procesos antropogénicos de emisión de óxidos de azufre a la atmósfera son combustión fija (aprox. 73%) y la industria (aprox. 20%). como la química, refinerías, siderometalurgía, papel Por último, se estima que el transporte contribuye en un 3 % a las emisiones totales de estos gases. SULFURO DE HIDRÓGENO Las emisiones antropogénicas de este gas son minoritarias respecto a las fuentes naturales. Ente estas están procesos de combustión inadecuados, la industria siderometalúrgica, refinerías, papel o procesos naturales derivados de actuaciones humanas (vertederos, estaciones depuradoras, pantanos,..). En el caso de las refinerías de crudo, asociados a este compuesto se suelen encontrar mercaptanos, compuestos de sustitución de los átomos de azufre por cadenas hidrocarbonadas. Estos compuestos presentan un olor característico, intenso y, también, muy desagradable. 3.3 EVOLUCIÓN Y DESTINO ÓXIDOS DE AZUFRE El SO2 es un gas muy estable, teniendo una vida media en la atmósfera de 5 días. La evolución de SO2 a SO3 tiene un mecanismo de oxidación que implica una activación fotoquímica que excita la molécula de SO2 para que pueda combinarse con una molécula de oxígeno, siendo esta oxidación más intensa en medio húmedo que seco. La formación del ácido depende de la existencia de núcleos de condensación, generalmente aerosoles con contenido en metales, que catalicen la reacción final. Este proceso está controlado por el pH, de modo que cuando éste excede de cierto valor se para la reacción. El problema surge cuando existen concentraciones apreciables de algún compuesto que tampone el medio (caso del amoníaco), pues eso provoca una estabilización del pH en valores que no paralizan el proceso de generación de ácido sulfúrico. Este ácido en condiciones adecuadas puede producir sulfato amónico (NH4HSO4), que puede formar aerosoles, siendo su destino final, como en el caso de las anteriores formas de azufre, la deposición seca o húmeda en el suelo. 24 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS SULFURO DE HIDRÓGENO La vida media del sulfuro de hidrógeno en la atmósfera es de horas y su evolución típica es la oxidación (generalmente con O3) a SO2 de forma lenta (fase gaseosa) o rápida (vía partículas). 3.4 EFECTOS OXIDOS DE AZUFRE Efectos sobre el hombre. Existe una clara relación entre las enfermedades respiratorias del tracto superior y niveles de SO2. A causa de su inhalación se puede desencadenar un proceso de broncoconstricción transitoria en el tracto respiratorio superior. Se considera como un irritante de mediana potencia del aparato respiratorio. Este se manifiesta como fuertemente irritante en concentraciones superiores a 8.000 µg/m3 (la concentración de SO2 en las zonas urbanas es del orden de 25 a 500 µg/m3), peligrosidad que aumenta al actuar en combinación con otros contaminantes y con la humedad. El aumento por encima de las concentraciones medias de 700 µg/m3 en dos horas y 400 µg/m3 en doce horas provoca irritación sobre los ojos y problemas respiratorios, constituyendo pues un riesgo para las personas normales, acentuándose este riesgo en el caso de personas asmáticas, las cuales son más sensibles. Hay que considerar que los sulfatos (fundamentalmente de amonio) y el ácido sulfúrico se presentan habitualmente en partículas de diámetro inferior a 1 µm, tamaño que permite su llegada hasta las vías respiratorias inferiores. En estas circunstancias, es posible que una vez inhaladas permanezcan en los pulmones durante periodos largos de tiempo. El ácido sulfúrico presenta un poder de irritación mayor que los sulfatos, afectando especialmente a los ancianos, enfermos cardiopulmonares crónicos, asmáticos y niños sensibles. Los efectos crónicos de la exposición a SO2 y sulfatos se evidencian en estudios de mortalidad, observándose un mayor número de muertes tempranas asociadas a enfermedades pulmonares y cardiovasculares. Por ejemplo, los aumentos significativos de ácido sulfúrico y de sulfatos fueron los causantes de los episodios de Londres y Donora, con aumento significativo de muertes por bronquitis, neumonías y enfermedades cardiacas. Al ser el ácido sulfúrico higroscópico, llega a formar del orden del 20% de las partículas del aire urbano. De hecho la mayoría de la neblina urbana 25 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS es debida a la formación de aerosoles resultantes de las reacciones combinadas del SO2, las partículas, los óxidos de nitrógeno y los hidrocarburos, contribuyendo así notablemente a la contaminación del aire. La humedad favorece la formación de aerosoles en los que participan compuestos sulfurados de forma notable. Una fracción importante de los sulfatos e ion sulfato presentes en el aire urbano forman gotas de 0,2 a 0,9 µm, contribuyendo sustancialmente a la reducción de la visibilidad. Efectos sobre la flora. Los efectos provocados por el SO2 (sustancia a la que las plantas se muestran especialmente sensibles) a consecuencia de procesos agudos de exposición tienen síntomas muy característicos, que en el caso de las hojas, se manifiestan como manchas iniciales que pueden desembocar en necrosis de los tejidos. En los casos crónicos, las hojas adoptan una coloración amarillo-rojiza. El mecanismo de la toxicidad de este compuesto en los vegetales es en gran medida desconocido. Es probable, sin embargo, que esta toxicidad se deba mucho más a sus propiedades óxidoreductoras que a su acidez. El comportamiento de las diferentes especies vegetales ante la acción de esta toxicidad es muy variable. Existe gran diferencia respecto a la sensibilidaad de las plantas a este compuesto. Los musgos y líquenes son muy sensibles seguidos de coníferas y herbáceas. Por último árboles de hoja caduca presentan menor sensibilidad. Esta noción tiene un interés extremo cuando se trata de saber qué tipo de cultivo o de vegetación debe plantarse en una zona industrial. Efecto sobre los materiales. Los efectos de los óxidos de azufre sobre los materiales principalmente son: ¾ Corrosión metálica: debida fundamentalmente a la formación de ácido sulfúrico o sulfuroso, especialmente en ambiente húmedo y a temperaturas ambientales cálidas. ¾ Ataque de los materiales de construcción, formando sulfatos, que lava la lluvia. ¾ Deterioro de fibras sintéticas, plásticos en general, cuero, etc. 26 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS RESUMEN: CONTAMINANTES AZUFRADOS Características de interés El dióxido de azufre es estable y sufre en la atmósfera grandes desplazamientos El trióxido de azufre es muy reactivo, presenta baja presencia en la atmósfera Fuentes más importantes En general, más del 90% de los óxidos de azufre se emiten como dióxido de azufre. Su principal origen son los procesos de combustión para la producción de energía mediante combustibles fósiles, que pueden llega a contener hasta un 6% de azufre en su composición (especialmente carbones). La combustión en instalaciones fijas son la principal fuente (73%), el transporte (focos móviles) supone el 3% y la industria el 20% aproximadamente. Evolución y destino El dióxido de azufre es estable, permanece durante periodos, que pueden ser importantes, en la atmósfera. Su evolución posterior es la oxidación a trióxido de azufre y formación de ácido sulfúrico en condiciones adecuadas. Por último éste puede producir sulfato amónico en presencia de amoniaco en la atmósfera. Acido o sulfatos pueden formar aerosoles, siendo su destino final la deposición, seca o húmeda en el suelo. Efectos mas importantes Hombre: Afecciones respiratorias, con mayor efecto en grupos de riesgo (niños, ancianos asmáticos o personas con otros problemas cardiorrespiratorios) Vegetación: Alta sensibilidad, especialmente musgos, líquenes y coníferas. Materiales: Corrosión metálica y ataque a materiales de construcción y fibras sintéticas. Global: Reducción de la visibilidad por formación de aerosoles 27 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS 28 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS 4 COMPUESTOS INORGÁNICOS DE CARBONO Los compuestos inorgánicos de carbono que se van a estudiar son el dióxido y monóxido de carbono. El primero aunque es un gas esencial para la vida, como consecuencia de la combustión de productos fósiles para la generación de energía, está incrementándose paulatinamente en la atmósfera lo que puede tener como consecuencia el aumento del efecto invernadero con efectos todavía en gran medida impredecibles. El monoxido de carbono se genera también en procesos de combustión. En este caso combustión incompleta de sustancias orgánicas. Por su alta toxicidad y cantidades emitidas (principalmente por el transporte) se le podrían presumir unos efectos muy evidentes, no obstante por su rápida dispersión y procesos de oxidación hacen que en general las concentraciones en inmisión no tengan consecuencias negativas. 4.1 CARACTERÍSTICAS ANHÍDRIDO CARBÓNICO (CO2) El dióxido de carbono es un gas esencial para la vida, es emitido y absorbido por las plantas (en el proceso de la fotosíntesis) y emitido por los animales (respiración). Es un gas incoloro e inodoro, no tóxico y más denso que el aire. Es muy soluble por lo que la gran reserva de este gas se encuentra en los océanos. Está presente en la atmósfera en un valor de concentración que actualmente es de unas 350 ppmv, mientras que era del orden de 280 ppmv antes de la revolución industrial, y continúa aumentando a un ritmo de 0.5% anual. En principio cabría pensar que no debería ser considerado como contaminante al no ser tóxico. Sin embargo, el desequilibrio inducido en su ciclo por la actividad humana tiene consecuencias negativas, como es el calentamiento global. Por lo tanto, se trata de un gas esencial para la vida, pero cuya superabundancia le hace tener que ser considerado un contaminante. MONÓXIDO DE CARBONO (CO) 29 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS Es un gas ligero (densidad, 96.5% de la del aire). Además, presenta una escasa solubilidad en agua y es inflamable. Es un gas incoloro e inodoro y fuertemente tóxico, pero que en la atmósfera se encuentra, generalmente, en concentraciones lo suficientemente bajas para que no manifieste este carácter. Su presencia natural en la atmósfera del hemisferio norte es sobre 230 µg/m3 y 60 µg/m3. Constituye el contaminante de mayor abundancia en la capa más baja de la atmósfera, sobre todo en el entorno de las grandes ciudades 4.2 FUENTES DIÓXIDO DE CARBONO (CO2) Las fuentes naturales son primordialmente las plantas, incendios y los volcanes, mientras las antropogénicas están constituidas por los procesos de combustión de combustibles fósiles y de la madera. Por otra parte, la deforestación tiene como consecuencia la mayor presencia de este gas en la atmósfera por reducción de su consumo (menor fotosíntesis) e incremento de su emisión (combustión o descomposición de la madera). El CO2 es el producto final de toda combustión completa. El aprovechamiento de la energía contenida en los combustibles fósiles se basa en un proceso de combustión, que es irreversible, en el que se genera CO2, tal y como muestra la reacción global e ideal siguiente: CnHm + (n+n/4)(O2 + 3,76 N2) → nCO2 + (m/2)H2O + 3,76 (n+m/4)N2 así como otros contaminantes (CO, SO2, NO, NO2, hidrocarburos inquemados, ...). De este modo los principales focos emisores antropogénicos son procesos de producción de energía, basados en la combustión: Industrial: ..…………..22 % Urbana: Transporte…………...25 % Centrales Térmicas…30 % ……………20 % 30 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS MONÓXIDO DE CARBONO (CO) Su origen natural se debe a procesos de combustión u oxidación de hidrocarburos (metano, terpenos, etc.). En general, la presencia de este gas por procesos antropogénicos, es el producto de la combustión incompleta de sustancias orgánicas, lo cual tiene lugar siempre que la cantidad de oxígeno en la combustión sea insuficiente Los principales focos antropogénicos emisores de CO son el transporte (aprox. 75%), la industria (15 %) y centrales térmicas (aprox. 4%). En las ciudades se pueden alcanzar concentraciones de 5 a 20 ppmv donde el foco principal lo constituyen los tubos de escape de los automóviles, pues expulsan gases con un contenido de CO que puede alcanzar el 10%. Otras fuentes (minoritarias) de CO en la atmósfera son: Reacción a elevada temperatura entre el CO2 y materiales de carbono. Disociación del CO2 a altas temperaturas. Oxidación del metano en la atmósfera. Procesos de producción y degradación de la clorofila en las plantas 4.3 EVOLUCIÓN Y DESTINO DIÓXIDO DE CARBONO La evolución y destino de dióxido de carbono va marcada por el ciclo del carbono, que de forma muy simple se describe a continuación. En la naturaleza encontramos CO2 gas tanto libre en la atmósfera (en una cantidad aproximada de 700 · 109 toneladas) como disuelto en los mares (50.000 · 109 toneladas). Las plantas utilizan este CO2 para sintetizar compuestos orgánicos, los cuales pasan también a los organismos que se alimentan de estas plantas. El ciclo se cierra mediante procesos como la respiración de los organismos, la descomposición de la materia orgánica y la combustión de materiales orgánicos. 31 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS Este ciclo tiene la particularidad de mover una cantidad de elemento que no es ni con mucho cercana a la total, puesto que existen diversos puntos en el mismo donde se acumulan cantidades importantes (acumulaciones de restos vegetales y animales que terminan transformados en humus, carbón, petróleo y otros hidrocarburos fósiles). La utilización masiva de estos combustibles está lanzando a la atmósfera cantidades importantes de CO2, sin que se sepa hasta el momento el efecto que ésta dinámica puede causar en este ciclo y el resto de los ciclos biogeoquímicos. ONÓXIDO DE CARBONO (CO): En la atmósfera el CO se fotooxida por ataque de un radical hidróxilo (OH), formando la molécula más estable del dióxido de carbono: CO + OH + hv → CO2 + H* La velocidad de esta oxidación es muy lenta, por lo que se observan vidas medias del orden de 2 a 4 meses. 4.4 EFECTOS DIOXIDO DE CARBONO (CO2) Es de destacar su participación en el efecto invernadero como uno de los gases que absorben la radiación infrarroja reflejada por la superficie terrestre. Aunque en este proceso participan otros gases que se estudiarán en otros grupos de contaminantes, se comenta este efecto en el presente capítulo por ser el CO2 el principal responsable. Efecto invernadero. Los rayos luminosos procedentes de la radiación espontánea del Sol al llegar a la Tierra atraviesan la atmósfera, que es sustancialmente transparente a ellos e interaccionan con la materia. Parte de esa radiación, del orden de un 30%, se devuelve al espacio, es decir, se refleja. El 70% restante, después de numerosas interacciones, calienta la materia. La materia emite a su vez energía, pero siempre a longitudes de onda superiores, en la franja del visible e infrarrojo. 32 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS En las capas bajas de la atmósfera existen gases que absorben la radiación infrarroja convirtiéndola en calor, por lo que ésta no se emite fuera de la Tierra. Así se forma una capa protectora del calor que origina temperaturas templadas en la superficie terrestre, al impedir su enfriamiento. Este efecto es el equivalente al utilizado en los invernaderos, pues se interpone entre el Sol y las plantas una capa de vidrio o de plástico, que son transparentes a la radiación visible y opacos al infrarrojo. El calentamiento medio supuestamente debido a este fenómeno es de unos 33º C, por lo que la temperatura media en la superficie de la Tierra es 15º C en lugar de –18º C. Ni el oxígeno ni el nitrógeno absorben la radiación infrarroja de la atmósfera, pero sin embargo otros constituyentes sí lo hacen, entre los que destacaremos el vapor de agua, el dióxido de carbono, el metano, el protóxido de nitrógeno, el ozono y los CFC’s. La concentración de estos gases (a excepción del vapor de agua) no ha hecho mas que aumentar recientemente, por lo que este efecto puede estar incrementándose paulatinamente. La tabla muestra los ritmos de crecimiento medio anual: TABLA 3: AUMENTO ANUAL MEDIO DE CONCENTRACIÓN DE LOS GASES DEL EFECTO INVERNADERO GAS AUMENTO ANUAL MEDIO DE CONCENTRACIÓN CO2 0,5% CH4 0,9% N2O 0,25% CFC’s 4% La eficacia de cada uno de estos gases en el efecto invernadero es distinto, así el CH4 es 60 veces más absorbente que el CO2 y los CFC’s son del orden de miles de veces más absorbentes que el CO2. La tabla muestra la contribución relativa de cada uno de ellos, determinada en 1990, a excepción del agua. 33 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS TABLA 4 CONTRIBUCIÓN RELATIVA DE CADA GAS CON EFECTO INVERNADERO APRECIABLE GAS CONTRIBUCIÓN CO2 53 - 535% CH4 13 - 15% N2O 7 - 4% CFCs 20 - 21% O3 troposférico 2% Otros 3% La minimización en las emisiones de CO2, N2O y O3 troposférico vienen de reducir la deforestación, utilizar eficientemente la energía proveniente de la combustión o recurrir a energías alternativas con emisiones nulas. El metano proviene primordialmente de fermentaciones naturales, pero éstas aumentarían si aumentase la temperatura con el efecto invernadero, por lo que su control no parece sencillo. La limitación en el uso de los CFC’s parece necesaria por que además presenta un efecto añadido, la destrucción de la capa de ozono. ¿Cuáles serían las consecuencias de un aumento del efecto invernadero? No se tiene certeza, pues existen muchas ligaduras a nivel global en este problema. Se especula con la posibilidad de incremento del nivel del mar, cambios en los ecosistemas, cambio de la distribución geográfica de enfermedades, etc. Muchos de estos posibles efectos están basados en modelos todavía no muy refinados. Por ejemplo, un aspecto relevante ligado al calentamiento global es el nivel de los mares, el cual puede subir por efecto de la dilatación térmica del agua y por la eventual fusión de los hielos. Esta fusión no es necesariamente una consecuencia directa del calentamiento, pues éste se puede traducir en mayores precipitaciones en las zonas polares y por una mayor evaporación del agua en las zonas cálidas, aumentando con ello su capacidad de almacenamiento. La evaporación mas intensa del agua puede conducir a una humedad ambiente y nubosidad mayores y ello traer efectos de realimentación positiva, como sería el aumento del efecto invernadero inducido por el vapor de agua o una realimentación negativa, como una reflexión de la radiación solar mayor por las nubes. Por otro lado, los estudios más cuidadosos sobre la evolución de la temperatura medida en la superficie indican un calentamiento del orden de 0,5º C en el último siglo. Esto puede significar una tendencia al calentamiento o simplemente una parte de un ciclo oscilatorio natural, por lo que 34 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS no se pueden extraer conclusiones extrapolables hacia el futuro. Adicionalmente, no solo resulta importante la evolución de la temperatura media del planeta, sino la regional, es decir la distribución regional de esa temperatura. Las ligaduras físicas y/o químicas de interés para la evaluación del cambio climático global y regional son complejas y actualmente muchas de ellas mal conocidas. Una observación mas detallada de la Tierra, principalmente mediante satélite, puede aportar los datos necesarios para poder acometer en el futuro modernizaciones, conducentes a predicciones, de validez. MONÓXIDO DE CARBONO (CO) Efectos sobre el hombre. Debido a su densidad, la emisión a nivel del suelo de CO (tubos de escape) facilita su dispersión rápida en el aire, así como el calentamiento del aire en la zona debido al movimiento de los vehículos. De este modo, su presencia a cierta altura es bastante escasa disminuyendo sus efectos negativos, a excepción de individuos que estén trabajando en la vía pública o los peatones. A este nivel, se pueden medir valores instantáneos de hasta 200 mg/m3. Los valores medios en una ciudad con alta densidad de tráfico es de 5-25 mg/m3. Su fácil dispersión, junto con los procesos de oxidación, que son superiores en las capas altas de la troposfera (tropopausa) tiene como resultado que, pese a la elevada aportación anual de CO a la atmósfera, no se detectan los aumentos de concentración correspondientes. El CO es el producto de contaminación más importante en las zonas de denso tráfico. Desde el punto de vista sanitario, el CO se combina con la hemoglobina de la sangre formando carboxihemoglobina que ocasiona una reducción en el transporte de oxígeno a los tejidos. Esta circunstancia se debe a que la afinidad de la hemoglobina por el CO es 250 veces superior a la que presenta por el oxígeno. Esta situación puede provocar (si la saturación no sobrepasa el 10%, por encima de este nivel produce alteraciones más graves, incluso la muerte) trastornos psicomotores que se manifiestan como síntomas de cansancio, cefaleas y alteraciones de la coordinación. Cuando la saturación no es superior a un 5%, se producen alteraciones de la función cardíaca y pulmonar y se aumenta el umbral visual. Este tipo de afecciones comienzan con concentraciones en aire de 100 mg/m3. La carboxihemoglobina formada es reconvertida espontáneamente en un 50% a oxihemoglobina en un período del orden de 3 a 4 horas. 35 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS Efectos sobre la flora. En general, las especies vegetales son poco sensibles a esta sustancia. No obstante, a altas concentraciones de CO (por encima de 150 mg/m3) se detectan trastornos respiratorios con caída generalizada de las hojas, acarreando en ocasiones la muerte de la planta. Se cree que el mecanismo de acción afecta directamente a las hormonas del crecimiento. RESUMEN: COMPUESTOS INORGÁNICOS DE CARBONO Características de interés El dióxido de carbono es un gas esencial para la vida, pero su incremento en la atmósfera puede producir un aumento del efecto invernadero. El monóxido de carbono en un gas ligero y muy tóxico Fuentes mas importantes Las fuentes más importantes antropogénicas de estos gases (minoritarias frente a las naturales) son los procesos de combustión de combustibles fósiles y madera, en general materia orgánica.. ¾ El dióxido de carbono es el producto final de toda combustión completa. ¾ El monóxido de carbono es producto de una combustión incompleta La producción de energía en centrales térmicas es el principal foco de emisión del dióxido de carbono y el transporte en el caso del monóxido de carbono. Otros focos son combustiones en diferentes industrias o actividades domésticas Evolución y destino Dióxido de carbono: ciclo del carbono Monóxido de carbono: Oxidación lenta por ataque de radical hidróxilo, formando dióxido de carbono. No obstante presenta una vida media prolongada (3 meses aprox.) Efectos más importantes Dóxido de carbono: Incremento del efecto invernadero. Monóxido de carbono: Alta toxicidad por inhibición del transporte de oxígeno a los tejidos al formar carboxihemoglobina en la sangre. 36 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS 5 COMPUESTOS NITROGENADOS Los principales contaminantes nitrogenados son el monóxido y dióxido de nitrógeno, emitidos mayoritariamente por procesos de combustión a altas temperaturas (transporte y otros procesos de producción de energía). Estos compuestos intervienen en la producción de lluvia ácida, generación de contaminantes fotoquímicos (secundarios) además de presentar toxicidad propia, afectando al sistema inmunitario y respiratorio. Otros compuestos nitrogenados emitidos directamente por focos contaminantes son el amoniaco y ácido nítrico, pero éstos, en general se emiten de forma menor y localizada, manifestando sus efectos en las proximidades del foco. 5.1 CARACTERÍSTICAS ÓXIDOS DE NITRÓGENO (NOX) De las siete formas oxidadas que presenta el N en la atmósfera, solamente tres de ellas, el N2O, el NO y el NO2, tienen cierto interés medioambiental. Las restantes formas no están ausentes totalmente, sino que se mantienen en equilibrio con éstas pero en proporciones muy bajas. El N2O es un gas incoloro, no tóxico y con presencia alta en la troposfera de forma natural (570 µg/m3) como consecuencia de procesos biológicos de nitrificación y desnitrificación. El NO y el NO2 conjuntamente se conocen como NOX. El NO es un gas incoloro e inodoro, mientras que el NO2 es pardo rojizo y de olor muy asfixiante. Ambos son gases tóxicos. Son muy reactivos y su presencia en la atmósfera, en parte por esto, es baja, de 0.05 a 30 µg/m3. ÁCIDO NÍTRICO Como contaminante primario presenta un carácter muy local, pues sólo aparece en las proximidades de las instalaciones industriales que lo consumen o fabrican. Fuera de estas zonas, y a salvo de accidentes en estas plantas in- 37 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS dustriales, no se suele considerar como un parámetro importante dentro de la contaminación atmosférica. AMONIACO Es un gas incoloro de olor característico, poco tóxico. Es un compuesto que se encuentra de forma natural en concentraciones bajas en la atmósfera (0.1 µg/m3 aire marino y 4 aire continental). 5.2 FUENTES ÓXIDOS DE NITRÓGENO N2O: Su emisión principal es aquella derivada de proceso naturales (procesos de combustión y nitrificación/desnitrificación). Aquella derivada de actividades antropogénicas es, principalmente, como consecuencia de procesos de combustión y la utilización masiva de fertilizantes nitrogenados. NOX: De forma natural se producen en las tormentas (rayos), incendios, erupciones volcánicas y procesos de nitrificación/desnitrificación. El origen antropogénico más habitual es la oxidación del nitrógeno del aire en los procesos de combustión a temperaturas elevadas. Los motores de combustión interna son la fuente de estos compuestos más importante en las ciudades, recayendo en los motores Diesel, por su mayor cubicaje, la producción mayoritaria. El transporte se estima que emite un 45 % de los NOx antropogénicos, otras actividades de producción de energía el 30 % y la industria (siderurgia, fertilizantes, explosivos, cemento, refinerías, etc.) un 15%, el resto, actividades agrícolas y otros. En la formación de estos compuestos en procesos de combustión tienen importancia los siguientes parámetros: ¾ Temperatura: Por encima de 1.500º C se dispara su formación ¾ Oxígeno/combustible: El combustible es más ávido por el oxígeno que el nitrógeno, por ello si la combustión se produce con una relación adecuada oxígeno/combustible la producción de NOx será menor. ¾ Tiempo: La formación de NOx es más lenta que el proceso de combustión, si el enfriamiento de los gases de combustión es rápido, menor será la producción de estos compuestos. 38 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS La emisión de estos compuestos suele ser mayoritariamente en forma de NO y un porcentaje menor (menos del 10%) como NO2. ÁCIDO NÍTRICO Su emisión directa se debe a ciertas actividades industriales como la fabricación del mismo, ciertos fertilizantes, etc. AMONIACO Su presencia suele estar asociada a ciertos procesos biológicos (descomposición de la materia orgánica, excreción animal, etc.). Los índices de concentración altos, sin embargo, suelen ser muy ocasionales pues se asocian a escapes o accidentes en las plantas industriales donde se emplea o se fabrica. Actividades que pueden emitir o favorecer la emisión de este gas son la fabricación de ácido nítrico, fabricación y uso de fertilizantes nitrogenados, depuradoras de aguas residuales, vertederos y ganadería intensiva. 5.3 EVOLUCIÓN Y DESTINO ÓXIDOS DE NITRÓGENO N2O: La vida media en la atmósfera de N2O es de 30 años. Este gas en las capas bajas de la atmósfera (principalmente, estratosfera) puede oxidarse formando NOx. NOx: La producción de estos compuestos suele ser mayoritariamente en forma de NO y un porcentaje menor como NO2. El NO se oxida a NO2 por procesos termoquímicos (en foco) o fotoquímicos (atmósfera) La vida media de los NOx es corta, aproximadamente un día y su evolución típica es la formación de ácido nítrico y paso a nitrato amónico, finalmente deposición seca o húmeda. ÁCIDO NÍTRICO 39 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS El ácido nítrico se encuentra en la atmósfera en forma aerosoles que se depositarán en el suelo mediante un proceso seco o húmedo. AMONIACO La vida media del amoniaco en la atmósfera es de 5 días y su evolución es la de formación de amonio (NH4+) en superficies húmedas o su deposición como tal, produciéndose en el suelo procesos de nitrificación. En condiciones adecuadas puede reaccionar en fase gas o condensado con ácidos para generar nitrato y sulfato amónico formando aerosoles. 5.4 EFECTOS N2O: Su principal importancia medioambiental es como consecuencia de la formación de otros óxidos de nitrogeno (NOx) por procesos de oxidación en la estratosfera y troposfera. Por otra parte, como se vio en el capítulo correspondiente, se estima que contribuye al efecto invernadero en un 7%. NOx: Son compuestos muy tóxicos, más incluso que el CO, pero las concentraciones a que se desarrollan en las ciudades no son suficientes para desencadenar efectos de consideración. Sin embargo, su participación en la formación de diversos contaminantes secundarios es lo que les hace acreedores de nuestra atención como contaminantes atmosféricos. Uno de estas contaminaciones es la generación de ácido nítrico que es un ácido fuerte y agente corrosivo, contribuyendo a la lluvia ácida. Otro proceso de generación de contaminantes secundarios es la formación de smog fotoquímico, resultado de la interacción de estos compuestos con los hidrocarburos inquemados en presencia de la luz solar. Esta combinación es precursora de oxidantes fuertes en la atmósfera, entre otros ozono troposférico. Efectos sobre el hombre. Entre los NOx el componente más estudiado es el NO2, puesto que es el más tóxico (hasta 4 veces más que el NO). Sus efectos en humanos y animales se centran sobre todo en el aparato respiratorio, habiéndose observado que cuando se supera una concentración media de NO2 de 190 µg/Nm3 en el 40% de los días, aumenta la frecuencia de las infecciones de las vías respiratorias, parece ser debido a la disminución de la 40 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS respuesta inmunológica. Valores medios de NOx en el aire urbano suelen ser del orden de 100 µg/m3. Por otra parte, incrementan la sensibilidad pulmonar a los broncoconstrictores, afectando, por lo tanto, especialmente a las personas asmáticas. Debido a que el NO2 es un gas con color y la facilidad de estos compuestos para derivar en aerosoles de ácido nítrico o nitrato amónico pueden actuar disminuyendo la visibilidad. Efectos sobre la flora. En plantas presentan baja toxicidad, aunque concentraciones muy altas (del orden de los picos de concentración encontrados en una ciudad contaminada –superiores a 1000 µg/m3-) pueden tener como resultado alteraciones (desfoliación y clorosis) y pérdidas de producción en algunas especies ÁCIDO NÍTRICO Como contaminante primario su efectos fundamental es la participación en procesos de corrosión de materiales. AMONIACO Este carácter ocasional o su baja concentración habitual no debe restar importancia a los efectos que puedan derivarse de su presencia, pues gracias a su sinergia con el SO2 potencia el efecto más dañino del mismo al facilitar la formación de ácido sulfúrico en la atmósfera además de favorecer adicionalmente la corrosión por reducción de la tensión superficial del agua. Concentraciones muy elevadas (superiores a 18 mg/m3) producen olor característico. 41 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS RESUMEN: COMPUESTOS NITROGENADOS Características de interés Interés medioambiental tres óxidos: ¾ N2O: Abundante, estable y no tóxico. ¾ NO: Baja presencia, reactivo, incoloro y tóxico ¾ NO2: Baja presencia, reactivo, rojizo y muy tóxico NO y NO2 conjuntamente se conocen como NOx Fuentes mas importantes (Oxidos de nitrógeno) N2O: Básicamente natural, pero también combustiones y emisión derivada de uso de fertilizantes nitrogenados. NOx:: Procesos de combustión a altas temperaturas, principalmente el transporte: Su generación depende de: ¾ Temperatura ¾ Relación oxígeno/combustible ¾ Tiempo Aunque se suelen emitir conjuntamente NO y NO2, la concentración de NO es mayoritaria. Evolución y destino N2O: Es un gas muy estable, con vida media de 30 años.. Se puede oxidar, formando Nox, principalmente en la estratosfera, de ahí su importancia medioambiental NOx: Muy reactivos, tendencia a oxidarse y formar ácido nítrico. Efectos más importantes N2O: Contribución al efecto invernadero en un 7%. NOx: ¾ Toxicidad ¾ Inmunodepresión ¾ Facilita procesos de broncocontricción ¾ Contribución a formación de lluvia ácida por formación de ácidos ¾ Contribución a la formación de smog fotoquímico (Ver contaminantes secundarios) ¾ Disminución de visibilidad por: • Formación de aerosoles • Color de NO2 42 6 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS HIDROCARBUROS Estos contaminantes constituyen un grupo muy heterogéneo que tienen en común el hecho de tener en su composición carbono e hidrógeno. La emisión de hidrocarburos proviene de una variedad de fuentes, tanto naturales como antropogénicas. Entre estas últimas, el transporte es la más importante. Los efectos de éstos son muy variados y dependen del grupo según su estructura. Estos van desde el efecto invernadero (metano) a la formación del “smóg fotoquímico” urbano. 6.1 CARACTERÍSTICAS Son un grupo de compuestos cuya característica común es la de presentar en su estructura únicamente átomos de carbono y de hidrógeno. Muchas sustancias pertenecen a este grupo, gran parte de ellas derivadas del petróleo. El estado físico de estos compuestos depende del número de átomos de carbono que conforman su estructura, así como de la disposición espacial de los mismos. Estos pueden ser de cadena abierta (alifáticos) o cíclicos (alicíclicos o aromáticos –núcleo bencénico-) Dentro de la amplia gama de compuestos que forman parte de las mezclas que constituyen los hidrocarburos, los que tienen de 1 a 4 átomos de carbono son gases a la temperatura ordinaria, y por tanto, presentan gran interés desde el punto de vista de contaminación atmosférica. Otros hidrocarburos importantes por su volatilidad, fuentes y efectos son los aromáticos como benceno, xileno y tolueno Otros contaminantes importantes, especialmente por su toxicidad, son los PAH´s o HAP (hidrocarburos aromáticos policíclicos). Estos son aproximadamente 100 compuestos formados por 2 o más anillos bencénicos que comparten 2 átomos en común. Uno de los más tóxicos es el 3, 4 benzopireno que presenta 5 anillos. Para su estudio la OMS toma como referencia 6 de estos compuestos, todos derivados de procesos de combustión. Una forma genérica e inespecifica de valorar los hidrocarburos en aire y sustancias afines es la de hacerlo como Compuestos Orgánicos Volátiles (COV´s), que en general incluye aquellos compuestos orgánicos que se encuentran en la atmósfera en forma gaseosa (por lo general con 5 átomos de carbono o menos) 43 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS 6.2 FUENTES Las fuentes naturales emiten fundamentalmente metano (CH4), debido a procesos biológicos de degradación de materia orgánica. ), también puede se importante la emisión de hidrocarburos más complejos por la vegetación como son los terpenos, emitidos por coníferas e Isopreno, producido por árboles de hoja caduca. Estas fuentes son más intensas que las antropogénicas, constituidas primordialmente por procesos de extracción, refino, transporte y uso del petróleo y derivados, la combustión de biomasa, minería, actividades agropecuarias, etc. A pesar de que la emisión antropogénica es muy inferior a la debida a procesos naturales, la emisión de compuestos orgánicos antrópogénicos es importante por su reactividad en la atmósfera, toxicidad de algún grupo y por la alta sensibilidad del olfato humano a algunos de ellos. El transporte supone la emisión de más del 50% de los hidrocarburos por actividades humanas. Si se analiza una muestra de aire de una zona urbana se detecta la presencia de hidrocarburos alifáticos, así como hidrocarburos aromáticos ligeros en concentraciones en torno a 2-3 mg/m3. Estos hidrocarburos provienen de la evaporación de productos petrolíferos los depósitos y de los carburadores de los vehículos, sobre todo en la parada del motor y cuándo éste aún está caliente. Sin embargo, la fuente principal reside en la combustión incompleta del carburante durante el ciclo de funcionamiento del motor. Los PAH´s se suelen encontrar en las fracciones más pesadas del petróleo, en el hollín como consecuencia de combustiones incompletas (adheridos a las partículas emitidas en focos de combustión) así como se pueden producir por la pirólisis de materia orgánica a altas temperaturas. Ciertas bacterias, algas y plantas pueden sintetizar estos compuestos pero su presencia generalmente está asociada a la combustión incompleta de la materia orgánica. 6.3 EVOLUCIÓN Y DESTINO La vida media de estos compuestos en la atmósfera es muy variable según la especie. La del metano puede ser de años mientras que la del etileno, horas. Estos compuestos orgánicos generalmente se oxidan por ataque de un radical hidróxilo (OH-) con la ayuda de la radiación solar dado que el oxígeno atmosférico no es lo suficientemente agresivo para producir una oxidación directa. Posteriormente se producen reacciones que pueden ser muy complejas 44 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS y, en muchos casos, aun poco conocidas dependiendo de la especie química. El origen del radical OH- está en la fotólisis3 de ciertas sustancias presentes en la atmósfera. La velocidad de las reacciones de oxidación depende del compuesto que se trate, así el etileno tarde del orden de una hora en desaparecer, mientras que el metano tarda mil veces más. Como ejemplo de un proceso de oxidación de un compuesto orgánico se describe a continuación el experimentado por el metano. La trayectoria de oxidación comienza (entre otros caminos posibles) con la reacción elemental que produce el radical metileno y agua: CH4 + OH- → CH3- + H2O El radical metileno es oxidado por el oxígeno molecular, dando el radical metilperóxilo: CH3- + O2 → CH3O2 Este radical puede oxidar al monóxido de nitrógeno (NO), que es un contaminante procedente de la combustión, para dar dióxido de nitrógeno (N02) y un radical metilalkoxi: CH3O2 + NO → CH3O + NO2 Una nueva reacción con el oxígeno produce formaldehido (en sí un contaminante), que es relativamente estable, e hidroperóxilo (HO2): CH3O + O2 → HO2 + CH2O El radical hidroperóxilo oxida a su vez al monóxido de nitrógeno en dióxido de nitrógeno, liberando el radical hidróxilo, que había sido consumido en la primera reacción: HO2 + NO → OH* + NO2 El resumen de todos estos procesos químicos, de los que aquí sólo se ha dado un esquema, que en su conjunto se denomina fotooxidación atmosférica, es: 3 Por fotólisis se entiende una reacción de descomposición de una especie química A por absorción de un fotón para formar una especie en estado excitado A* muy inestable, de modo que muy rápidamente A* se descompone en B + C. * A + hv → A * A →B+C 45 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS La regeneración del OH* (reacción en cadena), que queda disponible para seguir oxidando hidrocarburos. La formación de formaldehido, el cual puede a su vez ser fotolizado y oxidado y conversión del NO en NO2, el cual produce ozono (O3) al fotolizarse, como se verá mas adelante. El resultado final es la presencia de oxidantes fuertes en la atmósfera, que irritan las vías respiratorias, dañan la vegetación y endurecen los materiales poliméricos. Finalmente se puede decir que los óxidos de nitrógeno catalizan, en cierto sentido, las reacciones de los hidrocarburos con los oxidantes, por lo que la lucha contra el smog (contaminante secundario que se describirá más adelante) requiere la reducción de los óxidos de nitrógeno y de los hidrocarburos inquemados del sector transporte (fuentes móviles) y de las calefacciones (fuentes estacionarias) en las zonas urbanas. Otros hidrocarburos se oxidan de manera similar al metano, aunque la química global es muy compleja y no se conoce con profundidad y detalle. Por otra parte, en general los PAH´s en el ambiente atmosférico son fotodegradables cuando están sometidos a una alta exposición a radiación ultravioleta. 6.4 EFECTOS La toxicidad de los hidrocarburos es muy variable según la especie química y el receptor. En general, los aromáticos son mucho más tóxicos que el resto. El etileno se conoce por su fitotoxicidad. El metano contribuye al efecto invernadero, se estima, en un 13%, y su crecimiento anual es del 0.9%. Los PAH´s tienen efectos cancerígenos, pero con una alta variabilidad. El más tóxico es el 3,4 benzopireno, que es poco estable y rápidamente destruido por la luz solar y otros compuestos atmosféricos. En el hombre su absorción es rápida y paso a tejidos grasos, pero no son bioacumulables ya que se produce una rápida metabolización. 46 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS Por último, como se apunto en el punto anterior, los hidrocarburos tienen influencia sobre la presencia de oxidantes fuertes en la atmósfera, como se verá en el capítulo de contaminantes secundarios. RESUMEN: HIDROCARBUROS Características de interés Los más importantes dentro de la contaminación atmosférica son más los volátiles: ¾ 1 - 4 átomos de carbono ¾ Aromáticos Los Hidrocarburos Aromáticos Policíclicos son importantes por su alta toxicidad La medición de Compuestos Orgánicos Volátiles (COV´s) es una valoración inespecífica de los hidrocarburos y sustancias afines. Fuentes mas importantes Las emisiones naturales son muy superiores a las antropogénicas. Dentro de estas últimas, es el transporte el foco más importante. El principal proceso de emisión de los HAP son combustiones incompletas de materia orgánica Evolución y destino La vida media de los hidrocarburos es muy variable (metano, años y elileno, horas) En general, degradación mediante fotooxidación con reacciones muy complejas y, en muchos casos, aún en estudio. Efectos más importantes Toxicidad variable: Más los aromáticos y HAP´s. Efecto invernadero: Metano Smog fotoquímico: 47 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS 48 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS 7 COMPUESTOS ORGANOHALOGENADOS SIMPLES Se incluyen en este término gran cantidad de sustancias derivadas de hidrocarburos simples (1 o 2 átomos de carbono) en donde uno o varios hidrógenos son sustituidos por halógenos, principalmente cloro, bromo o flúor. Dentro de estos grupos encontramos disolventes, plaguicidas, propelententes y refrigerantes. Muchas de estas sustancias deben su importancia ambiental a su actuación como reductores de la capa de ozono. 7.1 CARACTERÍSTICAS Los clorofluorocarbonos (CFC’s), cuyo uso ha estado muy expandido, principalmente como fluidos refrigerantes, propulsores de atomizadores, disolventes y espumantes. Dentro de este grupo los más importantes son CFC11 (CCl3F1) utilizado principalmente como propelente y el CFC12 (CCl2F2) utilizado como refrigerante. Estas sustancias son estables, no inflamables, no tóxicos y buenos disolventes. Otros compuestos organohalogenados que pueden tener importancia en la degradación de la capa de ozono son los siguientes: ¾ Los halones, derivados bromofluorados de hidrocarburos volátiles, que se emplean para la extinción de incendios y actúan de manera similar a los CFCs sobre la capa de ozono estratosférica. ¾ Cloruro de metilo: emisiones naturales e incineración ¾ Bromuro de metilo: emisiones naturales y uso como biocida ¾ Disolventes como tricloroetano, tricloroetileno, percloroetileno,.. 7.2 FUENTES La producción y emisión de los CFC´s es antropogénica, principalmente en procesos de fabricación y uso de los mismos, como en el caso de los disolventes clorados mencionados y halones. Los usos más comunes que han tenido los CFC´s han sido: 49 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS Disolventes industriales. Refrigerantes. Construcción de materiales aislantes. Propelentes. Fabricación de espumas. Por otro lado sustancias como cloruro o bromuro de metilo pueden tener un origen natural, además de procesos de incineración el primero y fabricación y uso como plaguicida el segundo (principalmente en cultivos de invernadero). 7.3 EVOLUCIÓN Y DESTINO La vida media de estas sustancias es muy variable según su composición. Se estima que la vida media de los CFC´s supera los 100 años, por otra parte compuestos con cloro como cloruro de metilo o ciertos disolventes como tricloro etano, tricloroetileno, percloroetileno, etc. presentan una vida media en la atmósfera de semanas a meses. El bromuro de metilo presenta una vida media estimadas de años. La larga permanencia de los CFC´s en la atmósfera hace que puedan llegar hasta la estratosfera. Se estima que los CFC´s tardan en llegar a la capa de ozono 10 a 20 años. En esta capa, la presencia de radiación ultravioleta hace que se descompongan estas sustancias liberando los átomos de cloro, siendo esta propiedad la que da lugar a la destrucción de la capa de ozono. Reacciones de este tipo ocurrirán con otros organohalogenados simples como los vistos, aunque hay que tener en cuenta que su menor vida media hará más difícil su acción en la estratosfera. 7.4 EFECTOS DESTRUCCIÓN DE LA CAPA DE OZONO Los anteriores compuestos tienen como principal efecto ambiental su acción en la destrucción de la capa de ozono estratosférica. A continuación se explicará este efecto, provocado no sólo por los compuestos organohalogenados simples referidos, sino por otros como son óxidos de 50 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS nitrógeno, ciertos constituyentes del ciclo del carbono y compuestos hidrogenados. Cómo intervienen todas estas sustancias en este proceso se verá en el presente capítulo. Las primeras medidas en esta capa sobre cantidad y variación datan de 1930, siendo en los años 70 cuando se detectan las primeras relaciones entre las variaciones de esta capa estratosférica y sustancias emitidas a nivel del suelo como consecuencia de la actividad humana. Tras demostrarse que la capa de ozono podía ser destruida por compuestos inyectados a la atmósfera de origen antrópico, se ha comenzado un estudio exhaustivo de la química atmosférica estratosférica y de los fenómenos de carácter meteorológico que pueden influir En la discusión de este efecto es necesario repasar primero la química responsable de la formación de ozono en la estratosfera, las reacciones implicadas en su equilibrio de formación-destrucción y, finalmente, aquéllas originadas por la presencia de las anteriores sustancias en las que se destruye ozono de forma neta. Hasta la estratosfera las radiaciones solares llegan con la radiación ultravioleta prácticamente intacta, pues ha atravesado muy poca atmósfera. La radiación ultravioleta es muy energética4 y es capaz de disociar la molécula de oxígeno para dar oxígeno atómico, en un proceso que tiene lugar a alturas del orden de 80 Km.: O2 + hν → 2O (1) A más baja altura, un átomo de oxígeno puede reaccionar con una molécula de oxígeno para dar ozono: O + O2 + M → O3 + M (2) donde M es un tercer cuerpo capaz de aceptar energía. El ozono puede a su vez ser fotolizado (descompuesto en átomos y moléculas más simples por efecto de la radiación solar) en oxígeno molecular y atómico, O3 + hν → O2 + O (3) 4 De la radiación solar, la parte que tiene longitud de onda menor es la ultravioleta, creciendo este parámetro al pasar al visible, λ = 0,4 a 0,8 µm (violeta, azul, verde, amarillo, naranja y rojo, de menos a más longitud de onda) y finalmente al infrarrojo, λ = 1 a 100 µm. 51 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS Es posible también la recombinación de ozono y oxígeno atómico para restablecer el oxígeno molecular: O + O3 → 2 O 2 (4) Como consecuencia de este esquema químico, se establece un equilibrio dinámico entre las especies oxígeno molecular (O2), oxígeno atómico (O) y el ozono (O3) por competencia entre las reacciones anteriores. Esto ocasiona la presencia de ozono en la estratosfera, principalmente entre los 15 y 60 km. de altura, aunque es máxima entre 25 y 40 km. La reacción (3) causa la absorción de rayos ultravioleta de longitud de onda inferior a 0,290 µm = 290 nm (ultravioletas B), lo cual explica el aumento de temperatura con la altura en la estratosfera. Esta absorción impide su llegada a la superficie de la Tierra, permitiendo la vida tal y como la conocemos, pues el efecto de la llegada de estos rayos sería muy perjudicial La capa de ozono es muy frágil, pues este compuesto es muy reactivo y las reacciones anteriores no son las únicas que participan en su equilibrio. Los óxidos de nitrógeno naturales (NO y NO2), creados por las descargas eléctricas atmosféricas en las regiones tropicales ascienden a la estratosfera e intervienen. Se encuentra asimismo el radical hidróxilo (OH) y el hidroperóxilo (HO2) formados por fotólisis del ozono y posterior reacción con el agua. Si denominamos X al NO o al OH, un camino químico posible es: X + O3 → XO + O2 XO + O → X + O2 El efecto neto es el consumo del ozono y oxígeno atómico para formar oxígeno molecular y la restitución de la especie X, por lo que se la considera un catalizador de la destrucción del ozono. Si sumamos miembro a miembro las dos ecuaciones anteriores obtenemos: O3 + O → 2O2 una reacción global en la que se sugiere que el O3 y el O reaccionan directamente. Esta reacción es virtual, pues es el resumen de un proceso químico más complejo. En el seno de la atmósfera se llevan a cabo reacciones similares a éstas, que logran el mismo efecto, trabajando independientemente de ellas o en combinación. A estas reacciones es necesario añadir las de fotólisis. La contaminación de óxidos de nitrógeno a nivel del suelo no es capaz de intervenir en procesos como el descrito, dado que su reactividad hace muy 52 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS difícil que alcancen la altura a que se dan las reacciones en las condiciones favorables. Aun así, los óxidos que alcanzasen esta zona serían oxidados a ácido nítrico por el ozono. Los óxidos de nitrógeno generados directamente en la estratosfera sí pueden constituir un peligro dado que desencadenan estas reacciones de eliminación de ozono, razón por la que se considera potencialmente peligrosa la aviación supersónica civil masificada. El óxido de nitroso (N2O), que es una molécula estable y no tóxica, puede alcanzar la estratosfera, pues además no es fotolizable por lo fotones disponibles en la superficie. En consecuencia puede acumularse y difundirse o ser transportado hasta la estratosfera en tiempos característicos del orden de años. En ella es fotolizado por efecto de fotones mas energéticos y produce óxidos de nitrógeno (NO y NO2), que son mucho mas reactivos y participan en la destrucción del ozono, tal y como hemos visto. El N2O es producido en baja proporción por la combustión, especialmente si es pobre y a baja temperatura. Así mismo se produce por las reacciones involucradas en los catalizadores de gases de escape de los automóviles. Las bacteria que desnitrifican los suelos son otra fuente importante de N2O Las emisiones de N2O han ido aumentando desde algunas décadas y seguirán aumentando. En este año la concentración media en la troposfera es del orden de 300 ppbv y aumenta a razón de un 0,25% por año. La familia de compuestos más agresivos con el ozono estratosférico la constituyen los clorofluorocarbonos o CFC’s. Alcanzan la estratosfera fácilmente pues no son atacados por el radical hidroxilo (OH) ni son fotolizados. Su concentración es del orden de 0.1-1 ppbv y crece a un ritmo del 4% anual. Una vez en la estratosfera son fotolizados por los fotones mas energéticos presentes en ella y liberan átomos de cloro (Cl), que reacciona con el ozono estratosférico para dar óxido de cloro: Cl + O3 → ClO + O2 El óxido de cloro reacciona a su vez con el oxígeno atómico para producir cloro atómico de nuevo: ClO + O → Cl + O2 La pareja Cl/ClO representa el mismo papel destructor del ozono que la NO/NO2 y OH/HO2, que denominaremos genéricamente X/XO. 53 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS Por esta razón los clorofluorocarbonos están siendo sustituidos progresivamente por otros refrigerantes menos estables en la troposfera, como los hidroclorofluorocarbonos (HCFC), aunque al descomponerse originan productos tóxicos. El desequilibrio así creado muestra que se pueden producir efectos en lugares muy alejados de las fuentes de producción de contaminantes y muchos años después. El equilibrio original sólo se alcanzará muchos años después de que cesen las emisiones. Hoy en día se reconoce la necesidad del cese total de producción de CFC’s, lo cual no podrá lograrse hasta dentro de unos años. Los efectos que puede tener la disminución de la capa de ozono como consecuencia de la actividad antropogénica, con el consecuente incremento de exposición de la radiación ultravioleta, pueden manifestarse en el hombre (incremento en el número de cánceres de piel y alteraciones oculares y del sistema inmunitario), los animales (afecciones en estados juveniles de ciertas especies) y plantas (disminución del fitoplancton, reducción de la producción de ciertas especies cultivadas); así como tener unas consecuencias globales, relacionadas con la alteración del balance de energía. 54 Efectos prevcisibles CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS RESUMEN: C. ORGANOHALOGENADOS SIMPLES Características de interés Derivados halogenados (principalmente cloro, bromo y flúor) de hidrocarburos simples. Los más importantes por su transcendencia medioambiental son los CFC´s. Son sustancias estables, no tóxicas y principalmente empleadas como propelentes o refrigerantes. Su producción está muy regulada Otras sustancias de interés son el cloruro y bromuro de metilo, ciertos disolventes clorados y los halones. Fuentes mas importantes Los CFC´s son sustancias de origen antropogénico, otros organohalogenados pueden tener origen natural La emisión de los CFC´s se debe a procesos de fabricación y uso Evolución y destino Vida media variable según sustancias. Los CFC´s pueden tener una vida media de más de 100 años. Esta estabilidad facilita su llegada hasta la capa de ozono estratosféico. Efectos más importantes CFC´s: Principales responsables de la destrucción de la capa de ozono (70 % contribución). Otros gases responsables: Bromuro de metilo (10%) y Oxidos de nitrógeno. Efectos previsibles destrucción capa de ozono: ¾ Inhibición del desarrollo fases juveniles de diferentes especies ¾ Alteración del balance de energía ¾ Hombre: • Cataratas • Cáncer de piel • Alteración del sistema inmunológico Contribución al efecto invernadero estimada en un 20% 55 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS 56 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS 8 DIOXINAS Y FURANOS Las dioxinas y furanos, o simplemente dioxinas, son los nombres comunes por los que se conoce a dos grupos de sustancias organocloradas. Entre las principales particularidades que caracterizan a estas sustancias cabe destacar las propiedades altamente tóxicas de algunas de ellas, su bioacumulación, el hecho de que son generadas en una gran variedad de procesos industriales y de combustión, y su persistencia en el medio ambiente, en el cual se encuentran ampliamente distribuidas en concentraciones muy pequeñas. 8.1 CARACTERÍSTICAS "Dioxinas" es el nombre genérico bajo el que se conocen los compuestos químicos denominados policlorodibenzo-p-dioxinas y policlorodibenzofuranos, abreviadamente PCDD/PCDF o PCDD/F. Son éteres aromáticos policlorados formados por dos anillos bencénicos unidos a través de 1 ó 2 átomos de oxígeno (furanos y dioxinas, respectivamente). Estos grupos los constituyen 210 compuestos que varían según el número de átomos de cloro (hasta 8) y su posición. Entre sus características fundamentales figuran su elevada estabilidad térmica y su baja degradabilidad lo que les confiere una gran persistencia en el medio ambiente. Además son bioacumulables y, debido a su carácter lipófilo, se depositan especialmente en el tejido adiposo de los organismos animales. 8.2 FUENTES El origen de las dioxinas es muy diverso existiendo tanto fuentes de origen natural como antropogénico. Las principales fuentes de origen natural son los incendios forestales y las erupciones volcánicas aunque también hay determinadas reacciones enzimáticas y fotolíticas que producen dioxinas. Entre las fuentes de origen antropogénico, muy mayoritarias respecto a las naturales, figuran: Procesos de combustión a gran escala (incineradoras de RSU, incineradoras de residuos industriales, incineradoras de residuos hospitalarios y centrales térmicas que utilizan combustibles fósiles); 57 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS Procesos de combustión en pequeña escala (motores de explosión de los automóviles, sistemas domésticos de calefacción); Diversos procesos químicos e industriales, en los que se forman PCDD/PCDF como subproductos puesto que no son compuestos que se fabriquen ni que tengan una utilidad conocida (fabricación de compuestos organoclorados, blanqueo de pasta de papel con cloro, industria textil, etc.); Accidentes (incendios de plásticos o materiales organoclorados, incendios o explosión de transformadores que contengan PCB´s); y Productos de desecho (lodos de depuradoras y potabilizadoras, lixiviados de vertederos, aguas residuales domésticas). Los procesos de combustión a gran escala son los que mayor contribución aportan en la emisión de dioxinas a la atmósfera. Se han propuesto diversas teorías sobre la formación de estos contaminantes durante el proceso de combustión, pudiendo ser sus rutas de formación una combinación de distintos fenómenos dependiendo de las condiciones que prevalezcan: Los PCDD/PCDF están presentes como constituyentes traza en los residuos que se incineran y, debido a su gran estabilidad térmica, persisten al proceso de combustión. Esto es originado fundamentalmente por la existencia de ciertas zonas “frías” en las que la temperatura de combustión es más baja. Los PCDD/PCDF se producen durante el proceso de incineración a partir de precursores tales como los PCB´s, anillos bencénicos clorados, pentaclorofenol, etc. Estos precursores pueden estar presentes en el residuo o bien formarse por la combustión de plásticos como el PVC. Sin embargo, se ha demostrado que no existe una relación directa entre la incineración de plásticos de PVC y la formación de PCDD/PCDF. La presencia de PCBs, clorofenol, etc. en el residuo puede originar un aumento en las emisiones de dioxinas. El rango de temperaturas en el cual se produce su formación es entre 300 y 800º C. Los PCDD/PCDF se forman también como resultado de reacciones entre los elementos que constituyen estos compuestos: carbono, hidrógeno, oxígeno y cloro. Dichas reacciones se conocen con el nombre de síntesis “de novo” de PCDD/PCDF y tienen lugar en los gases producto de la combustión. Sin embargo, también se produce la formación de estos contaminantes en las cenizas volantes, que contienen carbono residual, a temperaturas comprendidas entre 300-400º C y en presencia de ácido clorhídrico, oxígeno y vapor de agua que forman parte de los gases de combustión. Se piensa que estas reacciones están catalizadas por diversos metales, óxidos metálicos, silicatos, etc. presentes en las cenizas. 58 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS 8.3 EVOLUCIÓN Y DESTINO Las dioxinas son compuestos bastante estables en condiciones ambientales normales y por ello perduran mucho tiempo en la naturaleza. No obstante, en el medio ambiente se ven sometidos a una serie de factores ambientales a través de los cuales pueden experimentar una gran variedad de procesos que originarán una redistribución de estos contaminantes en todo el ecosistema. Estos procesos son básicamente: Procesos de transporte: Implican únicamente mecanismos físicos o biológicos que dan lugar a transferencia entre diferentes sistemas (aire-suelo, suelo-agua,..) ¾ Deposición atmosférica: • Seca: Dioxinas adsorbidas a partículas en suspensión sedi- mentan en el suelo. • Húmeda: La lluvia arrastra en su caída al suelo dioxinas en fase vapor y aquellas adsorbidas a partículas ¾ Volatilización: El paso a la fase vapor o volatilización es uno de los mecanismos por los que las dioxinas pueden volver de nuevo a la atmósfera desde el suelo o el agua. No obstante, las dioxinas son poco volátiles (menos cuanto más es el grado de cloración). ¾ Sedimentación acuática: Por su baja solubilidad en agua y la fuerte tendencia a adherirse a las partículas en suspensión, estas sustancias cuando llegan a los sistemas acuáticos tienden a acumularse rápidamente en los sedimentos tras la decantación del material particulado. ¾ Erosión: Por el viento, agua u otro agente es un proceso por el cual se produce transferencia de las dioxinas adsorbidas a partículas. ¾ Lixiviación: Las dioxinas contenidas en los suelos son solubilizadas y trasportadas hasta, normalmente, algún sistema acuático. ¾ Bioacumulación/Biomagnificación (ver glosario): Mediante estos procesos, de gran transcendencia ambiental, se produce el transporte y transferencia de las dioxinas entre los distintos seres vivos a través de la cadena alimentaria; no sólo son procesos de transporte sino también de concentración de estos contaminantes en los seres vivos. La lipofilia y baja solubilidad en agua que caracteriza a las dioxinas hace que sean especialmente afines por los tejidos de los seres vivos ricos en grasas; estas propiedades, junto con la resistencia a la degradación son los responsables de que una vez en el organismo tiendan a acumularse en él pudiendo llegar a concentraciones varios ór- 59 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS denes de magnitud con respecto al medio que le rodea. Este hecho es uno de los principales motivos de controversia por la amenaza para la salud que puede representar, ya que esta bioconcentración podría llegar a niveles tóxicos. Procesos de transformación: Son procesos físicos, químicos o bioquímicos que implican la modificación de la estructura química de estos compuestos y que, por tanto, contribuyen a su degradación ambiental, aunque no obstante hay que decir que tales procesos ocurren muy lentamente en condiciones ambientales normales dada su gran estabilidad. ¾ Fotólisis: La fotólisis a través de la luz solar constituye una vía importante de degradación de estos compuestos en el medio ambiente, sobre todo los que se encuentran en la atmósfera. En este medio la fotolisis en fase vapor es relativamente rápida mientras que la adsorción en partículas parece inhibir bastante este proceso. En suelos y aguas ésta degradación es menor y sólo afecta a capas superficiales. Por otra parte, a menor grado de cloración mayor facilidad de degradación. A modo de ejemplo, la vida media de dioxinas en fase vapor ha sido calculada en aproximadamente 200 horas (2378-TCDD) y 500 (OCDD). La vida media de 2467-TCDD en el suelo en ausencia de luz solar se ha estimado en 10 años; en aguas superficiales claras en 118 horas en invierno y 21 horas en verano. ¾ Biodegradación: La degradación por procesos bioquímicos puede tener lugar a través e microorganismos (degradación microbiológica) o en organismos superiores (degradación metabólica). La primera en condiciones de laboratorio ideales se ha demostrado muy eficaz con ciertos hongos, en la naturaleza no se han podido detectar microorganismos capaces de degradar efectivamente estas sustancias en condiciones habituales. En organismos superiores las dioxinas se han mostrado extraordinariamente resistentes a la metabilización. ¾ Degradación química: A pesar de su alta estabilidad química, en condiciones de laboratorio pueden forzarse determinadas reacciones de degradación, pero estas reacciones es muy improbable que se produzcan en condiciones naturales. Distribución final en el medio: Por efecto de los anteriores procesos las dioxinas inicialmente liberadas en el medio quedarán finalmente redistribuidas en diferentes partes del ecosistema, generando unos niveles residuales de fondo de carácter ubicuo en el aire, agua y suelo. Estos niveles pueden ser localmente incre- 60 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS mentados por algunos focos puntuales de contaminación. Los seres vivos en contacto con el medio incorporarán también estos contaminantes en su organismo en forma proporcional a los niveles existentes en el medio. 8.4 EFECTOS La toxicidad de estos compuestos depende del grado de cloración así como de la posición que ocupen los átomos de cloro. Existen 210 isómeros diferentes de los cuales el más tóxico es el que tiene ocupadas las posiciones 2, 3, 7, y 8 por átomos de cloro simultáneamente (2, 3, 7, 8 -TCDD). Por este motivo, y dadas las diferencias que muestran en cuanto a su toxicidad, las concentraciones de PCDD/PCDF se expresan en relación a este isómero. Con este fin, se ha determinado un factor de toxicidad equivalente a nivel internacional (I-TEF) para cada uno de los 17 compuestos que poseen átomos de cloro en, al menos, las cuatro posiciones antes indicadas ya que son los que presentan una toxicidad importante. Así, multiplicando la concentración medida para un isómero por el I-TEF correspondiente se obtiene un valor que corresponde a la cantidad de 2, 3, 7, 8 -TCDD que produciría los mismos efectos (I-TEQ). La toxicidad de las dioxinas se manifiesta en muchos órganos y tipos celulares en animales expuestos a dosis subletales, o en el intervalo transcurrido desde la exposición a una dosis letal y la muerte del animal. Una lista de efectos se encuentra a continuación, cuya aparición e intensidad está en función de la dosis y la especie considerada: Perdida de peso y anorexia Alteración de parámetros hemáticos Alteraciones hepáticas Edema dermal y general Alteraciones dermales (cloracné, hiperpigmentación,..) Alteraciones del sistema urorenal Hiperplasia e hipertrofia del epitelio gastrointestinal Alteraciones pulmonares y cardiovasculares Inmunotoxicidad 61 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS Disminución de la fertilidad Teratogenia Carcinogénesis: En 1.997, el IARC (Agencia Internacional de Investigación del Cáncer -Lyón-) establece que la 2, 3, 7, 8 Tetraclorodibenzo-paraDioxina incrementa el riesgo de cáncer de pulmón En humanos la principal vía de entrada en el organismo de estas sustancias es la oral (consumo de alimentos y bebidas), siendo la inhalación de aire, generalmente, de menor importancia. En el hombre se han documentado una serie de lesiones y síntomas tras la exposición a la 2, 3, 7, 8 -TCDD, como los que se reflejan a continuación Sin embargo, en casi todos los estudios realizados en exposiciones a estos compuestos no se puede asegurar que únicamente estén presentes las dioxinas sino que los síntomas se deben a la presencia de una mezcla de sustancias en que éstas se incluyen. Manifestaciones en la piel ¾ Cloracné. ¾ Hiperqueratosis. ¾ Hiperpigmentación. ¾ Hirsutismo. ¾ Elastosis. Sistema interno ¾ Fibrosis de hígado. ¾ Aumento de transaminasas en sangre. ¾ Aumento del colesterol y triglicéridos. ¾ Perdida de apetito y peso. ¾ Dolores musculares. ¾ Inflamación de ganglios linfáticos. ¾ Desórdenes cardiovasculares, digestivos, tracto urinario, respiratorio y páncreas. Efectos neurológicos ¾ Disfunción sexual. 62 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS ¾ Dolor de cabeza. ¾ Neuropatía. ¾ Perdida de audición, visión, gusto y olfato. Efectos psiquiátricos ¾ Trastornos del sueño. ¾ Depresión. ¾ Estados de ansiedad. 63 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS RESUMEN: DIOXINAS Y FURANOS Características de interés Son 210 compuestos orgánicos clorados (hasta 8 átomos de cloro). Persistentes Muy tóxicos Bioacumulables El más tóxico de estos compuestos es la 2, 3, 7, 8,-tetracloro dibenzodioxina. Así en la valoración de la concentración de dioxinas se tienen en cuenta aquellas con cloro en al menos las posiciones 2, 3, 7 y 8 (17 isómeros). Fuentes mas importantes La principales fuentes (casi exclusivas) son antropogénicas. Especialmente procesos de combustión a gran escala (incineradoras, centrales térmicas, etc), a pequeña escala (automóviles, calefacciones, etc) y diversos procesos industriales (fabricación de compuestos organoclorados, ciertos plaguicidas, blanqueo de pasta de papel, etc). Evolución y destino Son compuestos altamente estables y se encuentran ampliamente dispersados por el medio ambiente debido a diferentes proceso de transporte. El principal proceso de degradación es la fotolisis, aunque ésta es muy variable en función de las características químicas del compuesto y las condiciones ambientales. Efectos más importantes Son sustancias bioacumulables y biomagnificables. Presentan alta toxicidad con manifestaciones muy variables según la especie considerada y la dosis. En el hombre se han demostrado diferentes patologías en piel, sistema interno, así como alteraciones neurológicas y psiquiátricas. La 2, 3, 7, 8 TCDD ha demostrado poder carcinogénico. 64 9 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS METALES PESADOS Son contaminantes persistentes, muchos de ellos tóxicos a bajas concentraciones y alguno de ellos se encuentran implicados en procesos de bioacumulación y biomagnificación. En general este tipo de contaminación es localizada y asociada a diferentes procesos industriales, excepto en el caso del plomo que puede tener una presencia significativa, especialmente en el ambiente urbano, como consecuencia de su uso como aditivo de carburantes, aunque la tendencia es a su disminución debido al creciente uso de gasolinas sin este metal. 9.1 CARACTERÍSTICAS Una de las características de este tipo de contaminantes es su menor presencia natural en la atmósfera, en general, respecto a los aportes antropogénicos y el hecho de que no son degradados ni química ni biológicamente, por lo que se consideran contaminantes persistentes en el medio. Esta persistencia, junto con la dificultad de eliminación de alguno de ellos por parte de los sistemas metabólicos de organismos animales y vegetales puede tener como consecuencia un fenómeno de acumulación en los tejidos biológicos de los individuos o a lo largo de la cadena trófica, (procesos ya conocidos de bioacumulación y biomagnificación). En la atmósfera puede encontrarse en diferentes formas (elemental o combinados) y estados (particulados (principalmente) o vapor). Dentro de los metales el plomo es aquel con más importancia dentro del ámbito de la contaminación atmosférica debido a que al ser un aditivo de las gasolinas su emisión está bastante generalizada, siendo un importante contaminante urbano. 9.2 FUENTES La presencia natural en la atmósfera se debe principalmente a volcanes, incendios o erosión del suelo. Por otra parte, la emisión antropogénica se debe principalmente a actividades mineras, industria metalúrgica, de plaguicidas, catalizadores y procesos de combustión, en este caso, su emisión es como óxidos. Con respecto al porcentaje de emisión antropogénica de los metales 65 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS respecto a la natural, son mayoritarios los aportes de cadmio, mercurio, níquel y, en especial, de plomo (> 90%). En el caso del plomo y sus derivados, especialmente los óxidos, tienen dos posibles orígenes: localmente, se encuentran en las proximidades de fábricas que preparan o utilizan este metal en estado de fusión, sobre todo alrededor de las que se dedican a la recuperación de residuos plumbíferos, pero, en general, su presencia en la atmósfera de las ciudades se debe a la introducción de compuestos orgánicos en los combustibles líquidos para motores de automóvil. Estos compuestos (los tetraalquilplomos, por ejemplo, como el tetrametil, tetraetil, etc.) son conocidos por su propiedad de conferir un cierto poder antidetonante a las gasolinas. Durante la combustión de la mezcla carburada en los cilindros, estos compuestos sufren una destrucción más o menos profunda, y el plomo se encuentra en el gas de escape en forma de metal, de óxidos o incluso de compuestos diversos por reacción con otros constituyentes de aditivos. Actualmente su uso como aditivo de gasolinas está prohibido en los Estados Unidos y se va prohibiendo progresivamente en los países industrializados. Además daña el catalizador que se usa para la reducción de los contaminantes en el tubo de escape de los motores alternativos usados en los vehículos automóviles. 9.3 EVOLUCIÓN Y DESTINO El destino final de los metales en la atmósfera, en general, es una deposición rápida. No obstante, también se han encontrado concentraciones de metales por encima de los valores naturales en zonas muy alejadas de los posibles focos emisores, probablemente por traslado de material particulado por diferentes procesos meteorológicos. 9.4 EFECTOS Es este un grupo de contaminantes de especial relevancia por el riesgo que representan para la salud humana. El riesgo que representa su presencia en el aire se debe a que son inhalados y pueden ser bioacumulados en el organismo, pudiendo alcanzar concentraciones que los conviertan en agentes tóxicos. Desde el punto de vista sanitario, la acumulación de plomo puede producir alteraciones en el comportamiento, afectar a la inteligencia de los niños y producir malformaciones en los fetos de madres gestantes. Por otra parte, en 66 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS torrente sanguíneo ya se pone de manifiesto su carácter tóxico pues interfiere en la síntesis del grupo hemo, dificultando así el desarrollo y maduración de los glóbulos rojos, y actúa en el tubo digestivo donde puede favorecer la aparición de úlceras. El plomo que se acumula en los huesos parece que altera la osificación normal del esqueleto debido a trastornos en la fijación del calcio. Es capaz, asimismo, de dificultar la actividad enzimática. En el caso concreto de los adultos, población menos sensible a los efectos descritos, una acumulación de plomo podría llegar a causar daños importantes en el sistema nervioso. Se ha comprobado que de la cantidad total de plomo inhalado, el 35% (de media) se introduce en el torrente sanguíneo de donde se distribuye por todo el organismo acumulándose una cantidad no determinada en los huesos, mientras que el resto es expulsado al exterior a través de la orina. Existen otros metales cuyos efectos son más o menos conocidos. La toxicidad y bioacumulación y efectos patológicos dependen del elemento en cuestión. En este sentido son especialmente importantes el mercurio, cadmio, níquel, etc. No obstante la exposición por parte de los organismos vivos no suele deberse a procesos de contaminación atmosférica. Aunque alguno de estos metales han sido responsables en zonas localizadas de procesos de contaminación atmosférica especial no se les considera contaminantes generalizados. 67 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS RESUMEN: METALES PESADOS Características de interés Son contaminantes persistentes, muchos de ellos, tóxicos a bajas concentraciones y algunos son bioacumulables. La emisión por procesos antropogénicos es superior, en general, que por fenómenos naturales, especialmente en el caso del cadmio, mercurio, níquel y, sobre todo, plomo (90%). Fuentes mas importantes Las emisiones antropogénicas se deben a actividades variadas como minería, siderometalurgia, fabricación de ciertos plaguicidas, catalizadores y procesos de combustión. En el caso del plomo su presencia, especialmente en las ciudades, se debe a la utilización de compuestos orgánicos con plomo como aditivos de gasolinas. Evolución y destino Emisión y, en general, rápida deposición. Efectos más importantes Diferentes alteraciones según el metal. Especialmente tóxicos son el mercurio, cadmio y níquel. El plomo en el hombre puede provocar diferentes afecciones en: ¾ Sistema nervioso ¾ Desarrollo de glóbulos rojos ¾ Sistema digestivo ¾ Desarrollo del feto 68 10 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS OTROS CONTAMINANTES Existe una gran variedad de sustancias orgánicas o inorgánicas que pueden constituir en determinadas circunstancias contaminación atmosférica. A continuación se relacionan alguna de las más importantes y se mencionarán aquellas características más destacables. CLORO Y CLORURO DE HIDRÓGENO Es un gas incoloro de olor sofocante, muy soluble en agua, produciendo ácido clorhídrico. Presenta efectos tóxicos, especialmente para las plantas, y corrosión. Niveles del orden de 1 ppmv de ácido clorhídrico (ClH) o cloro (Cl2) pueden afectar seriamente la vida de las plantas. Estos niveles sólo se alcanzan debido a escapes o vertidos accidentales. Su origen natural se debe a la oxidación por medio de radicales -OH del cloruro de metilo emitido por los océanos. Actividades antropogénicas productoras son metalurgia del cobre, fabricación de cloro, carbonato de sosa, potasa, PVC, compuestos organoclorados, vidrio, incineración de residuos, etc. En algunas zonas se cree que es responsable junto con otros ácidos, aunque en mucha menor proporción, de la lluvia ácida. FLÚOR Y FLUORURO DE HIDRÓGENO El fluoruro de hidrógeno es un gas humeante o líquido incoloro (P.E. 19.5º C) cuya solución acuosa es el ácido fluorhídrico. Al igual que en el caso del ClH, es tóxico, especialmente para las plantas, así como muchas sales (fluoruros) y corrosivos. Los fluoruros constituyen tóxicos acumulativos para las plantas, necrotizando áreas de las hojas. Se encuentran niveles de umbral de toxicidad tan bajos como 0, 1 ppbv. Por otra parte, los fluoruros sólidos o gaseosos se acumulan en los forrajes. El consumo de este forraje por el ganado puede provocar fluorosis. El flúor está muy extendido en la naturaleza en forma de fluoruros y acompaña, casi siempre, al fósforo en sus minerales. Por ser éstos la materia prima de numerosas industrias de transformación destinadas, especialmente, a la producción de abonos (ácido fosfórico, fosfatos de amonio, superfosfatos, 69 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS etc.), los tratamientos por calcinación o ataque sulfúrico van acompañados de emisiones fluoradas más o menos abundantes. La industria de la elaboración del aluminio a partir de la bauxita por electrólisis en fase ígnea, utiliza la criolita como fundente (material compuesto a base de un hexafluoraluminato de sodio). A las elevadas temperaturas en que tiene lugar el preparado se producen emisiones de productos fluorados. Por otra parte, el origen de estos compuestos en el medio atmosférico también puede ser natural (emisión marina y volcanes). Por último no se deben dejar aparte, finalmente, las emisiones de productos malolientes que constituyen, para las personas a ellos expuestas, una incomodidad a veces intolerable e incluso un verdadero perjuicio (se han detectado multitud de síntomas patológicos asociados a malos olores). Este tipo de contaminación está cobrando cada día mayor importancia tanto por las exigencias de calidad de vida de una población más exigente como por el hecho de que es un problema en crecimiento desde que proliferan las plantas de tratamiento de residuos, vertederos y aguas residuales. Pero también existen algunas industrias que se rodean de una atmósfera desagradable: ocurre así en fábricas de productos cuya materia prima son huesos o residuos de los mataderos y de descuartizamiento, tenerías, papeleras, etc. El mayor número de denuncias por contaminación atmosférica derivan de procesos de generación de malos olores, aunque no sea el tipo de contaminación con efectos más perjudiciales para la salud. 70 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS 11 CONTAMINANTES SECUNDARIOS Los contaminantes secundarios son aquellos que se forman por la interacción química entre contaminantes primarios o éstos y compuestos habituales de la atmósfera, en procesos que puede intervenir la radiación solar. Los procesos que intervienen en su formación, así como los efectos más destacados son comentados a continuación. 11.1 CONTAMINANTES FOTOQUÍMICOS 11.1.1 CARACTERÍSTICAS En zonas muy contaminadas, especialmente con sustancias provenientes de la combustión (hidrocarburos inquemados y óxidos de nitrógeno), si se alcanzan las condiciones climáticas adecuadas (insolación, situación anticiclónica, inversión térmica), se puede formar la denominada niebla fotoquímica (“el smog”). Como consecuencia de esta situación aparecen en la atmósfera oxidantes generados por las interacciones de NOX, hidrocarburos y el oxígeno, en presencia de la radiación ultravioleta de los rayos del Sol. El mecanismo de formación de estos contaminantes fotoquímicos es complejo e involucra diferentes etapas, permaneciendo desconocido el proceso completo de formación. La niebla fotoquímica se caracteriza por un contenido alto de oxidantes (ozono (O3), dióxido de nitrógeno (NO2), peróxido de hidrógeno (H202), compuestos con grupo nitrato del tipo peroxiácilo y otros tipos de compuestos conteniendo el grupo peróxido e hidroperóxido). Está constituida, además, por partículas compuestas de ácido nítrico (NO3H), ácido sulfúrico (SO4H2), formados por oxidación de dióxido de nitrógeno (NO2) y de azufre (SO2), nitratos, sulfatos, sales de amonio, metales, hidrocarburos oxidados y agua. Se trata en definitiva de una composición química compleja, haciendo intervenir las fases gaseosa, líquida y sólida y que cuenta con la radiación solar para su evolución a partir de varios contaminantes. 71 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS 11.1.2 EFECTOS El síntoma más común ante la presencia de oxidantes de la niebla fotoquímica es la irritación de los ojos y garganta. Por otra parte se ha detectado un aumento de la morbilidad y mortandad en sujetos sensibles y grupos de riesgo, aunque se piensa que puede tener un efecto significativo en estos procesos el aumento de temperatura asociado a situaciones anticiclónicas que favorecen la presencia de estas sustancias. De hecho, se han realizado pruebas epidemiológicas en la ciudad de Los Ángeles, dando como resultado la ausencia de episodios de mortalidad inducida cuando la concentración de estos oxidantes se mantiene entre 0.5 y 0.9 ppm. No obstante se ha observado un aumento de las irritaciones en vías respiratorias y ojos en aquellas personas con especial sensibilidad (pacientes con afecciones asmáticas y broncopulmonares). Por otra parte, donde existe la niebla fotoquímica se detectan olores y disminuye la visibilidad Efectos sobre la vegetación. Son especialmente fitotóxicos, aunque la toxicidad depende de la especie considerada. En general producen bronceado y barnizado característico en el envés de las plantas sensibles. Efectos sobre los materiales. Cuarteado de materiales poliméricos y decoloración de pigmentos. Procesos de formación El proceso de formación comienza con la descomposición del NO2 en NO y oxígeno atómico (O) por acción de la radiación solar. El O reacciona con el O2 de la atmósfera dando lugar a O3, el cual reacciona a su vez con NO para formar de nuevo NO2, siempre en ausencia de hidrocarburos. La producción de ozono se encuentra fortalecida aún más en el caso de existir radicales oxigenados orgánicos (ROX). Estos radicales reaccionan rápidamente con el NO de la descomposición de NO2, reoxidando el mismo a NO2. Este NO2 se sigue descomponiendo ante la presencia de la radiación solar, formando más ozono. El ozono presente en exceso produce radicales libres muy reactivos si existen hidrocarburos con los que interaccionar: ROy + O3 → RO- 72 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS Estos radicales libres reaccionan con otros radicales, contaminantes primarios y componentes del aire, dando lugar a una mezcla de productos oxidados. Los hidrocarburos son, pues, esenciales para la formación de la niebla fotoquímica y su reactividad, medida por su capacidad de fotooxidar el monóxido de nitrógeno a dióxido, puede ser muy diferente: los más activos son las olefinas (exceptuando el etileno), seguidos de los aromáticos (salvo benceno y tolueno) y por último los alifáticos. El acetileno es prácticamente inactivo, como lo puede ser la capacidad irritante de los productos de la reacción. Esta contaminación se localiza en el entorno urbano (presencia masiva de hidrocarburos) y presenta un perfil muy característico al poner en relación su concentración con la hora del día. Es el responsable de la boina grisácea que envuelve ciertas ciudades y puede llegar a ser muy peligroso si se prolongan por mucho tiempo los factores que contribuyen a su formación. Presentan especial importancia dentro del proceso de smog fotoquímico el PAN y el ozono, que a continuación se comentarán. El nitrato de peroxiacetilo o PAN es uno de los oxidantes orgánicos principales y es un fuerte irritante, aunque lo es mucho más el nitrato de peroxibenzilo o PBN. Estos son compuestos con una estructura química genérica que responde a la fórmula R-CO-OO-NO2. El PAN se forma por la combinación de un radical peroxiacetilo y una molécula de NO2 en procesos como los anteriormente vistos. Ozono troposférico. Se ha comprobado que el ozono troposférico no deja de aumentar y actualmente se encuentra muy regulado. Altera la función de las mucosas del aparato respiratorio, y necrotiza los tejidos de ciertos vegetales a concentraciones del orden de 40 ppbv. La destrucción de bosques europeos, anteriormente atribuida a la lluvia ácida exclusivamente, ha de ser incluida entre los efectos del ozono, combinado con otros contaminantes y efectos. Con un ritmo de crecimiento anual del 2% pronto resultará imposible en muchas zonas cumplir con la normativa de limitación, de unas 55 ppb durante 8 horas, para la protección de la salud y 100 ppbv durante una hora, para la protección de los vegetales, impuesta por la legislación europea. Las reacciones fotoquímicas aportan un 80% del ozono troposférico, mientras que la estratosfera aporta el resto. En cuanto a los sumideros de ozono, la destrucción por fotólisis, la fotoquímica y la absorción del suelo y los vegetales parecen tener una contribución semejante. Los precursores del ozono troposférico se encuentran evolucionando tal y como muestra la tabla 2. 73 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS TABLA 2 RITMO DE CRECIMIENTO DE LOS PRECURSORES DEL OZONO TROPOSFÉRICO RITMO DE CRECIMIENTO ANUAL PRECURSOR CH4 0,7% CO 1a 3% en el hemisferio Norte 0 a 1% en el hemisferio Sur Hidrocarburos 0,8% a 1% NOx 1% a 2,5% Por ello cabe esperar que la concentración de ozono en la troposfera continúe aumentando, especialmente por el aumento de los NOx. RESUMEN: CONTAMINANTES FOTOQUÍMICOS Características de interés Se puede formar niebla fotoquímica (smog fotoquímico) cuando se dan las siguientes condiciones: ¾ Emisión de hidrocarburos y Nox (transporte urbano). ¾ Insolación (radiación ultravioleta). ¾ Inversión térmica (dificulta la dispersión de contaminantes). Esta niebla está caracterizada por la presencia de alto contenido de oxidantes, partículas ácidas, hidrocarburos oxidados y agua. El mecanismo de formación de estos componentes es complejo e involucra diferentes etapas, permaneciendo desconocido el proceso completo de formación. Los oxidantes más importantes dentro de este proceso son: ¾ Pan (nitrato de peroxiacetilo) ¾ Ozono Efectos mas importantes Irritaciones en ojos y garganta Olor Menor visibilidad Fitotoxicidad Alteración de ciertos materiales 74 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS 11.2 CONTAMINACIÓN ÁCIDA 11.2.1 CARACTERÍSTICAS Se entiende como tal la pérdida de la capacidad neutralizante del suelo y del agua como consecuencia de la deposición, en forma de compuestos ácidos, de los óxidos de azufre y nitrógeno atmosféricos. Es este un ejemplo claro de la interrelación de los diferentes compartimentos en que normalmente se divide el medio para su estudio, puesto que es este un efecto producido tras la interrelación de la atmósfera, suelo, agua y biosfera. La acidificación se ha convertido en un problema de grandes dimensiones, tanto desde el punto de vista de intensidad como de extensión espacial. La gran cantidad de SOX y NOX lanzados a la atmósfera propician contaminaciones severas que se ponen de manifiesto en zonas geográficas muy alejadas de los puntos de emisión, proceso de transporte que se ve favorecido por la estabilidad de estos compuestos. Proceso de formación: El proceso por el que se genera esta acidificación consta de las siguientes etapas: Azufre elemental fijado en los combustibles fósiles (ciclo biogeoquímico). Nitrógeno elemental en el aire y en los mismos combustibles. Ambos se liberan en la combustión de dichos combustibles, entrando en la atmósfera como SOX y NOX. Tras sufrir diversos procesos (de transporte y transformación química) precipitan y terminan depositándose de nuevo en la tierra, lo cual se lleva a cabo por dos vías Deposición seca: En las zonas próximas al foco emisor, los óxidos se depositan en forma de aerosoles o gaseosa, siendo ésta la forma predominante en dichas zonas. Deposición húmeda: Las transformaciones químicas que sufren estos óxidos en la atmósfera llevan a su oxidación a formas ácidas (H2SO4 y HNO3) las cuales se disuelven en las gotas de agua que forman las nubes y en las propias gotas de agua de lluvia, depositándose en el suelo. 75 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS De esta forma también pueden depositarse los óxidos no transformados. La proporción de deposición seca y húmeda de SO2 depende de la velocidad de oxidación, la cual se ve regulada por varios factores, como variaciones de concentración de este elemento y por la presencia de otras sustancias que retiren del medio compuestos oxidantes. Las precipitaciones se consideran ácidas cuando el pH alcanza un valor de 5.6 (valor correspondiente al de equilibrio del CO2 atmosférico con el agua). Entre los efectos generales que puede tener la lluvia ácida podemos encontrar tanto en el medio acuático como terrestre disminución del pH, pudiendo llegar a valores incompatibles con la vida y movilización de metales, que tienen como consecuencia el empobrecimiento de la vida (incluso desaparición de vida piscícola) en los lagos más afectados y degradación de cultivos y bosques. Por otra parte, la lluvia ácida tiene influencia en la degradación de los materiales de construcción y artísticos (mal de la piedra) y corrosión metálica. RESUMEN: CONTAMINACIÓN ÁCIDA Características de interés Perdida de capacidad neutralizante del suelo y del agua. Origen: Deposición de ácido nítrico y, especialmente, sulfúrico derivados de las emisiones contaminantes de óxidos de nitrógeno y dióxido de azufre.(Ver capítulo correspondiente) Sus efectos se pueden manifestar en zonas muy alejadas de los puntos de emisión. Se denomina precipitación ácida cuando el pH alcanza un valor de 5.6 (correspondiente al del equilibrio del CO2 atmosférico y el agua). Efectos mas importantes Alteraciones importantes en ecosistemas terrestres y acuáticos derivados de: ¾ Disminución del pH ¾ Movilización de metales Corrosión metálica y favorece el “mal de la piedra”. 76 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS 12 GLOSARIO* ÁCIDO NÍTRICO. Liquido humeante incoloro o amarillento de fórmula HNO3. Es muy corrosivo y sus vapores son muy tóxicos. El ácido nítrico y los nitratos (principalmente el nitrato de amonio) están presentes en la atmósfera en forma de aerosoles: el ácido se forma a partir del óxido de nitrógeno y reacciona después con el amoniaco para dar nitrato de amonio. ÁCIDO SULFÚRICO. Liquido oleaginoso denso, incoloro en estado puro; fórmula H2SO4. Es enormemente corrosivo y tóxico. El ácido sulfúrico es el más utilizado de todos los productos químicos. Como contaminante, aparece en la atmósfera, hidratado en función de la temperatura y la humedad ambiental, en forma de aerosol llamado “niebla de ácido sulfúrico”, producido por reacciones de oxidación lentas del dióxido de azufre atmosférico o emitido directamente por las chimeneas. Estos aerosoles son más difíciles de eliminar que el dióxido de azufre gaseoso, su tiempo de permanencia en la atmósfera es más largo y pueden recorrer grandes distancias gracias al viento. Pueden alcanzar los alvéolos pulmonares si haber sido detenidos por los órganos respiratorios superiores. Potencialmente muy dañinos, inhiben la actividad de los macrófagos pulmonares. Sin embargo, terminan por formar sulfatos como consecuencia de las posibilidades de reacciones de química atmosférica in situ con los numerosísimos aerosoles de sales de calcio de origen marino o terrestre siempre presentes en la atmósfera. AEROSOL. Suspensión, en un medio gaseoso, de partículas sólidas o líquidas que presentan una velocidad de caída despreciable. Las partículas sólidas forman un “aerosol de partículas sólidas” (y no un aerosol sólido), las partículas liquidas un “aerosol de partículas liquidas” o de microgotillas (y no un “aerosol liquido”). Las dimensiones de las partículas de un aerosol exceden con frecuencia de los limites coloidales normales (que son de 1 nm a 1 µm). AIRE. Mezcla gaseosa que compone la atmósfera terrestre. La composición aproximada del aire es, en volumen, de 78% de nitrógeno, 20,95% de oxigeno, 0,93% de argón y 0,03% de dióxido de carbono con cantidades mínimas de otras muchas sustancias. El contenido en vapor de agua es muy variable y depende de las condiciones atmosféricas. El aire se considera puro cuando ninguno de los componentes menores está presente con una concentración susceptible de perjudicar la salud de los seres humanos o de los animales, de dañar la vegetación o provocar una disminución del bienestar (por ejemplo * Gran número de estas definiciones se inspiran en vocabularios normalizados publicados por diferentes organizaciones internacionales (OMS, ICRS, CEI, ISO, etc.) 77 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS por la presencia de aerosoles, de polvos o de olores, o incluso por la absorción de la luz solar). ALCANO. Hidrocarburo alifático saturado (es decir que no contiene dobles enlaces carbono-carbono). Los alcanos tienen como fórmula general CnH2n+2. Los cuatro primeros miembros de la serie son el metano, el etano, el propano y el butano. “Alcano” es el nombre químico sistemático de cada uno de estos compuestos; se utiliza igualmente el término “parafina”. Los componentes básicos de la gasolina y de otros productos petrolífero son alcanos. AL QUENO. Hidrocarburo alifático que contiene al menos un doble enlace carbono-carbono. Los alquenos que contienen dos enlaces dobles se llaman dienos, los que contienen tres trienos, etc. “Aqueino” es el nombre químico sistemático de cada uno de estos compuestos; se utiliza igualmente el término “olefina” para designar a estos carburos de hidrogeno no saturados (etilénicos y acetilénicos). AMONIACO. Gas incoloro de fuerte olor asfixiante; fórmula: NH3. En la naturaleza es producido, entre otras reacciones, por la descomposición de materias vegetales. Es un componente normal del aire en el campo, donde se observan regularmente niveles de 5-10 µg/m3. BENCENO. Liquido claro incoloro, volátil e inflamable. Hidrocarburo aromático, fórmula C6H6. El benceno se utiliza a gran escala en las industrias químicas; es un constituyente menor de la gasolina. Es fuertemente tóxico; está probado que la exposición profesional a sus vapores entraña un aumento del riesgo de leucemia. BIOACUMULACIÓN. Acumulación de un elemento o compuesto en organismos vivos o en partes de los mismos. BIOMAGNIFICACIÓN. Bioacumulación ascendente a lo largo de la cadena trófica. CAPA DE OZONO (U OZONOSFERA). Capa de la atmósfera que se extiende entre los 10 y los 50 km aproximadamente (por encima de la superficie terrestre), y en la cual el porcentaje de ozono es relativamente elevado. La concentración máxima se presente generalmente, hacia los 20 ó 25 km. CFC´s. Clorofluorocarbonados, nombre colectivo para hidrocarburos volátiles que contienen fluor y cloro. Comúnmente, y equivocadamente, llamados freones. 78 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS CLOROSIS. Estado de deterioro de las planta verdes, caracterizado por el amarilleamiento y la decoloración, como consecuencia de la ausencia de ciertos oligoelementos o de la presencia de compuestos tóxicos en el suelo. Los mismos efectos aparentes se producen cuando la contaminación atmosférica (SO2, HF, etc.) sobrepasa un umbral crítico, variable según las especies y el estado vegetativo. CLORACNÉ. Acné clórica. CLORURO DE HIDRÓGENO. Gas incoloro, fórmula HCl, de olor sofocante, que despide vapores visibles en el aire húmedo. Es muy soluble en agua, siendo conocida la solución con el nombre de ácido clorhídrico. Tanto el gas como la solución son tóxicos, corrosivos y fitotóxicos (aunque lo sean menos para las plantas que el fluoruro de hidrógeno). El cloruro de hidrógeno era un contaminante muy abundante en el siglo XIX, porque era expulsado en grandes cantidades por las fábricas que utilizaban el procedimiento de pastel de sal (calentado del cloruro de sodio con el ácido sulfúrico). En nuestros días tiene una importancia relativamente baja como contaminante. COMBUSTIBLES FÓSILES. Nombre genérico de los combustibles que se han formado a partir de los residuos vegetales y animales (por ejemplo carbón y petróleo). COMBUSTIÓN. Reacción química en la cual un material se combina con el oxigeno con desprendimiento de calor. La combustión de las sustancias que contienen carbono e hidrógeno se llama combustión completa cuando estos dos elementos se oxidan íntegramente en dióxido de carbono y en agua. Una combustión incompleta puede dar como resultado: 1) la presencia de cantidades apreciables de carbono en las cenizas; 2) la emisión de una parte del carbono en forma de monóxido de carbono, y 3) la reacción de las moléculas de combustible para formar una serie de productos mas complejos que las propias moléculas de combustible. Si estos productos escapan a la combustión, serán lanzados en forma de humos. Se conseguirá una combustión mas completa de los productos volátiles si parte del aire (aire secundario) entra por encima y por debajo del lecho de combustión (el aire primario entra a través del combustible. El exceso de aire en relación con la cantidad teóricamente necesaria para la combustión completa, debe ser regulado al mínimo compatible con una combustión completa (y una ausencia de humos) para evitar una perdida excesiva de calor en los gases de chimenea, una mala transferencia de calor y la oxidación del dióxido de azufre en trióxido de azufre. Cuando la alimentación de combustible se hace por la parte superior del lecho de combustión, puede producirse humo. La combustión toroidal es un sistema en el cual se mantiene un torbellino en el hogar de la caldera, lo que 79 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS aumenta el tiempo de estancia del combustible en el hogar y mejora la combustión. Esta combustión necesita pues poco o ningún exceso de aire. CONTAMINACIÓN. Introducción o presencia de contaminantes, o la modificación indeseable de la composición de un medio liquido o gaseoso. Cuando se trata de la lucha contra la contaminación del aire, se llama “modificación indeseable” aquella que produce efectos dañinos o nocivos. La contaminación del aire, según la definición de Engeneers Joint Council es “la presencia en la atmósfera ambiente de uno o varios contaminantes como polvos, humos, gases, bruma, olores o vapores en cantidades, características y duración tales que esta presencia puede dañar a la salud del hombre, de las plantas y de los animales, así como al estado de los bienes o impedir al ser humano gozar, sin incomodidad, de la vida y de los bienes”. CONTAMINANTE (O POLUANTE). Materia sólida, liquida o gaseosa indeseable presente en un medio liquido o gaseoso. Un contaminante primario es el lanzado a la atmósfera por una fuente identificable. Un contaminante secundario es un contaminante formado por reacción química en la atmósfera. El smog oxidante es un contaminante secundario en relación a sus constituyentes que son por si mismos contaminantes. En lo que concierne a la contaminación atmosférica, los términos “poluante” y “contaminante” se utilizan como sinónimos. Sin embargo, ciertos autores, hacen una distinción, considerando el contaminante como una aportación de un constituyente, existente ya en la atmósfera, que causa una modificación en la composición de esta, composición que se aparta así de su valor medio global, pero sin embargo sin que se produzca un efecto nocivo perceptible a corto o medio plazo (por ejemplo CO2). DIÓXIDO DE AZUFRE. Gas o liquido incoloro (punto de ebullición: -10º C) de olor sofocante, fórmula SO2; fuertemente irritante y tóxico. El dióxido de azufre es un componente natural de la atmósfera, producido por la descomposición bacteriana de sulfatos en el suelo, por la oxidación del hidrógeno sulfurado procedente de la descomposición de materias orgánicas, por los volcanes, etc. Se estima que un tercio del dióxido de azufre de la atmósfera procede de la actividad humana, principalmente de la utilización de combustibles fósiles. El dióxido de azufre es uno de los contaminantes corrientemente medidos en red y se toma como indicador general de la contaminación en los niveles de alerta. Durante episodios celebres de contaminación atmosférica, se midieron altas concentraciones de SO2, sin embargo, es difícil precisar hasta que punto el dióxido de azufre es responsable del incremento en la mortalidad que pudo observarse en esos momentos. No hay prueba evidente de su nocividad para el hombre si en los niveles medios en el aire de las ciudades sólo se tuviera en cuenta el SO2 en ausencia de humos y polvos, sin embargo, no hay duda en cuanto a su responsabilidad en la corrosión de me- 80 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS tales y en la alteración de materiales de construcción, en particular piedras calcáreas. DIÓXIDO DE CARBONO. Gas incoloro e inodoro, de fórmula CO2. Es aproximadamente un 50% mas pesado que el aire del cual es un constituyente normal. Se forma en ciertos procesos naturales y durante la combustión de sustancias que contienen carbono. EDEMA. Acumulación excesiva de liquido seroalbuminoso en el tejido celular debido a diversas causas: disminución de la presión osmótica del plasma por reducción de las proteínas; aumento de la presión hidrostática en los capilares por insuficiencia cardiaca; mayor permeabilidad de las paredes capilares u obstrucción de las vais linfáticas. EFECTO INVERNADERO. Calentamiento de las capas inferiores de la atmósfera debido al hecho de que la radiación solar, de longitud de onda relativamente corta, penetra en la atmósfera sin sufrir una absorción apreciable y sólo es fuertemente absorbida en la superficie terrestre, mientras que la radiación terrestre, de longitud de onda larga, es absorbida por la atmósfera en una proporción mucho más importante. Este fenómeno ha sido llamado así por analogía con un invernadero en el cual el vidrio es mucho más transparente a las radiaciones solares de longitud de onda corta que a los rayos infrarrojos que provienen del interior del invernadero. Se han expresado temores a propósito del aumento de contenido de dióxido de carbono en la atmósfera. Esta podría ser la causa de la intensificación del efecto invernadero, y como consecuencia de un aumento de la temperatura, que si continuase durante algunos milenios, produciría modificaciones radicales en el clima del planeta. EPISODIO. Término utilizado en la literatura sobre la contaminación atmosférica para un número muy restringido de incidentes graves en el transcurso de los cuales, en ciertas circunstancias (inversión persistente de la temperatura, masa de aire estancada sobre una ciudad rodeada de colinas, fuga accidental de contaminantes industriales, etc.), la contaminación alcanza niveles anormalmente elevados manteniéndose durante un cierto lapso de tiempo. Tales situaciones son responsables de un aumento de la morbilidad y de la mortalidad. FITOTOXICIDAD. Propiedad de una sustancia, sólida, liquida o gaseosa, de ser dañina para las plantas; éste es el caso de numerosos contaminantes. FLUOROSIS. Envenenamiento crónico por flúor. Caquexia fluórica; enfermedad crónica del ganado que se halla próximo a fábricas que despiden emanaciones de flúor, caracterizada por rigidez muscular, fragilidad de los huesos y parálisis. 81 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS FLUORURO DE HIDRÓGENO. Gas humeante o liquido incoloro (punto de ebullición 19,5 º C), fórmula HF. Su solución acuosa se llama ácido fluorhídrico. Los dos son muy corrosivos y tóxicos. Muchas sales del ácido fluorhídrico (fluoruros) son también muy tóxicas. El ácido y los fluoruros causan daños a los cultivos próximos a las fábricas que los emiten, particularmente a aquellas que fabrican superfosfatos y sobre todo a las fundiciones de aluminio. Pueden tomarse medidas para evitar las emisiones de estas fábricas, pero no se ha encontrado todavía una solución para las emisiones mas débiles del ácido fluorhídrico y de compuestos como los hexafluorurosilicatos (“silicofloruros”) que provienen de las fábricas de briquetas. FREÓN ®. Nombre comercial reservado para ciertos hidrocarburos fluorados, utilizado exclusivamente por sus propiedades frigorígenas y no como sinónimo de hidrocarburo fluorado. FRIGORÍGENO. Fluido de baja temperatura de ebullición (SO2, NH4, freones, etc) utilizado para las transferencias de calor en los aparatos de refrigeración. Las sustancias empleadas con mas frecuencia para este fin son los fluorocarbonos, que son también corrientemente utilizados como “agentes propulsores” en las bombas para aerosoles. Pueden distinguirse unos de otros por sus nombres químicos o por sus designaciones internacionales. Estas últimas consisten en un numero precedido de la letra R (por ejemplo, R12 es el diclorofluorometano, R22 es el clorodifluorometano). Hay quienes temen que estos fluorocarbono se acumulen en las capas superiores de la atmósfera y puedan causar un empobrecimiento de ozono en la ozonosfera, lo que dejaría pasar una proporción mas grande de la radiación solar hasta el suelo, con los efectos nocivos que de ello resultaría para la salud de los seres vivos. GASOLINA. Destilado de petróleo cuyo intervalo de destilación se sitúa normalmente entre 30 y 220º C y que, combinado con ciertos aditivos, se destina a la alimentación de motores de encendido por chispa. Por extensión, este término se aplica igualmente a otros productos cuyo intervalo de destilación esta comprendido en los limites arriba mencionados (por ejemplo gasolina natural). Para los medios por los cuales, la gasolina y su combustión, pueden contribuir a la contaminación del aire ver entre otros monóxidos de carbono, hidrocarburo, óxidos de nitrógeno, smog y plomo tetraetilo. HALONES. Nombre que se da a los hidrocarburos volátiles que contienen flúor y bromo, es decir, los bromofluorocarbonados. HIDROCARBURO. Compuesto orgánico cuyos únicos elementos componentes son el carbono y el hidrogeno. Los átomos de carbono pueden estar orientados en cadenas abiertas, ramificadas o no (ver alcano y alqueno) y en ciclos cerrados. Hay dos tipos de hidrocarburos cíclicos: los “compuestos alici- 82 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS clicos” –que tienen al menos tres átomos de carbono en ciclos cerrados y cuyas propiedades son semejantes a las de las cadenas abiertas que tienen la misma masa molecular relativa- y los “hidrocarburos aromáticos”. La estructura molecular de los hidrocarburos aromáticos está basada en la del benceno que es la mas simple de esta familia y que contiene seis átomos de carbono unidos por tres enlaces simples y tres doble carbono-carbono. Cuando estos compuestos contienen al menos dos ciclos, se llaman “policíclicos”. Se utiliza igualmente el término “polinuclear”, sobre todo en la expresión “hidrocarburo polinuclear aromático” (HPA). Los constituyentes principales de la gasolina y de otros carburantes petrolíferos son hidrocarburos de cadena abierta. Estos compuestos no son peligrosos para la salud, ni siquiera en las concentraciones regulares del aire de las ciudades. Por el contrario, muchos hidrocarburos aromáticos son fuertemente tóxicos. La gasolina los contiene actualmente en pequeñas cantidades, pero es posible que se decida aumentar su proporción para compensar su bajo poder antidetonante debido a la reducción del contenido en plomo. Tal modificación plantearía, sin embargo, algunos problemas. Los hidrocarburos policíclicos mas conocidos son el antraceno, el naftaleno y la benzo [a] piridina. Teniendo en cuenta el poder cancerígeno de algunos de ellos, se excluye la posibilidad de recuperar el índice de octano añadiéndolos a la gasolina. HIPERPLASIA. Multiplicación anormal de los elementos de los tejidos. HIPERTROFIA. Desarrollo exagerado de los elementos anatómicos de una parte u órgano sin alteración de la estructura de los mismos, que da por resultado el aumento de peso y volumen del órgano. HOLLINES. Finas partículas de carbono que provienen de una combustión incompleta. HUMO. (refiriéndose a los separadores aerológicos). Conjunto de gases de combustión y de partículas arrastradas por ellos. (Por extensión, se aplica también a los gases cargados de partículas procedentes de un proceso químico o de una operación metalúrgica), ( en meteorología). Suspensión en la atmósfera de pequeñas partículas procedentes de combustiones diversas. Este término utilizado, utilizado en química, es definido menos restrictivamente como aerosol sólido (por ejemplo, humo de oxido de magnesio) o liquido (por ejemplo, humo de tabaco) procedente de una combustión, de una descomposición térmica, o de una evaporación que de lugar a vapores tensos y persistentes. La definición de este término en la legislación sobre la contaminación del aire puede variar, pero se refiere generalmente a las emisiones procedentes de una chimenea; la capacidad de este tipo de emisión puede ser expresada en unidades de la escala de Ringelmann. 83 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS INMISSION (INMISIÓN). Término alemán. En la R.F.A., las inmisiones son definidas oficialmente como “los contaminantes atmosféricos, el ruido, las vibraciones, la luz, el calor, las radiaciones y otros factores del medio ambiente a los cuales están expuestos los seres humanos, los animales, las plantas y los materiales”. Deben distinguirse de las emisiones (Emissionen) que se definen como “contaminantes atmosféricos, ruido, vibraciones, luz, calor radiaciones y otros fenómenos análogos emitidos por una instalación“ (Ley federal sobre la protección contra los contaminantes ambientales, 15 de marzo de 1974) (R.F.A.). LIXIVIACIÓN. Separación de los componentes de un material por acción de un disolvente adecuado. En el medio ambiente este disolvente suele ser el agua. MERCAPTANO. Sustancia orgánica que contiene un grupo –SH. Los mercaptanos son los análogos azufrados de los alcoholes y de los fenoles. Tienen un olor desagradable (el olor de los turones se debe a un mercaptano) y se añaden frecuentemente a los gases inodoros (por ejemplo al gas natural) para señalar inmediatamente cualquier fuga. El olor desagradable asociado a las refinerías de petróleo se debe en parte a los mercaptanos. A veces se les llama “tioles”. METANO. Gas incoloro e inodoro; formula CH4. Se inflama y da lugar en concentraciones críticas a mezclas explosivas con el aire. El metano es el principal constituyente de la mayor parte de los gases naturales y un constituyente mayor del gas de hulla. Se forma en el transcurso de la descomposición de materias orgánicas, sobre todo en los pantanos, de ahí su nombre corriente de “gas de los pantanos”. MONOXIDO DE CARBONO. Gas incoloro, casi inodoro, inflamable, formula CO. Se produce especialmente durante la combustión incompleta por falta de aire de materias orgánicas (por ejemplo, en los motores de automóviles). Normalmente en estado de trazas en la atmósfera, es muy tóxico en concentraciones superiores a 100 cm3/m3 (0,01%). Su afinidad por la hemoglobina, con la cual se combina para formar la carboxihemoglobina, es de 200 a 300 veces la del oxigeno. Esto trae como consecuencia la reducción de la capacidad de fijación y de transporte del oxigeno por la hemoglobina y que cause la muerte por asfixia. La concentración de monóxido de carbono en las calles de las ciudades, debida en gran parte a los gases de escape de los automóviles, puede ser lo suficientemente elevada como para resultar peligrosa, como puede serlo la que resulta del tabaquismo en habitaciones de atmósfera limitada. NIEBLA. Suspensión en la atmósfera de gotas muy pequeñas de agua, que reducen la visibilidad horizontal sobre la superficie del globo a menos de un kilometro 84 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS (cf. OMM). Niebla de advección. Niebla que se forma en la parte inferior de una masa de aire húmedo que se desplaza por sobre una superficie más fría . Niebla de evaporación. Niebla en la cual se alcanza la saturación en una masa de aire frío y estable por la evaporación rápida en la superficie del agua cálida subyacente. Niebla frontal. Niebla a lo largo de un frente, en cuya formación interviene la mezcla de las dos masas de aire que están presentes. Niebla al Sol. Niebla de radiación de débil extensión vertical, aunque frecuentemente densa, que deja ver las estrellas de noche y al sol de día. Niebla de inversión. Niebla provocada por la extensión hacia abajo, hasta el suelo, de una capa nubosa de stratus formada bajo un inversión. Niebla helada. Suspensión en la atmósfera de numerosos y minúsculos cristales de hielo, que reducen la visibilidad en la superficie del globo. Niebla de mezcla. Niebla ligera y de corta duración producida por la mezcla de dos masas de aire húmedo pero no saturado y de distintas temperaturas. Niebla de radiación. Niebla debida a la radiación nocturna, suficiente para inducir en la proximidad del suelo o, un enfriamiento del aire hasta la condensación del vapor de agua contenido en el aire. Niebla marina. Niebla de advección que se forma sobre el mar. Niebla de pendiente. Niebla formada sobre las pendientes de una colina o montaña expuestas al viento, a consecuencia de la ascensión forzada del aire, de la detención y del enfriamiento adiabático correspondiente. NITRÓGENO. Elemento gaseoso; número atómico 7, masa atómica relativa 14,0067, símbolo N. Es el constituyente principal del aire (4/5e). Su combinación con el oxigeno da compuestos NOx algunos de los cuales son enormemente tóxicos. NUCLEO (ATMOSFÉRICO). Partícula microscópica privilegiada sobre la que opera el paso del vapor de agua atmosférico a las fases liquida o sólida (cf. OMM). Núcleo de condensación: Núcleo sobre el cual se opera la condensación del vapor de agua . OXIDACIÓN. Pérdida de electrones que conlleva un aumento de la valencia. En su origen, este término significaba combinación con el oxigeno, actualmente se le da un sentido mas amplio. OXIDANTE. Sustancia oxidante, que como tal causan la oxidación. Los oxidantes atmosféricos son principalmente el ozono, el dióxido de nitrógeno y los peróxidos orgánicos. Liberan todo el yodo de las soluciones neutras de yoduro de potasio. Las concentraciones de “oxidantes” mencionadas en la literatura sobre la contaminación del aire, y medidas por este método, se calculan suponiendo que todo el yodo es liberado por el ozono, con el fin de facilitar la presentación de los resultados. OXIDOS DE NITROGENO. Designados generalmente por “NOx”; serie de siete compuestos, tres de los cuales tienen importancia en la atmósfera. El 85 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS óxido nitroso (protóxido de nitrógeno o gas hilarante), N2O, es un gas incoloro que desempeña sin duda un papel importante en el ciclo del nitrógeno. Es el mas abundante de los compuestos nitrogenados de la atmósfera, pero carece de interés como contaminante. El monóxido de nitrógeno (oxido nítrico), NO en un gas tóxico incoloro que reacciona espontáneamente con el oxigeno y muy fuertemente con el ozono para formar dióxido. Se produce en procesos de combustión, por ejemplo en las calderas y en los motores de combustión interna. Cuanto más elevada es la temperatura, mayor es la cantidad producida. Participa activamente en las reacciones atmosféricas causantes del smog fotoquímico. El dióxido de nitrógeno, NO2 es un gas fuertemente tóxico (vapores nitrosos) de color marrón rojizo. A temperatura ordinaria, el vapor es una mezcla en equilibrio de NO2 y del dímero N2O4. Este último se disocia si se calienta y aumenta el contenido en NO2. Por encima de los 140º C, el NO2 se disocia en NO y en oxigeno. El término “dióxido de nitrógeno” y la formula NO2 designan la mezcla en equilibrio. El termino “óxidos de nitrógeno” y el símbolo NOx son utilizados en la literatura sobre la contaminación del aire para designar la mezcla en el aire de NO y NO2. Cuantitativamente, la concentración de NOx se define como la concentración en NO2 realmente presente mas la concentración en NO2 resultante de la oxidación del NO presente. En los métodos analíticos corrientes, se mide primero el NO2 presente, se oxida el NO y se mide el suplemento de NO2 producido, lo que por diferencia da la concentración de NO. OXIGENO. Elemento gaseoso, número atómico 8, masa relativa 15,9994, símbolo O. El oxígeno molecular O2 representa aproximadamente el 20,95% en volumen del aire seco en la baja atmósfera; es indispensable para el mantenimiento de prácticamente todas las formas de vida. El oxigeno atómico O aparece en gran cantidad por encima de los 20 km de altitud y predomina a los 100 km. OZONO. Alotropo triatómico del oxígeno, gas azul claro, de olor picante característico; fórmula O3. Agente oxidante fuertemente activo y muy tóxico, está considerado como contaminante importante en concentraciones superiores a 120 µg/m3. Aparece en concentraciones mucho mas elevadas que esta tasa en la alta atmósfera, donde se forma por la acción de la radiación solar ultravioleta de longitud de onda corta, mezclándose una fracción en la baja atmósfera. Se forma también por las descargas eléctricas atmosféricas y por reacciones fotoquímicas en las que intervienen los hidrocarburos y los óxidos de nitrógeno (por ejemplo gas de escape de los motores de combustión interna). PARTÍCULA. Pequeña parte de materia líquida o sólida. 86 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS PLOMO. Elemento metálico, número atómico 82, masa atómica relativa 207,2, símbolo Pb. Muy tóxicos, el plomo (en forma de polvos) y sus componentes tienen un efecto acumulativo. Los compuestos pueden ser retenidos en los huesos, e inmediatamente liberados a la circulación sanguínea. Polvos conteniendo compuestos de plomo son enviados al aire no solamente por fábricas que utilicen este metal, sino también por la mayor parte de los centros metalúrgicos no ferrosos. Está también presente en las aglomeraciones y cerca de las vías de gran circulación, a causa de las emisiones de los automóviles que utilizan un carburante con un aditivo de plomo. PLOMO TETRAETILO. Liquido incoloro, fórmula Pb (C2H5)4, utilizado como agente antidetonante en la gasolina. Es tóxico por absorción cutánea y por inhalación. Ciertas autoridades consideran a esta sustancia como más peligrosa que otros compuestos de este metal. Vapores conteniendo plomo pueden ser enviados a la atmósfera por las estaciones de servicio y por los vehículos. El plomo contenido en la gasolina se encuentra también en forma de emisiones de plomo en los gases de escape. No está sin embargo, probado que las concentraciones actuales o previsibles sean dañinas, salvo en caso de concentración en la cadena alimentaria (es por lo que está prohibido que los animales pasten en las bandas laterales de 30 a 50 m de las vías de gran circulación). PLOMO TETRAMETILO. Liquido incoloro, fórmula Pb (CH3)4, agente antidetonante como el plomo tetraetilo, pero más activo que él; puede ser pues utilizado como aditivo en la gasolina en menores concentraciones consiguiendo el mismo efecto. Esta ventaja está descompensada por su volatilidad más elevada que aumenta el riesgo tóxico, por eso su uso está prohibido en muchos países. POLICLOROBIFENILO (PCB). Uno de los componentes de una serie de compuestos organoclorados que contienen dos núcleos fenilos unidos y una proporción variable de cloro. La mayor parte de los productos comerciales contienen muchos isómeros diferentes; algunos contienen también policlorotrifenilos. Los PCBs son muy usados en la industria eléctrica, sobre todo en los transformadores. También se utilizan como lubricantes, líquidos hidráulicos, plastificantes, ignífugos, etc. Son muy estables y se han propagado ampliamente en el medio ambiente. Sus efectos sobre la salud suscitan grandes preocupaciones. Se ha constatado recientemente la presencia de policlorobifenilos en la leche materna. POLVOS. Término general que designa a las partículas sólidas de dimensiones y procedencias diversas que pueden generalmente permanecer cierto tiempo en suspensión en un gas.. Las normas nacionales pueden ser más precisas e indicar el diámetro de las partículas o dar una definición haciendo intervenir un tamiz cu- 87 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS yas mallas estén especificadas. Los polvos presentes en la atmósfera pueden tener un origen natural o provenir de actividades humanas. POLVOS GRUESOS. Término general que designa a las partículas gruesas, a veces definidas como aquellas cuyo diámetro es superior a 75 µm. POLVOS RESPIRABLES. Materia particular en suspensión que puede depositarse en cantidad notable en el pulmón. No hay acuerdo general en cuanto a los tipos y dimensiones de las partículas; por ello, esta denominación puede tener significados diferentes según los autores. RADIACIÓN. a) Emisión o transporte de energía en forma de ondas electromagnéticas o de corpúsculos. b) Esta misma energía llamada también “energía radiante”. El término 2radiación” se reserva para una radiación monocromática. En radiofísica, la radiación es 1) electromagnética o de quantos de energía (rayos X y gamma; 2) corpuscular: a) de partículas cargadas (partículas alfa, electrones, protones, deutones); b) de partículas neutras (neutrones). La localización en el espectro electromagnético de los tipos de radiación aquí tratados se ilustra con el siguiente diagrama: Longitud de onda (m) 10-14 10-13 10-12 10-11 10-10 10-9 10-8 10-7 10-6 10-5 10-4 10-3 10-2 10-1 1 Rayos X cósmicos Fotones ultra violeta visible Rayos infrarrojo Rayos radar microondas gamma λ =3,8 x 10 −7 m λ =7,6 x 10 −7 m RADICAL LIBRE. Fragmento molecular o ion que tiene uno o varios electrones periféricos, lo que lo hace muy activo, aunque el tiempo de vida de los radicales libres sea generalmente corto, su gran reactividad les permite participar en reacciones químicas que no podrían realizarse de otra forma. En la atmósfera, ciertos radicales libres desempeñan un papel importante en la producción de aldehídos, de cetonas, de acetilnitroperóxido y de otros constituyentes del smog fotoquímico. 88 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS REACCIÓN FOTOQUIMICA. Reacción química provocada principalmente in situen la atmósfera por acción de la luz. Tales reacciones pueden ser desencadenadas únicamente por la absorción de fotones altamente energéticos; son principalmente debidas a una excitación electrónica y no pueden efectuarse en el campo del infrarrojo lejano. Son generalmente producidas por la luz visible y sobre todo ultravioleta. Estas reacciones son responsables entre otras cosas de la producción de smog fotoquímico y de las disociaciones observadas a gran altura. SEDIMENTACIÓN. Separación, a causa del peso, de las partículas en suspensión en un fluido. SMOG. Término inglés que denomina una niebla ácida fuertemente contaminada por humos, como la que existía frecuentemente en Londres. Este fenómeno está favorecido por la inversión de temperatura en invierno. Designan también una bruma lacrimógena (como en Los Angeles) producida por reacciones fotoquímicas favorecidas por el efecto de una radiación solar importante sobre el aire contaminado por los gases de escape de los automóviles en presencia de una inversión de temperatura. Este último tipo de smog se llama “smog fotoquímico” o “smog oxidante”. SULFATOS. Sales de ácido sulfúrico H2SO4. Entre los diversos sulfatos presentes en la atmósfera en forma de aerosol, el sulfato de amonio posee propiedades ácidas en solución acuosa y es corrosivo. Se origina parcialmente en la reacción entre los óxidos de azufre y el amoniaco. SULFURO DE HIDROGENO (ácido sulfhídrico). Gas incoloro de olor desagradable (a huevo podrido) perceptible incluso en pequeña concentración, fórmula H2S. Es extremadamente tóxico. El sulfuro de hidrógeno es un constituyente natural de la atmósfera aunque en pequeñas proporciones, por lo que no es perceptible ni peligroso (salvo en la proximidad de ciertos volcanes). Fugas accidentales procedentes de ciertas operaciones industriales han causado incidentes graves; incluso una fuga en una refinería de gas natural ha provocado muchas muertes. El sulfuro de hidrógeno afecta al olfato de tal manera que la presencia de gas no es detectada ni siquiera cuando las concentraciones superan ampliamente el límite de seguridad, lo que explica en parte, junto a la rapidez de acción de la dosis letal, el número de accidentes mortales observados. TERATOGENIA. Generación de malformaciones en fases de desarrollo. 2, 3, 7, 8 TETRACLORO DIBENZO (b,e) [1,4] DIOXINA. Compuesto que puede formarse como subproducto en la preparación de diversos compuestos 89 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS clorados del benceno, particularmente el triclorofenol y sus derivados, así como por procesos de combustión de materia orgánica con cloro.. Algunos de los primeros, utilizados como herbicidas, pueden ser contaminados por este compuesto de dioxina. Habitualmente conocido como “TCDD” o “dioxina”, es una de las sustancias más tóxicas; también es teratógena. Las otra dibenzodioxinas cloradas presentan propiedades similares. Se han dado casos de fallecimiento o de enfermedad debidos a la exposición profesional a la TCDD; se ha dado también el caso de que el compuesto se ha formado como consecuencia de un sobrecalentamiento accidental, etc., causando una contaminación atmosférica muy grave. TRIOXIDO DE AZUFRE. Oxido de azufre; fórmula SO3. Existe en estado sólido al menos en tres formas de las cuales una sola es estable, transformándose lentamente las otras dos en esta última. El trióxido de azufre se licúa completamente a los 44,5º C. Todas las formas del trióxido de azufre son extremadamente activas, corrosivas y tóxicas. Reaccionan inmediatamente con el agua para formar ácido sulfúrico en concentraciones que dependen de la temperatura y se disocian a alta temperatura formando dióxido de azufre y oxígeno. Cuando los combustibles arden a alta temperatura (en instalaciones industriales, por ejemplo), un 5% de azufre aparece en los gases calientes de la chimenea en forma de trióxido de azufre. Cuando la temperatura disminuye, se combina con el vapor de agua para formar una niebla de ácido sulfúrico. El trióxido de azufre no existe como tal en la atmósfera, a causa de la humedad ambiente. Cuando se publican los resultados de las concentraciones en trióxido de azufre, hay que considerar que son concentraciones en ácido sulfúrico expresadas por comodidad como de trióxido de azufre. TROPOPAUSA. Limite superior de la troposfera. Por acuerdo: la “primera tropopausa” se define como el nivel más bajo en el cual el gradiente vertical de temperatura llega a ser igual o inferior a 2º C/km, siempre que el gradiente medio entre este nivel y todos los niveles superiores, distantes menos de 2 km, no exceda 2º C/km TROPOSFERA. Capa inferior de la atmósfera terrestre comprendida entre el suelo y una altura que varía aproximadamente entre 9 km en los polos y 17 km en el ecuador, y en la cual la temperatura disminuye con regularidad con la altura . VISIBILIDAD. La distancia mas grande a la cual un objeto de color negro y de una dimensión dada es visible e identificable en silueta en el cielo, o cuando se trata de una observación nocturna, sería visible e identificable si la claridad ambiente se aumentase hasta la intensidad normal diurna Se puede medir la visibilidad nocturna utilizando luces no focalizadas y de intensidad determinada en lugar del objeto de color negro. Se puede también determinar la visibilidad con un aparato midiendo la atenuación de la luz en el trayecto largo. Los datos de visibilidad son generalmente observaciones hechas en todo el horizonte. 90 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS 13 BIBLIOGRAFÍA Derek Elson (1990), “La contaminación atmosférica”. Ed. Cátedra (Madrid, España). X. Domenech (1991), “Química Atmosférica. Origen y efectos de la contaminación”. Ed. Miraguano (Madrid, España). J. Manuel Sanz Sa (1991), “La contaminación Atmosférica”.Ed. Centro de Publicaciones del M.O.P.T.M.A. (Madrid, España). M.O.P.T.M.A. (1993), “Calidad del Aire en España 1990”. Ed. Centro de publicaciones del M.O.P.T.M.A. (Madrid, España). B. Magnus Francis. (1994), “Toxic Substances In The Environment”. Ed. John Wiley & Sons (New York, U.S.A.). J. Casanovas y Col (CID-CSIC), Daniel Fraisse (CNRS), Marco Gavinelli y Col (GEOS) (1996), “Dioxinas y Furanos. Problemática ambiental y metodología analítica”. Ed. Centro de publicaciones del M.O.P.T.M.A. (Madrid, España). ACID AIR POLLUTION. B. Stonehouse. 1986. ACID DEPOSITITION AND THE ACIDIFICATION OF SOILS AND WATERS. J. O. Reuss – D. W. Johnson. 1986. ACID DEPOSITION AND VEHICLE EMISSONS. Larry W. Canter. 1986. ACID DEPOSITION: SULPHUR AND NITROGEN OXIDES. A. H. Legge and S. V. Krupa. 1990. ACIDIFICATION OF FRESHWATERS. M. Cresser – A. Edwars. 1987. ACUTE EFFECTS ON HEALTH OF SMOG EPISODES. W.H.O. 1990. AIR POLLUTION. John H. Seinfeld. 91 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS AIR POLLUTION AND CANCER IN MAN. IARC Scientific Publications, nº 16. 1997. AIR POLLUTION AND HEATH EFFECTS. A Suvey of Research Proyect in European Countries Who Collaborating Centro for Air Quality. 1990. ASSESING TOXIC EFFECTS OF ENVIRNMENTAL POLLUTANTS. S.D. Lee and J. Brian Mudd. 1979. ATMOSPHERIC CHEMICAL COMPOUNDS. T.E. Gredel – D. T. HawkinsL.D. Claxton. 1986. ATMOSPHERIC CHEMISTRY FUNDAMENTALS AND EXPERIMENTAL TECHNIQUES. B.J. Finlayson – Pitts and J.N. Pitts Jr. 1986. ATMOSPHERIC POLLUTANTS IN FOREST AREAS. H.W. georgii. 1986. CHEMISTRY OF ACID RAIN, THE. R.W. Johnson – G.E. Gordon. 1987. CHEMISTRY OF THE NATURAL ATMOSPHERE. Peter Warneck. 1988. EFFECTS OR AIR POLLUTION Arthur C. Stern. 1977. INFORME SOBRE ACTIVIDADES Y EXPRESIÓN DE RESULTADOS OBTENIDOS EN LA RED NACIONAL DE VIGILANCIA Y PREVENCIÓN DE LA CONTAMINACIÓN ATMOSFÉRICA. Mº De Sanidad y Consumo. PARTICULATE AIR POLLUTION. Fco. J. Sosa, Publio L. Fajardo, Louis Theodore. 1980. POLLUTION IN THE URBAN ENVIRONMENT M. W. H. Chan. 1987. GLOBAL ATMOSPHERIC CHEMICAL CHANGE. C.N. Hewitt and W.T.Sturges. 92 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS 14 PÁGINAS WEB LEGISLACIÓN Ecoiuris: www.ecoiuris.com Brisa Web: www.min.es/brisaweb/brisaweb.htm BOE: www.boe.es DOCE (Diario Oficial de las Comunidades Europeas): europa.eu.int/eurlex/es/oj/index.html EPA: www.epa.gov/epahome/locate1.htm Ministerio de Industria: www.min.es/legisind/ (Legislación Industrial) AENOR (Normas UNE): www.aenor.es/busnor.htm) ISO (Normas ISO): www.iso.ch Ministerio de Medio Ambiente: www.mma.es OCDE: www.oecd.org Agencia Europea de Medio Ambiente: www.eea.eu.int Boletín Oficial del Estado digital (y otros): http://www.cde.ua.es/boe/ VARIOS CONTAMINACION ATMOSFERICA Y CEREBRO: http://www.arcride.edu.ar/servicios/comunica/publica/ceridivu/atmos.htm La UAM Azcapotzalco y el Gobierno de la Ciudad de México han creado una página http://www.calidad-del-aire.gob.mx/sima/ddf/_res-imk.html que 93 CONTAMINANTES: CARACTERÍSTICAS, ORIGEN Y EFECTOS proporciona los detalles de la calidad del aire de la Ciudad de México por zonas. Partículas Suspendidas: http://spin.com.mx/~rlibros/noticiasdelmundo/anteriores/gmp1.html Oficina del Aire y Radiación: www.epa.gov/oar/airtoxic.htm (contaminantes) www.epa.gov/ttn/uatw.htm (unified air toxic waste) www.epa.gov/opptintr/p2home/ (office of pollution prevention toxics) www.epa.gov/epahome/browse.htm (distintas oficinas de la EPA) Centro para la reducción del riesgo medioambiental y prevención de la Contaminación: cct.seas.ucla.edu/cct.cerrpp.html Red de medida de la contaminación atmosférica de Asturias: www.fomento.asturias.org/mamb/ BUSCADORES Yahoo: www.yahoo.com y www.yahoo.es Altavista: http://www.magallanes.net/cgibin/query?mss=simple&pg=q&lang=esp&country=esp&what=web y http://www.altavista.com/ 94