TRATAMIENTO DEL VARICOCELE POR TÉCNICAS
Anuncio

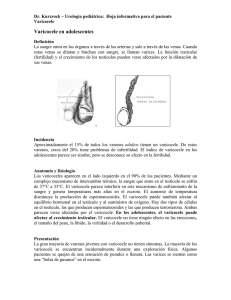
monográfico: varicocele e infertilidad masculina Arch. Esp. Urol., 57, 9 (929-939), 2004 TRATAMIENTO DEL VARICOCELE POR TÉCNICAS MICROQUIRÚRGICAS. Daniel Pascual Regueiro, Luis Rodríguez Vela, Alberto Gonzalvo Ibarra, Ángel García de Jalón Martínez, Eva Mallén Mateo y Luis Ángel Rioja Sanz. Servicio de Urología. Hospital Universitario Miguel Servet. Zaragoza. España. Resumen.- Tras una extensa revisión bibliográfica, exponemos de forma sencilla en este trabajo las posibilidades del tratamiento quirúrgico del varicocele, con especial desarrollo de las técnicas microquirúrgicas. Dichas técnicas no han sufrido muchas variaciones en los últimos años, encontrándose su uso generalizado dentro de la comunidad urológica. La menor incidencia de recidiva y de hidrocele por lesión linfática, hace que las técnicas retroperitoneales sean menos utilizadas a favor de las técnicas inguinales o subinguinales, microquirúrgicas o no. Para una mejor comprensión, tanto de la indicación quirúrgica como del desarrollo de las técnicas, hacemos unos breves comentarios anatómicos y fisiopatológicos del varicocele. Palabras clave: Varicocele. Infertilidad. Microcirugía. Summary.- We performed an extensive bibliographic search, and review the alternatives for surgical treatment of varicocele, especially microsurgical techniques. The surgical techniques for varicocele have not suffered much variation over the last years, being their use generalized among urologists. The lower incidence of relapse and secondary hydrocele to lymphatic lesion make retroperitoneal techniques be used less frequently in favour of inguinal or subinguinal techniques, microsurgical or not. For better understanding of the surgical indications and development of techniques we offer some short anatomical and physiopathological comments about varicocele. Keywords: Varicocele. Infertility. Microsurgery. Correspondencia INTRODUCCIÓN Dr. Luis Rodríguez Vela Servicio de Urología Hospital Universitario Miguel Servet Paseo Isabel la Católica 1-3 50009 Zaragoza. (España) El varicocele consiste en una dilatación varicosa de las venas espermáticas y/o del plexo pampiniforme testicular secundaria a un reflujo venoso. Se presenta en el 15% de la población general, en el 35% de los varones con infertilidad primaria, y en el 81% de los varones con infertilidad secundaria. La corrección del varicocele es con mucho la operación que se lleva a cabo con mayor frecuencia en el tratamiento de la infertilidad masculina. 930 D. Pascual Regueiro, L. Rodríguez Vela, A. Gondalvo Ibarra y cols. La patología varicosa testicular ha sido considerada, y sigue todavía siéndolo, como una de las causas más frecuentes de infertilidad masculina. Tal creencia se ha sustentado en algunas de estas consideraciones (Tabla I): a) Su incidencia es más elevada en hombres infértiles que en la población general. b) Se ha asociado con anomalías en la calidad seminal y en la histología testicular en el 20 al 50% de los varones. c) Después de la corrección del varicocele numerosas publicaciones han comprobado, en porcentajes variables, mejoría en la calidad seminal (del 40 al 80%) y en la frecuencia de embarazos (del 20 al 60%). Sin embargo en la literatura aparecen importantes controversias sobre el varicocele y la infertilidad, llegando algunos autores a negar cualquier relación basándose en que: a) Muchos varones con varicocele no presentan alteración en la calidad seminal y su fertilidad es normal. b) Su corrección no siempre mejora los parámetros seminales (del 20 al 60%). c) Existen embarazos en parejas de pacientes cuyo semen no mejora tras el tratamiento. d) Para algunos autores el porcentaje de embarazos tras la cirugía no es superior al que se consigue de manera espontánea en grupos control (15%). A pesar de ello, y aunque la fisiopatología del varicocele sobre la fertilidad siga siendo en parte un enigma, la asociación de ésta patología con microrquidia, alteraciones de los parámetros seminales, alteración de su función endocrina e histológica ha sido, claramente, establecida por numerosos autores, insistiendo en el varicocele como factor causal de infertilidad y en el beneficio de su tratamiento. En nuestra experiencia en el tratamiento de pacientes con infertilidad asociada a varicocele hemos podido observar una mejoría estadísticamente significativa (p>0.05) de la concentración de los espermatozoides, así como de su morfología y movilidad, tras el tratamiento del mismo, comparando el seminograma previo y a los nueve meses de la cirugía. Varios aspectos pueden explicar el por qué unos varicoceles conllevan hacia la orquiopatía varicosa (microrquidia, alteración seminal, lesiones histológicas, etc.) y otros no: 1. La existencia de distintos tipos de varicocele, según el plexo afectado. 2. Que existan conexiones entre los distintos plexos TABLA I. VARICOCELE E INFERTILIDAD SI Su incidencia es más elevada en hombres infértiles que en la población general. NO Muchos varones con varicocele no presentan alteración en la calidad seminal y su fertilidad es normal. Se ha asociado con anomalías en la calidad seminal y en la histología testicular en el 20 al 50% de los varones. Su corrección no siempre mejora los parámetros seminales (del 20 al 60%) y existen embarazos en parejas de pacientes cuyo semen no mejora tras el tratamiento. Después de la corrección del varicocele numerosas publicaciones han comprobado, en porcentajes variables, mejoría en la calidad seminal (del 40 al 80%) y en la frecuencia de embarazos (del 20 al 60%). Para algunos autores el porcentaje de embarazos tras la cirugía no es superior al que se consigue de manera espontánea en grupos control (15%). TRATAMIENTO DEL VARICOCELE POR TÉCNICAS MICROQUIRÚRGICAS venosos. Conexiones entre el plexo anterior con el cremastérico y deferencial y conexiones entre el lado izquierdo y el derecho. 3. Que la orquiopatía varicosa tenga una evolución progresiva, con distinto grado, en el tiempo, de la insuficiencia o alteración en el drenaje venoso. Se trataría de una patología vascular dinámica que alteraría la espermatogénesis en grado e intensidad diferentes. 4. Presencia de factores concomitantes en el varón o patología en el factor femenino. Teoría de los cofactores. BREVE RECUERDO ANATÓMICO El testículo tiene numerosas variantes anatómicas de drenaje venoso. (Seyferth, 1981; Bahaslu, 1983; Bigot, 1985; Murray, 1985). El plexo pampiniforme es el principal drenaje venoso del testículo, drenando a través de la vena espermática interna en la vena renal en el lado izquierdo y en la vena cava inferior en el lado derecho. Además, la sangre venosa testicular puede drenar: • a través de la vena cremastérica, vía vena epigástrica inferior, en la vena ilíaca externa. • a través de la vena deferencial, vía vena vesical inferior, en la vena hipogástrica. • la parte más distal del plexo pampiniforme drena, vía vena escrotal anterior, en la vena femoral, y a través de la vena escrotal posterior en la vena pudenda interna. 931 Por otra parte, existen varias venas comunicantes entre el lado izquierdo y el derecho, comprobándose en estudios necrópsicos que el tronco de la vena espermática interna se divide a nivel de L4 en una rama medial y otra lateral. (Mohamed) La división medial posteriormente se anastomosa con venas ureterales ipsilaterales y venas ureterales contralaterales en aproximadamente un 55% de los estudios realizados, a nivel de L3. La división lateral se anastomosa con venas colónicas y de la cápsula renal y perirrenales, de forma casi constante. (Mohamed) Esta comunicación con venas contralaterales explicaría el efecto de un varicocele izquierdo sobre la espermatogénesis en ambos testículos así como la recurrencia o persistencia del varicocele tras la cirugía. La ausencia de comunicantes contralaterales en un 45% de los casos, explicaría el porqué no todos los hombres con varicocele tienen alterada su espermatogénesis. Para finalizar este apartado debemos referirnos a la presencia de pequeños paquetes venosos testiculares que atraviesan el gubernaculum y drenan en la vena escrotal posterior. Estas pequeñas venas estarían presentes en un 48% de las disecciones quirúrgicas. (Beck, PN Schlegel & M Goldstein) La ligadura cuidadosa de estos paquetes venosos, condicionará una baja tasa de recidivas, que se mueve entorno al 0,5%, mientras que cuando no se realiza su ligadura la incidencia de recidivas estaría entre un 5 y 20%. (Szabo 1984, Kaye 1988) TABLA II. VARICOCELE: Tipos clínicos de Nistal TIPO I Varicocele espermático (axial) 80% Se debe a hiperpresión de la vena renal y fallo de la vena espermática interna. Suele condicionar la presencia de lesiones histológicas más graves, tanto locales como difusas. TIPO II Varicocele cremastérico (externo) 5%. Por hiperpresión de la vena ilíaca y fallo del plexo venoso posterior. Produce escasa repercusión testicular, afectando fundamentalmente a la función del epidídimo. TIPO III Mixto 15%. Por fallo de varios plexos venosos simultáneamente. 932 D. Pascual Regueiro, L. Rodríguez Vela, A. Gondalvo Ibarra y cols. CLASIFICACIÓN ANATOMOFISIOPATOLÓGICA: y bloqueo en la maduración del mismo en un 36%. Existen 3 tipos clínicos de varicocele descritos por Nistal (Tabla II): -Tipo I: Varicocele espermático (axial) Supone el 80% de los varicoceles. Se debe a hiperpresión de la vena renal y fallo de la vena espermática interna. Suele condicionar la presencia de lesiones histológicas más graves, tanto locales como difusas. - Tipo II: Varicocele cremastérico (externo) 5%. Por hiperpresión de la vena ilíaca y fallo del plexo venoso posterior. Produce escasa repercusión testicular, afectando fundamentalmente a la función del epidídimo. - Tipo III: Mixto 15%. Por fallo de varios plexos venosos simultáneamente. Por otro lado, los hallazgos más representativos del estudio con microscopía electrónica en estos pacientes suelen ser: - Fenómenos de detención de la maduración en estadio de espermatocito primario. - Espermátides mal orientadas en relación con las células de Sertoli. - Anomalías en los complejos de unión Sertoli-células germinales. REPERCUSIÓN DEL VARICOCELE Los hallazgos histológicos más frecuentemente observados bajo el microscopio óptico, en los pacientes con varicocele son (Tabla III): - Disminución del epitelio germinal. - Detención de la maduración en estadio de espermátide. - Desprendimiento de células espermatogónicas. En un estudio realizado por nosotros en pacientes con varicocele e infertilidad asociada, la biopsia testicular mostró como alteraciones: descamación del epiteliio germinativo en un 62% de los casos Los estudios en animales y humanos han demostrado la asociación existente entre el varicocele y la progresión y tiempo de duración de la disminución de la función testicular. El tiempo de evolución influye en la severidad de las alteraciones histológicas y seminales. Diferentes estudios histológicos han demostrado alteraciones testiculares en edad temprana y estas alteraciones son progresivas, lo que sugiere que sería preciso tratar cuanto antes esta patología. Todos estos hallazgos histológicos condicionan generalmente una alteración de la calidad del semen. Frecuentemente existe una relación directa entre el volumen del varicocele y las alteraciones de los parámetros seminales. Generalmente se aprecia un empeoramiento de la calidad seminal con oligoastenozoospermia relacionada con el grado del varicocele. Si existe una atrofia testicular con alteraciones seminales severas las posibilidades de recuperación son escasas. TABLA III. VARICOCELE: Hallazgos histológicos Microscopía óptica Microscopía electrónica Disminución del epitelio germinal Fenómenos de detención de la maduración en estadio de espermatocito primario Detención de la maduración en estadio de espermátide Espermátides mal orientadas en relación con las células de Sertoli Desprendimiento de células espermatogónicas Anomalías en los complejos de unión Sertolicélulas germinales TRATAMIENTO DEL VARICOCELE POR TÉCNICAS MICROQUIRÚRGICAS Los varicoceles tipo I y II pueden evolucionar hacia la forma mixta, afectando a más de un plexo venoso, dañando al testículo intensamente por múltiples mecanismos y produciendo lesiones irreversibles. La presencia de un varicocele suele condicionar que el testículo del lado afecto este disminuido de tamaño y consistencia en relación con el contralateral. Así pues, el tamaño testicular aporta un gran valor pronóstico sobre la fertilidad presente y futura. El descenso del volumen testicular con alteraciones histológicas tempranas es un dato objetivo que nos indica la necesidad de tratamiento del varicocele. El abordaje inguinal o subinguinal es el que goza de mayor popularidad. Presenta la ventaja de permitir sacar por fuera de la herida el cordón inguinal y de esta manera es más fácil identificar la arteria testicular, los linfáticos, vena espermática interna y las pequeñas venas periarteriales. Además, este abordaje Diferentes estudios han comprobado el aumento del tamaño testicular y la recuperación de sus funciones tras la corrección de un varicocele en la adolescencia. La normalización del tamaño testicular no se produce en la edad adulta. A pesar de algunos informes contradictorios, parece que las cifras séricas de testosterona y gonadotrofinas son, esencialmente, normales en los pacientes con varicocele. Tan sólo en los casos de oligozoospermia severa y varicocele, se puede apreciar una endocrinopatía subyacente con la afectación del eje hipotálamo hipófiso-testicular. BREVE DESCRIPCIÓN DE LAS DIFERENTES TÉCNICAS QUIRÚRGICAS • Abordajes Retroperitoneales: Ivanissevich-Palomo (1960): (Figura 1) Es una técnica rápida, se realiza mediante una incisión transversa por encima del anillo inguinal interno, apertura de los músculos oblicuos y exposición de arteria testicular y vena espermática interna cerca del uréter a nivel retroperitoneal. Generalmente, a este nivel la arteria testicular aún no se ha dicotomizado y se diferencia claramente de los troncos venosos próximos, evitándose así su lesión. El principal inconveniente de esta técnica es su alta incidencia de recidivas (15%) y la presencia de hidroceles secundarios (Goldstein). • Abordaje Inguinal: Varicocelectomía Inguinal: Las principales variantes técnicas inguinales son: - Buntz (1921) - Jiménez Cruz (1981) 933 FIGURA 1: Técnica retroperitoneal: IvanissevichPalomo 934 D. Pascual Regueiro, L. Rodríguez Vela, A. Gondalvo Ibarra y cols. inguinal permite acceder a la vena espermática externa e incluso puede permitirnos detectar las venas del gubernáculum testis que pueden realizar un by-pass del cordón espermático y producir recurrencia si no son ligadas. Se realiza un incisión de unos 5 cm. a nivel del canal inguinal o del anillo inguinal externo, se incide la aponeurosis del músculo oblicuo mayor y posteriormente se libera el cordón espermático pasando un Penrose o un vessel-loop por su parte posterior. Se abre el cordón espermático (Figura 2) y se van liberando y ligando la vena/s espermáticas internas y las pequeñas venas periarteriales. Deben preservarse la arteria testicular, los vasos linfáticos y el conducto deferente con sus vasos. Posteriormente ayudados por el Penrose se eleva el cordón espermático y las venas espermáticas externas que trascurren paralelamente al cordón espermático o que perforan el canal inguinal deben ser identificadas y ligadas. Puede realizarse peroperatoriamente un control con eco-doppler para comprobar que ha desaparecido el reflujo venoso. Este abordaje inguinal convencional presenta una incidencia de recidivas entre un 8 y un 10%. La complicación más frecuente es el hidrocele con una incidencia entre un 3 y un 15%. La aparición de hidrocele se debe a una ligadura inadvertida de linfáticos (Szabo). Inguinal (Buntz), obtuvimos los siguientes resultados: En 87 casos se utilizó una vía retroperitoneal y en 91 casos un abordaje inguinal. Pudimos observar una tasa global de persistencia del varicocele tras la intervención del 2.1%, y una tasa de recidiva global del mismo del 14 %. La recidiva del varicocele tratado mediante abordaje retroperitoneal fue de un 24%, mientras que la vía inguinal presentaba una tasa de un 5.5%, siendo las diferencias estadísticamente significativas (p<0.05), al igual que han demostrado otros estudios. • Varicocelectomia Laparoscópica: Es una técnica descrita por Sánchez de Badajoz en 1988, y dado que en este monográfico hay un capítulo dedicado enteramente a esta técnica, no vamos a insistir más en su descripción. En nuestro grupo dejamos de realizarla por 2 motivos: mayor tiempo quirúrgico que la cirugía convencional y, dado que es un abordaje retroperitoneal, presenta los mismos inconvenientes que el Ivanissevich-Palomo, mayor tasa de recidivas y mayor incidencia de hidrocele. En un estudio realizado por nuestro Servicio sobre un total de 178 varicoceles, y en relación a la disyuntiva en cuanto a la utilización de una vía retroperitoneal (Ivanissevitch-Palomo) o un abordaje • Técnicas Radiológicas de Oclusión y Escleroterapia: La oclusión de la vena espermática interna con balón o coil ha sido empleada con éxito en el tratamiento del varicocele, permitiendo la fácil preservación arterial y linfática, consiguiendo eliminar el riesgo de la atrofia testicular y del hidrocele post-quirúrgico. No obstante, ya sea mediante oclusión o escleroterapia presenta los mismos índices de recidiva que FIGURA 2 : Disección del cordón espermático. FIGURA 3: Abordaje subinguinal. Técnica de Marmar. TRATAMIENTO DEL VARICOCELE POR TÉCNICAS MICROQUIRÚRGICAS el abordaje retroperitoneal quirúrgico o laparoscopico. Dado que existe un capítulo en este monográfico dedicado a esta técnica, tampoco vamos a entrar en su descripción. TRATAMIENTOS MICROQUIRÚRGICOS • Tratamiento microquirúrgico subinguinal según técnica de Marmar (Figura 3) Describimos a continuación la técnica subinguinal microquirúrgica con anestesia local descrita por Marmar. Se comienza la intervención identificando el anillo inguinal externo e inyectando sobre la piel un anestésico, concretamente 1-3 cc. de Xilocaína al 1%. Posteriormente se realiza incisión posterior de 2-3 cm. a ese nivel y se libera hasta exponer el cordón espermático. Se anestesia un pequeño segmento de este cordón y con un clamp de Babcock se tracciona del cordón anestesiado. En este momento se seda al paciente con 10 mg./mL de Propafenol (Dipriván®). Se pasan dos Penrose por debajo del cordón espermático. En este punto se tracciona del Penrose hasta localizar las venas cremastéricas que se ligan. Se usa la disección microscópica para preservar los linfáticos y la arteria testicular. Si es preciso se utiliza- 935 rán 2 ó 3 mL. de Hidroclorhidrato de Papaverina para localizar la arteria, pues al aplicar esta sustancia sobre el campo quirúrgico se consigue evitar el espasmo arterial y consecuentemente facilitar su localización. Se ligan todas las venas del cordón espermático que excedan de 2 mm. de diámetro. En algunos casos se inyectarán entre 0,2 y 1,5 mL de Tetradecilsulfato de Sodio al 3% (Sotradecol®), agente esclerosante venoso, en las venas del campo quirúrgico previo clampaje proximal y distal del cordón inguinal mediante el cinchamiento de ambos Penrose. Posteriormente se finaliza el acto quirúrgico con el cierre por planos. Marmar en 466 procedimientos quirúrgicos refiere una incidencia de recurrencia con esta técnica del 2.1%. Las complicaciones más frecuentes fueron molestias epididimarias (5.5%) e hidrocele 0.8%. (Marmar) • Varicocelectomia inguinal o subinguinal microquirurgica con liberacion del testiculo. (Figura 4) Esta técnica permite la exposición del testículo a través de una pequeña incisión inguinal y proporciona un acceso visual directo a todos los posibles trayectos del drenaje venoso testicular. El microscopio intraoperatorio y las gafas lupas de 5x permiten la identificación de la arteria testicular, los vasos linfáticos y los pequeños vasos venosos. Según Goldstein, esta técnica mínimamente invasiva, condiciona una disminución importante en la aparición de hidrocele, lesión sobre la arteria testicular y recidiva del varicocele. Dado que existe el riesgo de lesionar la arteria testicular al llevar a cabo un bloqueo anestésico local a ciegas sobre el cordón espermático, es preferible utilizar una anestesia general suave o bien anestesia regional. FIGURA 4: Abordaje inguinal con liberación del testículo. Técnica microquirúrgica. Inicialmente se identifica el anillo inguinal externo invaginando la piel del escroto y a continuación se practica una incisión desde dicho anillo inguinal externo hacia afuera en una extensión de 3-4 cm. La incisión se profundiza a través de la fascia superficial, se retiran la arteria y vena epigástricas así como su tejido graso circundante y a continuación se separa la fascia dejando a la vista la aponeurosis del oblicuo mayor. 936 D. Pascual Regueiro, L. Rodríguez Vela, A. Gondalvo Ibarra y cols. TABLA IV. VARICOCELE: Técnicas quirúrgicas. IVANISSEVICH- PALOMO • Retroperitoneales • Inguinales BUNTZ JIMÉNEZ CRUZ • Laparoscópicas SÁNCHEZ DE BADAJOZ • Microquirúrgicas Subinguinal: MARMAR Inguinal o subinguinal con liberación del testículo Llegados a este punto decidimos si continuamos la intervención por vía inguinal, abriendo la aponeurosis del oblicuo mayor, o por vía subinguinal, justo por debajo del anillo inguinal externo dejando la fascia intacta. Las molestias post-operatorias son algo menores cuando se lleva a acabo la técnica subinguinalmente sin abrir la fascia. Sin embargo, a través de este abordaje se identifican más venas, la arteria se encuentra dividida y sus latidos están a menudo atenuados como consecuencia de la compresión ejercida en el borde del anillo inguinal externo. En la Tabla V se indican los criterios de Goldstein para llevar a cabo la intervención por vía inguinal (apertura del oblicuo mayor) o por vía subinguinal (fascia intacta). En general, el abordaje subinguinal es preferible en los pacientes con historia de cirugía inguinal previa. En estas circunstancias, el cordón se encuentra pegado generalmente a la superficie profunda del oblicuo mayor y al abrir la fascia se corre el riesgo de lesionarlo. Además, el abordaje subinguinal es mejor en pacientes obesos en los cuales la apertura y cierre de la fascia serían difíciles a través de una pequeña incisión; también es mejor en los pacientes con anillo inguinal externo alto, en localización atípica o muy amplio, así como en varones con cordones inguinales largos y testículos bajos. En estos pacientes el nivel del anillo inguinal externo está bastante próximal al testículo y abriendo la fascia no lograremos una disminución significativa del número de venas a ligar o de las ramas de la arteria testicular. El oblicuo mayor se debe abrir en niños y adolescentes prepúberes sin cirugía inguinal previa. En los niños la arteria testicular es muy fina y la presión arterial sistémica es baja por lo que la identificación de la arteria a través del abordaje subinguinal se hace muy difícil. La fascia se debe abrir asimismo en pacientes con un sólo testículo en los que la preservación de la arteria cobra una singular importancia. La TABLA V. CRITERIOS DE GOLDSTEIN PARA LA ELECCIÓN DE LA VÍA DE ABORDAJE Abordaje Inguinal Niños o adolescentes prepúberes Testículo único Anillo inguinal estrecho y bajo Pacientes delgados Abordaje subinguinal Historia de cirugía inguinal previa obesidad Anillo inguinal en situación atípica y muy amplio Anillo inguinal alto Cordón largo con testículo bajo TRATAMIENTO DEL VARICOCELE POR TÉCNICAS MICROQUIRÚRGICAS exposición más alta del cordón, que se consigue cuando se abre la fascia, permite generalmente la identificación de la arteria antes de que ésta se ramifique, en un punto en el que sus latidos son más fácilmente apreciados. La fascia debe abrirse en pacientes delgados con anillos inguinales estrechos y bajos. Ello permite una microdisección más rápida y sencilla. Si se opta por el abordaje inguinal la aponeurosis del oblicuo mayor se abre en toda la longitud de la incisión siguiendo la dirección de sus fibras, a través del anillo inguinal externo. Un punto de Vicryl de 3-0 colocado en el extremo de la incisión del oblicuo mayor facilitará su posterior cierre. Si se decide llevar a cabo el abordaje subinguinal no se abre el oblicuo mayor y el cordón espermático se coge, justo por debajo del anillo inguinal externo, con una pinza de Babcock y se exterioriza a través de la herida. La rama ileoinguinal y genital de los nervios genitofemorales se separan del cordón que queda independizado gracias a un drenaje de Penrose ancho. A continuación el cordón se diseca con el dedo ampliamente en dirección caudal hasta el escroto y el testículo es exteriorizado a continuación a través de la herida. Todas las venas espermáticas externas se identifican y ligan con seda de 4-0 seccionándose posteriormente. El gubernaculum es examinado por si existieran vasos venosos desde la túnica vaginalis, que son cauterizadas o ligadas. En este momento se inyectan 2 ml de bupivacaína al 0,75% en el espacio de la túnica vaginal con una aguja de calibre 25G, lo cual disminuye el dolor del post-operatorio. A continuación se reintroduce el testículo en el escroto y se coloca un drenaje de Penrose en el lecho del cordón. A partir de este momento es conveniente utilizar el microscopio operatorio o gafas lupas. Nosotros empleamos rutinariamente gafas de 4 aumentos que son fáciles de utilizar, disponibles en todos hospitales y que aportan los aumentos suficientes para una correcta disección sin dañar la arteria testicular. En este momento abrimos las fascias espermáticas externa e interna e irrigamos con papaverina al 1% el cordón para visualizar la existencia de pulsaciones que nos permitan identificar la arteria testicular. Posteriormente la disecaremos con un disector micro- 937 quirúrgico separándola del tejido subyacente (pequeñas venas y linfáticos) y la rodearemos con un lazo microvascular o una seda del cero para su identificación. Si sospechamos que ya tenemos la arteria pero no conseguimos identificar sus latidos con claridad podemos llevar a cabo un test de oclusión parcial elevando la arteria con los extremos del disector hasta que ésta se ocluya totalmente y a continuación la vamos descendiendo lentamente hasta que la columna pulsátil de sangre aparece justo sobre el disector. Si la arteria aún así no se identifica inmediatamente disecaremos el cordón cuidadosamente comenzando por la vena más grande. Liberamos los linfáticos que se adhieren a las venas y tras ello buscamos la arteria adherida a la parte inferior de las venas de mayor calibre. Aproximadamente en un 50% de los casos la arteria testicular se encuentra adherida a la parte inferior de una vena de gran calibre. Ligaremos todas las venas individualizadas del cordón, salvo las venas deferenciales, con seda de 4-0 y después seccionaremos dichas venas. Si los conductos deferentes se acompañan de venas dilatadas de un diámetro mayor de 3mm las disecaremos al margen de la arteria deferencial para su posterior ligadura. Los conductos deferentes se acompañan siempre de 2 paquetes vasculares. Al menos un paquete de venas deferenciales debe ser preservado para evitar la congestión venosa. Al finalizar la disección se palpa el cordón con el dedo índice con el fin de asegurarnos de que todas las venas se han identificado y ligado. Las pequeñas venas adheridas a la arteria testicular serán disecadas y ligadas o bien, si su diámetro es menor de 1mm, las cauterizaremos con un bisturí bipolar microquirúrgico para seccionarlas posteriormente. Al finalizar la disección sólo la arteria testicular, los linfáticos y los conductos deferentes con sus vasos permanecen intactos. En este momento inspeccionaremos nuevamente el cordón buscando signos de sangrado y tras ello cerraremos el cremáster y lo recolocaremos en su lecho anatómico. Cerramos la aponeurosis del oblicuo mayor, si la habíamos abierto, con Vicryl de 3/0. Cerramos la fascia de Scarpa y la fascia superficial con Vicryl de 3/0 y la piel la cerramos con grapas o seda 4/0. Finalmente colocaremos un suspensorio rellenado con gasas. El paciente puede ser dado de 938 D. Pascual Regueiro, L. Rodríguez Vela, A. Gondalvo Ibarra y cols. alta el mismo día de la cirugía administrándole un tratamiento con analgésicos y/o antiinflamatorios durante 4-5 días. 12. Esta técnica con el uso de microscopio operatorio permite una preservación de la arteria testicular y de los linfáticos disminuyendo el riesgo de formación de hidrocele y disminuyendo la incidencia de atrofia testicular. En la serie de Goldstein la incidencia de recidiva es del 0.5%. Comparándola con la tecnica subinguinal, el abordaje inguinal reduce el número de venas que deben ser ligadas y evita la administración de agentes esclerosantes. *13. BIBLIOGRAFIA y LECTURAS RECOMENDADAS (*lectura de interés y **lectura fundamental) 1. *2. 3. 4. 5. 6. **7. 8. 9. 10. 11. ÁLVAREZ, E.: “Varicocele y fertilidad.” Andrología, teoría y práctica. Madrid: Díaz de Santos.102. 1989. ARRONDO, J.L.; BARBERANA, F.J.; URTASUN, F.: “Varicocele.” Andrología Práctica. (J.L. Arrondo y J. Pomerol Eds.). Ed. Masson-Salvat Medicina. Pag:198. Barcelona. 1994. BAYO, A.: “Cirugía convencional del varicocele.” Libro de resumenes del 7 Congreso Nacional de Andrología. (Editor: A. Astobieta), pag:167, Bilbao. 1995. BECK, E.M.; SCHLEGEL, P.N.; GOLDSTEIN, M.: “Intraoperative varicocele anatomy: a macroscopic and microscopic study.” J. Urol. 148: 1190. 1992. BIASE, J.N.; NAGLER, H.M.: “The varicocele: current concepts and controversies.” Current Oponion in Urology. 2:463. 1992. BRAEDEL, H.U.; STEFFENS, J.; ZIEGLER, M. y cols.: “Out-patient sclerotherapy od idiopathic leftsided varicocele in children and adults.” Br. J. Urol. 65:536. 1990. CAYAN, S.; KADIOGLU, T.C.; TEFEKLI, A. y cols.: “Comparison of results and complications of high ligation surgery and microsurgical high inguinal varicocelectomy in the treatment of varicocele.” Urology. 55:750. 2000. CENTOLA, G.M.; LEE, K.; COCKEIT, A.T.K.: “Relationship between testicular volumen and presence of varicocele.” Fertil Steril. 30:479. 1987. COCKETT, A.T.K.; URRY, R.L.; DOUGHERTY, K.A.: “The varicocele and semen characteristics.” J. Urol. 121:435. 1979. CHEHVAL, M.J.; PURCELL, M.H.: “Deterioration of semen parameters over time in men with untreated varicocele: evidence of progressive testicular damage.” Fertil Steril. 57:174.1992. CHEHVAL, M.J.; PURCELL, M.H.: “Varicocelectomy: incidence of external spermatic vein involvement in the clinical varicocele.” Urology. 39:573. 1992. 14. **15. 16. *17. *18. 19. *20. 21. 22. 23. 24. 25. 26. 27. *28. DE PORTILLO, L.: “Técnicas radiológicas combinadas con cirugía convencional en el tratamiento del varicocele.” Libro de resumenes del 7 Congreso Nacional de Andrología. (Editor: A. Astobieta), pag:174, Bilbao. 1995. DUBIN, L.; AMELAR, R.D.: “Varicocelectomy: 986 cases in a twelve year study.” Urology. 10:446. 1977. FIELDS, D.W.; GOLDSTEIN, M.: “Pain and the time to recovery after inguinal versus subinguinal varicocelectomy: A randomized prospective double blind study.” Presented al the Annual Meeting of the American Fertility Society. San Antonio, TX. Abstract. 1994. GOLDSTEIN, M.; GILBERT, B.R.; DICKER, A.P.; DWOSH, J.; GNECCO, C.: “Microsurgical inguinal varicocelectomy with delivery of the testis: An artery and lymphatic sparing technique.” J. Urol. 148:1808. 1992. GOLDSTEIN, M.; YOUNG, G.P.H.; EINER-JENSEN, N.: “Testicular artery damage due to infiltration with a finegauge needle: Experimental evidence suggesting that blind spermatic cord block should be abandoned.” Surg. Forum. 34:653. 1983. GOLDSTEIN, M.: “Complications and results of varicocelectomy.” Goldstein M, eds. Surgery of Male Infertility. New York: Saunders. 194. 1995. GOLDSTEIN, M.: “Mini incision microsurgical inguinal or subinguinal varicocelectomy with delivery of the testis.” Goldstein M, eds. Surgery of Male Infertility. New York: Saunders. 173. 1995. GOLDSTEIN, M.: “Varicocelectomy: General considerations.” Goldstein M, eds. Surgery of Male Infertility. New York: Saunders. 169. 1995. GOLDSTEIN, M.: “Varicocelectomy: Subinguinal approach.” Goldstein M, eds. Surgery of Male Infertility. New York: Saunders.178. 1995. GOLDSTEIN, M.: “Surgical therapy of male infertility (editorial).” J. Urol. 149:1373. 1993. GORELICK, J.I.; GOLDSTEIN, M.: “Loss of fertility in men with varicocele.” Fertil Steril. 59:613. 1993. HENDRY, W.F.: “Effects of left varicocele ligation in subfertile males with absent or atrophic right testes.” Fertil Steril. 57:1342. 1992. HIROKAWA, M.Ê; MATSUSHITA, K.Ê; IWAMOTO, T. y cols.: “ Assesment of Palomo’s operative method for infertile varicocele.” Andrologia. 25:47. 1993. HIRSCH, I.R.; ABDEL-MEGUID, T.A.; GOMELLA, L.G.: “Postsurgical outcomes assessment following varicocele ligation: Laparoscopic versus subinguinal approach.” Urology.51:810. 1998. HOMONNAI, Z.T.; FAINMAN, N.; ENGELHARD, Y. y cols.: “Varicocelectomy and male fertility: Comparison of semen quality and recurrence of varicocele following varicocelectomy by two techniques.” Int. J. Androl.3:447. 1980. JAROW, J.P.; OGLE, S.R.; ESKEW, A.: “Seminal improvement following repair of ultrasound detected subclinical varicoceles.” J. Urol. 155:1287. 1996. JIMÉNEZ CRUZ, F.; ALLONA, A.; NAVIO, S. Y cols.: “Modificación de la técnica de Buntz en la cirugía del varicocele: resultados.” Actas Urol. Esp.7:401. 939 29. 30. *31. 32. **33. 34. **35. *36. *37. 38. 39. 40. *41. 1983. KASS, E.J.; BELMAN, A.B.: “Reversal of testicular growth failure by varicocele ligation.” J. Urol.137:475. 1987. KASS, E.J.; CHANDRA, E.S.; BELMAN, A.B.: “Testicular histology in the adolescent with a varicocele.” Pediatrics.79:996. 1987. KASS, E.J.; FREITAS, J.E.; BOUR, J.B.: “Adolescent varicocele: objective indications for treatment.” J. Urol.142:579. 1989. KAUFFMAN, S.L.; KADIR, S.; BARTH, K.H. y cols.: “Mechanisms of recurrent varicocele after balloon occlusion or surgical ligation of the internal spermatic vein.” Radiology.147:435. 1983. LEMACK, G.E.; UZZO, R.G.; SCHLEGEL, P.N. y cols.: “Microsurgical repair of the adolescent varicocele.” J. Urol.160:179. 1998. LIPSHULTZ, L.I.; CORRIERE, J.N.: “Progressive testicular atrophy in the varicocele patient.” J. Urol.117:175. 1977. MARMAR, J.L.; DE BENEDICTIS, T.J.; PRAISS, D.: “The management of varicoceles by microdissection of the spermatic cord at the external inguinal ring.” Fertil Steril.43:583. 1985. MEACHAM, R.B.; TOWNSEND, R.R.; RADEMACHER, D.; DROSE, J.A.: “The incidence of varicocele in the general population when evaluated by physical examination, gray scale sonography and color doppler sonography.” J. Urol.151:1535. 1994. MINEVICH, E.; WACKSMAN, J.; LEWIS, A.G.; SHELDON, C.A.: “Inguinal microsurgical varicocelectomy in the adolescent: Technique and preliminary results.” J. Urol.159:1022. 1998. MONZÓN, F.: “Corrección quirúrgica del varicocele por vía laparcópica.” Libro de resumenes del 7 Congreso Nacional de Andrología. (Editor: A. Astobieta), pag:185, Bilbao. 1995. NAGLER, H.M.; PENG, B.C.H.; TOMASHEFSKY, P.: “The cofactor effect: varicocele and infertility.” Fertil Steril.54:143. 1990. NILSSON, S.; EDVINSSON, A.; NILSSON, B.: “Improvement of semen and pregnancy rate after ligation and division of the internal spermatic vein: Fact or fiction?.” Br. J. Urol.51:591. 1979. NISTAL, M.; REDONDO, E.: “Varicocele, histología y etiopatogenia.” III Congreso Nacional de Andrología. Edita ASESA: 59. 1987. 42. 43. 44. 45. 46. 47. 48. 49. 50. *51. *52. 53. 54. 55. *56. OKUYAMA, A.; NAKAMURA, M.; NAMIKI, M. y cols.: “Surgical repair of varicocele at puberty: Preventive treatment for fertility improvement.” J. Urol.139:562. 1988. PALOMO, A.: “Radical cure of varicocele by a new technique: preliminary report.” J. Urol.61:604. 1949. PINTO, K.J.; KROOVAND, R.L.; JAROW, J.P.: “Varicocele related testicular atrophy and its predictive effect upon fertility.” J. Urol.152: 788. 1994. RAGETH, J.C.Ê; UNGER, C.Ê; DARUNGA, D. y cols.: “Long-term results of varicocelectomy.” Urol. Int.48:327. 1992. ROTHMAN, L.P.; NEWMARK, M.; KARSON, R.: “The recurrent varicocele. A poorly recognized problem.” Fertil Steril.35:552. 1981. SÁNCHEZ DE BADAJOZ, E.; DÍAZ RAMÍREZ, F.: “Tratamiento laparoscópico del varicocele.” Arch. Esp. Urol.44:263. 1991. SAWCZUK, I.S.; HENSLE, T.W.; BURBIGE, K.A. y cols.: “Varicocele: effect on testicular volume in prepubertal and pubertal male.” Urology.41:466. 1993. SAYFAN, J.; SOFFER, Y.; ORDA, R.: “Varicocele treatment: Prospective randomized trial of 3 methods.” J. Urol.148:1447. 1992. SCHERR, D.; GOLDSTEIN, M.: “Comparison of bilateral versus unilateral varicocelectomy in men with palpable bilateral varicoceles.” J. Urol.162:85. 1999. SCHLESINGER, M.H.; ILENE, F.; WILETS, I.F. y cols.: “Treatment outcome after varicocelectomy.” Urologic Clinics of North America. 21: 517. 1994. STECKEL, J.; DICKER, A.; GOLDSTEIN, M.: “Relationship between varicocele size and response to varicocelectomy.” J. Urol.149:769. 1993. SZABO, R.; KESSLER, R.: “Hydrocele following internal spermatic vein ligation: A retrospective study and review of the literature.” J. Urol. 132:924. 1984. VERMEULEN, A.; VANDEWEGHE, M.: “Improved fertility after varicocele corrrection: Fact or fiction?.” Fertil Steril.42:249. 1984. WISHAHI, M.M.: “Detailed anatomy of the internal spermatic vein and the ovarian vein. Human cadaver study and operative spermatic venography: clinical aspects.” J. Urol.145:780. 1991. WORLD HEALTH ORGANIZATION.: “Comparison among different methods for the diagnosis of varicocele.” Fertil Steril.43:575. 1985.