Intercambio Isotópico de Deuterio entre el Hidrógeno y el Agua en
Anuncio

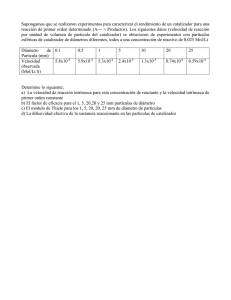
REPÚBLICA ARGENTINA COMISIÓN NACIONAL DE ENERGÍA ATÓMICA INFORME N- 56 Intercambio Isotópico de Deuterio entre el Hidrógeno y el Agua en Fase Vapor por WALTER J. BARAN y RUBÉN BUENOS 1961 F. AIRES CRETELLA I N T E R C A M B I O ISOTÓPICO D E D E U T E R I O E N T R E EL HIDROGENO Y EL A G U A EN FASE VAPOR WALTER J. BARAN y RUBÉN F. CRETELLA El objeto del presente trabajo ha sido diseñar u n dispositivo apto para la medida de actividades catalíticas de la reacción de intercambio isotópico H 0 2 (v) + H D — H D O (v) + HE [1] y determinar experimentalmente, haciendo uso de consideraciones cinéticas para interpretar los resultados, las condiciones óptimas de funcionamiento. INTRODUCCIÓN E n todo proceso industrial para la obtención del óxido de deuterio ( D 2 O ) , también llamado "agua pesada", adquiere singular importancia la etapa del preenriquecimiento, es decir, la de llevar la concentración, que e n el agua natural es del orden de 0,015 moles % , a 2 moles % D 0 aproximadamente. Entre las reacciones de intercambio isotópico de deuterio que se pueden utilizar para ello, se encuentran las que se verifican entre el hidrógeno y el agua en fase gaseosa. D e las p o sibles reacciones entre ambas especies químicas elegimos la [ 1 ] , que predomina a bajas concentraciones de deuterio y c u y a constante de equilibrio K a 2 5 ° C es, según cálculos teóricos, igual a 3,62, pudiéndose demostrar que dicha constante es igual al factor de separación a del proceso. 2 D e la observación de las tablas que dan la variación de K con la t e m p e r a t u r a se deduce la conveniencia de trabajar a bajas temperaturas, pero c o m o en esas condiciones la velocidad de reacción resulta ser pequeña, enfrentamos una situación de c o m p r o m i s o que obliga a trabajar a unos 8 2 ° C en donde a = 2,83 y la tensión de v a p o r del agua 384,9 m m H g , lo que permite la m e z c l a casi e q u i m o l a r entre el hidrógeno y el agua. A d e m á s se puede aumentar la velocidad de reacción sin modificar el equilibrio, utilizando catalizadores apropiados. A s í , durante el desarrollo de nuestro trabajo empleamos u n catalizador de Pt cuyas características eran: Pt al 4 % sobre carbón activado, que pasa a través de malla 20, pero queda retenido e n el siguiente t a m a ñ o de malla y c u y a densidad es de 1,8 g / c m (Baker Platinum Limited. Londres). 1 3 1 I. Kirshembaum, Physical properties and analysis of heavy water, 48, 1951. ? Preparazione e comportarnento di alcuni catalizzatori per la reazione di scambio isotópico del deuterio fra idrogeno e vapor d'acque, B. Brigoli, E. Cerrai, R. Renzoni, M . Silvestri, suplemento al vol. V, serie X, del "Nuovo Cimento", N° 3, primer semestre, 479, 1957. Trabajo presentado para su publicación en mayo de 1961. 4 Reacción de intercambio isotópico D e s i g n a n d o las concentraciones de las especies moleculares intervienen en la r e a c c i ó n de la siguiente m a n e r a que 2 (H 0) + 2 (HDO) = a (HD) = z (HD) = b (HDO) = x (Ha) + y c o n k y k las velocidades específicas de i n t e r c a m b i o de izquierda a derecha y de derecha a izquierda, respectivamente, la v e l o c i d a d absoluta del sistema, vale decir, la de d e s c o m p o s i c i ó n del H D O , se puede expresar x 2 dx - — dt dz = — x (b = dt z) z (a - x) \J\ ki ¿2 a b b a en el equilibrio siendo x 0 0 1 ka K kj. x°° b — z r o y z°° las concentraciones en el equilibrio. Si son bajas las concentraciones de deuterio, x°° • b K-a y como xo + z = x 0 0 0 se obtiene, + z°° reemplazando, siendo y = b / a la inversa de la relación m o l a r hidrógeno-agua y considerando despreciable la concentración inicial de deuterio en el hidrógeno. Para el cálculo de x°° se utilizó el v a l o r de K e m a n a d o de log K = 212,878 ^ - 0,15052 ecuación basada en datos teóricos (funciones de p a r t i c i ó n ) . Descripción del aparato E l dispositivo q u e h e m o s e m p l e a d o en nuestras experiencias se halla representado en el diagrama q u e figura a continuación. En él puede apreciarse el circuito q u e describe el h i d r ó g e n o proveniente del t u b o de almacenaje, el acceso del m i s m o a la cámara de h u m i d i - 5 ficación, su salida de la cámara de catálisis y el recipiente posterior destinado a la condensación del agua que lo satura y con la cual ha intercambiado deuterio. Precisamente el análisis isotópico de dicha agua es lo que nos ha permitido seguir el curso de la reacción. 1: T u b o de almacenaje de hidrógeno; conc. 0,010 moles % D 0 (obtenida por c o m b u s t i ó n ) . M e d i d o r del caudal de hidrógeno. 2 Entrada del hidrógeno a la cámara de humidificación. Columna de humidificación. Entrada del agua. T e r m ó m e t r o para controlar su temperatura. Termostato con b o m b a circulante. Salida del agua. T e r m ó m e t r o para controlar la temperatura en la parte m e dia de la columna. 12: Cámara catalítica. 14: T u b o condensador donde se recoge el agua del intercambio. que participó 16: T r a m p a con nieve carbónica para retener el resto de hum e d a d del hidrógeno. 17 Diseño Integrador para la medida de la cantidad de hidrógeno que circula. del aparato El diseño del equipo empleado demandó la resolución de serie de problemas. Los principales fueron: 1) M e z c l a equimolar del H 2 una c o n vapor de agua. Ello es consecuencia del carácter equimolar de la reacción en estudio, y señalamos que, luego de ensayar numerosos dispositivos, se utilizó c o n t o d o éxito una c o l u m n a inundada, de vidrio, de 33 c m de longitud y 5,5 c m de diámetro intern o , rellena c o n trozos de b r o n c e fosforado de malla 2 0 0 , 6 p r o c u r a n d o que el agua cubriera totalmente el r e l l e n o durante las experiencias para evitar condensaciones locales. A fin de m a n t e n e r la temperatura del agua ( e l h i d r ó g e n o la enfría al atravesarla), se la h i z o circular a través de u n termostato regulado eléctricamente al 0,1° C. C o m o control se colocaron termómetros en la c o l u m n a . Resistencias externas accionadas p o r transformadores de f u n c i o n a m i e n t o variable c o m p e n s a r o n las pérdidas de calor. C o n u n dispositivo de este tipo a l c a n z a m o s una h u m e d a d m o l a r del 100 % hasta caudales de 100 1/h, valor que adoptamos c o m o límite para la m e z c l a e q u i m o l a r en nuestro equipo. 2) C o m b u s t i ó n del h i d r ó g e n o q u e sale del aparato. L a cinética de la r e a c c i ó n considerada está gobernada por una constante de equilibrio, para c u y a determinación práctica fue necesario m e d i r s i m p l e m e n t e la c o n c e n t r a c i ó n e n deuterio de las especies moleculares H D O y H D . C o n ese fin debimos q u e m a r este último, pues el aparato de m e d i c i ó n se basa en el m é t o d o del flotador q u e utiliza agua al estado líquido. Para caudales bajos de H e m p l e a m o s u n tubo de vidrio de 3 c m de diámetro interno, relleno de C u , d o n d e se u n í a n las corrientes de h i d r ó g e n o y c o m b u r e n t e ( o x í g e n o ) . Este tubo se c o l o c ó en u n h o r n o eléctrico a 6 0 0 ° C, y para evitar la fusión del e x t r e m o del tubo de acceso de h i d r ó g e n o , se colocaron dedalillos de material refractario. C o m o este dispositivo era p r o p e n s o a las explosiones al trabajar c o n caudales considerables de H , para este ú l t i m o r a n g o se utilizó u n c a ñ o de Cu de sin relleno, y c o m o q u e m a d o r pro2 2 piamente dicho, el cabezal de u n soplete oxiacetilénico. 3) Cámara catalítica. A fin de evitar condensaciones, se la u b i c ó en la parte superior de la c o l u m n a de h u m i d i f i c a c i ó n , y para i m p e d i r el e n v e n e n a m i e n t o del catalizador p o r m o j a d o , se protegió a la cámara catalítica c o n u n t u b o q u e la rodea totalmente y q u e sólo admite el pasaje del h i d r ó g e n o h ú m e d o p o r agujeros practicados e n la parte superior. L a temperatura del catalizador ha sido controlada m e d i a n t e u n t e r m ó m e t r o c u y o b u l b o fue alojado e n su seno, y regulada p o r m e d i o de resistencias eléctricas externas accionadas p o r transformadores de relación de transformación variable. A n t e s de iniciar una serie de experiencias, el catalizador fue sometido a u n proceso de activación que consistía en calentarlo a 1 1 0 ° C, haciéndole pasar una corriente de h i d r ó g e n o seco durante 2 horas. Se hace notar que siendo m á s fácil disponer, a los efectos de la experiencia, de agua q u e de h i d r ó g e n o enriquecido, se p r o c e d i ó a estudiar la [ 1 ] en sentido inverso, y a que la v e l o c i d a d de descomposición del H D O es igual a la de f o r m a c i ó n del H D , según y a q u e d ó establecido en la [ 7 ] . 7 Resultados experimentales L a determinación de la constante de equilibrio se realizó a m u y bajos caudales a los efectos de aproximarnos a las condiciones estáticas, obteniéndose en u n rango de temperaturas de 9 0 - 1 1 0 ° C valores comprendidos entre 2,08 y 1,81, pudiéndose adoptar c o m o valor prom e d i o 2 , el cual se halla en perfecta concordancia c o n el determinado p o r A . Farkas a 1 0 0 ° C . 3 C o m o medida del intercambio utilizamos la diferencia de concentraciones isotópicas entre el valor experimental y el correspondiente al equilibrio, este último obtenido p o r vía teórica y suponiendo las mismas condiciones operativas. 0.020 ao/8 0.0/6 0.014 0.012 0.0/0 0.008 0.006 0.0O4 O.002 O ¿0 40 60 60 /OO 120 í40 160 Gráfico 1 Para c u m p l i r c o n la cantidad m í n i m a de ser independiente del gráfico 1 se muestran 3 la finalidad de nuestro trabajo, determinamos catalizador para la cual el intercambio resulta caudal ( p o r l o m e n o s hasta 1 0 0 1 / h ) . E n el los resultados de las experiencias realizadas Orthohydrogen, Parahydrogen and heavy hydrogen, A. Farkas, Cambridge, University Press., Londres, 1935. 8 con ese objeto. D e esa forma elegimos u n V ( v o l u m e n del cataliz a d o r ) de 1,7 c m , pues en esas condiciones el i n t e r c a m b i o n o dep e n d e del caudal, y a q u e las pequeñas diferencias que se observan están dentro del error c o n q u e se d e t e r m i n a n las concentraciones isotópicas ( ± 0,002 m o l e s % D 2 O ) . T a m b i é n h e m o s fijado las mejores condiciones de sobrecalentamiento, e n t e n d i e n d o p o r tal la diferencia de temperaturas entre la del catalizador y la del agua; fijada esta última e n 8 2 ° C, la primera n o p u e d e alejarse demasiado debido a que la constante de equilibrio d i s m i n u y e c o n la temperatura, n i tamp o c o acercarse m u c h o para evitar condensaciones q u e inactivarían el catalizador. El gráfico 2 corresponde a las experiencias realizadas c o n ese fin y del m i s m o se deduce q u e el m e j o r sobrecalentamiento se halla c o m p r e n d i d o entre 5 y 1 5 ° C, en d o n d e el i n t e r c a m b i o resulta ser independiente del sobrecalentamiento. Se observa u n a zona de m e j o r i n t e r c a m b i o , p e r o se deshecha debido al p e q u e ñ o valor del sobrecalentamiento. c 3 I ¿x*x-x° At=tc-t o Ht Gráfico 2 D e s t a q u e m o s q u e durante las experiencias realizadas c o n el o b jeto de determinar la cantidad m í n i m a de catalizador se p u d o c o m probar q u e a pesar de a u m e n t a r el caudal en f o r m a considerable, a ú n más allá del límite fijado, el i n t e r c a m b i o n o se anulaba. E n u n principio supusimos la existencia de u n a actividad catalítica ajena al catalizador p r o p i a m e n t e dicho, y para verificarlo l l e v a m o s a c a b o experiencias sin catalizador ni lana de v i d r i o q u e le sirve de soporte, 9 en una nueva cámara catalítica desprovista de todo contacto metálico (resistencias y pasantes de tungsteno). L o s resultados obtenidos indicaron que la diferencia de concentraciones entre x ( v a l o r experimental) y x ( v a l o r inicial) subsistía ( v e r tabla 1 ) . D e la observación cuidadosa de los datos correspondientes puede sacarse u n valor p r o m e d i o de x = 0,071 moles % L \ 0 , y c o m o x = 0,075 moles % 0 0 X 0 0 7 5 » > 1,05 ± 0,06, valor q u e corresponde D U , resulta que — = . x 0,071 a u n plato teórico e n la destilación . 2 4 Concluimos, p o r lo tanto, que en realidad n o h a y intercambio en ausencia de catalizador, sino simplemente destilación y q u e el vapor producido ( m á s p o b r e ) es el que a c o m p a ñ a al hidrógeno. L u e g o , en el cálculo de x es necesario usar x = 0,071 en lugar de 0,075; en otras palabras, introducimos u n factor de corrección f c u y o valor es 0,95 ± 0,06, válido para todas las experiencias. 0 3 0 Medida de la actividad catalítica en m a r c h a se define la velocidad de reacción r c o m o el n ú m e r o E n u n a reacción catalizada de moles convertidos p o r unidad de tiempo y de v o l u m e n de 5 catalizador . Es decir, (Xp ~ r = X ) t-V, D e s i g n a n d o c o n xo — x la llamada conversión, es decir, el n ú m e r o de moles convertidos p o r unidad de v o l u m e n de alimentación, resulta (xo ~ ) • (Ve/Q)l x _ _ . , ~ ~ \ T — t ( x — x ) Li 0 1 representando f función de, Li la actividad del catalizador y Q el caudal de la m e z c l a gaseosa. Para u n segundo catalizador c o n el cual se obtenga la m i s m a conversión en condiciones operativas semejantes (temperatura del catalizador, temperatura del agua, e t c . ) , resulta MVVQ) 1 = 1*0^(3)8 designando c o n L^ la actividad de este 4 catalizador. Urey (/. Chem. Soc, 1947, pág. 562) ha demostrado que el factor de separación en la concentración de agua pesada por destilación es función de las presiones de vapor del H 0 y del D 0 ; dicho factor, pues, depende de la temperatura y a 80° C vale 1,04. Reaction Kinetics in Chemical Engineering, O. A . Hougen, "Chem. Eng. Progress Monograph", serie N° 1, vol. 47, pág. 36, 1951. 2 5 2 10 S u p o n i e n d o L i = 1 para el Pt, y a q u e es e l m e j o r c o n o c i d o de esta r e a c c i ó n , (V /Q) c D e esta forma mero ( P t ) . catalizador 2 v a l o r a m o s u n segundo catalizador respecto del pri- Con ese fin h e m o s e n s a y a d o c o m o catalizador A l e n f o r m a granular, q u e pasa a través de malla 2 0 , p e r o queda retenido e n el t a m a ñ o siguiente de m a l l a , c o n u n a c o m p o s i c i ó n q u í m i c a de 8 0 % A l , 1 0 % Si, 4 % Z n , 1 % M n , 5 % F e c o n vestigios de T i , C u y M g , siendo su densidad real ( d e t e r m i n a d a p o r p i c n o m e t r í a ) de 1 , 7 5 g / c m . 3 Las experiencias siguientes resultados: realizadas c o n d i c h o catalizador V O T 5,72 cm = 0 T c x 3 arrojaron los ( 1 0 g) x x 0 x x —x 0 H 0 2 5 96 82 0,071 0,055 0,070 86 96 82 0,071 0,055 0,071 0,001 — D a d o el p e q u e ñ o v a l o r de la c o n v e r s i ó n , se a u m e n t ó la cantidad de catalizador hasta c o l m a r la c á m a r a catalítica ( V m á x i m o ) . C V T Q = 9,73 cm C T c Jti 3 ( 1 7 g) x„ x 0 0 x x 0 x ri,í)0 5 96 82 0,071 0,055 0,067 0,004 86 96 82 0,071 0,055 0,070 0,001 Para e l catalizador de A l se eligieron las c o n d i c i o n e s m á s favorables, es decir, caudal m í n i m o ( Q = 5 1 / h ) y v o l u m e n m á x i m o de catalizador ( V = 9 , 7 3 c m ) , resultando, a pesar de ello, u n a con3 0 versión de 0,00041 para un (V /Q)B = 3 , 4 7 seg, q u e C es el máximo posible para nuestras c o n d i c i o n e s de trabajo. Este escaso v a l o r de c o n v e r s i ó n fue c o m p a r a d o c o n el o b t e n i d o usando P t e n las c o n d i c i o n e s m e n o s favorables ( V p e q u e ñ o y Q grande). C H V 91 100 82 C = 0,24 cm 0,071 3 0,052 0,070 0,001 Esta e x p e r i e n c i a fue repetida 1 0 v e c e s , obteniéndose idénticos resultados. L u e g o , ( V / Q ) i = 0 , 0 0 4 7 seg, c o n l o q u e resulta u n a conversión de 0 , 0 0 4 1 . T o d a sustancia ensayada c u y a c o n v e r s i ó n es infer i o r a la d e l P t e n estas c o n d i c i o n e s debe ser desechada, y a q u e carece de valor práctico a los fines catalíticos q u e se buscan. C E n nuestro caso particular la c o n v e r s i ó n del P t es 1 0 veces m a y o r q u e la del A l . Si a pesar de ello s u p o n e m o s q u e las conversiones son del m i s m o orden, se obtiene L Q 0 , 0 0 1 3 para Li = 1 ; es decir, la actividad catalítica d e l A l e n s a y a d o es, a p r o x i m a d a m e n t e , u n a s 8 0 0 veces m e n o r q u e la del Pt. = D e la m i s m a f o r m a se p u e d e n v a l o r a r otros posibles catalizadores de la r e a c c i ó n . i l 11 Conclusiones C o n un dispositivo c o m o el construido y utilizando agua a 8 2 ° C, hemos conseguido humidificar equimolarmente hidrógeno. A d e m á s , empleando un catalizador apropiado ( P t ) en cantidad conveniente, hemos determinado: 1) que el sobrecalentamiento adecuado varía en u n rango c o m p r e n d i d o entre 5 y 15° C ; 2 ) que el catalizador de aluminio ensayado carece prácticamente de actividad para la reac­ ción en estudio. Destacamos que en todas las experiencias se ha debido tener en cuenta la existencia de un empobrecimiento inicial ajeno al inter­ cambio, provocado p o r un proceso elemental de destilación, para de esa forma evitar interpretaciones erróneas. TABLA 1 V : Ocm c 3 (sin catalizador). x : 0,075 moles D 0 % (sin corregir). u 2 Q : caudal de hidrógeno H (litros/hora). T : temperatura del catalizador (°C). c T H.,O : temperatura del agua de humidificación (°C). 757 mm Hg: presión atmosférica. Q T H T Ax : x — x X 0 10 107 82 0,071 0,054 0,017 16 99 82 0,072 0,055 0,017 20 111 82 0,070 0,054 0,016 21 113 82 0,069 0,054 0,015 30 98 82 0,071 0,055 0,016 30 98 82 0,071 0,055 0,016 42 98 82 0,071 0,055 0,016 43 98 82 0,070 0,055 0,015 47 110 82 0,071 0,054 0,017 52 95 82 0,070 0,055 0,015 56 98 82 0,072 0,055 0,017 66 99 82 0,070 0,055 0,015 80 109 82 0,072 0,054 0,018 85 100 82 0,070 0,055 0,015 87 100 82 0,071 0,055 0,016 90 98 82 0,070 0,055 0,015 90 98 82 0,072 0,055 0,017 95 105 82 0,069 0,055 0,014 110 102 82 0,070 0,055 0,015 137 102 82 0,073 0,055 0,018 200 96 82 0,071 0,055 0,016 Valor promedio: 0,071 0 0 Editado pjr el Departamento de Información de la COMISIÓN NACIONAL DE ENERGÍA ATÓMICA Av. del L i b e r t a d o r G e n e r a l San M a r t í n 8 2 5 0 Buenos Aires - República Argentina Septiembre 1 9 6 1