niveles adecuados de cobalamina en sus formas activas
Anuncio

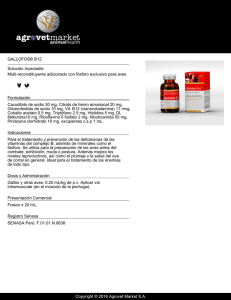
NIVELES ADECUADOS DE COBALAMINA EN SUS FORMAS ACTIVAS Fórmula líquida altamente concentrada de Metilcobalamina, Adenosilcobalamina, Piridoxal-5fosfato y Tiamina. INTRODUCCIÓN La cobalamina es una vitamina hidrosoluble absolutamente esencial, aunque necesaria como cofactor para el correcto funcionamiento de sólo dos enzimas en la bioquímica humana. La cianocobalamina (CnCbl) es la forma más utilizada para suplementación en la industria farmacéutica; se encuentran trazas de esta forma en los tejidos, pero no se ha podido demostrar con claridad que tiene un papel bioquímico. Para poder utilizar la CnCbl, el organismo humano debe remover el cianuro, desintoxicarse de este, reducir la cobalamina de su estado de oxidación +3 a +1, y convertirla en una de las dos formas de coenzimas metabólicamente activas. Las dos formas de vitamina B12 metabólicamente activas son la metilcobalamina (MeCbl) y la adenosilcobalamina (AdeCbl). A la AdeCbl también se le llama cobamamida, cobinamida o dibencozida. El uso clínico de la MetCbl y AdeCbl en combinación pueden producir mejores resultados que la suplementación con CnCbl o Hidroxicobalamina1. NATURALEZA DE LA COBALAMINA El término cobalamina, en general, se usa para describir un grupo de compuestos corrinoides que contienen cobalto, una ribosa, fosfato y una base (5,6-dimetilbenzimidazol2. Esto hace de la cobalamina, la vitamina con la estructura más compleja3. La cobalamina contiene en el centro de su anillo de corrina, un átomo de cobalto; esta estructura se asemeja al anillo porfirínico de la hemoglobina, a la de los citocromos y de la clorofila. No se conoce otro uso para el cobalto en la bioquímica humana. Para que la B12 pueda actuar como cofactor, el cobalto debe estar en su estado de oxidación +1, también llamado Cob(I)alamina, sin embargo, las moléculas de cobalamina también se pueden encontrar en un estado de oxidación +3 (Cob(III)alamina) o +2 (Coba(II)alamina), que deben ser reducidas a Cob(I)alamina para su aprovechamiento. El compuesto comúnmente identificado como vitamina B12 es la CnCbl, a pesar de que no existe naturalmente en plantas, microorganismos o tejidos animales 4. O H2N O O H2N NH2 CH3 CH3 O H3C R N H3C O H N CO+ N H2N CH3 NH2 N CH3 CH3 CH3 NH2 O NH O CH3 O O N P CH3 O HO HO CH3 N O Amarillo: Cobalto Azul: Anillo de corrina Naranja: Enlace de fosfato Verde: Azúcar ribosa Morado: Base nitrogenada HO 1. Estructura química la Cobalamina. Figura 1.Figura Estructura química de ladeCobalamina. La CnCbl contiene un átomo de cianuro y un átomo de cobalto en estado de oxidación +3, mientras que la vitamina B12 biológicamente activa contiene un átomo de cobalto en estado de oxidación +1. Para que el organismo pueda utilizarlo, la molécula de cianuro debe ser removida y eliminada a través de la fase II de desintoxicación utilizando una molécula de glutatión (GSH). Evidentemente, la deficiencia de glutatión puede inducir una deficiencia funcional de B12, aún cuando los niveles plasmáticos de CnCbl se encuentren “normales”. Cabe anotar que en pacientes fumadores, la inhalación crónica de niveles bajos de 73 cianuro suele causar una deficiencia funcional de B12 precipitando la formación de CnCbl a partir de la Cobalamina3. Es importante estar conscientes de que la mayoría de laboratorios miden niveles plasmáticos de cianocobalamina y no sus formas activas5. Cianocobalamina descianurización El ser humano no sintetiza la vitamina B12, por lo tanto su aporte dietario es absolutamente esencial. A pesar de esta limitante, disponemos de la maquinaria bioquímica para su conversión a MetCbl y AdeCbl. cob(III)alamina reducción La vitamina B12 es sintetizada naturalmente por bacterias presentes en la microbiota de los animales, y por eso abunda en alimentos de este origen. Para poder aprovechar la CnCbl de algunos suplementos dietarios y poder convertirla en las coenzimas funcionales requeridas, se requieren al menos 4 pasos: (Ver Figura 2.) 1. Descianurización: Dependiente de GSH y NADPH (B3) y FAD (B2). 2. Reducción del cobalto de las formas +3 a +2 ó +1: Dependiente de NADH y FAD y tocofe- roles (Vit E). 3. Síntesis de MetCbl en el citosol: Dependiente de S-adenosilmetionina (SAM). 4. Síntesis de AdeCbl en la mitocondria: requiere de ATP. Al parecer se necesita alfa-tocoferol para poder reducir el cobalto desde +3 a +2 y +1, por lo tanto, la deficiencia de vitamina E puede disminuir la capacidad de formar MetCbl y AdeCbl6. El óxido nitroso, usado en cirugía y dentistería por sus efectos anestésicos y analgésicos, inactiva las formas de coenzimas de B12 al oxidar la Cob(I)alamina a Cob(II)alamina y Cob(III)alamina y a su vez interfiere con la Metionina Sintetasa7. ABSORCIÓN La óptima absorción de B12 a nivel intestinal depende de su acoplamiento con la proteína-R (haptocorrina, secretada por las glándulas salivales y mucosa gástrica) y el factor intrínseco secretado por las células parietales del estómago. Además, el estómago debe lograr una acidificación adecuada (pH entre 1 y 2) y producir suficiente pepsina para lograr digerir las proteínas ligadas a la B12. Primero, el complejo Cobalamina-proteína-R es sometido a las acciones de las enzimas pancreáticas en el intestino delgado, permitiendo la liberación de la cobalamina, que luego se une al 74 NIVELES ADECUADOS DE COBALAMINA EN SUS FORMAS ACTIVAS NAPH (B3 depediente) GSH FAD (B2 dependiente) hidroxicob(III)alamina NADH FAD or FMN CITOSOL cob(II)alamina SAM SAH reducción Metilcob(II)alamina THF homocisteína NADH FAD or FMN metionina 5MTHF cob(I)alamina cob(I)alamina ATP MITOCONDRIA Adenosilcob(I)alamina Figura 2. Síntesis de las formas activas de B12 a partir de cianocobalamina. factor intrínseco (una glicoproteína secretada porlas células parietales del estómago estimuladas por la presencia de alimentos) para ser absorbida en el íleodistal. Luego la cobalamina se separa del factor intrínseco en el enterocito para unirse a la transcobalamina I (TC I), II (TC II) o III (TC III) 3-4 horas después, para su distribución sanguínea a los tejidos. Aunque la TC I se une al 80% de la B12 que es transportada en la sangre, la TC II es la forma mediante la cual la B12 se entrega a los tejidos a través de receptores específicos. El hígado capta aproximadamente el 50% de la B12 y el remanente es transportado a los otros tejidos. Aunque la absorción de la B12 en general es baja, 50% de 1μg (0.5 μg), 20% de 5μg (1 μg), 5% de 25 μg (1.25 μg) y 1% en dosis muy altas (hasta 38 μg), la absorción total de la B12 aumenta junto con el incremento de la ingesta aún en ausencia de factor intrínseco8. Se conoce además que la capacidad de absorción, como tal, no se ve afectada por la edad, sin embargo la mayor prevalencia de gastritis atrófica relacionada con la edad explica la mayor probabilidad de deficiencia de B12 asociada con edad avanzada. solo el 50% de la dosis oral es retenida en los tejidos, pero también habría que asegurar suficiencia de los cofactores necesarios para su conversión a MetCbl y AdenCbl10. Cbl de alimentos Saliva Circulación Enterohepática HC Hígado Bilis HC + Cbl HC - Cbl FI FI FI- Cbl Ácido Pepsina HC - Cbl Pancreas Proteasas FI- Cbl Cubilina Proteína amninonless Lisosoma Vaso sanguíneo FI- Cbl Cbl: Cobalamina HC: Haptocorrinas FI: Factor Intrínseco TC: Transcobalamina HC- Cbl 80% TC- Cbl 20% Figura 3. Ruta de Absorción B12. La OH-Cbl, MetCbl y AdeCbl son las tres isoformas de B12 que se encuentran en los tejidos, sin embargo, la MetCbl y la AdeCbl son las únicas que actúan como cofactores enzimáticos en humanos. La forma más abundante es la AdeCbl y se encuentra dentro de las mitocondrias, mientras que la MetCbl se encuentra en el citosol8. La evidencia muestra que la MetCbl es utilizada más eficientemente que la CnCbl, para aumentar los niveles de las formas de coenzimas funcionales de B12. Aunque se han detectado cantidades similares de MetCbl y de CnCbl luego de la administración oral, la suplementación con MetCbl, es mucho más eficiente para asegurar el almacenamiento a nivel hepático en comparación con CnCbl, pues la excreción urinaria de MetCbl es un tercio de la excreción urinaria de CnCbl, cuando son administrados en dosis iguales, indicando una retención tisular sustancialmente mayor de la MetCbl9. Alrededor del 35% de la AdeCbl es absorbida luego de su administración oral, de la cual, el 77% es retenida en los tejidos corporales. En el caso de la CnCbl, A pesar de que en pacientes con anemia perniciosa los anticuerpos impiden la producción o la persistencia de factor intrínseco (necesario para la absorción de B12), se ha encontrado que la suplementación con dosis altas de B12 (por encima de 1000 mcg) en sus formas activas logra sus objetivos, indicando que existe un mecanismo de absorción independiente de factor intrínseco11,12. RECIRCULACIÓN ENTEROHEPÁTICA La B12 es secretada continuamente en la bilis (1.4 μg/ día). En individuos sanos, la mayoría de la B12 (50%) es reabsorbida, por lo que las pérdidas totales en heces es de 0.7 μg/día, aproximadamente. La reabsorción también depende del factor intrínseco, haciendo de su ausencia un factor aún más importante en el desarrollo de la deficiencia de B12 que el vegetarianismo13. EXCRECIÓN Si la cantidad circulante de B12 excede su capacidad de unión a la TC y HC, el exceso es excretado en la orina. Esto ocurre típicamente luego de una inyección de B12. Sin embargo la mayor pérdida de B12 se da a través de las heces, incluyendo la B12 no absorbida de los alimentos y la bilis, células descamadas, secreciones gástricas e intestinales, y B12 sintetizada por las bacterias en el colon. Normalmente se puede perder hasta el 0.2% de los depósitos totales de B12 al día independientemente del tamaño de los depósitos14. FUNCIONES La única función biológica de la MetCbl en los seres humanos es la de participar como cofactor de la enzima Metionina-Sintetasa. Esta enzima se localiza en el citosol de las células y ayuda en la transferencia de grupos metilos desde el 5-metil-tetrahidrofolato a la homocisteína para la regeneración de metionina. La AdeCbl participa en reacciones de intercambio de grupos de hidrógeno con grupos orgánicos. En los seres humanos, la AdeCbl es necesaria para la enzima Metilmalonil-CoA-mutasa, la cual efectúa la isomerización catabólica de Metilmalonil-Coa a Succinil-CoA (utilizado para la síntesis de porfirinas) y como intermediaria en las vías de degradación de valina, isoleucina, treonina, metionina, timina, ácidos grasos y colesterol1. 75 La deficiencia de AdeCbl resulta en un incremento de los niveles de metilmanolil-CoA y usualmente en un incremento de la glicina. En general, las dos formas activas de B12 son necesarias para la: • Síntesis de ADN. • Síntesis de ácidos grasos. • Producción de energía. • Biosíntesis de: - Aminoácidos. - Serina. - Metionina. - Glicina. - Purinas. - Desoxitimidina monofosfato. PRINCIPALES IMPLICACIONES CLÍNICAS CONOCIDAS a) Efectos hematológicos: La anemia megaloblástica es la observación clínica más evidente de la deficiencia de B12. Los síntomas que caracterizan esta condición incluyen: palidez de la piel asociado a disminución de la tolerancia al ejercicio, fatiga, disnea, sensación de falta de energía y palpitaciones. Para fines de diagnóstico diferencial, recordamos que estos efectos hematopoyéticos son indistinguibles de aquellos ocasionados por la deficiencia de folato. La deficiencia de B12 conlleva a la anemia porque interfiere con la síntesis normal de ADN, lo que resulta en cambios megaloblásticos (macrocitosis) en los eritrocitos. Primero se observa un aumento del ancho de distribución eritrocitario y luego un aumento del volumen corpuscular medio. Con el tiempo, pueden añadirse a la anemia, la neutropenia y la trombocitopenia. b) Efectos neurológicos: Las complicaciones neurológicas están presentes en el 75-90% de los individuos con deficiencia de B12 e inclusive, en 25% de los casos, suele ser la única manifestación clínica de dicha deficiencia. Existe una correlación inversamente proporcional con el grado de anemia, es decir, a mayor anemia menores manifestaciones neurológicas y viceversa15. Los síntomas neurológicos correspondientes incluyen: parestesias y/o hipoestesias que usualmente son más 76 NIVELES ADECUADOS DE COBALAMINA EN SUS FORMAS ACTIVAS acentuadas en los miembros inferiores, y alteración de la sensibilidad vibratoria y posicional. También se pueden observar alteraciones en patrones neuromusculares, cambios cognitivos como pérdida de la memoria, déficit de atención, desorientación, demencia con o sin cambios del ánimo, alteraciones visuales, insomnio, impotencia, pobre control de la vejiga e intestino, y otros trastornos resultantes de disfunciones neurológicas y distonías de nervios craneanos y periféricos. En la deficiencia de B12, los ácidos grasos de cadena impar se acumulan en la membrana de las células del SNC ocasionando los síntomas neurológicos. El uso de metformina está asociado con la deficiencia de B12 y neuropatía clínica en paciente con DM216. c) Efectos gastrointestinales: Por el papel imprescindible que juega la B12 en la regeneración de tejidos, la deficiencia de B12 entra en un ciclo vicioso a nivel gastrointestinal, donde los daños a la pared gástrica e intestinal precipitan la misma deficiencia de B12. Pueden resultar glositis con pérdida del apetito, gastritis, reflujo gastroesofágico, flatulencias, estreñimiento, aumento de la permeabilidad intestinal, etc. Cuando tal condición se ve agravada por un mediador autoinmune, como en el caso de la anemia perniciosa, el deterioro del paciente se acelera sustancialmente. Los pacientes que están en tratamiento con dosis bajas de ácido acetil salicílico (AAS) presentan mayor riesgo de desarrollar deficiencia de B12, probablemente debido a que los efectos tóxicos del AAS sobre la mucosa gástrica pueden ocasionar una disminución en la secreción de factor intrínseco17. DIAGNÓSTICO DE LA DEFICIENCIA En Colombia, la prevalencia de valores de vitamina B12 menor de 221 pmol/L es de 21% en menores de 18 años, 30% en mujeres embarazadas y 37% en mujeres adultas18. La detección de una insuficiencia de B12 antes de que muestre manifestaciones clínicas depende de los análisis bioquímicos; los ácidos orgánicos cuyo aumento en la insuficiencia son mucho más sensibles que los niveles séricos de B12. El ácido metilmalónico en orina o en suero y/o niveles de homocisteína se encuentran elevados en el 95% de los casos con deficiencia de B12, mientras que la medición de B12 en suero sólo detecta la deficiencia en el 69% de los casos que la presentan19. Cerebro Sentidos Faciales - Atrofia óptica. - Anosmia. - Pérdida del gusto. - Glositis. - Estado mental alterado. - Defectos cognitivos. - "Demencia Megaloblastica": depresión, manía, irritabilidad, paranoia, delirios. - Perdida del apetito. Médula Espinal - Mielopatía. - Degeneración esponjosa. Anormalidades en Infantes y Niños - Retraso o regresión del desarrollo. - Discapacidad permanente. - No sonríe. - Dificultad al alimentarse. - Hipotonía, letargo. - Hiperirritabilidad, convulsiones. - Temblores, mioclonus. - Microcefalia. - Movimientos Coreoatetósicos. Sistema Reproductivo - Infertilidad. Sangre Periférica - Eritrocitos macrocíticos. - Macroovalocitos Anisocitosis. - Formas fragmentadas. - Neutrófilos hipersegmentados, 1% con seis lóbulos, 5% con 5 lóbulos. - Leucopenla. - Posibles células blancas inmaduras. - Trombocitopenia. - Pancitopenia. - Nivel elevado de LDH. - Bilirrubina indirecta AST elevados. - Haptoglobina disminuido. - Metilmalonato y/o homocisteína elevados. Parestesias - Pérdida de propiocepción: vibración, posición, marcha atáxica. - Debilidad en extremidades. - Espasticidad (hipereflexia). - Signo de Romberg positivo. - Signo de Lhermitte positivo. - Nivel sensitivo cutáneo segmentado. Sistema Nervioso Autónomo - Hipotensión postural. - Incontinencia. - Impotencia. - Taquicardia y arritmias. - Diarrea. Sistema Nervioso Periférico - Pérdida de sensibilidad cutánea. - Hiporeflexia. - Debilidad simétrica y cansancio. - Parestesias. Médula Ósea - Precursores eritroides aumentados e hipercelularidad. - Cromatina nuclear inmadura y abierta. - Disincronía entre la maduración del citoplasma y el núcleo. - Bandas gigantes, metamielocitos. - Cariorexis, displasia. - Resultados anormales en citometría de flujo y en el análisis citogenético. Figura 4. Potenciales consecuencias de una deficiencia de B12. 77 CAUSA PATOGENESIS Deficiencia dietaria Ingesta insuficiente, muy frecuente en dieta vegana. Anemia perniciosa Falta de factor intrínseco Gastrectomia Falta de factor intrínseco Gastritis atrófica, Hipoclorhidria, uso de antiácidos y metformina Inhabilidad para digerir la B12 unida a proteínas y captación y/o conversión bacteriana Sobrecrecimiento de bacterias en el intestino delgado Captación y/o conversión bacteriana de la B12 Parasitosis intestinal Captación de la B12 por parte del parásito Enfermedad o resección del íleo terminal Inhabilidad para absorber B12 Insuficiencia pancreática Incapacidad para digerir B12 unida a proteínas Tabla 1. Factores de riesgo para desarrollar deficiencia de B12. NIVELES ELEVADOS DE B12 Ocurre también encontrar niveles séricos elevados de B12 y a pesar de esto, es posible que coexista la hipercobalaminemia con una deficiencia funcional de B12, sobre todo si el ácido metilmalónico o la homocisteína están elevados. Sin embargo, es importante tener en cuenta que existen otras causas de hipercobalaminemia además de una suplementación excesiva de B12 (usualmente por vía endovenosa o intramuscular), entre otras: - Neoplasias sólidas, por aumento de recambio celular: hepatocarcinoma, metástasis hepáticas secundarias, cáncer de mama, cáncer de colon, cáncer gástrico y tumores pancreáticos. - Malignidades sanguíneas, principalmente por liberación de holocobalamina por granulocitos tumorales y sus precursores en leucemia mielomonocítica crónica, síndromes hiperesosinofílicos, síndromes mielodisplásicos, leucemias agudas y leucemia promielocítica. - Enfermedades hepáticas, por liberación excesiva de B12 y disminución de síntesis de TCB II: hepatitis aguda y hepatitis alcohólica. - Enfermedad renal crónica, por acumulación de TCBs20. SUPLEMENTACIÓN CON B12 B12 Inyectada. Los requerimientos diarios de B12 son de 2.4 μg, sin embargo se estima que para evitar una deficiencia fun- 78 NIVELES ADECUADOS DE COBALAMINA EN SUS FORMAS ACTIVAS cional medida por metilmalonato, los requerimientos diarios son en realidad alrededor de 4 a 7 μg. Existen múltiples esquemas para la suplementación parenteral de B12 (excluyendo el uso inapropiado de cianocobalamina). Se estima un máximo de retención del 10% de la dosis inyectada, por lo cual se debe aplicar varias veces por semana durante 2 a 4 semanas. La vía intramuscular de administración se caracteriza por ser ampliamente reconocida como dolorosa, lo que podría comprometer la adherencia al tratamiento más allá del costo mensual total. Adoptando este esquema se puede esperar un aumento de reticulocitos luego de la primera semana de tratamiento y corrección de la anemia megaloblástica en 8 semanas. Es posible observar un aumento transitorio de los síntomas neurológicos al principio que luego suelen desaparecer con el pasar de las semanas o meses. Suplementación Oral con Altas Dosis de B12. La suplementación oral con altas dosis de B12 es efectiva y su popularidad a nivel mundial está creciendo. Su absorción por difusión pasiva es del 4%, por lo tanto, administrar una dosis oral de 1000 μg entrega hasta 40 μg, igualmente cuando es ingerida con alimentos. Un estudio aleatorizado que comparó una dosis oral de 2000 μg diarios con terapia parenteral (7 inyecciones de 1000 μg de cianocobalamina en un mes, seguido por inyecciones mensuales) en pacientes con anemia perniciosa, gastritis atrófica o un antecedente de resección ileal, mostró en ambos grupos reducciones similares de VCM, aumento del hematocrito a los 4 meses y resolución de los síntomas neurológicos. Sin embargo, los niveles de metilmalonato en el grupo que recibió la suplementación oral fueron significativamente menores y los niveles de B12 fueron significativamente más elevados21. La dosis recomendada en adultos va desde los 1000 mcg hasta los 4000 mcg al día de B12, en niños se sugiere dosis de hasta 1000 mcg al día, ambos por vía oral. En el caso de la anemia perniciosa, la necesidad de suplementar la B12 suele persistir durante toda la vida, como apoyo constante a un tratamiento que debe centrarse sobre el manejo de la autoinmunidad. Marcadores para la Evaluación de la Respuesta a la Suplementación de B12 sis para administración parenteral de hasta 10.000 μg para aplicación semanal e históricamente se ha descrito la aparición de acné con dosis periódicas de hasta 5.000 μg IM. Adicionalmente, la desintoxicación y eliminación del cianuro inyectado en tales dosis, aunque lejos de ser dosis consideradas como tóxicas, genera inevitablemente un gasto metabólico importante. Debido a la absorción limitada de la B12 oral, el riesgo de presentar efectos adversos es tan bajo que hasta el momento no se han observado2. Contraindicaciones • Aumento del conteo de eritrocitos. Hasta el momento no se conocen contraindicaciones de la suplementación con B12, se puede administrar en mujeres embarazadas, mujeres en estado de lactancia, niños y pacientes adultos mayores. Se sugiere monitoreo de homocisteína y metilmalonato en pacientes con niveles séricos de B12 aparentemente elevados antes de iniciar la suplementación y después de tres meses de suplementación. • Disminución del volumen corpuscular me dio (termina de ajustarse a los cientoveinte días). DOSIS ALTAS DE COBALAMINA CON PIRIDOXAL-5-FOSFATO Y TIAMINA • Aumento del conteo de reticulocitos (pico a los 5-8 días). La piridoxina funciona como coenzima en el metabolismo de aminoácidos, glucógeno y bases esfingoides. Su forma activa es el piridoxal-5-fosfato (P-5-F), es la que mayormente se acumula en los tejidos animales, en especial, en el hígado. La dosis diaria recomendada para no caer en su deficiencia es de 2 mg/día; los síntomas clínicos clásicos de dicha deficiencia son: dermatitis seborreica, anemia microcítica, convulsiones epileptiformes, depresión, confusión e hiperhomocisteinemia con sus consecuencias. Por otro lado la tiamina, también llamada aneurina, está involucrada principalmente en reacciones de descarboxilación de α-ketoácidos y transketolación; ella participa en las funciones mitocondriales, la síntesis de acetilcolina, síntesis de dopamina, entre otras. Su deficiencia puede engendrar anorexia, pérdida de peso, apatía, disfunciones de funciones cognitivas como alteraciones de la memoria a corto plazo, confusión e irritabilidad, debilidad muscular y hasta una forma de falla cardíaca llamada beriberi. 1. Indicadores de respuesta hematológica. • Aumento de hemoglobina. • Aumento del hematocrito. 2. Nivel sérico o plasmático de B12. • La concentración plasmática de B12 refleja tanto la ingesta como los depósitos. • El límite inferior está alrededor de 170- 250 pg/ ml, dependiendo del método utilizado por el laboratorio. Sin embargo, un nivel de laboratorio por encima de este punto de corte no indica necesariamente un estado adecuado de B12, ya que el ni- vel plasmático puede estar mantenido por los depósitos de B12 en los tejidos. 3. Disminución de ácido metilmalónico en orina. 4. Disminución de homocisteína sérica. 5. Disminución de ácido formiminoglutámico (FI GLU) propionato y metilcitrato. 6. Aumento de Holotranscobalamina. ¿Existen Efectos Adversos Causados por la Suplementación con B12? Hasta el momento, no se han identificado efectos adversos en la suplementación oral con B12. En el mercado se encuentra cianocobalamina en do- La combinación en dosis altas de B12, B6 y B1 es común en fórmulas para aplicación parenteral (IM), pero generalmente se usa la forma inactiva sintética de la B6 (piridoxina) y la forma inactiva sintética y tóxica B12 (cianocobalamina). Esta combinación es muy utilizada para manejo de dolores crónicos, dolores agudizados musculares y neuríticos. La combinación de las formas orales activas, naturales y no tóxicas de estas 3 vitaminas mejora sustancialmente su acumulación en te- 79 jidos, biodisponibilidad celular y uso mitocondrial, garantizando mayor efectividad y sin el dolor producido por la aplicación intramuscular. Adicionalmente, el uso de la metilcobalamina y la adenosilcobalamina permite evitar los efectos potencialmente tóxicos del cianuro, junto con el desgaste metabólico asociado a su desintoxicación2. MODO DE USO A. Dosis en adultos con deficiencia funcional (sinto- matología asociada y marcadores funcionales alte- rados), por día, con o sin alimentos: - Metilcobalamina ………………. 975 mcg - Adenisolcobalamina…………… 975 mcg - Piridoxal-5-fosfato……………… 5 mg - Tiamina clorhidrato..…………… 5 mg B. Dosis en niños con deficiencia funcional (sintoma- tología asociada y marcadores funcionales altera- dos), por día, con o sin alimentos: ½ de la dosis para adultos. C. Duplicar la dosis en deficiencia severa (niveles séricos menores a 250 pg/ml). Usar durante 3 meses antes de reevaluar la sintomatología relacionada y marcadores relacionados como: ácido metilmalónico en orina, homocisteína sérica, hemoglobina, hematocrito, conteo de eritrocitos, volumen corpuscular medio, conteo de reticulocitos, nivel sérico o plasmático de B12, holotranscobalamina, y ácido formiminoglutámico (FIGLU) propionato y metilcitrato. BIBLIOGRAFÍA 1. Kelly, G. (1997). The Coenzyme Forms of Vitamin B12: Toward an Understanding of their Therapeutic Potential. Alternative Medicine Review, 2(6), 459 - 471. 2. Institute of Medicine (US) Standing Committee on the Scientific Evaluation of Dietary Reference Intakes and its Panel on Folate, Other B Vitamins, and Choline. (1998). Dietary Reference Intakes for Thiamin, Riboflavin, Niacin, Vitamin B6, Folate, Vitamin B12, Pantothenic Acid, Biotin, and Choline. (N. A. (US), Ed.) National Academies Press (US). 3. Richard S. Lord, J. A. (2008). Laboratory evaluations for integrative and functional medicine (2ª ed.). Duluth, Georgia, USA: Metametrix Institute. 4. Qureshi AA, R. D. (1994). Inherited disorders of cobalamin metabolism. Crit Rev Oncol Hematol, 17, 133-151. 80 NIVELES ADECUADOS DE COBALAMINA EN SUS FORMAS ACTIVAS 5. Pezacka E, G. R. (1990). Glutathionylcobalamin as an intermediate in the formation of cobalamin coenzymes. Biochem Biophys Res Comm, 2, 443-450. 6. Pappu AS, F. P. (1978). Possible interrelationship between vitamins E and B12 in the disturbance in methylmalonate metabolism in vitamin E deficiency. Biochem J, 172, 115-121. 7. Glusker JP. (1995). Vitamin B12 and the B12 coenzymes. Vitam Horm, 50, 1-76. 8. Cooper BA, R. D. (1987). Inherited defects of vitamin B12 metabolism. Ann Rev Nutr, 7, 291-320. 9. Okuda K, Y. K. (1973). Intestinal absorption and concurrent chemical changes of methylcobalamin. J Lab Clin Med, 81, 557-567. 10. Heinrich HC, G. E. (1964). Metabolism of the vitamin B12coenzyme in rats and man. Ann NY Acad Sci, 112, 871-903. 11. Lederle FA. (1991). Oral cobalamin for pernicious anemia. Medicines best kept secret? JAMA, 265, 94-95. 12. Berlin H, B. G. (1978). Vitamin B12 body stores during oral and parenteral treatment of pernicious anemia. Acta Med Scand, 204, 81-84. 13. El Kholty S, G. J. (Nov de 1991). Portal and biliary phases of enterohepatic circulation of corrinoids in humans. Gastroenterology, 101(5), 1399-1408. 14. Amin S, S. T. (Jan de 1980). Long-term clearance of [57Co] cyanocobalamin in vegans and pernicious anaemia. Clin Sci (Lond), 58(1), 101-103. 15. Savage D, G. I. (April de 1994). Vitamin B12 deficiency is the primary cause of megaloblastic anaemia in Zimbabwe. Br J Haematol., 86(4), 844-850. 16. Singh AK, K. A. (October de 2013). Association of B12 deficiency and clinical neuropathy with metformin use in type 2 diabetes patients. Journal of Postgraduate Medicine, 59(4), 253-257. 17. Van Oijen MG, L. R., & study., B. (1 de oct de 2004). Association of aspirin use with vitamin B12 deficiency (results of the BACH study). Am J Cardiol, 94(7), 975-977. 18. Ministerio de Proteccion Social. (2010). Encuesta Nacional de Salud Colombia 2010. 19. Stabler, S. (10 de Jan de 2013). Clinical practice. Vitamin B12 deficiency. N Engl J Med, 368(2), 149-160. 20. E. Andres, K. S. (2013). The pathophysiology of elevated vitamin B12 in clinical practice. Q J Med, 106, 505-515. 21. Stabler, S. P. (2013). Vitamin B12 Deficiency. The new england journal of medicine, 368, 149-160.