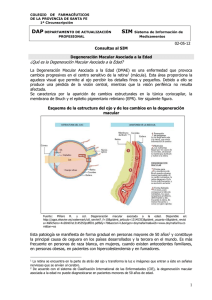
Degeneracion macular asociada a la edad (Dmae). Guía clínica
Anuncio

Artículo científico Degeneracion macular asociada a la edad (dmae). Guía clínica optométrica, a partir de estudios basados en la evidencia › Manuel Ángel García García 1 O.C. 18.197 1 Óptico- Optometrista. Hospital Torrevieja Oftalmólogo. Hospital Torrevieja 2 › Eva María Salinas Martínez 2 Objetivos. Actualizar al Óptico- Optometrista en los actuales tratamientos de la degeneración macular asociada a la edad (DMAE). Orientar sobre las pautas a seguir; desde recomendaciones higiénico-dietéticas hasta asesoramiento en ayudas de baja visión, a pacientes ya diagnosticados. Detección temprana de la enfermedad y derivación oportuna para estudio oftalmológico en su fase inicial. Métodos. Se ha realizado una búsqueda de las publicaciones científicas en relación con el objeto de esta guía, de forma que las recomendaciones terapéuticas estén basadas en conocimientos científicos. Resultados. La importancia en la detección precoz es indispensable. Actualmente ranibizumab o bevacizumab, en España, en monoterapia sigue siendo el tratamiento de elección en el tratamiento de la DMAE neovascular. Conclusiones. Los diferentes estudios basados en la evidencia resultan adecuados para la realización de una guía de actuación clínica optométrica. La actuación optométrica dentro de los servicios de oftalmología es clave para un mejor manejo de pacientes con DMAE Palabras clave Degeneración macular asociada a la edad (DMAE), ranibizumab, bevacizumab, pegaptanib, aflibercep, terapia fotodinámica, factor de crecimiento del endotelio vascular (VEGF). INTRODUCCIóN Definición L y clasificación a degeneración macular asociada a la edad (DMAE) es una enfermedad que se caracteriza por la aparición de una, o más, de las siguientes alteraciones degenerativas progresivas en la mácula: > Formación de drusas. >A lteraciones del epitelio pigmentario de la retina (EPR) como hipo e hiperpigmentación. › nº 487 >A trofia geográfica del EPR y la coriocapilar que afecta el centro de la fóvea. >N eovasos (maculopatía exudativa o neovascular). La DMAE constituye, actualmente, la principal causa de ceguera en personas mayores de 50 años en los países desarrollados, con una prevalencia que oscila en el 2-10%. Las variaciones en la estimación de esta enfermedad dependen de varios factores, principalmente de su definición y de la edad1. No obstante, todos los estudios epidemiológicos concluyen que la prevalencia de DMAE aumenta claramente con la edad, en especial más allá de los 70 años. Existen diferentes clasificaciones: el sistema Wisconsin2; la clasificación internacional; la clasificación AREDS (Age-Related Eye Disease Study)3. Todas ellas coinciden en diferenciar entre estadios iniciales (MAE, maculopatía asociada a la edad) y estadios avanzados (DMAE o MAE tardía). Dentro de estos últimos entre la forma atrófica y neovascular o exudativa. ÓPTICA La clasificación AREDS define estadios tempranos e intermedios de MAE con fines pronósticos y de recomendaciones de tratamiento, por lo que resulta especialmente interesante. El estudio AREDS es un estudio multicéntrico prospectivo diseñado para el estudio del curso de la enfermedad, factores de riesgo y efectos de vitaminas antioxidantes y minerales en la DMAE. OFTÁLMICA del total de casos y afecta aproximadamente a un 10% de las personas mayores de 60 años. DMAE húmeda, exudativa, neovascular Se acepta que un 10% aproximadamente de los pacientes con DMAE presentan esta forma neovascular pero, sus efectos sobre la visión, son muy marcados. Tipos de DMAE El cuadro clínico puede ser muy variado: MAE > Desprendimiento exudativo del epitelio Se incluyen en este tipo la nula o presencia de pocas drusas de (<63µm de diámetro), combinación de pequeñas drusas intermedias (63-124 µm) o anomalías del EPR y las abundantes drusas intermedias o una de, al menos ,125µm o atrofia geográfica, que no afecta el centro de la fóvea. DMAE atrófica, seca Conlleva una desaparición progresiva del epitelio pigmentario retiniano, produciéndose cambios pigmentarios; zonas de atrofia que lentamente van creciendo y drusas que van de manera progresiva coalesciendo (Figura 1). Las áreas afectadas pierden capacidad visual, ya que la pérdida del EPR se asocia a una alteración importante de los fotorreceptores. El estadio final de este proceso se denomina atrofia geográfica. Este tipo de DMAE es el más frecuente y representa casi un 90% Figura 1. pigmentario provocando metamorfopsias. > Membranas neovasculares coroideas (MNVC) provocando hemorragias (Figura 2 y 3), que originan un escotoma central y disminución de la visión. > Formación de una cicatriz disciforme ma- cular a causa de los procesos anteriores, produciendo un escotoma central absoluto. Este proceso puede ocurrir de forma rápida, lo que la rápida actuación ante este tipo de patología resulta indispensable. Esta enfermedad suele ser bilateral, pero asimétrica. Se estima que un paciente con un ojo afectado tiene una probabilidad cercana al 50% de que su otro ojo también se afecte en un plazo de 5 años. Afecta aproximadamente a un 2% de las personas mayores de 60 años. Este tipo de DMAE es responsable del 90% del total de casos de ceguera atribuidos a la enfermedad y la pérdida visual se produce de manera más rápida y agresiva que en la de tipo seco. No se conocen sus causas, aunque hay factores de riesgo aparte de la edad, como el consumo de tabaco y factores genéticos que muestran asociaciones consistentes. Aunque hay alternativas terapéuticas, estas lesiones son irreversibles y suponen una causa importante de alteraciones de la visión y calidad de vida por la afección en mayor o menor grado de la visión central. Historia natural Figura 2. Es muy rara en personas menores de 50 años. Aunque no está plenamente demostrado, hay una fuerte asociación entre la presencia de drusas y el desarrollo de formas avanzadas. La presencia de numerosas drusas de tamaño intermedio, de drusas irregulares («blandas») o de drusas grandes sí parece incrementar el riesgo de aparición de Diciembre 2013 › Artículo Científico Degeneración macular asociada a la edad (DMAE). Guía clínica optométrica, a partir de estudios basados en la evidencia la fase tardía1. Las drusas «duras» no parecen incrementar el riesgo de maculopatía y es raro no encontrar alguna en personas mayores. La variante atrófica se caracteriza por una formación redonda u ovalada de atrofia del epitelio pigmentario en la mácula. >D ieta rica en zeaxantina y luteína, pre- Clínicamente produce una cierta visión borrosa central y alteraciones en la percepción del contraste y también del color. El tipo neovascular se produce por el crecimiento anormal de vasos sanguíneos que, además, origina escapes de fluido o hemorragias que pueden aparecer bruscamente, llevando a pérdida de visión central y metamorfopsias. La fase más evolucionada es la formación de una cicatriz disciforme que lleva a ceguera central completa e irreversible. Con un ojo afectado, el riesgo de afección del otro es elevado. Tratamiento Impacto La DMAE, fundamentalmente la forma neovascular, representa la primera causa de ceguera en personas mayores de países desarrollados. La forma atrófica, o incluso las etapas previas también pueden afectar a la visión. Raramente lleva a ceguera completa ya que la visión periférica no suele afectarse, pero la afectación en la autonomía y calidad de vida es importante. En personas mayores supone un gran problema, ya que se une a los problemas de dependencia ya existentes, o los genera de forma brusca. TRATAMIENTO MÉDICO Y FARMACOLÓGICO de las formas no exudativas MAE y DMAE seca Cuando exista alto riesgo, como drusas blandas coalescentes o MNVC en el otro ojo: Vitaminas antioxidantes (E, C y β-carotenos) y suplementos minerales (Zinc) pueden reducir el riesgo de pérdida de visión moderada en pacientes con MAE temprana/intermedia y DMAE atrófica12. Suplementación diaria con vitamina C, E, óxido de Zinc, óxido de Cobre y β-caroteno disminuyo la pérdida de visión moderada de un 23% a 29%, y de un 20% a un 28% el riesgo de desarrollar DMAE avanzada (atrofia subfoveal o MNVC)13-14 En fumadores los suplementos no deben contener β-carotenos, ya que pueden incrementar el riesgo de cáncer de pulmón15-16 Tratamiento de la forma exudativa DMAE neovascular activa > MNVC extrafoveal (>200µ de fóvea) Recomendaciones higiénico-dietéticas >S uspender hábito tabáquico, control de la hipertensión arterial (HTA), colesterol y obesidad4-8. Protección contra le exposición solar9. a sentes generalmente en frutas y verduras (espinacas, brécol, berros, maíz, naranja y la yema de huevo). Se aconsejan alimentos ricos en omega3 (pescado azul y nueces)10-11. bien definida, fotocoagulación láser17-18, aunque el beneficio disminuye debido al crecimiento recurrente llegando el 50% de los pacientes tratados a desarrollar MNVC subfoveal durante los 5 años posteriores al tratamiento. Actualmente se opta por el tratamiento intravitreo b Figura 3. AGF de MNVC clásica. a) tiempo inicial. b) tiempo intermedio. c) tiempo final › nº 487 c ÓPTICA Figura 4a. Figura 4b. con antiangiogénicos si la MNCV se encuentra en el polo posterior. Inyecciones intravítreas de antian- > Vitrectomía, cuando existe hemorra- Fármacos administrados por vía intravítrea (Figura 4a y 4b), mediante inyecciones realizadas de forma periódica, ya que su vida media es corta. gia submacular masiva como consecuencia de la forma exudativa 19 y en algunas membranas neovasculares yuxtapapilares cuya extensión no afecte la zona avascular foveal. 20 > M NVC yuxta y subfoveales, trata- miento mediante terapia fotodinámica (TFD) e inyecciones intravitreas de fármacos antiangiogénicos (IV AA): giogénicos Actualmente, el tratamiento más eficaz. Tratamiento farmacológico con preparados anti-factor crecimiento endotelial vascular (VEGF): Empleo de verteporfina (Visudyne®) combinado con estimulación láser de longitud de onda roja. En DMAE exudativa combinada con intravítreas, en algunos casos refractarios y para reducir el número de inyecciones. 21 Pegaptinib (Macugen®) Aptámero contra la isoforma 165 del VEGF. La inyección intravítrea de 0,3mg cada seis semanas durante 1 año, como tratamiento de lesiones subfoveales activas de tamaño inferior a 12 áreas de disco, con componente neovascular mayor del 50%. Con un 70% de perder menos de 3 líneas de visión en comparación con el 55% del grupo control y una mejoría visual del 5%23 En la variante llamada vasculopatía coroidea polipoide idiopática (VCPI) parece más eficaz que en la DMAE 22, aunque suele utilizarse en combinación con anti-VEGF (factor de crecimiento del endotelio vascular). Ranibizumab (Lucentis®) Fragmento de anticuerpo anti-VEGF. Se une a todas las isoformas biológicamente activas del VEGF-A. La inyección intravitrea de 0,5mg mensual se ha demostrado efectivo en el tratamiento de T erapia F otodinámica a OFTÁLMICA b Figura 5. OCT. a) MNVC clásica sub-yuxtafoveal. AVcc 0.4 b) 4 meses tras tratamiento mediante racibizumab. Inyección mensual, 3 sesiones. AVcc 0.7dif. Sin presencia de fluido subrretiniano Diciembre 2013 › Degeneración macular asociada a la edad (DMAE). Guía clínica optométrica, a partir de estudios basados en la evidencia ALGORITMO DE TRATAMIENTO MEDICO DMAE NEOVASCULAR ACTIVA Artículo Científico DMAE neovascular MNVC extrafoveal Fotocoagulación Láser/IV AA Hemorragia submacular masiva Vitrectomía MNVC Yuxta/Subfoveal Terapía combinada: TFD+AA Pegaptinib Macugen® Inyecciones Intravitreas de AA (IV AA) Ranibizumab Lucentis® Bevacizumab Avastin® Aflibercep Eylea® que ranibizumab o bevacizumab en mola MNVC subfoveal, con una mejora de la noterapia sigue siendo el tratamiento de agudeza visual que alcanza su máximo a los el fármaco elección en el tratamiento de la DMAE 4 meses24, considerándose comoMAE DMAE de primera elección. Se realiza una inyecneovascular en la actualidad.31 ción cada 4 semanas los tres primeros meses Aflibercep (Eylea®) (Figura 5), y posteriormente cada mes si ATRÓFICA EXUDATIVA Anual Nuevo fármaco para el tratamiento de se evidencia reactivación, llegando a una la DMAE exudativa, ya aprobado por media de 5,6 inyecciones el primer año de Semestral Mensual la FDA en USA. En España se aprobará tratamiento25 próximamente. Bevacizumab (Avastin®). El primer anti-VEGF aprobado por la Es un agente anti-VEGF, que presenta FDA para la administración sistémica una gran afinidad de unión con todas en el tratamiento del cáncer colorrectal. las isoformas del VEGF, y también con Aceptado por la FDA en febrero 2004, se el PIGF (factor de crecimiento placeninició un estudio conocido como SANA tario).La afinidad de unión al VEGF-A Study (SystemicAvastinforNeovascular es notablemente superior a la de ranibiDMAE Study). zumab, tanto que podría permitir un intervalo de administración mayor (cada 8 Eficacia demostrada en el tratamiento semanas en vez de cada 4). 32-34 26-30 . Al igual que de la MNVC subfoveal También están en marcha estudios para el Ranibizumab se une a todas las isosu utilización en edema maculares y formas del VEGF-A, aunque aproximaobstrucciones venosas. 35-36 damente es tres veces mayor y 20 veces más potente. Medicamento usado en hospitales, que actualmente debe ser solicitado como uso compasivo en dosis de 1,25mg. Actualmente también se utiliza terapia combinada de antiangiogénicos con terapia fotodinámica, consiguiendo resultados visuales similares a los obtenidos en monoterapia pero con un menor número de inyecciones intravitreas 21, aun› nº 487 SEGUIMIENTO El seguimiento de los pacientes con DMAE es de vital importancia. Dependiendo del tratamiento realizado y del tipo de DMAE, el seguimiento será diferente, aunque siempre implicara la realización de una concreta batería de pruebas. En este aspecto la OCT (tomografía de coherencia óptica), permite una valoración de los pacientes importantísima. Aportar un informe indicando, si es posible: Pegaptinib Macugen® Ranibizumab Lucentis® Bevacizumab Avastin® ALGORITMO DE SEGUIMIENTO MAE DMAE ATRÓFICA EXUDATIVA Semestral Mensual Anual Aflibercep Eylea® ÓPTICA OFTÁLMICA durante el primer año y cada 3 meses el segundo año. Evitando el seguimiento con AGF (angiografía fluoresceínica). Está por determinar lo que hacer a partir del segundo año, que dependerá de la evolución de la enfermedad. Se espaciarán las revisiones, conforme se alcance la estabilidad de la visión.38 CONCLUSIÓNES el tipo de DMAE; la AV con su mejor corrección y las recomendaciones de estilo de vida; fármacos antioxidantes (en caso necesario); ayudas visuales prescritas y necesidad de rápida derivación a oftalmólogo, en caso de pérdida de visión central o metamorfopsias. Se aconseja para este propósito facilitar al paciente una rejilla de Amsler para autoevaluación en casa. Especialmente útil ,en casos de buena visión en ambos ojos, ya que si se afecta un ojo puede pasar desapercibido para el paciente. Cuando se trata del “primer ojo” del paciente, se debe advertir de la bilateralidad y simetría de la enfermedad, con una velocidad de progresión/crecimiento de 1/10 de diámetro de papila/año en el caso de la forma atrófica. En el caso de forma neovascular la tendencia a la bilateralización es de: 4% el primer año, 10% el segundo año, 17% el tercer año y alrededor del 25% a los 5 años.37 Explicar que, ante alteración visual, pérdida de visión central o metamorfopsia, acudan de inmediato para valoración optométrica y rápida derivación a oftalmólogo (tiempo recomendado 1 semana), junto con informe indicando, como mínimo, la AV con la mejor corrección posible. En DMAE neovascular que se traten mediante inyecciones de antiangiogénicos se realizaran revisiones mensuales oftalmológicas/optométricas con la siguiente batería de pruebas: > Toma de AV mediante optotipos ET- La degeneración macular asociada a la edad es una de las causas más importantes de pérdida significativa de visión en adultos en los países desarrollados. El impacto de la enfermedad, en términos económicos, de pérdida de productividad y de calidad de vida, es devastador. Hasta que los medios para curar la DMAE estén suficientemente desarrollados, los optometristas tenemos la necesidad de comprender la etiopatogenia de la enfermedad, con el fin de reducir el riesgo del paciente de sufrir una pérdida severa de visión, mediante la identificación temprana y la derivación oportuna para detenerla en su fase inicial. A su vez, el optometrista debe poseer el conocimiento necesario sobre las nuevas terapias para implicarse en la valoración ocular del paciente; a la vez que educar e informar sobre la historia natural de anormalidades asociadas al problema macular. En ciertos casos la visión puede mantenerse, o cuanto menos retardar su desarrollo, si el paciente es informado y educado para buscar atención oftalmológica de forma inmediata. Una mejor comprensión del paciente con DMAE sobre su enfermedad, ayudará al cumplimiento más estricto de las recomendaciones sobre el cuidado de su vista, y en algunos casos puede ayudar a preservar una visión de más calidad y durante más tiempo. Por último, el optometrista está involucrado en la atención visual avanzada de los pacientes con DMAE a través del área que ocupa: DRS (estudio para el tratamiento precoz de la retinopatía diabética). 1) la detección precoz y su vinculación a la práctica clínica junto al oftalmólogo. > Biomicroscopía de mácula. > OCT (tomografía de coherencia óptica) 2) las ayudas de baja visión y la rehabilitación visual. Diciembre 2013 › Degeneración macular asociada a la edad (DMAE). Guía clínica optométrica, a partir de estudios basados en la evidencia BIBLIOGRAFÍA Artículo Científico 1. Klein R, Klein BE, Jensen SC, Meuer SM. The five-year incidence and progression of age-related maculopathy: the Beaver Dam Eye Study. Ophthalmology. 1997 Jan;104(1):7-21. 2. Klein R, Davis MD, Magli YL, Segal P, Klein BE, Hubbard L. The Wisconsin age-related maculopathy grading system. Ophthalmology 1991; 98: 1128-1134. 3. Age-Related Eye Disease Study (AREDS) Research Group. A simplified severity scale for age-related macular degeneration: AREDS Report no.18. Arch Ophthalmol. 2005 Nov;123(11):1570-4. 4. Seddon JM, Willett WC, Speizer FE, Hankinson SE. A prospective study of cigarette smoking and age-related macular degeneration in women. JAMA 1996;276:1141-6. 5. Risk factors for the incidence of advanced agerelated macular degeneration in the Age-Related Eye Disease Study (AREDS): AREDS report no.19. Ophthalmology 2005; 112:533-9. 6. Klein R, Klein BE, Wong TY, et al. The association of cataract and cataract surgery with the long-term incidence of age-related maculopathy: the Beaver Dam eye study. Arch Ophthalmol. 2002;120:1551–1558. 7. Risk factors associated with age-related macular degeneration. A case-control study in the age-related eye disease study: age-related eye disease study report number 3. Age-Related Eye Disease Study Research Group. Ophthalmology 2000; 107:2224-32. 8. Mares-Perlman JA, Brady WE, Klein R, et al. Dietary fat and age-related maculopathy. Arch Ophthlamol 1995; 113:743-8 9. Tomany SC, Cruickshanks KJ, Klein R, et al. The Beaver Dam Eye Study: sunlight and the 10-year incidence of age-related maculopathy. Arch Ophthalmol. 2004;122:750–757. doi: 10.1001/archopht.122.5.750. 10. Cohen SY, Mauget-Faysse M, Oubraham H, Algan M, Conrath J, Roquet W. Impact of eating habits on macular pathology assessed by macular pigment optical density measure. Fr Ophtalmol. 2010 Apr;33(4):234-40. Epub 2010 Mar 11. 11. Bernstein PS. Nutritional Interventions against Age-Related Macular Degeneration. ActaHortic. 2009 Aug 31;841:103-112. 12. A randomized, placebo-controlled, clinical trial of high-dose supplementation with vitamins C and E, beta carotene, and zinc for age-related macular degeneration and vision loss: AREDS report no.8 Arch Ophthalmol 2001; 119:141736. 13. A randomized, placebo-controlled, clinical trial of high-dose supplementation with vitamins C and E and beta carotene for age-related cataract and vision loss: AREDS report no.9. Arch Ophthalmol 2001; 119:1439-52. 14. Chew EY, Davis MD, Seddon JM, et al. The effect of antioxidant and zinc supplements on change in drusen size/area in the Age-Related › nº 487 Eye Disease Study (AREDS). Invest Ophthalmol Vis Sci 2002; 43:E-Abstract 1903. tion. Ophthalmic Surg Lasers Imaging 2005; 36:331-5. 15. The effect of vitamin E and beta carotene on the incidence of lung cancer and other cancers in male smokers. The Alpha-Tocopherol, Beta Carotene Cancer Prevention Study Group. N Engl J Med 1994; 330:1029-35. 28. Rich RM, Rosenfeld PJ, Pliafito CA, Dubovy SR, Davis JL, Flynn HW Jr., Gonzalez S, Feuer WJ, Lin RC, Lalwani GA, Nguyen JK, Kumar G. Sort-term safety and efficacy of intravitrealbevacizumab (avastin) for neovascular age-related macular degeneration. Retina 2006; 26:495-511. 16. Omenn GS, Goodman GE, Thornquist MD, et al. Effects of a combination of beta carotene and vitamin A on lung cancer and cardiovascular disease. N Engl J Med 1996; 334:11505. 17. Argon laser photocoagulation for neovascularmaculopathy. Five-year results from randomized clinical trials. Macular Photocoagulation Study Group. Arch Ophthalmol 1991; 109:1109-14. 18. Moisseiev J, Alhalel A, Masuri R, Treister G. The impact of the macular photocoagulation study results on the treatment of exudative agerelated macular degeneration. Arch Ophthalmol 1995; 113:185-9. 19. Merrill PT, LoRusso FJ, Lomeo MD, Saxe Sj Khan MM, Lambert HM. Surgical removal of subfovealchoroidalneovascularization in agerealted macular degeneration. Ophthalmology 1999; 106:782-789. 20. Kokame GT, Yamaoka S. Subretinal surgery for peripapillarysubretinalneovascular membranes. Retina 2005; 25:564-569. 21. Navea A, Mataix J, Desco MC, Garcia-Pous M, Palacios E. One-year follow-up of combined customized therapy. Photodynamic therapy and bevacizumab for exudative age-related macular degeneration. Retina 2009 Jan;29(1):13-9. 22. Gomi F, Tano Y. Polypoidal choroidal vasculopathy and treatments. Curr Opin Ophthalmol. 2008 May;19(3):208-12. 23. Gragoudas ES, Adamis AP, Cunningham ET, Jr., et al. Pegaptanib for neovascular age-related macular degeneration. N Engl J Med 2004; 351:2805-16 24. Rosenfeld PJ, Brown DM, Heier JS, Boyer DS, Kaiser PK, Chung CY, Kim RY. MARINA Study Group. Ranibizumab for neovascular agerelated macular degeneration. N Engl J Med 2006; 355:1419-31. 29. Spaide RF, Laud K, Fine HF, Klancnik JM Jr., Meyerle CB, Yannuzzi LA, Sorenson J, Slakter J, Fisher YL, Cooney MJ. Intravitrealbevacizumab treatment of choroidal neovascularization secondary to age-related macular degeneration. Retina 2006; 26:383-90 30. Costa RA, Jorge R, Calucci D, Cardillo JA, Melo LA Jr., Scott IU. Intravitrealbevacizumab for choroidal neovascularization caused by AMD (IBeNA Study): results of a phase 1 dose-escalation study. Invest Ophthalmol Vis Sci 2006; 47:4569-78. 31. Chiang A, Regillo CD. Preferred therapies for neovascular age-related macular degeneration. CurrOpinOphthalmol 2011 May;22(3):199-204 32. Ohr M, Kaiser PK. Intravitrealaflibercept injection for neovascular (wet) age-related macular degeneration. Expert OpinPharmacother. 2012 mar;13(4):585–91. 33. Nguyen QD, Shah SM, Browning DJ, Hudson H, Sonkin P, Hariprasad SM, et al. A phase I study of intravitreal vascular endothelial growth factor trap-eye in patients with neovascular agerelated macular degeneration. Ophthalmology. 2009 nov;116(11):2141–2148.e1. 34. Brown DM, Heier JS, Ciulla T, Benz M, Abraham P, Yancopoulos G, et al. Primary endpoint results of a phase II study of vascular endothelial growth factor trap-eye in wet agerelated macular degeneration. Ophthalmology. 2011 jun;118(6):1089–97. 35.Boyer D, Heier J, Brown DM, Clark WL, Vitti R, Berliner AJ, et al. Vascular Endothelial Growth Factor Trap-Eye for Macular Edema Secondary to Central Retinal Vein Occlusion: Six-Month Results of the Phase 3 COPERNICUS Study. Ophthalmology. 2012 may;119(5):1024–32. 25. Brown DM, Kaiser PK, Michels M, Soubrane G, Heier JS, Kim RY, Sy P, Schneider S; ANCHOR Study Group. Ranibizumab versus verteporfin for neovascular age-related macular degeneration. N Engl J Med. 2006; 355:1432-44. 36. Do DV, Nguyen QD, Boyer D, SchmidtErfurth U, Brown DM, Vitti R, et al. One-Year Outcomes of the DA VINCI Study of VEGF Trap-Eye in Eyes with Diabetic Macular Edema. Ophthalmology [Internet]. 2012 abr [citado 2012 may 21] 26. Fung AE, Lalwani GA, Rosenfeld PJ, Dubovy SR, Michels S, Feuer WJ, Puliafito CA, Davis JL, Flynn HW Jr., Esquiabro M. An optical coherence tomography-guided, variable dosing regimen with intravitreal Ranibizumab (Lucentis) for neovascular age-related macular degeneration. Am J Ophthalmol 2007; 143:566-83. 37. Ruíz-Moreno JM, Arias L, Armadá F, Boixadera A, García A, Gómez-Ulla F, Monés J, Piñeiro A, Suárez M. Guías de práctica clínica de la Serv: tratamiento de la degeneración macular asociada a la edad (DMAE) exudativa. RuízMoreno JM et al. ArchSocEspOftalmol 2009; 84:333-344. 27. Rosenfeld PJ, Moshfeghi AA, Puliafito CA. Optical coherence tomography findings after an intraitreal injection of bevacizumab (avastin) for neovascular age-related macular degenera- 38. Salinas_Martinez EM, et al. Protocolo degeneración macular asociada a la edad. Unidad de retina médica. Torrevieja Salud. Departamento Salud 22. 2007.