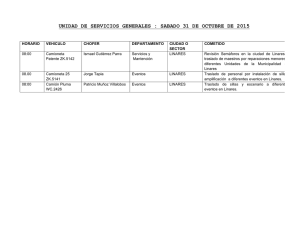
Problemes Xavi
Anuncio

GRADO EN INGENIERÍA EN TECNOLOGÍAS AEROESPACIALES Ciencia de Materiales Problemas Xavi Paneque Linares 6 de Junio del 2012 Índice 1. Introducción a la ciencia de materiales................................................................................. 1 2. Estructura de los sólidos cristalinos ...................................................................................... 6 3. Solidificación, defectos cristalinos y difusión ...................................................................... 16 Defectos .................................................................................................................................. 16 Deslizamiento y endurecimiento por deformación ................................................................ 23 Difusión ................................................................................................................................... 28 4. Aleaciones metálicas. Diagramas de equilibrio de fases..................................................... 33 5. Aleaciones metálicas. El sistema Fe-C ................................................................................. 48 6. Polímeros............................................................................................................................. 57 7. Cerámicas ............................................................................................................................ 70 8. Materiales compuestos ....................................................................................................... 82 Grado en Ingeniería en Tecnologías Aeroespaciales 1 Ciencia de Materiales 1. Introducción a la ciencia de materiales 2.3. ¿Cuántos gramos hay en uma de un material? ¿Cuántos átomos hay en un mol de una sustancia? 1 1 2.7. Escribir , , · la , 1,66 · 10 1 6,022 · 10 1 , = 6,022 · 10 electrónica 4 4 3 3 4 :1 2 2 :1 2 2 :1 2 2 2.8. El óxido cálcico ( para á los siguientes iones , :1 2 2 3 3 = 1,66 · 10 á configuración :1 2 2 :1 2 2 · 3 3 3 3 3 3 4 4 4 4 4 4 5 5 5 5 5 4 4 ) presenta predominantemente enlace iónico. ¿Cuáles son los dos gases inertes que tienen idénticas configuraciones electrónicas a los iones y Para el calcio tenemos :1 2 2 3 3 Y para el oxígeno :1 2 2 2.9. Con respecto a la configuración electrónica, ¿qué tienen en común todos los elementos del grupo IA de la tabla periódica? Todos tienen en común que en la última capa contienen tan solo un electrón. 2.10. Indicar si las configuraciones electrónicas siguientes corresponden a un gas inerte, a un halógeno, a un metal alcalino, a un metal alcalinoterro o a un metal de transición. Justifica la respuesta Xavi Paneque Linares Página 1 Grado en Ingeniería en Tecnologías Aeroespaciales 2 Ciencia de Materiales ( ) : Halógeno ( ) : Alcalinoterro ( ) : Halógeno ( ) : Alcalino ( ) : Alcalinoterro ( ) : Alcalinoterro 2.18. El porcentaje de carácter iónico de un enlace entre los elementos A y B (siendo A el más electronegativo) se puede expresar aproximadamente mediante la siguiente expresión: % Donde y á ó = · son las electronegatividades relativas de los dos elementos. Determinar el % de carácter iónico de los enlaces interatómicos de los compuestos: , , , , El porcentaje de carácter iónico será para cada elemento respectivamente % = 100 1 % = 100 1 % = 100 1 Xavi Paneque Linares , , , , % = 100 1 % = 100 1 , = 73,35% = 6,06% = 93,43% , , , , = 14,79% = 51,45% Página 2 Grado en Ingeniería en Tecnologías Aeroespaciales 3 Ciencia de Materiales 2.19. Representar gráficamente la energía de enlace en función de las temperaturas de fusión de los materiales de la tabla. Utilizar este gráfico para calcular la energía de enlace aproximada del molibdeno, sabiendo que la temperatura de fusión es de Relación Tf-Ee y = 430,17x - 306,62 Temperatura de fusión (Cº) 4000 3500 3000 2500 2000 1500 1000 500 0 -500 0 2 4 6 Energía de enlace (eV/áto) 8 10 Según la línea de tendencia, la energía de enlace aproximada del molibdeno será 2617 = 430.17 · 306,62 = 5.37 á 2.20. Determinar el número de enlaces covalentes posibles en los átomos de los siguientes elementos; germanio, fósforo, selenio y cloro Xavi Paneque Linares Página 3 Grado en Ingeniería en Tecnologías Aeroespaciales 4 Ciencia de Materiales El número de enlaces covalentes posibles para un átomo particular depende del número de electrones de valencia. Para enlazarse covalentemente con hasta 8 :8 4=4 :8 electrones de valencia, un átomo puede átomos 6=2 :8 5=3 :8 7=1 2.21. ¿Qué tipos de enlace cabe esperar en cada uno de los siguientes materiales: xenón sólido, fluoruro cálcico ( ), bronce, teluro de cadmio ( ), goma y wolframio? Xavi Paneque Linares Página 4 Grado en Ingeniería en Tecnologías Aeroespaciales 5 Ciencia de Materiales Del xenón sólido tendremos enlaces de Van der Waals, del fluoruro cálcico tendremos enlaces iónicos. En el bronce tendremos enlace metálico. EL teluro de cadmio será covalente. En la goma aparecerán enlaces covalente y de Van der Waals. En el wolframio tendremos enlace metálico. 2.22. Explicar, mediante el enlace de hidrógeno, el anómalo comportamiento del agua al helarse. ¿Por qué aumenta el volumen después de solidificar? En estado líquido existen los puentes de hidrógeno y estos tienen una mayor longitud de enlace. La geometría molecular del agua está más restringida espacialmente en el estado sólido con estructura cristalina que en el estado líquido. Por ello el hielo es menor denso que el agua líquida. Xavi Paneque Linares Página 5 Grado en Ingeniería en Tecnologías Aeroespaciales 6 Ciencia de Materiales 2. Estructura de los sólidos cristalinos 3.9. El molibdeno tiene una estructura cristalina BCC, un radio atómico de , y un peso atómico de , / . Calcular y comparar su densidad , teórica con el valor experimental (densidad= / ) Dado que se trata de una estructura BCC tenemos = 2; = 4 3 Así pues la densidad teórica será · · = = 2 · 95,94 4 · 0,1363 · 10 3 = 10,22 · 6,022 · 10 Exactamente el valor de la experimental. 3.10. Calcular el radio de un átomo de Paladio sabiendo que el Pd tiene una estructura cristalina FCC, una densidad de , / y un peso atómico de / Dado que se trata de una estructura FCC tenemos = 4; =2 2 Así pues la densidad teórica será = · · = 4 · 106,4 2 2 · · 10 · 6,022 · 10 = 12 = 0,1376 3.13. El circonio tiene una estructura cristalina HC y una densidad de , / . ¿Cuál es el volumen de la celdilla unidad en metros cúbicos? Si la relación / es , calcular los valores de y de Dado que se trata de una estructura HC tenemos, por trigonometría = 6; Xavi Paneque Linares = 3 3 2 = 1,593 · 3 3 2 Página 6 Grado en Ingeniería en Tecnologías Aeroespaciales 7 Ciencia de Materiales Por otro lado el volumen debe cumplir · · = = 6 · 91,224 · 6,022 · 10 = 6,51 = 1,3962 · 10 Por tanto 1,593 · 3 3 2 = 1,3962 · 10 = 0,3231 = 0,5147 3.14. Utilizando los datos de peso atómico, estructura cristalina y radio atómico, calcular las densidades teóricas del aluminio, níquel, titanio y tungsteno y comparar estos valores con las densidades experimentales ( , respectivamente). La relación / para el titanio es , , , , , , , / . Aluminio (FCC) = · · = · · = · · = 4 · 26,982 2 2 · 0,1431 · 10 · 6,022 · 10 = 2,703 Níquel (FCC) = 4 · 58,71 2 2 · 0,1246 · 10 · 6,022 · 10 = 8,909 Tungsteno (BCC) = 2 · 95,94 4 · 0,1371 · 10 3 = 19,24 · 6,022 · 10 Titanio (BCC) Xavi Paneque Linares Página 7 Grado en Ingeniería en Tecnologías Aeroespaciales 8 Ciencia de Materiales · · = Titanio 2 · 47,90 = 4 · 0,1430 · 10 3 = 4,417 · 6,022 · 10 (HC). A partir del resultado del ejercicio anterior, donde = 1,58 · 3 3 (2 · 0,1445 · 10 ) = 9,908 · 10 2 · · = =2 = 6 · 47,90 9,908 · 10 · 6,022 · 10 = 4,82 3.19. El indio tiene una celdilla unidad tetragonal cuyos parámetros de red valen , y , y respectivamente. Determinar el número de átomos en la celdilla unidad, si el factor de empaquetamiento atómico y el radio atómico son , y , es , respectivamente. Calcular la densidad. El peso atómico del indio / . = 4 ·3 = · · = = 4 ·3 · = 4 4 · 3 · 0,1625 · 3 · 0,459 · 0,495 4 · 114,82 0,459 · 0,495 · (10 ) · 6,022 · 10 = 0,69 =4 = 7,313 3.25. Dibujar una celdilla unidad ortorrómbica y trazar en ella una dirección [ un plano ( ]y ) [2 1 1] Xavi Paneque Linares [0 2 1] Página 8 Grado en Ingeniería en Tecnologías Aeroespaciales 9 Ciencia de Materiales 3.28. Dentro de una celdilla unidad cúbica trazar las siguientes direcciones [ ], [ ], [ ], [ ], [ ] 3.27. Aquí se muestran las celdillas unidad de dos hipotéticos metales ¿Cuáles son los índices de las direcciones y de los planos? Dirección 1 1 0,5 1 [2 1 2] [0 0,5 1] [0 1 2] Dirección 2 Plano 1 (0,5 1 1) (2 1 1) Plano 2 0,5 Xavi Paneque Linares (0 2 0) Página 9 Grado en Ingeniería en Tecnologías Aeroespaciales 10 Ciencia de Materiales Dirección 1 [0 0,5 1] [0 1 2] Dirección 2 [0,5 0,5 1] [1 1 2] ( (0 2 0) Plano 1 0,5 ) Plano 2 0,5 0,5 1 (2 2 1) 3.29. Determinar los índices de las direcciones mostradas en las siguientes celdillas unidad cúbica Dirección A 0 0,5 2/3 [0 3 4] Dirección B 2/3 0 1/2 [4 0 3] Dirección C [1 1/2 1/6] [6 3 1] Dirección D 1/2 1/2 1/2 [1 1 1] 3.31. En los cristales tetragonales, citar los índices de las direcciones equivalentes a cada una de las siguientes: [ ], [ ] Las direcciones equivalentes a [0 1 1] son [0 1 1], [0 1 1], [0 1 1], [1 0 1], [1 0 1], [1 0 1], [1 0 1] Xavi Paneque Linares Página 10 Grado en Ingeniería en Tecnologías Aeroespaciales 11 Ciencia de Materiales Las direcciones equivalentes a [1 0 0] son [1 0 0], [1 0 0], [0 1 0], [0 1 0] 3.33. Determinar los índices de Miller de los planos mostrados en la siguiente celdilla unidad : (1 1 2) : (2 2 0) : (2 1 1) : (2 2 0) : (1 2 2) : (0 2 1) (2 1 1 2) 3.42. Calcular y comparar las densidades lineales de las direcciones [ [ ], [ ]y ] en la FCC En una estructura FCC el parámetro de celda es =2 2 Por tanto las densidades lineares son la longitud que ocupan los átomos entre la longitud total [ Xavi Paneque Linares ] = 2 = 2 2 2 = 0,71 [ ] = 4 2 = 4 =1 4 Página 11 Grado en Ingeniería en Tecnologías Aeroespaciales 12 Ciencia de Materiales [ ] = 2 = 3 2 2 6 = 0,41 3.45. Calcular y comparar las densidades planares de los planos ( )y( ) en la FCC Las densidades planares serán el cociente del área que ocupan los átomos entre el área tota que intercepta el plano. En el plano (1 0 0) tenemos dos átomos enteros interceptados. ( = ) 2 = 2 8 = 0,785 En el plano (1 1 1) tenemos dos átomos interceptados y el área por trigonometría es ( ) = 2 = 3 2 2 4 3 = 0,907 3.46. Calcular y comparar las densidades planares de los planos ( )y( ) en la BCC En una estructura BCC tenemos = 4 3 En el plano (1 0 0) se intercepta 1 átomo en total y la densidad será = = 16 3 = 0,589 En el plano (1 1 0) se interceptan 2 átomos en total y la densidad será = 2 2 = 2 16 2 3 = 0,833 3.50. Explicar por qué las propiedades de los materiales policristalinos casi siempre son isotrópicas Xavi Paneque Linares Página 12 Grado en Ingeniería en Tecnologías Aeroespaciales 13 Ciencia de Materiales La isotropía en materiales cristalinos es función de la simetría cristalina. En la mayoría de los materiales policristalinos, las orientaciones cristalográficas de los granos individuales son completamente al azar. En estas circunstancias, aunque cada gramo sea anisotrópico, el material compuesto de un conjunto de granos, se comporta isotrópicamente. 3.51. Utilizando los datos de la tabla correspondientes al aluminio, calcular la distancia interplanar del conjunto de planos ( ) El conjunto de planos (1 1 0) mantienen una distancia = + + = 2 2 + + = 2 2 · 0,1431 2 = 0,2862 3.53. Utilizando los datos de la tabla anterior correspondientes al hierro las distancias interplanares de los conjuntos de planos ( )y( , calcular ) El conjunto de planos (1 1 0) mantienen una distancia = + + = 4 3 + + 4 · 0,1241 3 = = 0,1655 3 El conjunto de planos (2 1 1) mantienen una distancia = + Xavi Paneque Linares + = 4 3 + + 4 · 0,1241 3 = = 0,1170 6 Página 13 Grado en Ingeniería en Tecnologías Aeroespaciales 14 Ciencia de Materiales 3.55. El metal niobio tiene una estructura cristalina BCC. Si el ángulo de difracción es (difracción de primer orden) para el conjunto de planos ( de emplea una radiación ) cuando se monocromática de una longitud de onda de , , calcular la distancia interplanar de este conjunto de planos y el radio atómico del átomo de niobio. En primer lugar obtenemos la distancia entre planos a partir de 2 sin = = = 2 sin 1 · 0,1659 = 0,1347 76 2 sin 2 Y el radio atómico será = + + = 4 3 + + 4 · 3 = = 0,1347 6 = 0,1429 3.57. La figura muestra un espectro de difracción de rayos X del plomo, utilizando radiación monocromática de longitud de onda de , . Se han anotado los índices de cada pico. Calcula la distancia interplanar de cada conjunto de planos indexados. Determinar también el parámetro de red del Pb para cada pico. Aplicando las ecuaciones 2 sin = = + + Se obtiene (grados) 30 Xavi Paneque Linares ( ) 0,2885 ( ) 0,4997 Página 14 Grado en Ingeniería en Tecnologías Aeroespaciales 15 Ciencia de Materiales 37 0,2430 0,4860 53 0,1728 0,4887 63 0,1476 0,4894 65 0,1435 0,4971 3.58. Los índices de los picos del espectro de difracción de Rayos X del Pb cumplen las reglas de difracción para FCC (por ejemplo , , deben ser todos pares o impares). Enumerar los índices , , de los cuatro primeros picos de difracción para cristales BCC con + + par Para estructuras BCC se cumple que cumple , , + + = y para la estructura FCC se son todos pares o impares. Así pues los cuatro primeros picos de difracción para cristales BCC son (2 0 0), (2 2 0), (2 2 2) Xavi Paneque Linares Página 15 Grado en Ingeniería en Tecnologías Aeroespaciales 16 Ciencia de Materiales 3. Solidificación, defectos cristalinos y difusión Defectos 4.1. Calcular la fracción de lugares atómicos vacantes que tiene el cobre a su ( temperatura de fusión de , ). Suponer una energía de activación de /á La fracción de lugares atómicos vacantes es = = , , · , · · · = 4,528 · 10 4.2. Calcular el número de vacantes por metro cúbico para el oro a de activación para la formación de vacantes es de , densidad y el peso atómico del Au son , . La energía /á / . Además, la , y / , respectivamente En primer lugar hay que calcular el número de átomos que hay en un metro cúbico 1 · 19,32 10 · 1 196,9 · 6,022 · 10 1 á = 5,91 · 10 á El número de vacantes será = = 5,91 · 10 · , , · , · · · = 3,67 · 10 4.3. Calcular la energía de activación para la formación de vacantes en el aluminio, sabiendo que el número de vacantes en equilibrio a . El peso atómico y la densidad (a , / , (773 K) es de ) del aluminio son , / · y , respectivamente. El número de átomos por metro cúbico es 1 · 2,62 10 · 1 26,98 · 6,022 · 10 1 á = 5,848 · 10 á Aplicando la ecuación resulta Xavi Paneque Linares Página 16 Grado en Ingeniería en Tecnologías Aeroespaciales 17 Ciencia de Materiales = 7,57 · 10 = 5,848 · 10 , · , · · · = 0,7504 á 4.4. En la siguiente tabla se dan el radio atómico, la estructura cristalina, la electronegatividad y la valencia más común de varios elementos. Para los no metálicos sólo se ha indicado el radio atómico. Indicar cuáles de estos elementos pueden formar con el níquel Los factores determinantes en el grado de solubilidad en disoluciones sustitucionales son - Tamaño del átomo (tolerancia del ±15%) - Electroquímica, cuanto mayor diferencia de electronegatividades mayor solubilidad sustitucional y menor intersticial. - Numero de valencia, mayor solubilidad cuanto mayor sea el número de valencia - Una misma estructura favorece la solubilidad a) Una disolución sólida sustitucional con solubilidad total Cobre, paladio y platino b) Una disolución sólida sustitucional con solubilidad parcial Plata, aluminio, criptón, hierro, níquel y zinc. Xavi Paneque Linares Página 17 Grado en Ingeniería en Tecnologías Aeroespaciales 18 Ciencia de Materiales c) Una disolución sólida intersticial Carbono, hidrógeno y oxígeno 4.5. Para la estructura FCC, los lugares intersticiales que pueden ocupar los átomos de soluto están situados en el centro de las aristas de las celdillas unidad. Calcular el radio de un átomo de soluto que puede colocarse en uno de estos lugares en función de radio Una arista del átomo del disolvente es =2 2 Por tanto el hueco que existe entre dos átomos en una arista es 2 = 2 = 2 2 = 2 1 = 0,41 4.6. Calcular la composición en porcentaje en peso de una aleación que contiene , , de titanio, de aluminio y , de vanadio. El porcentaje en peso es %= 218 = 89,97% 218 + 14,6 + 9,7 %= 14,6 = 6,03% 218 + 14,6 + 9,7 %= 9,7 = 4% 218 + 14,6 + 9,7 4.8. ¿Cuál es la composición, en porcentaje atómico, de una aleación que contiene , de zinc y de , de cobre, de plomo? Escribimos la cantidad de cada substancia en moles 99,7 Xavi Paneque Linares · 1 63,54 = 1,57 Página 18 Grado en Ingeniería en Tecnologías Aeroespaciales 19 Ciencia de Materiales 102 1 63,37 = 1,61 1 207,19 = 0,01 · 2,1 · El porcentaje es por tanto %= 1,57 = 49,2% 1,57 + 1,61 + 0,01 %= 1,61 = 50,5% 1,57 + 1,61 + 0,01 %= 0,01 = 0,3% 1,57 + 1,61 + 0,01 4.13. El níquel forma una disolución sólida sustitucional con el cobre. Calcular el número de átomos de níquel por centímetro cúbico en una aleación cobre-níquel, que contiene , % puros son de , y y , , % / en peso. Las densidades del níquel y del cobre , respectivamente. Suponemos 100 gramos de aleación y tenemos 100 · 1 1 · 100 58,71 · 6,022 · 10 1 á = 1,0257 · 10 á Calculemos ahora los centímetros cúbicos de aleación por cada 100 gramos 100 ó · 1 100 · 1 8,90 + 99 100 · 1 8,93 = 11,2 Por tanto el número de átomos de níquel por centímetro cúbico es 1,0257 · 10 11,2 = 9,16 · 10 4.14. El zinc forma una disolución sólida sustitucional con el cobre. Calcular el porcentaje en peso de zinc que debe añadirse al cobre para conseguir una aleación que contenga , · átomos de Zn por centímetro cúbico. Las densidades del zinc y del cobre puros son de , Xavi Paneque Linares y , / , respectivamente. Página 19 Grado en Ingeniería en Tecnologías Aeroespaciales 20 Ciencia de Materiales Considerando un centímetro cúbico tenemos 1,75 · 10 á · 1 6,022 · 10 á · 65,37 1 = 0,19 = 0,0266 Así pues el volumen de cobre será 1 0,266 = 0,973 8,692 Finalmente el porcentaje de masa que debemos añadir será 0,19 · 100 = 2,14% 8,692 + 0,19 4.15. Calcular el número de átomos de Zn que hay en zinc, que contiene , % y , % en peso 99 1 · 100 8,93 · de una aleación cobre- Supongamos 100 g de aleación 100 · 1 1 · 100 7,13 100 · + 1 1 · 100 65,37 · 1 10 6,022 · 10 1 = 1,12 · 10 á = 9,21 · 10 ó á Por tanto el número de átomos por metro cúbico es 9,21 · 10 1,12 · 10 = 8,21 · 10 4.17. Para las estructuras cristalinas FCC y BCC, el vector de Burguers b se puede expresar como = Donde [ ] es la longitud de la arista de la celdilla unidad y [ ] es la dirección cristalográfica de mayor densidad atómica lineal. Xavi Paneque Linares Página 20 Grado en Ingeniería en Tecnologías Aeroespaciales 21 Ciencia de Materiales ¿Cuáles son las representaciones del vector de Burguers en las estructuras cristalinas FCC, BCC y cúbica simple? Si la magnitud del vector de Burguers | | es | |= + + Determinar el valor de | | para el cobre y el hierro Para el cobre tenemos | |= 2 2 · 0,1278 · 1 + 1 + 0 = 0,2556 2 Para el hierro 4 · 0,1241 3 | |= · 1 + 1 + 1 = 0,2482 2 4.18. La energía superficial de un monocristal depende de la orientación cristalográfica con respecto a la superficie. Justificarlo. Un cristal FCC, como el aluminio, ¿tiene mayor energía en el plano ( ) o en el ( )? ¿Por qué? La superficie externa constituye uno de los límites más evidentes, se considera una imperfección puesto que representa el límite de la estructura cristalina, donde termina. Los átomos superficiales no están enlazados con el máximo de vecinos más próximos y, por lo tanto, están en un estado energético superior que los átomos de las posiciones interiores. Los enlaces no realizados de estos átomos superficiales aumentan la energía superficial, expresada en unidades de energía por unidad de área. Los materiales tienden a minimizar el área total de la superficie para disminuir esta Xavi Paneque Linares Página 21 Grado en Ingeniería en Tecnologías Aeroespaciales 22 Ciencia de Materiales energía. Así pues tendrá más energía aquel monocristal que tenga orientada al exterior una superficie con mayor densidad planar. Por lo tanto, en una estructura FCC tendrá más energía el plano (1 0 0). 4.22. Determinar el tamaño de grano medio de grano, en milímetros, de las probetas, cuyas microestructuras se reproducen en la figura. Suponer que está aumentada y utilizar al menos siete segmentos de recta. La media de los cortes es 9 + 7 + 9 + 8 + 10 + 9 + 7 = 8,43 7 La longitud de línea es = 5,5 Por tanto el tamaño de grano medio es = 55 = 0,065 8,43 · 100 4.24. Para un tamaño de grano ASTM 6, ¿cuántos granos hay aproximadamente en una pulgada cuadrada de una microestructura a 100 aumentos? Determinar el número ASTM para el tamaño de grano de la micrografía de la figura anterior, suponiendo 100 aumentos. Xavi Paneque Linares Página 22 Grado en Ingeniería en Tecnologías Aeroespaciales 23 Ciencia de Materiales =2 =2 = 32 En la fotografía anterior podemos ver unos 64 granos, por tanto 64 = 2 4.25. En la micrografía de un metal =5 se calculó que el número medio de granos por pulgada cuadrada era 24. Calcular el número ASTM para ese tamaño de grano. =2 = 24 = 5,585 Deslizamiento y endurecimiento por deformación 7.11. Algunas veces el producto se denomina factor de Schmid. Determinar la magnitud del factor de Schmid para un monocristal FCC con su dirección [ ] paralela al eje de carga Debemos encontrar el coseno del ángulo que forman la dirección de tracción con la normal al plano y con la dirección de deslizamiento. El plano de deslizamiento en una estructura FCC es (1 1 1) y la dirección de deslizamiento [1 1 0]. El primero es, por definición de producto escalar cos = (1,0,0)(1,1,1) 3 = 3 3 El segundo es cos = (1,0,0)(1, 1,0) 2 = 2 2 Por tanto el factor de Schmid resulta cos cos = 6 6 0,408 7.12. Consideremos un monocristal orientado de tal manera que a la normal al plano de deslizamiento y la dirección de deslizamiento forman ángulos de y respectivamente, con el eje de tracción. Si la tensión de cizalladura resuelta crítica es Xavi Paneque Linares Página 23 Grado en Ingeniería en Tecnologías Aeroespaciales 24 Ciencia de Materiales , ¿se deformará plásticamente si se aplica una tensión de ? Si no fuera así, ¿qué tensión sería necesaria? Si aplicamos una tensión de 45 MPa tenemos = 45 cos 60 cos 35 = 18,43 Y no se deformaría. Para deformarse plásticamente debemos hacer un esfuerzo de 20,7 = cos 60 cos 35 = 50,54 7.13. Un monocristal de cadmio está orientado de tal manera que la normal al plano de deslizamiento forma un ángulo de con el eje de tracción. Tres posibles , direcciones de deslizamiento forman ángulos de , con el eje de tracción. ¿Cuál de estas tres direcciones está mejor orientada para el deslizamiento? Si la deformación plástica empieza a una tensión de 1,55 MPa, determinar la tensión de cizalladura resuelta crítica para el cinc Si calculamos los esfuerzos con cada uno de los ángulos propuestos tenemos que el valor es máximo en 30 . La tensión de cizalladura para esta situación es = 1,55 cos 65 cos 30 = 0,5673 7.14. Consideremos un monocristal de níquel orientado de tal manera que se aplica una tracción en la dirección [ en una dirección [ ]. Si el deslizamiento ocurre en un plano ( )y ], y comienza cuando la tensión aplicada es de 13,9 MPa, calcule la tensión de cizalladura resuelta crítica cos = (0,0,1)( 1,0,1) 2 = 2 2 cos = (0,0,1)(1,1,1) 3 = 3 3 Por tanto el factor de Schmid resulta cos cos = 6 6 La tensión de cizalladura será Xavi Paneque Linares Página 24 Grado en Ingeniería en Tecnologías Aeroespaciales 25 Ciencia de Materiales = 13,9 6 = 5,67 6 7.15. La tensión de cizalladura resuelta crítica del cobre es 0,48 MPa. Determinar el valor máximo del límite elástico para un monocristal de Cu estirado a tracción El valor máximo será = 2 = 2 · 0,48 = 0,96 7.21. El límite elástico inferior del hierro con un diámetro de grano de 230 MPa. Para un tamaño de grano de · es , el límite elástico aumenta hasta 275 MPa. ¿Para qué tamaño de grano el límite elástico inferior será de 310 MPa? En este caso usaremos la ecuación 230 = = + + 275 = + = 75,36 10 = 15,46 / 6 · 10 Por tanto 310 = 75,36 15,76 = 4,34 · 10 7.24. Demostrar que en un ensayo de tracción % = · + %CW es el % de deformación en frío. Considerar que no hay cambio en el volumen de la probeta durante el proceso de deformación. Usando el resultado de la parte anterior, calcular el porcentaje de trabajo en frío experimentado por el latón naval cuando se aplica una tensión de 415 MPa Xavi Paneque Linares Página 25 Grado en Ingeniería en Tecnologías Aeroespaciales 26 Ciencia de Materiales Tenemos por definición %= Por otro lado, si se conserva el volumen = = Sustituyendo resulta %= Si recordamos la definición de alargamiento = Podemos escribir la expresión como %= +1 Cuando aplicamos 415 MPa, el gráfico nos indica un alargamiento de 0,16. Sustituyendo en la ecuación resulta Xavi Paneque Linares Página 26 Grado en Ingeniería en Tecnologías Aeroespaciales 27 Ciencia de Materiales %= 0,16 · 100 = 13,8% 0,16 + 1 7.25. Dos probetas cilíndricas previamente no deformadas de una aleación son endurecidas por deformación reduciendo el área de la sección. Para una probeta, los radio iniciales y deformados son 15 mm y 12 mm, respectivamente. La segunda probeta, con un radio inicial de 11 mm, una vez deformada debe tener la misma dureza que la primera probeta; calcular el radio de la segunda probeta después de la deformación Dado que deben tener la misma dureza, el coeficiente de trabajo en frío debe ser el mismo. Así pues se cumple 15 12 15 = 11 = 8,8 11 7.26. Dos probetas previamente no deformadas del mismo metal son deformadas por reducción del área de sus secciones transversales. Una tiene una sección circular y la otra rectangular; durante la deformación las secciones de las dos probetas deben conservar su forma. Las dimensiones antes y después de la deformación son las siguientes. ¿Cuál de estas probetas tendrá mayor dureza después de la deformación plástica? ¿Por qué? Tendrá mayor dureza la segunda probeta. Se puede comprobar fácilmente calculando y comparando los coeficientes de trabajo en frío %= 18 15,9 = 21,97% 18 %= 20 · 50 13,7 · 55,1 = 24,5% 20 · 50 Como la segunda probeta tiene un mayor porcentaje de trabajo en frío, esta será más dura. Xavi Paneque Linares Página 27 Grado en Ingeniería en Tecnologías Aeroespaciales 28 Ciencia de Materiales Difusión 5.6. Calcular el número de kilogramos de hidrógeno que pasa en una hora a través de una lámina de Pd de , de área y 6 mm de espesor a coeficiente de difusión de , · . Suponer un / , que las concentraciones de hidrógeno en los lados de alta y baja presión son de 2,0 y 0,4 kg de hidrógeno por metro cúbico de paladio y que se ha alcanzado el estado estacionario. Según la ley de Fick tenemos d = d = = · · 1,7 · 10 = 4,53 · 10 · 0,4 2 = 4,53 · 10 0,006 · 3600 · 0,25 = 4,08 · 10 5.7. Una lámina de acero de 2,5 mm de espesor está dentro de una atmósfera de nitrógeno a y se ha alcanzado la condición del estado estacionario de la difusión. El coeficiente de difusión del nitrógeno en acero a esta temperatura es de , · / y el flujo de difusión es , · / . También se sabe que la concentración de nitrógeno en la cara del acero de mayor presión es de / . ¿A qué distancia de esta superficie, que está a elevada presión, es la concentración de , / = ? Suponer un perfil de concentración lineal. d = d 1,2 · 10 · 0 2 = 1,0 · 10 = 1,8 · 10 5.8. La cara de una lámina de hierro BCC de 2 mm de espesor se expuso a una atmósfera gaseosa carburante y la otra cara a una atmósfera descarburante a . Después de alcanzar la condición de estado estacionario, el hierro se enfrió a temperatura ambiente. Se determinaron las concentraciones de carbono en las dos caras y resultaron , Xavi Paneque Linares y , % en peso. Calcular el coeficiente de difusión si el Página 28 Grado en Ingeniería en Tecnologías Aeroespaciales 29 Ciencia de Materiales flujo de difusión es , · / . Convertir las concentraciones del porcentaje en peso a kilogramos de carbono por metro cúbico de hierro. En primer lugar encontremos la masa de un metro cúbico de hierro 1 · 7874 1 = 7874 = 0,00015 · 7874 = 1,18 ; = 0,535 Por tanto el coeficiente de difusión resulta = d = d · 0,535 1,18 = 7,36 · 10 0,002 = 2,28 · 10 5.12. Una aleación hierro-carbono FCC que inicialmente contenía , % C en peso está expuesta a una atmósfera rica en oxígeno y virtualmente libre de carbono a 1325 K ( ). En estas condiciones el carbono difunde desde el interior de la aleación y reacciona en la superficie con el oxígeno de la atmósfera, manteniendo la concentración del carbono a % en las posiciones superficiales. (Este proceso de eliminación de carbono se denomina descarburación). ¿A qué distancia de la superficie la concentración del carbono será de tratamiento? El valor de a 1325 K es , · , % después de 10 h de / Tenemos =1 Xavi Paneque Linares erf( ) 0,25 0,55 =1 0 0,55 erf( ) erf( ) = 0,4545 Página 29 Grado en Ingeniería en Tecnologías Aeroespaciales 30 Ciencia de Materiales = = 0,4278 2 = 2 4,3 · 10 · 10 · 3600 · 0,4278 = 1,06 5.11. Determinar el tiempo necesario para alcanzar una concentración de , % de C a 4 mm de la superficie de una aleación Fe-C que inicialmente contenía , % C. La , % concentración de la superficie se mantiene a . Usar los datos de difusión en y la probeta se calienta a de la tabla Tenemos =1 = 2 erf( ) = 0,814 0,3 0,9 = 0,1 =1 0,1 4 · 0,66 · erf( ) = 5.13. El nitrógeno difunde en hierro puro a erf( ) = 0,75 0,004 4 · 0,66 · 7 · 10 = 24,1 . Si la concentración superficial se mantiene en , % N en peso, ¿cuál será la concentración a 2 mm de la superficie después de 25h? El coeficiente de difusión del nitrógeno en hierro es , · a Tenemos erf 2 = erf =1 0,002 2 · 1,9 · 10 erf( ) 0,2 · 25 · 3600 0 =1 0 = erf 0,7647 = 0,7 0,7 = 0,06% 5.15. Mediante tratamiento térmico carburante aplicado durante 15 h se ha conseguido una concentración de carbono de , % a 2 mm de la superficie. Calcular el tiempo necesario para conseguir esta concentración a 6 mm de profundidad para el mismo acero y mismo tratamiento. Como las concentraciones son las mismas para las dos condiciones se debe cumplir Xavi Paneque Linares Página 30 Grado en Ingeniería en Tecnologías Aeroespaciales 31 Ciencia de Materiales erf = erf = 2 2 15 2 = 6 = 135 5.16. Calcular los valores del coeficiente de difusión para la interdifusión del carbono en hierro BCC y hierro FCC a . ¿Cuál es mayor? Justifícalo = Para el primer caso tenemos = 6,2 · 10 · , = 1,70 · 10 · Para el segundo caso tenemos = 1 · 10 · , = 8,78 · 10 · Porque la difusión intersticial es más rápida que la difusión por vacantes ya que los átomos intersticiales son más pequeños y tienen más movilidad y además hay más posiciones intersticiales vacías que vacantes. 5.18. Con los datos de la tabla ¿a qué temperatura el coeficiente del Zn en Cu vale , · / ? 2,6 · 10 = 3.4 · 10 , = 897,5 · . 5.20. La energía de activación para la difusión del cobre en plata es ( Calcular el coeficiente de difusión a ( ) es , · ), sabiendo que . a / = 10 / = , · , = 4,79 · 10 · 5.24. El carbono difunde a través de una lámina de acero de 10 mm de espesor. Las concentraciones de carbono en las dos caras son , y , / , que se mantienen constantes. Si el factor de frecuencia y la energía de actuación son Xavi Paneque Linares Página 31 Grado en Ingeniería en Tecnologías Aeroespaciales 32 Ciencia de Materiales , · / y . / , respectivamente, calcular la temperatura a la cual el flujo de difusión es , · / El flujo es d d = = 6,3 · 10 = · 1,4 · 10 0,40 0,85 0,01 = 1,4 · 10 = 6,2 · 10 = 900 , 5.26. ¿A qué temperatura aproximada la carburación superficial del hierro 4 h produce el mismo efecto que la carburación a durante durante 12h? 1392 Como han de producir los mismos efectos, tenemos que se cumple = Sustituyendo por la ecuación = Resulta = Xavi Paneque Linares 12 · , · =4 , · = 1392 Página 32 Grado en Ingeniería en Tecnologías Aeroespaciales 33 Ciencia de Materiales 4. Aleaciones metálicas. Diagramas de equilibrio de fases 9.5. Citar las fases presentes y sus composiciones en las siguientes aleaciones a) 15% Sn-85% Pb a 100 grados centígrados Fases + . Composición 12%, 95% en Pb b) 25% Pb-75% Mg a 425 grados centígrados Fase con composición del 25% en plomo c) 85% Ag-15% Cu a 800 grados centígrados Fases + con 95 y 78% en plata d) 55% Zn-45% Cu a 600 grados centígrados Fases + con 52% y 58 en zinc e) 1,25 Kg Sn y 14 kg Pb a 200 grados centígrados Calculemos el porcentaje = Fases 1,25 · 100 = 8,2% 1,25 + 14 = 14 · 100 = 91,2% 1,25 + 14 con 8,2% en Sn f) 13,447 Kg Cu y 65,50 Kg Zn a 600 grados centígrados Calculemos el porcentaje = 13,447 · 100 = 17% 13,447 + 65,50 Fases + con 81% y = 65,50 · 100 = 83% 13,447 + 65,50 90% en Zn g) 21,7 mol Mg y 35,4 mol Pb a 400 grados centígrados Pasamos de moles a quilogramos Xavi Paneque Linares Página 33 Grado en Ingeniería en Tecnologías Aeroespaciales 34 Ciencia de Materiales 21,7 · 24,3 1 = 527,31 35,4 · 207,198 1 = 7334,53 Y por tanto = 527,31 · 100 = 6,7% 527,31 + 7334,53 Fases + = 94% y con 7334,53 · 100 = 93,3% 527,31 + 7334,53 81% en Pb h) 4,2 mol Cu y 1,1 mol Ag a 900 grados centígrados Pasamos de moles a quilogramos 4,2 · 63,54 1 = 266,87 1,1 · 107,87 1 = 118,657 Y por tanto = Fases 266,87 · 100 = 69,2% 266,87 + 118,657 + con 55% y = 118,657 · 100 = 30,8% 266,87 + 118,657 9% en Ag 9.6. ¿Qué fases y qué fracciones de masas aparecen al enfriar una aleación % – % Xavi Paneque Linares a los , , , y ? Página 34 Grado en Ingeniería en Tecnologías Aeroespaciales 35 Ciencia de Materiales A 1000 C tenemos estado líquido totalmente A 800 C tenemos fase totalmente A 500 C tenemos coexistencia de fase y . Por la regla de la palanca inversa tenemos, aproximadamente = A 300 = 58 58 52 = 75% 50 tenemos coexistencia entre = = 52 58 50 = 25% 50 y . Por la regla de la palanca inversa tenemos, aproximadamente = A 200 = 59 59 52 = 77,8% 50 tenemos coexistencia entre = = 52 59 50 = 22,2% 50 y . Por la regla de la palanca inversa tenemos, aproximadamente = = 59 59 52 = 87,5% 51 = = 52 59 51 = 12,5% 51 9.7. Determinar las cantidades relativas (fracciones de masa) de las fases presentes en las aleaciones y temperaturas del problema 9.5. a) 15% Sn-85% Pb a 100 grados centígrados Xavi Paneque Linares Página 35 Grado en Ingeniería en Tecnologías Aeroespaciales 36 Ciencia de Materiales Fases + . = · 100 = 95 95 85 · 100 = 12,05% 12 = · 100 = 85 95 12 · 100 = 87,95% 12 b) 25% Pb-75% Mg a 425 grados centígrados Fase en su totalidad c) 85% Ag-15% Cu a 800 grados centígrados Fases + con = · 100 = = 88 95 · 100 = 85 · 100 = 30% 85 85 95 78 · 100 = 70 85 d) 55% Zn-45% Cu a 600 grados centígrados Fases + con = · 100 = 50% = 50% e) 1,25 Kg Sn y 14 kg Pb a 200 grados centígrados Totalidad en de fase f) 13,447 Kg Cu y 65,50 Kg Zn a 600 grados centígrados Fases + con = · 100 = 90 90 83 · 100 = 77,78% 81 = 22,22% g) 21,7 mol Mg y 35,4 mol Pb a 400 grados centígrados Xavi Paneque Linares Página 36 Grado en Ingeniería en Tecnologías Aeroespaciales 37 Ciencia de Materiales Fases + con = · 100 = 93,3 81 · 100 = 94,6% 94 81 = 5,4% h) 4,2 mol Cu y 1,1 mol Ag a 900 grados centígrados Fases + con = · 100 = 55 308 · 100 = 52,6% 55 9 9.8. La figura adjunta es una parte del diagrama de fases = 47,4% . a. Con la ayuda de este diagrama explicar brevemente por qué se añade sal al hielo a temperatura inferior a Xavi Paneque Linares para fundirlo. Página 37 Grado en Ingeniería en Tecnologías Aeroespaciales 38 Ciencia de Materiales Se puede observar en el diagrama que la línea liquidus marca temperaturas más bajas como mayor es la proporción de sal hasta un mínimo de 20 en una proporción del 23% de sal aproximadamente. Así pues, la sal se añade para modificar la composición del agua con el objetivo de evitar que se forme hielo. b. ¿Qué concentración de sal se necesita para tener un disolución salina a una temperatura de % hielo y un % de ? Aplicando la ley de la palanca tenemos = = 19 19 0 = 0,75 = 4,75% 9.11. Una muestra de 7,5 Kg de una aleación magnesio-plomo consiste en una fase de disolución sólida que tiene la composición algo inferior al límite de solubilidad a a) ¿Cuál es la masa de plomo de la aleación? 7,5 · 0,16 = 1,2 b) Al calentar la aleación a fase , ¿Cuánto más plomo se podrá disolver en la sin exceder el límite de solubilidad? 7,5 · 0,32 = 2,4 = 2,4 1,2 = 1,2 9.12. Describir brevemente la segregación. Citar una consecuencia negativa de la segregación. Una importante consecuencia de la solidificación fuera del equilibrio para aleaciones isomorfas es una distribución no uniforme de los dos elementos dentro de los cristales denominada segregación. La región central de cada grano es la primera que ha solidificado y es rica en el elemento de alta temperatura de fusión, mientras que la concentración del elemento de baja temperatura de fusión va aumentando desde el Xavi Paneque Linares Página 38 Grado en Ingeniería en Tecnologías Aeroespaciales 39 Ciencia de Materiales centro al límite del grano. La siguiente imagen representa esquemáticamente este gradiente de concentración Esta estructura da lugar a propiedades inferiores a las óptimas. Si las muestras moldeadas, que tienen una microestructura segregada, se vuelven a calentar, la región del límite de grano funde en primer lugar, ya que es más rica en el elemento de temperatura de fusión menor. Esto suele producir una drástica pérdida de la integridad mecánica debido a la delgada película líquida que separa los granos. Además, esta fusión puede iniciarse a temperatura inferior a la temperatura de equilibrio solidus de la aleación. La segregación se puede eliminar por el tratamiento térmico de homogeneización, que se realiza calentando la aleación de composición conocida a una temperatura inferior al punto solidus. Durante este proceso, la difusión atómica genera granos de composición homogénea. 9.13. Se intenta fabricar una aleación cobre-níquel con una resistencia a la tracción mínima de 380 MPa y una ductilidad de % EI. ¿Es posible? En caso afirmativo, ¿cuál debe ser la composición? En caso negativo, ¿por qué? Xavi Paneque Linares Página 39 Grado en Ingeniería en Tecnologías Aeroespaciales 40 Ciencia de Materiales 9.14. En una aleación cobre-níquel, ¿es posible tener en equilibrio una fase líquida de composición 80% Cu – 20% Ni y fase 37% Ni – 80% Cu? En caso afirmativo, ¿a qué temperatura? En caso negativo, ¿por qué? La situación descrita es imposible dado que si tenemos una fase en equilibrio del 20% en níquel líquido, el máximo porcentaje de níquel del sólido será de aproximadamente 30%, nunca llegará al 37%. Por el mismo razonamiento, una fase del sólido con concentración 37% tendrá un líquido con un mínimo de níquel del 25% aproximadamente. Xavi Paneque Linares Página 40 Grado en Ingeniería en Tecnologías Aeroespaciales 41 Ciencia de Materiales 9.15. En una aleación cobre-plata, ¿es posible tener en equilibrio una fase 95% Cu) y una fase (5% Ag- 95% Ag – 5% Cu? En caso afirmativo, ¿a qué temperatura? En caso negativo ¿por qué? Sí es posible a una temperatura de 625 9.16. Una aleación plomo-estaño de composición 30% Sn – 70% Pb se calienta lentamente a partir de los a. ¿A qué temperatura empieza a formarse líquido? El líquido empezará a formarse a partir de la línea eutéctica, es decir, a partir de los 183 C. b. ¿Cuál es la composición de esta fase? Xavi Paneque Linares Página 41 Grado en Ingeniería en Tecnologías Aeroespaciales 42 Ciencia de Materiales 80,7% En esta fase tenemos una composición de19,3% 61,9% 38,1% en y un en líquido. c. ¿A qué temperatura funde completamente la aleación? Si seguimos la línea discontinua, vemos que corta con la línea liquidus cuando nos encontramos a una temperatura de 260 C aproximadamente. d. ¿Cuál es la composición de la última parte sólida antes de que se complete la fusión? Si trazamos una recta horizontal en el punto de corte de la línea liquidus, cortaremos la línea solidus. Observando la escala de composición para este punto obtenemos una composición del 13% de 9.20. Una aleación aproximadamente. % % se calienta a una temperatura comprendida + . Si la fracción de cada fase es 0,5 calcular la temperatura de la en la región aleación y las composiciones de las dos fases. Midiendo sobre el papel da una temperatura aproximada de 550 de cada fase serían 30% 50% y . La composición . 9.21. En las aleaciones de dos hipotéticos metales A y B, existen una fase y una fase rica en A rica en B. A partir de las fracciones de masas de dos aleaciones, que están a la misma temperatura, determinar la composición de los límites de fase (o límite de solubilidad) de las fases Composición de la aleación y a esta temperatura Fracción de fase Fracción de fase % % 0,78 0,22 % % 0,36 0,64 Aplicando la regla de la palanca inversa tenemos el siguiente sistema de ecuaciones = Xavi Paneque Linares = 30 = 0,22 = = 65 = 0,64 Página 42 Grado en Ingeniería en Tecnologías Aeroespaciales 43 Ciencia de Materiales La solución del cual es = 11,67% = 95% 9.23. ¿Es posible tener una aleación cobre-plata de composición 20% Ag-80% Cu que, en el equilibrio, consta de fase y = , y de líquido con las fracciones de masa = , ? En caso afirmativo, ¿cuál es la temperatura aproximada de esta aleación? En caso negativo explicar la causa. Debemos aplicar la regla de la palanca inversa y debe existir una combinación que cumpla = = 20 = 0,80 En el caso extremo tenemos = Xavi Paneque Linares 71,9 20 = 0,825 > 0,8 71,9 9 Página 43 Grado en Ingeniería en Tecnologías Aeroespaciales 44 Ciencia de Materiales Por tanto sí existe esa posibilidad en algún punto intermedio y corresponde a una temperatura aproximada (a ojo) de poco más de 800 C 9.28. ¿Es posible conseguir, a de masa primaria y , una aleación magnesio-plomo cuyas fracciones total sean , y , respectivamente? Justificar la respuesta Si tenemos 0,6 de primario la concentración será %= = 68 68 42 = 0,6 = 52,4% A esta concentración tenemos = 80 52,4 = 72,6% < 85% 80 42 Por tanto no es posible 9.30. Dada una aleación estaño-plomo que contiene 80% Sn y 20% Pb a determinar las fracciones de masas de a. Las fases y Xavi Paneque Linares Página 44 Grado en Ingeniería en Tecnologías Aeroespaciales 45 Ciencia de Materiales Considerando que el punto está sobre la línea eutéctica, tenemos que las fracciones de masa por la regla de la palanca son = = 97,8 80 = 22,4% 97,8 18,3 b. Los microconstituyentes Los microconstituyentes = c. El = = = 80 18,3 = 77,6% 97,8 18,3 primario y eutéctico primario y eutéctico vienen dados respectivamente por 80 61,9 = 50,4% 97,8 61,9 = = 97,8 80 = 49,6% 97,8 61,9 eutéctico El porcentaje de eutéctico es = = 77,6 50,4 = 27,6% 9.31. La microestructura de una aleación cobre plata a consta de primaria y eutéctico. Determinar la composición de la aleación sabiendo que las fracciones de masas de estos dos microconstituyentes son , %= Xavi Paneque Linares = 71,9 71,9 7,9 y , = 0,73 , repespectivamente. = 25,18% Página 45 Grado en Ingeniería en Tecnologías Aeroespaciales 46 Ciencia de Materiales 9.34. Esquematizar las microestructuras, indicando la composición aproximada, obtenidas al enfriar lentamente una aleación 85% Pb-15% Mg a las siguientes temperaturas: Para 600 Para 500 , , y tenemos líquido totalmente. tenemos una mezcla de compuesto más líquido de proporción respectivamente = Xavi Paneque Linares = 88 88 85 = 37,5% 80 = = 85 88 80 = 62,5% 80 Página 46 Grado en Ingeniería en Tecnologías Aeroespaciales 47 Ciencia de Materiales Para 270 nos encontramos en la isoterma eutéctica con proporciones = Para 200 = 96 96 85 = 68,8% 80 = tenemos una mezcla de compuesto = 85 96 80 = 31,3% 80 más de proporción = 85 80 = 25% 100 80 respectivamente = Xavi Paneque Linares = 100 100 85 = 75% 80 = Página 47 Grado en Ingeniería en Tecnologías Aeroespaciales 48 Ciencia de Materiales 5. Aleaciones metálicas. El sistema Fe-C 9.47. ¿Cuál es el porcentaje de carbono de un acero al carbono si la fracción de cementita es de , ? 6,7 0,022 = 0,1 0,022 = 0,69% 9.48. ¿Cuál es la fase proeuctectoide de un acero al carbono cuyas fracciones másicas de ferrita y de cementita son 0,86 y 0,14 respectivamente? ¿Por qué? 6,7 0,022 = 0,14 0,022 = 0,957% > 0,76% 9.49. Enfriar hasta temperaturas inferiores a Cementita 3,5 kg de austenita con 0,95% C a) ¿Cuál es la fase proeuctectoide? 0,95% > 0,76% Cementita b) ¿Cuántos kilogramos de ferrita y de fase proeuctectoide se forman? Xavi Paneque Linares Página 48 Grado en Ingeniería en Tecnologías Aeroespaciales 49 Ciencia de Materiales 6,7 0,95 = 0,861 6,7 0,022 = 3,5 = 3,5 · 0,861 = 3,01 3,01 = 0,49 c) ¿Cuántos kilogramos de perlita y de fase proeuctectoide se forman? = 0,95 0,76 = 0,032 6,7 0,76 = 3,5 = 0,032 · 3,5 = 0,112 0,112 = 3,388 d) Esquematizar y designar la microestructura resultante 9.50. Enfriar hasta temperaturas inferiores a 6 kg de austenita con 0,45% C. a) ¿Cuál es la fase proeuctectoide? Xavi Paneque Linares Página 49 Grado en Ingeniería en Tecnologías Aeroespaciales 50 Ciencia de Materiales La fase , ferrita b) ¿Cuántos kilogramos de ferrita y de fase proeuctectoide se forman? = 6,7 6,7 0,45 = 0,936 0,02 =6 = 0,936 · 6 = 5,62 5,62 = 0,384 c) ¿Cuántos kilogramos de perlita y de fase proeuctectoide se forman? = 0,45 0,77 0,022 = 0,572 0,022 =6 = 0,572 · 6 = 3,43 3,43 = 2,57 d) Esquematizar y designar la microestructura resultante Xavi Paneque Linares Página 50 Grado en Ingeniería en Tecnologías Aeroespaciales 51 Ciencia de Materiales 9.51. Calcular las fracciones másicas de perlita y de ferrita proeuctectoide que se generan en un acero al carbono con 0,35% C = 0,77 0,35 = 0,56 0,77 0,022 =1 0,56 = 0,44 9.52. La microestructura de un acero al carbono consta de perlita y de ferrita proeuctectoide; las fracciones másicas de estos dos constituyentes son 0,174 y 0,826 respectivamente. Determinar la concentración de carbono de esta aleación. = 0,77 = 0,826 0,77 0,022 = 0,152% 9.53. Las fracciones másicas de la ferrita y de la cementita de un acero al carbono son 0,91 y 0,09 respectivamente. Justificar si se trata de un acero hipo o hipereutectoide = 6,7 = 0,91 6,7 0,022 = 0,623% < 0,77 Hipoeutectoide 9.54. La microestructura de un acero al carbono consta de cementita proeuctectoide y de perlita; las fracciones de masa de estos constituyentes son 0,11 y 0,89 respectivamente. Determinar el porcentaje de carbono del acero. = 6,7 0,77 = 0,11 0,77 = 1,42% 9.55. Considerar 1,5 Kg de acero al carbono con 0,3% C enfriados hasta temperatura justamente inferior al eutectoide a) ¿Cuántos kilogramos de ferrita proeutectoide se forman? = 0,77 0,3 = 0,628 0,77 0,022 = 0,628 · 1,5 = 0,94 b) ¿Cuántos kilogramos de ferrita eutectoide se forman? = = Xavi Paneque Linares 6,7 0,3 = 0,958 6,7 0,022 Página 51 Grado en Ingeniería en Tecnologías Aeroespaciales 52 Ciencia de Materiales = 0,958 0,628 = 0,33 = 0,33 · 1,5 = 0,495 c) ¿Cuántos kilogramos de cementita se forman? =1 =1 0,958 = 0,042 = 0,042 · 1,5 = 0,062 9.57. ¿Existe un acero con fracción másica de cementita y de ferrita proeuctectoide de 0,057 y 0,36 respectivamente? ¿Por qué o por qué no? 0,77 = 0,36 0,77 0,022 = = 0,5 6,7 0,022 = 0,072 0,022 = 0,5 0,057 No existe 9.58. ¿Existe un acero con fracción másica de ferrita y de perlita de 0,086 y 0,0969 respectivamente? ¿Por qué o por qué no? = 6,7 = 0,086 6,7 0,022 = 6,7 6,126 = 0,0969 6,7 0,77 = 6,126 Sí existe 9.60. La fracción másica de cementita eutectoide en un acero es 0,109. ¿Es posible determinar, con este dato, la composición del acero? ¿Cuál es? Si no es posible, justifícalo Hay dos posibilidades según nos encontremos en el hipoeutéctico o en el hipereutéctico. Para el primer caso, situado en la fase hipereutéctica = = 6,7 0,022 0,022 6,7 0,77 = 0,109 0,77 = 0,93% Si en cambio estamos en la zona hipoeutéctica = Xavi Paneque Linares = 6,7 0,022 = 0,109 0,022 = 0,75% Página 52 Grado en Ingeniería en Tecnologías Aeroespaciales 53 Ciencia de Materiales 9.61. La fracción másica de ferrita eutectoide en un acero es 0,71. ¿Es posible determinar, con este dato, la composición del acero? ¿Cuál es? Si no es posible, justificarlo Hay dos posibilidades según nos encontremos en el hipoeutéctico o en el hipereutéctico. Para el primer caso, situado en la fase hipoeutéctica = = 6,7 6,7 0,022 0,77 = 0,71 0,77 0,022 = 0,62% Si en cambio estamos en la zona hipereutéctica = = 6,7 = 0,71 6,7 0,022 = 1,96% 9.63. Generalmente las propiedades de las aleaciones multifásicas se pueden relacionar según una ley de mezclas ( ó )= + Donde E representa una propiedad específica (módulo elástico, dureza, etc) y V es la fracción de volumen. Los subíndices y denotan la existencia de fases o microconstituyentes. Utilizar la relación anterior para determinar la dureza Brinell aproximada de un acero al carbono con 0,25% C. Suponer que las durezas Brinell de la ferrita aproximada de un acero al carbono con 0,25% C. Suponer que las durezas Brinell de la ferrita y de la perlita son 80 y 280, respectivamente, y que las fracciones volumétricas se aproximan a las fracciones másicas. Qué representa y cómo se determina la dureza Brinell? Dado que estamos en la zona hipoeutectoide = 0,77 0,25 = 0,695 0,77 0,022 =1 0,695 = 0,305 Por tanto la dureza de la aleación es Xavi Paneque Linares Página 53 Grado en Ingeniería en Tecnologías Aeroespaciales 54 Ciencia de Materiales = 0,695 · 80 + 0,305 · 280 = 140,96 LA dureza Brinell se determina mediante un penetrador duro esférico el cual se fuerza en la superficie del metal a ensayar. Los materiales más duros requieren cargas mayores y por tanto el numero de dureza Brinell, HB, es una función de tanto la magnitud de la carga como del diámetro de la huella resultante. El diámetro se convierte a un número HB mediante una tabla. Así pues, representa un valor tabulado que resulta útil para comparar durezas con otros materiales. 9.65. Un acero contiene 95,7% Fe, 4% W y 0,3% C. ¿Cuál es la temperatura eutectoide de esta aleación? ¿Cuál es la composición del eutectoide? ¿Cuál es la fase proeuctectoide? Suponer que no se producen cambios en las posiciones de otros límites de fase con la adición del W. Temperatura eutectoide 9.66. Un acero contiene = 900 , . Composición = 0,21%. Cementita % Fe, 6% Mn y 0,35% C. ¿Cuál es la temperatura eutectoide aproximada de esta aleación? ¿Cuál es la fase proeuctectoide cuando esta aleación se enfría justo por debajo del eutectoide? Calcular las cantidades relativas de fase proeuctectoide y de perlita. Suponer que no se producen cambios en las posiciones de otros límites de fase con la adición de Mn Temperatura eutectoide = = 680 . Composición 0,45 0,35 = 0,234 0,45 0,022 Xavi Paneque Linares = = 0,45%. Ferrita 0,35 0,45 0,022 = 0,766 0,022 Página 54 Grado en Ingeniería en Tecnologías Aeroespaciales 55 Ciencia de Materiales 10.2. Algunas transformaciones tienen una cinética que obedece a la ecuación de Avrami. Si el valor del parámetro es 1,5 después de 125 s la reacción alcanza un 25% de transformación, ¿Cuánto tiempo se necesita para llegar al 90% de transformación? La ecuación de Avrami es =1 , · 0,25 = 1 = 2,06 · 10 / Por tanto, para llegar al 90% , 0,9 = 1 · , · = 500 10.3. La velocidad de una transformación a menudo se expresa como el tiempo necesario para completar el 50% de la misma. Calcular la velocidad de una reacción que cumple la ley cinética de Avrami, suponiendo que las constantes y · y valen , , respectivamente, para el tiempo en segundos. · 0,5 = 1 = 37,233 = 1 = 1 = 0,027 37,233 10.4. Se sabe que la cinética de la recristalización de algunas aleaciones cumple la ecuación de Avrami y que el valor de en el exponencial es 5,0. Si a una temperatura la fracción recristalizada es 0,30 después de 100 min, determinar la velocidad de recristalización a esta temperatura. 0,3 = 1 0,5 = 1 , · · = 3,57 · 10 = 114,21 = 1 min = 1 = 8,76 · 10 114,21 10.5. La cinética de la transformación austenita-perlita cumple la reacción de Avrami. Utilizando los datos adjuntos de fracción transformada-tiempo, determinar el tiempo necesario para que el 95% de la austenita se transforme en perlita. Xavi Paneque Linares Fracción transformada Tiempo (s) 0,2 280 Página 55 Grado en Ingeniería en Tecnologías Aeroespaciales 56 Ciencia de Materiales 0,6 0,2 = 1 0,6 = 1 · · Xavi Paneque Linares = 3,385 = 1,162 · 10 425 0,95 = 1 , · , = 603 Página 56 Grado en Ingeniería en Tecnologías Aeroespaciales 57 Ciencia de Materiales 6. Polímeros 15.1. Diferencia polimorfismo de isomería Polimorfismo cualidad por la cual un determinado material puede cristalizar con dos o más estructuras cristalográficas. Es la cualidad por la que moléculas con igual composición química pueden tener diferente configuración atómica. Por tanto tienen misma constitución química, misma formula empírica pero distinta formula estereoquímica. 15.2. Esquematice las unidades monoméricas de los siguientes polímeros: policloruro de vinilo, polimetacrilato de metilo, nylon 66, policarbonato de bisfenol A a) Policloruro de vinilo b) Polimetacrilato de metilo c) Nylon 66 d) Policarbonato de bisfenol A Xavi Paneque Linares Página 57 Grado en Ingeniería en Tecnologías Aeroespaciales 58 Ciencia de Materiales 15.4. El peso molecular medio numérico del poliestireno es 500 000 g/mol. Calcule el del grado de polimerización medio numérico. El poliestireno tiene la estructura Donde la estructura del benceno es Y uno de los hidrógenos es sustituido por la estructura del poliestireno. Por tanto el peso molecular de cada unidad monomérica es 12 · 8 + 1 · 8 = 104 Y el grado de polimerización será = Xavi Paneque Linares 500000 = 4808 104 Página 58 Grado en Ingeniería en Tecnologías Aeroespaciales 59 Ciencia de Materiales 15.5. Calcule el peso molecular de la unidad monomérica del polipropileno. Calcule el peso molecular medio másico de un polipropileno cuyo grado de polimerización medio másico es 15 000. El polipropileno tiene la siguiente estructura Así pues el peso molecular de la unidad monomérica es 1 · 6 + 12 · 3 = 42 El peso molecular másico será, dado que todos las unidades monoméricas son iguales 0 = 42 · 15 000 = 631 000 15.6. Se han tabulado los pesos moleculares de un politetrafluoroetileno. Calcule el peso molecular medio numérico, el peso molecular medio másico, el grado de polimerización medio numérico y el grado de polimerización medio másico Intervalo de peso molecular (g/mol) 10 000 – 20 000 0,03 0,01 20 000 – 30 000 0,09 0,04 30 000 - 40 000 0,15 0,11 40 000 - 50 000 0,25 0,23 50 000 - 60 000 0,22 0,24 60 000 - 70 000 0,14 0,18 70 000 - 80 000 0,08 0,12 80 000 - 90 000 0,04 0,07 El peso molecular medio numérico viene dado por Xavi Paneque Linares Página 59 Grado en Ingeniería en Tecnologías Aeroespaciales 60 Ciencia de Materiales = = 15 000 · 0,03 + 25 000 · 0,09 + + 85 000 · 0,04 = 49 800 El peso molecular medio másico viene dado por = = 15 000 · 0,01 + 25 000 · 0,04 + + 85 000 · 0,07 = 55 200 El grado de polimerización medio numérico = = 49 800 = 498 100 El grado de polimerización medio másico = = 55 200 = 552 100 15.7. Se han tabulado los pesos moleculares de algunos polímeros. Intervalo de peso molecular (g/mol) 8 000 – 20 000 0,05 0,02 20 000 – 32 000 0,15 0,08 32 000 - 44 000 0,21 0,17 44 000 - 56 000 0,28 0,29 56 000 - 68 000 0,18 0,23 68 000 - 80 000 0,10 0,16 80 000 - 92 000 0,03 0,05 Calcule a) el peso molecular medio numérico = = 14 000 · 0,05 + 26 000 · 0,15 + + 86 000 · 0,03 = 47 720 b) el peso molecular medio másico = = 14 000 · 0,02 + 26 000 · 0,08 + Xavi Paneque Linares + 86 000 · 0,05 = 53 720 Página 60 Grado en Ingeniería en Tecnologías Aeroespaciales 61 Ciencia de Materiales c) si se sabe que el grado de polimerización medio numérico de este material es de 211, ¿a qué polímero de la tabla corresponde? ¿Por qué? = = 226,16 Tereftalato de polietileno (PET) d) ¿Cuál es el grado de polimerización medio másico de este material? = = 53 720 = 238 226,16 15.9. El polietileno de alta densidad se puede clorar induciendo la substitución aleatoria de átomos de hidrógeno por átomos de cloro. a) Determine la concentración de Cl (en % en peso) que se debe añadir para que la substitución alcance el 8% de los átomos de hidrógeno originales. La estructura del polietileno es Siguiendo la proporción tenemos que 8 de cada 100 H se substituyen por Cl. Y cada 100 de H tenemos 50 de C. Así pues % = 35,5 · 8 · 100 = 29% 35,5 · 8 + 92 · 1 + 12 · 50 b) ¿En qué difiere la cloración del polietileno de la del policloruro de vinilo? Para el PVC, tenemos un 25% de cloro ya substituido y por lo tanto la sustitución será menos al azar. 15.10. Explique la diferencia entre configuración y conformación de cadenas poliméricas Xavi Paneque Linares Página 61 Grado en Ingeniería en Tecnologías Aeroespaciales 62 Ciencia de Materiales La configuración de cadenas poliméricas hace referencia a la regularidad y la simetría de la disposición de los átomos en la cadena, la cual no cambia por simple rotación de los enlaces. En cambio la conformación es usada para hacer referencia a la forma o posición que adopta la molécula a través de rotación de sus enlaces. 15.11. La longitud total L de una molécula polimérica lineal depende de la longitud del enlace entre átomos de la cadena, del número total de enlaces en la molécula y del ángulo entre átomos de la cadena. Es decir: = Además, la distancia media cabeza-cola de una serie de moléculas poliméricas es igual a = Un polietileno lineal tiene un peso molecular medio numérico de calcule los valores medios / ; y para este material La masa molar de una unidad monomérica de polietileno es = 28 Por tanto el grado de polimerización numérico es = 300000 = 10 715 28 Así pues el número de enlaces será, dado que hay dos en cada unidad monomérica = 10 715 · 2 = 21 430 Para enlaces simples de carbono resulta Xavi Paneque Linares Página 62 Grado en Ingeniería en Tecnologías Aeroespaciales 63 Ciencia de Materiales = 0,154 = 109 Y por tanto = 21 430 · 0,154 · 10 = · sin 109 = 2686,76 2 = 22,54 15.12. Usando las definiciones de longitud total de la cadena molecular y de distancia media cabeza cola determinar, para el politetrafluoroetileno: a) el peso molecular medio numérico para = sin 2000 = 2 = · 0,154 · sin 109 2 = 15 900 Dado que hay dos enlaces por unidad monomérica, entonces tenemos unidades monoméricas 2 = 7950 Y por tanto el peso molecular medio numérico será = 2 · = 7950 · 100 = 795 000 b) el peso molecular medio numérico para = Dada tenemos = 15 = 0,154 · = 9488 Y el peso molecular medio numérico será = 2 · = 9488 · 100 = 474 400 2 15.13. Esquematice las porciones de una molécula lineal de polipropileno a) sindiotáctico Xavi Paneque Linares Página 63 Grado en Ingeniería en Tecnologías Aeroespaciales 64 Ciencia de Materiales b) atáctico c) isotáctico 15.14. Esquematice las estructuras de la unidad monomérica cis y trans para a) el butadieno b) el cloropreno 15.15. Esquematice la estructura de la unidad monomérica de cada uno de los siguientes copolímeros alternados a) poli (etileno-propileno) Xavi Paneque Linares Página 64 Grado en Ingeniería en Tecnologías Aeroespaciales 65 Ciencia de Materiales b) poli (butadieno-estireno) c) poli (isobutileno-isopreno) 15.16. El peso molecular medio numérico del copolímero alternado poli(acrilonitrilobutadieno) es . . / . Determine el número medio de unidades monoméricas de acrilonitrilo y de butadieno por molécula El acrilonitrilo y el butadieno tienen la estructura, respectivamente La masa molar total es = 107 Y por tanto el número medio de unidades monoméricas es = = 9346 15.17. Calcule el peso molecular medio numérico de un copolímero al azar de poli)isobutilenoisopreno) cuya fracción de unidades monoméricas del isobutileno es , . Suponga que esta concentración corresponde a un grado de polimerización medio numérico de 1500 Xavi Paneque Linares Página 65 Grado en Ingeniería en Tecnologías Aeroespaciales 66 Ciencia de Materiales El isobutileno y el isoporeno son Sus respectiva masas molares son = 56 = 68 Por tanto el peso molecular medio es = 56 · 1500 · 0,25 + 68 · 1500 · 0,75 = 97 500 15.18. Se sabe que un copolímero alternado tiene un peso molecular medio numérico de 100.000 g/mol y un grado de polimerización medio numérico de 2210. Si una unidad monomérica es el etileno, ¿cuál es la otra unidad monomérica: estireno, propileno, tetrafluoretileno o cloruro de vinilo? ¿Por qué? La masa molar será = = 100000 = 45,25 2210 Restando la del etileno = 45,25 0,5 · 28 = 62,45 0,5 El monómero que corresponde a esa masa molar es el cloruro de vinilo. 15.21. Un copolímero al azar de poli(estireno-butadieno) tiene un peso molecular medio másico de 350 000 g/mol y un grado de polimerización medio másico de 5000. Calcule las fracciones de unidades monoméricas de estireno y de butadieno en este copolímero. El estireno y el butadieno tienen una estructura Xavi Paneque Linares Página 66 Grado en Ingeniería en Tecnologías Aeroespaciales 67 Ciencia de Materiales La ecuación que se debe cumplir es = + (1 ) 350 000 = 5000 · 104 · = 0,32 + 5000 · 54 · (1 = 0,68 15.25. Calcule la densidad del polietileno totalmente cristalino. En la figura se muestra la celdilla unidad ortorrómbica del polietileno; cada celdilla unidad contiene el equivalente a dos unidades monoméricas del etileno. En dos unidades monoméricas tenemos = 28 El volumen de la celdilla es = 0,741 · 0,494 · 0,255 = 9,33 · 10 Xavi Paneque Linares Página 67 ) Grado en Ingeniería en Tecnologías Aeroespaciales 68 Ciencia de Materiales La densidad teórica es · = = · 0,028 · 2 9,33 · 10 · 6,022 · 10 = 996,24 15.26. La densidad del nylon 66 totalmente cristalino a temperatura ambiente es de 1,213 / . Además, a temperatura ambiente la celdilla unidad de este material es triclínica con los siguientes parámetros de red: = , = , = , = , = Si el volumen de una celdilla triclínica , = , es función de los parámetros de red = + Determine el número de unidades monoméricas asociado a cada celdilla unidad El volumen de la celdilla según la expresión es = 0,31 = 3,1 · 10 La densidad viene dada por = · · 1213 = 0,226 · 3,1 · 10 · 6,022 · 10 =1 15.27. La densidad y el porcentaje de cristalinidad asociado a dos materiales de polietileno son los siguientes a) Calcule las densidades del polietileno totalmente cristalino y totalmente amorfo Aplicando la ecuación Xavi Paneque Linares Página 68 Grado en Ingeniería en Tecnologías Aeroespaciales 69 Ciencia de Materiales % = ( ( ) ) (0,965 0,965( (0,925 0,464 = 0,925( 0,768 = ) ) ) ) = 0,87 = 0,98 b) Determine el porcentaje de cristalinidad de una muestra que tiene una densidad de , / %= Xavi Paneque Linares 0,98(0,95 0,95(0,98 0,87) = 75% 0,87) Página 69 Grado en Ingeniería en Tecnologías Aeroespaciales 70 Ciencia de Materiales 7. Cerámicas 13.3. Demostrar que el cociente mínimo entre los radios del catión y del anión es , en el caso de coordinación 4. La estructura en el caso de coordinación 4 es Xavi Paneque Linares Página 70 Grado en Ingeniería en Tecnologías Aeroespaciales 71 Ciencia de Materiales Por la geometría, el ángulo formado por el centro del catión unido a los centros de los aniones es de 109 (2 ) = 2( + ) (1 2 cos 109) +4 4 1=0 4 =2· ( 3 = + +2 ) 6 2 = 0,225 2 13.4. Demostrar que el cociente mínimo entre los radio del catión y del anión es , en el caso de coordinación 6. Sugerencia: Utilizar la estructura cristalina del NaCl, y suponer que los aniones y cationes se tocan a lo largo de las aristas y las diagonales de las caras ( + ) · 2 = (2 ) 2 2 = + = 2 1 = 0,414 13.5. Demostrar que el cociente mínimo entre los radio del catión y del anión es , en el caso de coordinación 8 Xavi Paneque Linares Página 71 Grado en Ingeniería en Tecnologías Aeroespaciales 72 Ciencia de Materiales = (2 ) + (2 ) = 8 + (2 ) = = (2 +2 ) 2 =2 2 2 +4 = (2 +2 ) Manipulando adecuadamente se llega a = 3 1 = 0,732 13.6. Basándose en la carga y el radio de los iones, indique las estructuras cristalinas de los siguientes materiales , , , . Justifique sus respuestas El óxido de calcio tiene una estructura parecida a la del cloruro sódico dado que el número de cationes y aniones es el mismo y corresponde a la forma . Su relación de radio es = 0,1 = 0,7143 0,14 º =6 El sulfuro de manganeso (II) tiene una estructura de sulfuro de zinc dado que = 0,067 = 0,3641 0,184 º =4 El bromuro de potasio tiene una estructura propia del cloruro sódico dado que = 0,138 = 0,7041 0,196 º =6 El bromuro de calcio tiene una estructura Xavi Paneque Linares Página 72 Grado en Ingeniería en Tecnologías Aeroespaciales 73 Ciencia de Materiales = 0,100 = 0,5102 0,196 º =6 13.7. ¿Cuál de los cationes de la tabla podría formar fluoruros con la estructura cristalina del cloruro de cesio? Justifique su respuesta Para tener la estructura cristalina como la del cloruro de cesio debemos tener un número de coordinación de 8. Así pues la relación de radios se debe encontrar entre 0,732 < <1 El radio del flúor es = 0,133 0,097356 < < 0,133 En este rango encontramos , Dado que el único catión con una sola carga positiva es el sodio, la respuesta es . 13.8. Calcule los factores de empaquetamiento atómico para la estructura cristalina = , del cloruro de cesio en el cual En el primer caso = · = 4 · 3 + 2 13.9. La tabla proporciona los radios iónicos del , = 0,729 +2 3 y del los cuales son , y respectivamente. Describa brevemente la estructura cristalina resultante para el . Explique por qué a esto se le denomina estructura de la antifluorita. Para el tenemos = Xavi Paneque Linares 0,138 = 0,9857 0,140 º=8 Página 73 Grado en Ingeniería en Tecnologías Aeroespaciales 74 Ciencia de Materiales Y por tanto tiene una estructura parecida a la del cloruro de cesio. Se denomina estructura antifluorita porque es la inversa a la estructura fluorita, en el sentido de que se han invertido las posiciones de los cationes y aniones. En ella los iones una disposición cúbica centrada en las caras expandida y los cationes forman ocupan los dos tipos de huecos tetraédricos. 13.12. El óxido de berilio ( en una distribución ) puede formar una estructura cristalina que consiste de iones . Si el radio iónico del es , , entonces: a) ¿Qué tipo de intersticios ocuparán los iones de ? Por la relación de radios tenemos = 0,035 = 0,25 0,140 Por tanto forma una estructura como la del sulfuro de zinc y los intersticios son huecos tetraédricos. b) ¿Qué fracción de estos lugares intersticiales estarán ocupados por iones ? Dado que un intercambio de posiciones da lugar una estructura equivalente, la fracción de los iones es del 50%. 13.13. El titanato de hierro consiste en una distribución , tiene la estructura de la ilmenita, la cual de iones a) ¿Qué lugares intersticiales ocuparán los iones ? ¿Por qué? De la tabla podemos comprobar que = 0,077 = 0,550 0,140 Por tanto el número de coordinación es 6 y ocupa huecos octaédricos b) ¿Qué lugares intersticiales ocuparán los iones Xavi Paneque Linares ? ¿Por qué? Página 74 Grado en Ingeniería en Tecnologías Aeroespaciales 75 Ciencia de Materiales De forma similar para el = 0,061 = 0,436 0,140 El radio está entre 0,414 y 0,732 por tanto los iones ocuparán huecos octaédricos. c) ¿Qué fracción de todos los lugares tetraédricos estarán ocupados? No hay lugares tetraédricos 13.14. Calcular la densidad del , sabiendo que tiene estructura del cloruro sódico Si tiene estructura de cloruro sódico entonces = · · = 4 · 58,69 + 4 · 16 (2 · 0,069 + 2 · 0,140) · 6,022 · 10 13.15. El óxido de hierro ( densidad de , / = 6,58 ) tiene la estructura cristalina del cloruro sódico y una . Determinar la longitud de la arista de la celdilla unidad, comparar este valor con la longitud dada en la tabla determinada a partir de los radios y suponiendo que los iones = · · = y justo se tocan a lo largo de las aristas. 4 · 55,84 + 4 · 16 = 5,70 · 6,022 · 10 = 0,437 Si se tocan a lo largo de las aristas =2 +2 = 2 · 0,140 + 2 · 0,077 = 0,434 Son muy parecidos 13.18. Una forma cristalina de sílice ( ) tiene una celdilla unidad cúbica; a partir de los resultados de difracción de rayos X se sabe que la celdilla unidad tiene una arista de longitud , y . Si la densidad medida es , / , ¿cuántos iones hay por celdilla unidad? La relación entre los iones es 2 Xavi Paneque Linares = =2 Página 75 Grado en Ingeniería en Tecnologías Aeroespaciales 76 Ciencia de Materiales Por tanto · · = = · 28,08 + 2 · · 16 = 2,32 0,7 · 6,022 · 10 = 16 =8 =8 13.19. Usando los radios de la tabla, calcular la densidad del medida es , / . La densidad . ¿Cómo puede explicar la ligera discrepancia entre los valores calculado y medido? = · · 132,9 + 35,45 = 2 · 0,181 + 2 · 0,170 3 = 4,20 · 6,022 · 10 Hay imperfecciones. 13.20. A partir de los resultados de la tabla, calcular la densidad del , el cual tiene la estructura de la fluorita. El lado de una de las 8 celdillas es =8· = · · 2 · 0,1 + 2 · 0,133 3 = 4 · 40 + 8 · 19 0,1558 · 6,022 · 10 13.21. Un hipotético material cerámico del tipo de , igual a , / = 0,1558 = 3,325 se sabe que tiene una densidad y una celdilla unidad de simetría cúbica con una celdilla de arista . Los pesos atómicos de los elementos A y X son 28,5 y 30,0 g/mol, respectivamente. Según esta información, ¿Cuál de las siguientes estructuras cristalinas son posibles para este material: cloruro sódico, cloruro de cesio o blenda? Justifique su respuesta La ecuación que se debe cumplir es = Xavi Paneque Linares · · = · 28,5 + · 30 = 2,10 0,57 · 6,022 · 10 Página 76 Grado en Ingeniería en Tecnologías Aeroespaciales 77 Ciencia de Materiales Esta ecuación se cumple para =4 =4 Por tanto es una estructura como la del cloruro de cesio o sulfuro de cinc ( 13.22. La celdilla unidad del ) tiene simetría cúbica con una celdilla unidad de arista igual a 0,839 , / . Si la densidad de este material es , calcular su factor de empaquetamiento. Para este cálculo, utilizar los radio iónicos listados en la tabla. = · · = 4 · 16 + 3 · 55,84 = 5,24 0,839 · 6,022 · 10 =8 Por tanto = 4 4 · 8 · 0,140 + 3 · 8 · 0,073 = 0,689 3 0,839 13.29. Cuando se calienta la arcilla de caolinita [ ( )( ) ] a una temperatura suficientemente elevada, el agua resultante se elimina. En estas circunstancias, ¿Cuál es la composición de los productos resultantes? ¿Cuáles son las temperaturas liquidus y solidus de este material? ( )( ) 2 + +2 Por tanto la composición del producto resultante es +2 La composición será = 2 · 27 + 3 · 16 = 45,9% 2 · 27 + 3 · 16 + 2 · 28 + 4 · 16 Observando el diagrama las temperaturas son 1800 Xavi Paneque Linares 1580 Página 77 Grado en Ingeniería en Tecnologías Aeroespaciales 78 Ciencia de Materiales 13.37. Explicar brevemente por qué existe una dispersión significativa en los valores de la resistencia a la fractura en los materiales cerámicos, y por qué la resistencia a la fractura aumenta con la disminución en el tamaño de la probeta. La resistencia a la fractura medida en los materiales cerámicos es sustancialmente menor que la predicha por la teoría basada en las fuerzas de enlace entre átomos. Esto puede explicarse por la presencia de pequeños defectos en el material, los cuales actúan como concentradores de la tensión, es decir, lugares en los cuales la magnitud de la tensión aplicada es amplificada. El grado de amplificación de la tensión depende de la longitud de la grieta y del radio de curvatura de su punta, siendo mayor para defectos largos y puntiagudos. 13.38. La resistencia a la tracción de los materiales frágiles puede determinarse utilizando variaciones de la ecuación 8.1. Calcular el radio crítico de la grieta para una probeta de vidrio que experimente fractura a tracción a una tensión aplicada de . Suponga que la longitud crítica de la grieta es de teórica a la fractura es de / =2 De la tabla , donde y la resistencia es el módulo de elasticidad. = 2 · 70 · 10 = 10 = 19,6 = 7 · 10 =4 13.39. La resistencia a la fractura del vidrio puede aumentarse eliminando por ataque químico una capa delgada superficial. Se cree que esto se debe a que se altera la geometría superficial de las fisuras (por ejemplo, la longitud de la grieta puede reducirse y puede aumentar el radio de la punta de la grieta). Determine el cociente entre los radio del extremo de la grieta en el vidrio original y después de atacado, para que la resistencia a la fractura aumenta en un factor de 4 si se elimina la mitad de la longitud de la grieta. Xavi Paneque Linares Página 78 Grado en Ingeniería en Tecnologías Aeroespaciales 79 Ciencia de Materiales =2 4 /2 =2 = 1 8 13.40. Se realiza un ensayo de flexión por tres puntos en probetas de espinela ( ) que tiene una sección de espesor igual a = , , la distancia entre puntos de apoyo es = , = y anchura igual a . Calcule el módulo de rotura (resistencia a la rotura por flexión) si la carga en el momento de la fractura es . El punto de deflexión máxima (flecha) ocurre en centro de la probeta y viene dado por = Donde Calcular es el módulo de elasticidad e es el momento de inercia de la sección recta. para una carga de = = 3 2 = . 3 · 347 · 0,025 = 101,25 2 · 0,0089 · 0,0038 311 · 0,025 = 1,036 · 10 1 48 · 24 · 10 · · 0,0089 · 0,0038 12 13.41. Una probeta circular de es cargada en flexión por tres puntos. Calcule el radio mínimo posible de la probeta sin que la probeta se rompa cuando se aplica una carga de , si se sabeque el módulo de rotura es entre los puntos de apoyo es = = y la separación , = 5560 · 0,0445 = 6,33 · 10 · 310 · 10 13.42. Se necesita seleccionar un material cerámico que va a ser sometido a flexión por tres puntos. La probeta debe tener una sección circular con un radio de , y no debe romperse ni debe experimentar una flecha mayor que , centro cuando se aplica una carga de apoyo es de , Xavi Paneque Linares en su . Si la distancia entre los puntos de , ¿Cuál de los materiales de la tabla es el mejo candidato? La Página 79 Grado en Ingeniería en Tecnologías Aeroespaciales 80 Ciencia de Materiales magnitud de la flecha en el centro de la probeta puede calcularse mediante la ecuación del problema 13.40. = = 12 El material es = 12 · = 445 · 0,0508 = 131,14 · 0,0038 445 · 0,0508 = 3,534 · 10 · 0,0038 · 0,000021 = 353,4 o 13.43. Se realizó un ensayo de flexión por tres puntos en una probeta de óxido de aluminio con una sección circular de Xavi Paneque Linares de diámetro; la probeta se rompió bajo Página 80 Grado en Ingeniería en Tecnologías Aeroespaciales 81 Ciencia de Materiales una carga de cuando la distancia entre los puntos de apoyo era de . Se realizó otro ensayo en otra probeta de este mismo material, pero con una probeta de sección cuadrada de de longitud. ¿A qué carga se romperá esta probeta si la separación entre puntos de apoyo se mantiene en = = Xavi Paneque Linares 3 2 = = ? 3000 · 0,04 = 305,5775 · 0,0025 3 · 0,04 = 305,5775 2 · 0,015 = 137 510 Página 81 Grado en Ingeniería en Tecnologías Aeroespaciales 82 Ciencia de Materiales 8. Materiales compuestos 17.4. Determine los valores máximo y mínimo de la conductividad térmica de un cermet que contiene un 90% en volumen de partículas de carburo de titanio ( en una matriz de níquel. Suponga que las conductividades térmicas del son / / y ) y del , respectivamente. Máximo = + = 0,1 · 67 + 0,9 · 27 = 31 Mínimo = Xavi Paneque Linares + = 67 · 27 = 28,71 0,1 · 27 + 0,9 · 67 Página 82 Grado en Ingeniería en Tecnologías Aeroespaciales 83 Ciencia de Materiales 17.5. Un material compuesto con partículas grandes se ha preparado agregando partículas de tungsteno en una matriz de cobre. Si las fracciones de volumen del tungsteno y del cobre son , y , respectivamente, calcule el límite superior de la rigidez específica de este compuesto con los datos siguientes: La máxima rigidez es = 11 · 0,4 + 40,7 · 0,6 = 288,2 = = + = 8,9 · 0,4 + 19,3 · 0,6 = 15,14 288,2 = 19,04 15,14 = 110 407 · 0,4 + · 0,6 = 17,6 8,9 19,3 6 17.5. ¿Cuál es la diferencia entre fase matriz y la fase dispersa en un material compuesto? Compare las características mecánicas de la matriz y de la fase dispersa de los compuestos con fibras. La fase matriz es continua y rodea la otra fase, la dispersa. Características mecánicas de la matriz: transmite los esfuerzos externos aplicados, resiste poco esfuerzo, es dúctil, tiene bajo módulo elástico. Características de la fase dispersa: rígida, resistente y soporta cargas a tracción pero menos a compresión. 17.7. ¿Cuál es la diferencia entre cemento y hormigón? Cite tres importantes limitaciones que restringen el uso del hormigón como material estructural. Explique tres técnicas utilizadas para aumentar la resistencia del hormigón mediante reforzamiento. El término hormigón se refiere a un material compuesto formado por un agregado de partículas unidas entre sí mediante cemento. Xavi Paneque Linares Página 83 Grado en Ingeniería en Tecnologías Aeroespaciales 84 Ciencia de Materiales Tres limitaciones del hormigón como material estructural son - Relativamente poco resistente - Extremadamente frágil - Resistencia a la tracción es 10 a 15 veces menor que la resistencia a la compresión - Dilataciones y contracciones importantes con las fluctuaciones de temperatura - El agua penetra a través de los poros externos y puede provocar grietas durante el tiempo frío como consecuencia de los ciclos congelación 17.8. En un compuesto reforzado con fibra, enumere tres funciones de la fase matriz, compare las características deseadas de la matriz y de la fase fibrosa y cite dos razones que justifiquen que la unión entre la matriz y la fase dispersa deba ser fuerte. La fase matriz de un material compuesto con fibras ejerce varias funciones. - En primer lugar, una las fibras y actúa como un medio que distribuye y transmite a las fibras los esfuerzos externos aplicados; sólo una pequeña fracción del esfuerzo aplicado es resistido por la matriz. Además, la matriz debe ser dúctil y, por otra parte, el módulo elástico de la fibra debe ser mucho mayor que el de la matriz. - En segundo lugar, la matriz protege las fibras del deterioro superficial que puede resultar de la abrasión mecánica o de reacciones químicas con el medio ambiente. Estas interacciones introducen defectos superficiales capaces de originar grietas, que podrían producir fallos con esfuerzos de tracción relativamente bajos - Finalmente la matriz separa las fibras y, en virtud de su relativa blandura y plasticidad, impide la propagación de grietas de una fibra a otra, que originaría fallos catastróficos. Dos razones que justifican la unión fuerte es la protección que ofrece la matriz a las fibras y el hecho de que la matriz separe las fibras que impide la propagación de grietas de una fibra a otra. Xavi Paneque Linares Página 84 Grado en Ingeniería en Tecnologías Aeroespaciales 85 Ciencia de Materiales 17.9. En alguna combinación matriz epoxi-fibra de vidrio, la relación crítica longituddiámetro de fibras vale 40. Utilizando los datos de la tabla determine la resistencia de la unión matriz-fibra. = 2 = · 2 = 1 3,5 · 10 · = 43,75 40 2 17.11. Se proyecta fabricar un compuesto epoxi reforzado con fibras continuas y % en volumen de fibras y los alineadas. El compuesto debe tener un máximo de valores mínimos del módulo de elasticidad y de la resistencia a la tracción longitudinales debe ser , · y , · , respectivamente. ¿Qué material es mejor candidato: fibras de vidrio, de carbono o de aramida? ¿Por qué? Suponga que la matriz epoxi tiene un módulo de elasticidad de resistencia a la tracción de , · y una . Los datos de la fibra están en la tabla; para el carbono suponga un valor intermedio entre los extremos. Para un 40% en volumen en fibras tenemos = 1,2 · 10 = 0,6 · 69 + 0,4 55 = 3,1 · 0,6 + 0,4 · + = 2896,5 = 132,885 La única fibra que cumple estas propiedades es el carbono 17.12. Un compuesto reforzado con fibra continua y alineada consta de un 70% en volumen de matriz de policarbonato y 30% de fibra de aramida; las características mecánicas de estos dos materiales son las siguientes Calcule para este compuesto, la resistencia a la tracción longitudinal y el módulo de elasticidad longitudinal. Xavi Paneque Linares Página 85 Grado en Ingeniería en Tecnologías Aeroespaciales 86 Ciencia de Materiales = + = = 0,3 · 3,6 + 0,7 · 0,045 = 1,1115 + = 0,3 · 131 + 0,7 · 2,4 = 40,98 17.13. Se proyecta fabricar un compuesto de epoxi reforzada con fibra de carbono continuo y orientado cuyo módulo de elasticidad mínimo sea , · en la dirección de alineación de la fibra. El máximo peso específico permitido es 1,40. Con los datos indicados en la tabla, ¿es posible este material compuesto? ¿Por qué sí o por qué no? Suponga que el peso específico del compuesto se determina utilizando una relación similar a la ecuación = 69 < + = 260 + 1 1,4 > 1,8 + 1 + · 2,4 > 0,2585 1,25 < 0,2727 Sí es posible con 0,2585 < < 0,2727 17.14. Se proyecta fabricar poliéster reforzado con fibra de vidrio continua y alineada con una resistencia a la tracción mínima de en la dirección longitudinal. El peso máximo específico posible es 1,8. Utilizando los datos adjuntos determine si es posible este compuesto y justifique su respuesta 1,25 < 3,5 · + 1 1,8 > 2,5 + 1 · 0,05 1,35 > 0,3478 < 0,3913 Sí es posible con Xavi Paneque Linares Página 86 Grado en Ingeniería en Tecnologías Aeroespaciales 87 Ciencia de Materiales 0,3478 < < 0,3913 17.15. ¿Es posible fabricar un compuesto con matriz epoxi y fibra de aramida y orientada con módulos elásticos longitudinal y transversal de , · y , respectivamente? ¿Por qué sí o por qué no? Suponga que el módulo de elasticidad de la matriz epoxi es de , · Longitudinal + 124(1 ) 3,4 · 124 124 + 3,4(1 ) 35 = 3,4 · 5,17 = = 0,738 = 0,648 No es posible 17.17. Los módulos de elasticidad en las direcciones longitudinal y transversal de un compuesto reforzado con fibras continuas y orientadas son , · , respectivamente. Si la fracción de volumen de la fibra es , y , · , determine los módulos de elasticidad de las fases matriz y fibra. 33,1 = · 0,7 + 0,3 3,66 = · + 0,3 0,7 De donde concluimos = 104 = 2,6 17.19. En un compuesto de nilón 66 reforzado con fibras continuas y alineadas de carbono, la fibra soporta el % de la carga aplicada en la dirección longitudinal. Utilizando los datos suministrados, determine la fracción de fibra que se necesita. ¿Cuál será la resistencia a la tracción de este compuesto? = Xavi Paneque Linares 0,97 260 · = 0,03 2,8 · = 0,258 Página 87 Grado en Ingeniería en Tecnologías Aeroespaciales 88 Ciencia de Materiales = 1,7 · 0,258 + 0,076(1 0,258) = 495 17.20. Suponga que el compuesto descrito en el problema 17.12 tiene un área de y está sometido a una carga longitudinal de 53 400 N. Calcule la relación de carga fibra-matriz. Calcule las cargas soportadas por las fases fibra y matriz. Calcule la magnitud del esfuerzo en cada fase. ¿Cuál es la deformación experimentada por el compuesto? = 131 · 0,3 = 23,39 2,4 · 0,7 = = = + = 51210,8 = 2189,2 0,3 · 3600 + 0,7 · 45 = 0,027 0,3 · 1,31 · 10 + 0,7 · 2,4 · 10 17.21. Un compuesto reforzado con fibra continua y alineada tiene una sección transversal de y está sometido a una carga de tracción externa. Si las tensiones soportadas por la fibra y por la matriz son 215 MPa y 5,38 MPa, respectivamente, la fuerza soportada por la fase fibra es 76 800 N y la deformación longitudinal total del compuesto es , · , determine la fuerza soportada por la matriz, el módulo de elasticidad del material compuesto en la dirección longitudinal y los módulos de elasticidad de las fases fibra y matriz. = 215 1,56 · 10 = = = 137,8 = 76800 = 357,21 5,38 5,38 1,56 · 10 = 3,45 = 612,79 215e6 = = 1 Xavi Paneque Linares · = 0,368 = 5,38 · 612,79 = 3296,81 = 137,8 · 0,368 + 3,45 · 0,632 = 52,9 Página 88 Grado en Ingeniería en Tecnologías Aeroespaciales 89 Ciencia de Materiales 17.22. Calcule la resistencia longitudinal de un compuesto con matriz epoxi y fibra d carbono alineada con una fracción de volumen de fibra de , diámetro medio de fibra de · suponiendo: (a) un , (b) una longitud media de fibra de 8 mm; (c) una resistencia a la rotura de la fibra de , · ; (d) una resistencia de la unión matriz-fibra de 75 MPa; (e) el esfuerzo de la matriz a la rotura del compuesto es 6,0 MPa y (f) una resistencia a la tracción de la matriz de 60 MPa. = < ( Xavi Paneque Linares 2 = 4,5 · 10 · 6 · 10 2 · 75 ) = 4,5 · 10 · 0,2 1 = 0,36 894,675 MPa 0,18 + 6 · 0,8 = 884,55 2·8 Página 89