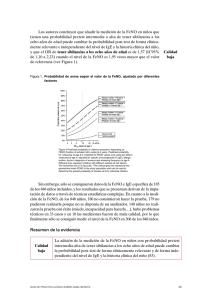
Resinas fenólicas
Anuncio

k OFICINA ESPAÑOLA DE PATENTES Y MARCAS 19 k ES 2 059 792 kInt. Cl. : C04B 26/12 11 N.◦ de publicación: 5 51 ESPAÑA C08K 5/10 C08L 61/06 B22C 1/22 k TRADUCCION DE PATENTE EUROPEA 12 kNúmero de solicitud europea: 89313422.1 kFecha de presentación : 21.12.89 kNúmero de publicación de la solicitud: 0 377 308 kFecha de publicación de la solicitud: 11.07.90 T3 86 86 87 87 k 54 Tı́tulo: Resinas fenólicas. k 73 Titular/es: Borden (UK) Limited k 72 Inventor/es: k 74 Agente: Elzaburu Márquez, Fernando 30 Prioridad: 22.12.88 GB 8829984 North Baddesley Southampton S05 9ZB, GB 45 Fecha de la publicación de la mención BOPI: 16.11.94 45 Fecha de la publicación del folleto de patente: 16.11.94 Aviso: k k Lemon, Peter Herbert Richard Bryan; King, James Godfrey; Murray, Graham; Leoni, Henri y Gerber, Arthur H. k En el plazo de nueve meses a contar desde la fecha de publicación en el Boletı́n europeo de patentes, de la mención de concesión de la patente europea, cualquier persona podrá oponerse ante la Oficina Europea de Patentes a la patente concedida. La oposición deberá formularse por escrito y estar motivada; sólo se considerará como formulada una vez que se haya realizado el pago de la tasa de oposición (art◦ 99.1 del Convenio sobre concesión de Patentes Europeas). Venta de fascı́culos: Oficina Española de Patentes y Marcas. C/Panamá, 1 – 28036 Madrid ES 2 059 792 T3 DESCRIPCION 5 10 15 Esta invención se refiere a resinas fenólicas. Más particularmente, se refiere a un método para producir composiciones de resinas fenólicas a partir de compuestos fenólicos esterificados que producen dichas composiciones de resinas por tratamiento con sustancias alcalinas. Las composiciones de resinas fenólicas producidas a partir de estos compuestos fenólicos esterificados en condiciones alcalinas tienen un contenido reducido de productos secundarios no reactivos. Es sabido que las resinas fenólicas alcalinas pueden curarse en condiciones alcalinas por reacción con ésteres orgánicos, incluidos lactonas y carbonatos orgánicos. Tal curado con ésteres de resinas resol fenólicas alcalinas se describe, inter alia, en los Documentos DE - C - 1.065.605, DE - C - 1.171.606, JP A - 49 - 16793, JP - A - 50 - 130627, GB - A - 2059975, EP - A - 0085512 y EP - A - 0086615. Según estas publicaciones, una resina resol fenólica muy alcalina en solución acuosa puede curarse a temperatura ambiente por reacción con un éster orgánico (incluidos lactonas y carbonatos), poniendo en contacto la resina con el éster en forma lı́quida o de gas. Tales resinas encuentran aplicación particularmente en la unión de materiales refractarios tales como arena, en la fabricación de moldes y machos para fundición y en el tratamiento de formaciones subterráneas. También se han propuesto otras aplicaciones de las resinas, tales como encolado de madera. 20 25 30 35 40 45 50 El endurecimiento de resinas fenólicas muy alcalinas con ésteres supone la saponificación del éster, pero con los productos hasta ahora producidos existe el inconveniente de que algunos productos de la reacción de saponificación no se incorporan a la estructura de la resina final, sino que permanecen en la masa curada como compuestos no resinosos, en forma de alcohol libre y en forma de la sal del componente ácido del éster. Aunque esto no es un inconveniente grave en algunas de las aplicaciones a las que se destinan los productos, la presencia de alcohol libre y sal en la composición curada se considera que es perjudicial en otras aplicaciones en las que se prevean productos fenólicos curados con ésteres, particularmente cuando se necesita gran resistencia eléctrica y/o resistencia al agua. En un intento de remediar al menos en parte esta deficiencia, en el Documento GB - A - 2.140.017 se propuso emplear un éster formiato o acetato de un fenol monovalente o polivalente reactivo con formaldehı́do, como el agente de curado de éster para el endurecimiento de resinas resoles fenólicas alcalinas. En este caso, el éster se obtiene por esterificación del o de los grupos fenólicos - OH del fenol monovalente o polivalente. Al mezclar este éster con resina resol fenólica alcalina, el éster se saponifica como consecuencia de la acción del álcali en el componente de resina y el fenol original, que formó el componente alcohol del éster, se libera y, de este modo, queda disponible para reaccionar para dar la estructura de la resina. Puesto que el fenol es reactivo con el formaldehı́do, sirve también para unirse a cualquier formaldehı́do que no esté combinado en la resina o se le libera posteriormente. La sal del componente ácido del éster permanece, en este caso, en la composición curada en forma de un producto secundario no - resinoso. Es una caracterı́stica adicional de los sistemas de resoles fenólicos curados con ésteres antes producidos, el que sólo son eficaces cuando se emplea un álcali fuerte. En la mayor parte de las aplicaciones prácticas, sólo los hidróxidos sódico o potásico producen composiciones satisfactorias. Las resinas fenólicas producidas con bases débiles no pueden endurecer utilizando ésteres o sólo pueden endurecer mediante un calentamiento a altas temperaturas. Los autores del invento han descubierto que estos y otros inconvenientes pueden evitarse o, por lo menos, reducirse sustancialmente si se emplean compuestos fenólicos que contienen sustituyentes metilol esterificados en el anillo fenólico, en presencia de una base y un disolvente polar, en la preparación de una composición de una resina fenólica curada. utilizando estos compuestos fenólicos esterificados, se evita la liberación de alcoholes durante la etapa de saponificación. En un primer aspecto, la presente invención proporciona una composición de una resina fenólica, que comprende 55 (1) un compuesto fenólico esterificado que contiene uno o más grupos hidroxilo fenólicos y/o uno o más grupos hidroxilo fenólicos esterificados y que contiene, además, uno o más grupos metilol esterificados que tienen la fórmula general 60 2 ES 2 059 792 T3 R | - C - OH | H 5 en donde R es H, un hidrocarbilo alifático o aromático o un grupo heterocı́clico en posición orto y/o para con respecto a un grupo hidroxilo fenólico o un grupo hidroxilo fenólico esterificado, 10 (2) una composición de una resina resol fenólica no esterificada, y (3) una base. 15 20 25 30 35 40 45 50 55 60 La invención proporciona también un método para producir una composición de resina fenólica curada, que comprende hacer reaccionar los componentes (1), (2) y (3) anteriores en presencia de agua y/u otro disolvente polar. El compuesto fenólico esterificado, empleado en la presente invención, es un fenol o un derivado de fenol que contiene uno o más grupos hidroxilo fenólicos y/o uno o más grupos hidroxilo fenólicos esterificados y que, además, contiene uno o más grupos metilol esterificados unidos a un átomo de carbono del anillo fenólico, en posición orto y/o para con respecto a por lo menos un grupo hidroxilo fenólico o a un grupo hidroxilo fenólico esterificado. Por tanto, debe entenderse que el compuesto fenólico esterificado empleado puede ser un fenol mono - , di - o poli - nuclear con grupos metilol, mono - , o di - o poli esterificado, en donde un átomo de carbono del anillo aromático está en posición orto o para con respecto a un grupo hidroxilo fenólico o a un grupo hidroxilo fenólico esterificado. Con la expresión “fenol mononuclear” se quiere indicar un compuesto no polı́mero que tiene un núcleo aromático al que está unido directamente por lo menos un grupo hidroxilo. Ejemplos de fenoles mononucleares incluyen, pero no están limitados, al propio fenol, homólogos de fenol, tales como o - , m - o p cresol, 3,5 - xilen - 1 - ol, t - butil - fenol, octil - fenol, n - nonil - fenol, y o - , ó p - fenilfenol y derivados de fenol, tales como resorcinol, floroglucinol, pirogalol. Los compuestos no polı́meros 4,4’ - dihidroxidifenilo, 4,4’ - dihidroxidifeniléter y 4,4’ - dihidroxidifeniltioéter pueden considerarse también fenoles mononucleares para el objetivo de la presente invención. Con las expresiones “fenol dinuclear” y “fenol polinuclear” se quiere indicar compuestos formados por la reacción de condensación de dos o más moléculas de un fenol mononuclear con una o más moléculas de un aldehı́do o una cetona reactivos con fenol. Por tanto, en la presente invención, el compuesto fenólico esterificado puede comprender un derivado, que contiene grupos metilol esterificados, de un producto de reacción de condensación, obtenido haciendo reaccionar dos o más moléculas de un fenol mononuclear con una o más moléculas de un aldehı́do o de una cetona reactivos con fenol, en donde el citado derivado contiene uno o más grupos hidroxilo fenólicos y/o uno o más grupos hidroxilo fenólicos esterificados y contiene uno o más grupos metilol esterificados en posición orto y/o para con respecto a un grupo hidroxilo fenólico o un grupo fenólico esterificado. Ejemplo de tales productos de reacción de condensación incluyen, pero no se limitan a productos de reacción resinosos de fenol, homólogos de fenol o sus derivados (por ejemplo, 0 - , m - ó p - cresol, 3,5 - xilen - 1 - ol, etilfenol, 0 - ó p - fenilfenol, resorcinol, floroglucinol, pirogalol, 4,4’ - dihidroxidifenilo, 4,4’ - dihidroxidifeniléter y 4,4’ - dihidroxidifeniltioéter) con un aldehı́do (tal como formaldehı́do, acetaldehı́do, furfuraldehı́do, benzaldehı́do y sus mezclas) o con una cetona (tal como acetona y ciclohexanona). Además, mezclas de fenoles reactivos con aldehı́dos, tales como isómeros de cresol mixtos, xilenoles y mezclas fenólicas, tales como las obtenidas a partir del fraccionamiento del alquitrán de hulla y lı́quido de cáscara de nuez de acajú, pueden emplearse como todo o parte del componente de fenol. Preferiblemente, el compuesto fenólico esterificado comprende un derivado, que contiene grupos metilol esterificados, de un producto de reacción de condensación, obtenido haciendo reaccionar formaldehı́do y un fenol mononuclear elegido entre fenol, o - , m - ó p - cresol, 3,5 - xilen - 1 - ol, resorcinol, floroglucinol, pirogalol o una de sus mezclas. Según una realización, el compuesto fenólico esterificado es un derivado de Bisfenol A que contiene grupos metilol esterificados. Según una realización diferente, el compuesto fenólico esterificado es una resina resol de fenol - formaldehı́do esterificada o parcialmente esterificada. Tı́picamente, el compuesto fenólico esterificado contiene uno o más grupos acetiloximetilo o grupos formiloximetilo. Los compuestos fenólicos dinucleares y polinucleares antes mencionados, que tienen grupos metilol esterificados en posición orto y/o para son especialmente útiles en la presente invención a la vista de su propia capacidad para formar composiciones de resinas curadas cuando reaccionan con una base en presencia de agua y/u otro disolvente polar. Por consiguiente, según un aspecto adicional, la presente invención proporciona una composición de resina fenólica que comprende un compuesto fenólico esterificado que comprende un derivado, que contiene grupos metilol esterificados, de un producto de reacción 3 ES 2 059 792 T3 de condensación obtenido haciendo reaccionar dos o más moléculas de un fenol mononuclear con una o más moléculas de un aldehı́do o una cetona reactivos con fenol, en donde el citado derivado contiene uno o más grupos hidroxilo fenólicos y/o uno o más grupos hidroxilo fenólicos esterificados y contiene uno o más grupos metilol esterificados que tienen la fórmula general 5 10 15 20 25 30 35 40 45 50 55 60 R | - C - OH | H en donde R es H, un grupo hidrocarbilo alifático o aromático o heterocı́clico en posición orto y/o para con respecto a un grupo hidroxilo fenólico o a un grupo hidroxilo fenólico esterificado y una base. El citado compuesto fenólico esterificado forma una composición de resina fenólica curada por reacción con una base en presencia de agua y/u otro disolvente polar. Tal compuesto fenólico esterificado puede usarse en un método para producir una composición de resina fenólica curada, que comprende hacer reaccionar el compuesto fenólico esterificado con una base, en presencia de agua y/u otro disolvente polar. Según se ha indicado anteriormente, los compuestos fenólicos que se usan según la presente invención en la producción de composiciones de resinas fenólicas contienen uno o más grupos metilol esterificados en posición orto y/o para con respecto a un grupo hidroxilo fenólico o un grupo hidroxilo fenólico esterificado. Con la expresión “grupo metilol esterificado”, según se usa aquı́, se indica un grupo organocarboniloximetileno o a su derivado sustituido. Con la expresión “grupo metilol” se indica un grupo de la fórmula general R | - C - OH, en donde R es H, un grupo hidrocarbilo alifático o aromático o un grupo heterocı́clico. | H Tı́picamente, los compuestos fenólicos que tienen uso en los diversos aspectos y realizaciones de la presente invención pueden prepararse a partir de un fenol o derivado de fenol apropiado que contiene grupos metilol, haciendo reaccionar el mismo con un reactivo de esterificación. El fenol o derivado de fenol que contiene grupos metilol puede producirse haciendo reaccionar formaldehı́do u otro aldehı́do (tal como acetaldehı́do, butiraldehı́do y furfuraldehı́do) con el fenol o su derivado apropiados. Por razones de disponibilidad y de coste razonable, unido a la repetitibilidad y a la falta de olores fuertes o nocivos, el tipo preferido de compuesto fenólico es uno basado en un producto de condensación de fenol y formaldehı́do. Tales productos de condensación pueden fabricarse de formas conocidas haciendo reaccionar fenol y formaldehı́do en presencia de catalizadores ácidos o básicos, si bien la preparación de tales productos no forma parte de esta invención. Cuando se emplean catalizadores básicos para este propósito, los productos de condensación de fenol - formaldehı́do resultantes (resinas resoles) poseerán grupos metilol libres en una proporción que dependerá principalmente de la relación de formaldehı́do a fenol, grupos que están unidos a átomos de carbono de anillos fenólicos en posición orto y/o para con respecto a los grupos hidroxilo fenólicos. Sin embargo, cuando se emplean catalizadores ácidos, los productos de condensación de fenol - formaldehı́do resultantes, normalmente no contienen grupos metilol. Tales productos, sin embargo, pueden formar materiales de partida apropiados si, utilizando formaldehı́do en condiciones neutras o alcalinas, se lleva a cabo una etapa de metilolación subsiguiente a la fabricación del producto de condensación catalizado con ácidos y antes de la esterificación. Similarmente, si el compuesto fenólico es producto de la reacción de condensación de un fenol y una cetona reactiva con fenol, será necesaria la metilolación antes de la esterificación. Tal metilolación puede realizarse fácilmente por reacción con formaldehı́do en condiciones neutras o alcalinas. De estos diversos métodos de preparación de fenol o derivados de fenol que contienen grupos metilol, se prefiere preparar un producto de condensación de fenol - formaldehı́do en presencia de un catalizador básico (es decir, una resina resol), ya que con ello se evita la necesidad de una etapa adicional de metilolación. En tal producto de condensación, la relación molar de fenol:formaldehı́do estará tı́picamente en el intervalo de 1:1,2 a 1:3,0, preferiblemente entre 1:1,5 y 1:3,0. La cantidad de álcali usada como catalizador de condensación será tı́picamente 1 - 2% en peso aproximadamente, basada en el peso del fenol, generalmente suficiente para mantener un pH de por lo menos 8, pero puede ser considerablemente más 4 ES 2 059 792 T3 5 10 15 20 25 alto. El grado de condensación de tal resina resol puede describirse convenientemente haciendo referencia a dos parámetros; los sólidos residuales por calentamiento a 100◦ C hasta peso constante y la viscosidad de la solución del resol. Las resinas resol lo más preferiblemente usadas como los derivados fenólicos que contienen grupos metilol para ser esterificadas para producir los compuestos fenólicos esterificados, tendrán un contenido de sólidos entre 30 y 95%, preferiblemente 50 a 85% en peso y una viscosidad entre 0,1 y 100 poises, preferiblemente 1 a 25 poises, a 25◦ C. Ejemplos tı́picos de catalizadores de condensación incluyen los óxidos e hidróxidos de sodio, potasio, litio, bario, calcio, magnesio y aminas y amonı́aco. El fenol o derivado de fenol que contiene grupos metilol, ası́ preparado, puede luego esterificarse para producir el compuesto fenólico esterificado deseado que contiene uno o más grupos metilol esterificados en posición orto y/o para con respecto a un grupo hidroxilo fenólico o un grupo hidroxilo fenólico esterificado. Los ésteres de los fenoles o derivados de fenoles que contienen grupos metilol considerados, son ésteres carboxilato orgánicos. Estos ésteres pueden derivar de cualquier ácido mono - , di - o poli - básico alifático, alicı́clico o aromático, capaz de formar ésteres con grupos metilol. También es posible que un compuesto fenólico esterificado que contiene grupos metilol contenga grupos éster derivados de más de uno de estos ácidos. Sin embargo, para la mayorı́a de los propósitos, los ésteres serán los formados a partir de ácidos carboxı́licos inferiores, especialmente ácido fórmico y ácido acético. Cuando aquı́ se hace referencia al componente ácido del grupo éster, sólo se pretende como descripción del tipo de grupo y no se pretende indicar que es necesario emplear el ácido propiamente dicho para la fabricación del éster de metilol. De hecho, el éster puede formarse de cualquier manera conocida y el procedimiento adoptado puede variarse, según es conocido por los expertos en la técnica, para adaptarlo a los compuestos particulares a producir. Ejemplos de algunos métodos de esterificación que pueden usarse, incluyen: (1) reacción de un compuesto de metilol con anhı́drido de ácido, anhı́drido mixto o cloruro de ácido, tı́picamente en presencia de un catalizador apropiado; (2) intercambio de ésteres entre un compuesto de metilol y un éster de ácido carboxı́lico apropiado en presencia de un catalizador adecuado o por intercambio de ácidos según se describe, por ejemplo, en el documento US 2.544.365; y 30 (3) tratamiento de un compuesto de metilol con ceteno, diceteno o sus derivados. También es posible producir los compuestos fenólicos deseados por acción de un anhı́drido de ácido sobre fenoles o derivados de fenol mono - , di - , o tri - dialquilaminometil sustituidos. 35 40 45 50 55 60 Por tanto, en algunos casos puede emplearse un anhı́drido de ácido carboxı́lico para esterificar el compuesto fenólico ventajosamente, en lugar del ácido carboxı́lico. Alternativamente, el éster puede formarse a partir del correspondiente cloruro de ácido. Según se ha mencionado anteriormente, un compuesto fenólico preferido utilizable en la presente invención comprende una resina fenólica que contiene grupos metilol esterificados. En tal caso, es la resina fenólica que contiene grupos metilol la que será esterificada. Sin embargo, en términos generales, las resinas fenólicas resol son sensibles a los ácidos y, en la mayorı́a de los casos, será necesario esterificar los grupos metilol, y opcionalmente los grupos hidroxilo fenólicos, en una resina fenólica por una vı́a indirecta, con objeto de impedir la gelificación de la resina. La tendencia a gelificar puede reducirse o eliminarse mediante bloqueo del grupo fenólico - OH esterificándole o eterificándole, según se describe, por ejemplo, en el Documento DE - C - 474.561. Obviamente, cualquier catalizador empleado para fomentar la reacción de esterificación no debe ser capaz de reaccionar posteriormente con los grupos metilol esterificados del producto de la reacción de esterificación en las condiciones de reacción usadas. Un ejemplo de un catalizador de esterificación apropiado es piridina. Un proceso preferido es formar el éster de acetato de compuestos fenólicos que contienen grupos metilol introduciendo cetona en una solución del compuesto fenólico que contiene metilol. En este caso, la cetona se genera preferiblemente inmediatamente antes de su uso, tı́picamente en un equipo según se describe en los documentos US 2.541.471 o 3.259.469. Haciendo reaccionar el compuesto fenólico con dicetona de manera similar, se obtiene el éster acetoacetato del compuesto fenólico. Por intercambio de éster pueden formarse otros ésteres. Grupos éster apropiados incluyen, pero no están restringidos a formiato, acetato, acetoacetato, acrilato, propionato, lactato, crotonato, metacrilato, butirato, isobutirato, caproato, caprilato, benzoato, toluato, p - amino - benzoato, p - hidroxibenzoato, salicilato, cinamato, laureato, miristato, palmitato, oleato, ricinoleato, estearato, oxalato, succinato, fumarato, maleato, adipato, ftalato, azelato y sebacato. Los ésteres acetato forman una clase especialmente preferida de compuestos según la presente invención. Ejemplos especı́ficos de compuestos fenólicos esterificados que son útiles en la presente invención incluyen 2 - acetiloximetilfenol, 2 - metacriloiloximetilfenol, 2 - saliciloiloximetilfenol, 2 - acetiloximetilfenol acetato, 2,6 - diacetiloximetil - p - cresol, 2,6 - diacetiloximetil - p - cresol acetato, 2,6 - diacetoacetiloximetil 5 ES 2 059 792 T3 - p - cresol, 2,4,6 - triacetiloximetilfenol, 2,4,6 - triacetiloximetilfenol acetato, 2,6 - diacetiloximetilfenol acetato, 2,2’,6,6’ - tetraacetiloximetil Bisfenol A y 2,2’,6,6’ - tetraacetiloximetil Bisfenol A diacetato. 5 10 15 Una clase particular de ésteres de metilol que es particularmente útil es la de los metilol hidroxibenzoatos ya que, por saponificación del éster en presencia de una base, el resto hidroxibenzoato, en virtud de sus grupos hidroxilo fenólicos, es capaz de unirse en la estructura de la resina fenólica y, en virtud de sus grupos carboxilato, es capaz de fijar cualquier ion metálico básico a la molécula completamente reticulada. Por tanto, en la saponificación de ésteres de hidroxibenzoato de compuestos fenólicos que contienen metilol, en presencia de una base, no se libera ningún componente alcohólico ni ninguna sal, a diferencia del caso de los sistemas de curado con ésteres de la técnica anterior para resinas fenólicas alcalinas. Otra clase que tiene aptitudes similares a las de los hidroxibenzoatos comprende los hidroxifenilalquilcarboxilatos que tendrán el mismo efecto que los hidroxibenzoatos, aunque los ácidos hidroxifenilalquilcarboxı́licos pueden formar ésteres más fácilmente con resinas fenólicas con grupos metilol. Estos ésteres de hidroxibenzoato e hidroxifenilalquilcarboxilato forman además un aspecto adicional de la presente invención. Consiguientemente, la presente invención proporciona un compuesto fenólico que contiene uno o más grupos hidroxilo fenólicos y/o uno o más grupos hidroxilo fenólicos esterificados y, en las posiciones orto y/o para del anillo fenólico con respecto a un grupo hidroxilo fenólico o a un grupo hidroxilo fenólico esterificado, uno o más grupos de la fórmula general (I) 20 (I) 25 30 35 40 45 50 55 60 en donde R es un grupo alquileno de 1 - 4 C, x = 0 o 1, y = 1 a 3 y z = 1 o 2, tal que cuando x = 0, z = 1. Una clase de compuestos fenólicos preferida según este aspecto de la invención comprende productos de condensación resinosos de fenol - formaldehı́do que contienen dos o más grupos sustituyentes de la fórmula general I anterior en las posiciones orto y/o para con respecto a grupos hidroxilo fenólicos o grupos hidroxilo fenólicos esterificados de la molécula. Ejemplos de los ésteres de hidroxibenzoato e hidroxifenilalquilcarboxilato incluyen los que se pueden derivar de los ácidos, ácido 3,5 - dihidroxibenzoico, ácido 4 - hidroxifenilacético, ácido 2,4,6 - trihidroxibenzoico, ácido 4 - hidroxibenzoico, ácido 4,4 - bis(4 - hidroxifenil)valérico, ácido gálico y ácido salicı́lico. Según aún otro aspecto, la invención proporciona un derivado de un producto de reacción de condensación, obtenido al hacer reaccionar dos o más moléculas de un fenol mononuclear elegido entre fenol, o - cresol, m - cresol, p - cresol, 3,5 - xilen - 1 - ol, resorcinol, floroglucinol y pirogalol, con una o más moléculas de un aldehı́do o una cetona reactivos con fenol, derivado que contiene uno o más grupos hidroxilo fenólicos y/o uno o más grupos hidroxilo fenólicos esterificados y contiene también uno o más grupos metilol esterificados que tienen la fórmula general R | - C - OH | H en donde R es H, un hidrocarbilo alifático o aromático o un grupo heterocı́clico unido en posición orto y/o para con respecto a un grupo fenólico, en donde uno o más de los grupos metilol esterificados contiene un grupo éster de ácido carboxı́lico elegido entre formiato, acetato, acetoacetato, acrilato, propionato, lactato, crotonato, metacrilato, butirato, isobutirato, caproato, caprilato, benzoato, toluato, p - aminobenzoato, cinamato, laureato, miristato, oxalato, succinato, fumarato, maleato, adipato, azelato, sebacato o un grupo de la fórmula 6 ES 2 059 792 T3 5 10 en donde R es un grupo alquileno de 1 - 4 C, x = 0 o 1, y = 1 a 3 y z = 1 o 2, tal que cuando x = 0, z = 1, derivado que experimenta reticulación por reacción con una base en presencia de agua y/u otro disolvente polar. 15 20 25 30 La lista de grupos éster apropiados, mencionados anteriormente, incluye algunos grupos éster derivados de ácidos que son por si mismos capaces de experimentar polimerización (por ejemplo, acrilato y metacrilato). Consiguientemente, es posible usar un compuesto fenólico como precursor de una resina fenólica curada, que contiene ésteres de metilol de tales ácidos. Por saponificación, en presencia de la base, se libera una sal polimerizable que luego se puede polimerizar para formar un material de alto peso molecular. Debido a que los resoles de fenol - formaldehı́do son tan inestables y tienen a formar materiales de peso molecular más alto por polimerización por condensación incluso a temperatura ambiente, las condiciones para la esterificación son muy crı́ticas. Por tanto, como se entenderá fácilmente por lo anterior, las condiciones de reacción empleadas convencionalmente en la preparación de ésteres a partir de ácidos carboxı́licos y alcoholes estables, tales como alcohol metı́lico y alcohol etı́lico, no siempre serán apropiados para la esterificación de los grupos metilol fijados a los núcleos aromáticos en las resinas resol de fenol - formaldehı́do. Además, la presencia de un ácido carboxı́lico puede, por sı́ mismo, provocar la polimerización de fenol - alcoholes de bajo peso molecular, presentes en una composición del resol. Por tanto, se prefiere añadir el ácido lentamente al resol, de manera que durante la reacción de esterificación prevalezcan unas condiciones sólo débilmente ácidas. Pueden usarse convenientemente disolventes, tales como ésteres o cetonas, particularmente en el caso de resoles de peso molecular más alto, para disolver el resol y facilitar una reacción uniforme. 35 40 45 50 55 60 Puesto que la reacción de esterificación desprende agua, puede acelerarse utilizando unas condiciones no acuosas, ası́ como utilizando un disolvente de bajo punto de ebullición capaz de formar un azeótropo con el agua. Los ésteres de la presente invención se preparan preferiblemente eligiendo unas condiciones que esterifiquen preferentemente el grupo - CH2 OH y no el grupo fenólico - OH. Sin embargo, según es evidente a partir de lo anterior, está dentro del alcance de los diversos aspectos y realizaciones de la presente invención, usar derivados fenólicos que contienen metilol esterificados, en donde alguno e incluso todos los grupos hidroxilo fenólicos propiamente dichos están esterificados. Estos últimos generalmente reaccionarán más lentamente, pero también presentarán una mayor estabilidad frente al almacenamiento debido a la inactivación del grupo - OH fenólico. Generalmente, cuando se usa un ácido para esterificar el compuesto fenólico, la cantidad preferida de ácido usada será igual, sobre una base molar, al contenido de grupos metilol libres. Sin embargo, en los casos en que está presente una pluralidad de grupos metilol, es posible esterificar solamente una parte de los grupos metilol, de suerte que los grupos metilol no esterificados restantes, permiten que en una etapa posterior, el producto se polimerice térmicamente. Por ejemplo, este podrı́a ser un medio conveniente para conservar en el producto un grado de termoplasticidad. Por otro lado, puede necesitarse un exceso de ácido para inducir la esterificación a bajas temperaturas. Idealmente, cualquier ácido residual libre deberı́a separarse a partir del compuesto fenólico que contiene metilol esterificado antes de que este último reaccione con una base en presencia de agua u otro disolvente polar para producir una composición de resinas fenólicas, ya que cualquier ácido residual libre presente en el compuesto fenólico esterificado competirá con el compuesto fenólico esterificado para reaccionar con la base. Según se ha mencionado anteriormente, los compuestos fenólicos esterificados reaccionan con una base en presencia de agua u otro disolvente polar. Ejemplos de disolventes polares que pueden usarse en la presente invención en lugar de agua incluyen metanol, etanol, alcoholes industriales metilados (IMS), 7 ES 2 059 792 T3 formamida, N,N - dimetilformamida, dimetilacetamida, trietanolamina y glicerol. 5 10 15 20 25 30 35 En la aplicación de la presente invención para la producción de machos y moldes de fundición los autores de esta invención han descubierto que la resistencia de los machos de arena se mejora si una parte o todo el disolvente polar usado es un glicol, tal como etilenglicol o dietilenglicol, un éter - alcohol, tal como metoxietanol, etoxietanol, fenoxietanol o etildigol (es decir, éter etı́lico de dietilenglicol), o un cetoalcohol, tal como diacetona - alcohol. Adiciones totales de disolvente tı́picas están en el intervalo de 1 a 50%, preferiblemente 1 - 30%, en peso basado en el peso total de los otros componentes en la composición. El uso de un disolvente polar no acuoso será deseable en aplicaciones de la invención en las que la presencia de agua podrı́a tener un efecto pernicioso sobre las propiedades del producto final. La base usada en la presente invención puede ser cualquier material o mezclas de materiales que, cuando se añaden en una cantidad apropiada a la composición que comprende un compuesto fenólico esterificado que contiene uno o más grupos metilol esterificados, transforma a la composición en alcalina lo que, en el caso de sistemas acuosos, significa que la base es una que es capaz de aumentar el pH de la composición hasta un valor por encima de 7. La cantidad de base requerida para lograr esta alcalinidad deseada en la composición depende ampliamente de la identidad de la base usada y de si la composición a la que se añade la base contiene cualquier especie quı́mica que sea reactiva con la base. Por ejemplo, si el compuesto fenólico esterificado contiene cualquier grupo quı́mico reactivo con bases y/o si la composición que contiene el compuesto fenólico esterificado, contiene adicionalmente cualquier compuesto reactivo con bases, grupos o compuestos que tendrı́an el efecto de neutralizar la base cuando se añadiera, entonces, obviamente, la base deberı́a usarse en una cantidad que esté en exceso con respecto a la cantidad requerida para neutralizar tales grupos quı́micos reactivos con bases y/o tales compuestos reactivos con bases, presentes. La mayor parte de las bases inorgánicas y muchas aminas orgánicas son apropiadas para reaccionar con los compuestos fenólicos esterificados. La facilidad con la que saponifican a los ésteres del resol determina la velocidad de gelificación y la temperatura mı́nima a la que tiene lugar la gelificación. La base, usada para saponificar el compuesto fenólico que contiene metilol esterificado para formar una composición de resina fenólica según la invención, puede estar en forma de un gas, un lı́quido de bajo punto de ebullición o de su vapor, un material lı́quido o una solución de un álcali o unsólido. Materiales apropiados incluyen: (i) óxidos e hidróxidos de metales alcalinos y alcalino - térreos, por ejemplo sodio, potasio, litio, bario, calcio y magnesio; (ii) óxidos e hidróxidos de otros metales que presentan propiedades alcalinas o anfóteras, tales como óxido de zinc; y 40 45 50 55 60 (iii) amonı́aco, hidróxidos de amonio cuaternario, aminas secundarias y terciarias alifáticas, alicı́clicas o aromáticas y bases de Mannich, por ejemplo dimetilamina, trimetilamina, trietilamina, N,N dimetiletilamina, dietilentriamina, trietilentetramina, 2,4 - bis(dimetilaminometil)fenol y 2,4,6 tri(dimetilaminometil)fenol. Todas las bases tienden a acelerar la velocidad de gelificación por calor de los resoles de fenol - formaldehı́do, pero el efecto es más pronunciado con las resinas esterificadas. Debido al actual énfasis puesto en relación con el ahorro de energı́a, la aceleración del curado por calor y, lo que es más importante, el causar la gelificación a temperatura ambiente son propiedades importantes de los materiales de la presente invención. La velocidad de reacción entre la base y el compuesto fenólico que contiene metilol esterificado se influencia, entre otros, por la solubilidad y por la funcionalidad de la base y, cuando la base es un material alcalino inorgánico, por la posición del catión en la serie electroquı́mica. Según los hallazgos de los autores de esta invención, en general la velocidad de reacción entre la base y el compuesto fenólico que contiene metilol esterificado, cuando la base es una amina secundaria, es más baja que si la base en una amina terciaria que, a su vez, es más baja que cuando la base es un óxido o hidróxido de un metal alcalino o alcalino - térreo. Los autores de esta invención han descubierto que óxidos e hidróxidos de metales alcalinos y alcalino - térreos pueden dar lugar a un curado extremadamente rápido, a temperatura ambiente, de algunas resinas de resoles fenólicos que contienen metilol esterificado. Sin embargo, hay algunas aplicaciones en las que puede ser útil o deseable hacer que el compuesto fenólico que contiene metilol esterificado experimente el curado sólo lentamente, quizás sólo a temperaturas elevadas, y en tales aplicaciones pueden usarse las aminas secundarias y terciarias que reaccionan más lentamente. 8 ES 2 059 792 T3 5 10 15 Hay una aplicación particular en la que el uso de una base de Mannich como material básico en la presente invención, supone ciertas ventajas. Este es el caso en la producción de resinas fenólicas curadas que tienen un contenido reducido de iones inorgánicos, especialmente cationes metálicos, y que, por tanto, son más eléctricamente aislantes. Además, los autores de esta invención han descubierto que la presencia de agua u otro disolvente polar no es necesaria para que la reacción prosiga en el caso en el que la base empleada es una base de Mannich. Consiguientemente, la presente invención, en un aspecto adicional, proporciona un método de producir una resina fenólica curada que tiene un contenido reducido de iones inorgánicos, reacción que comprende (1) un compuesto fenólico esterificado que comprende un derivado que contiene grupos metilol esterificados, de un producto de reacción de condensación obtenido por reacción de dos o más moléculas de un fenol mononuclear y una o más moléculas de un aldehı́do o cetona reactivos con fenol, derivado que contiene uno o más grupos hidroxilo fenólicos y/o uno o más grupos hidroxilo fenólicos esterificados y que contiene uno o más grupos metilol esterificados en posición orto y/o para con respecto a un grupo hidroxilo fenólico o grupo hidroxilo fenólico esterificado, y (2) una base de Mannich. Preferiblemente, la base de Mannich es 2,4,6 - tri(dimetilaminometil)fenol. 20 25 30 35 40 45 50 55 60 Los autores de esta invención han descubierto que cuando se emplea (en presencia de agua u otro disolvente polar) un compuesto básico de metal alcalino - térreo, especialmente un óxido o hidróxido de magnesio o calcio, para saponificar el compuesto fenólico esterificado, se produce una resina fenólica gelificada que tiene buena resistencia de gel. Ası́, en una realización preferida, la base usada en la presente invención será un óxido o hidróxido de magnesio o calcio. Aunque no se desea sustentar ninguna teorı́a particular, se considera que las altas resistencias de gel obtenidas por el uso de un compuesto básico alcalino - térreo resultan, por lo menos parcialmente, de una interacción de “puenteo” electrónica entre el ion metálico bivalente alcalino - térreo y los grupos hidroxi de los materiales fenólicos. Esto parece inducir una copulación extra entre las moléculas de la resina fenólica, fomentando con ello un gel más duro. Este efecto sorprendentemente no queda restringido a los compuestos fenólicos esterificados que comprenden fenoles di - o poli - nucleares que contienen una pluralidad de grupos metilol esterificados, sino que también se observa cuando el compuesto fenólico esterificado es un fenol mononuclear, según se ha descrito anteriormente, que contiene uno o más grupos metilol esterificados. Ası́, en un aspecto adicional, la presente invención proporciona un método de preparar una composición de una resina fenólica que comprende hacer reaccionar un compuesto fenólico que comprende un fenol mononuclear esterificado que contiene uno o más grupos hidroxilo fenólicos y/o uno o más grupos hidroxilo fenólicos esterificados y que contiene, además, uno o más grupos metilol esterificados unidos al anillo aromático en una posición orto y/o para con respecto a un grupo hidroxilo fenólico o un grupo hidroxilo fenólico esterificado, con un compuesto básico de un metal alcalino - térreo en presencia de agua y/u otro disolvente polar. La presente invención proporciona también el uso, como un precursor quı́mico de una resina fenólica gelificada, de un fenol mononuclear esterificado que contiene uno o más grupos hidroxilo fenólicos y/o uno o más grupos hidroxilo esterificados y que contiene, además, uno o más grupos metilol esterificados unidos al anillo aromático en una posición orto y/o para con respecto a un grupo hidroxilo fenólico o un grupo hidroxilo fenólico esterificado, formando el citado fenol mononuclear esterificado una resina fenólica gelificada por reacción con un compuesto básico alcalino - térreo en presencia de agua y/u otro disolvente polar. Normalmente, la base se empleará en una cantidad que quı́micamente (estequiométricamente) es equivalente al contenido de grupos éster del compuesto fenólico (± 10%). Sin embargo, en algunas aplicaciones, puede ser necesario o deseable tener presentes ésteres libres y, en otros casos, puede estar presente un exceso de base. En el caso en el que la base usada en la presente invención es un compuesto de metal alcalino, la relación molar del fenol total:metal alcalino total en la composición estará tı́picamente en el intervalo de 1:0,3 a 1:1,4. El uso de cualquier relación más alta puede dar como resultado una reacción demasiado rápida, en tanto que relaciones menores que 0,3 moles de álcali por mol de fenol puede dejar éster sin reaccionar y, por tanto, dar lugar a resistencias finales más bajas. Preferiblemente, la relación molar de fenol total: álcali total en la composición estará en el intervalo de 1:0,5 a 1:1,1. De lo anterior, se comprenderá que bases relativamente débiles, por ejemplo hidróxido cálcico o magnésico, puedan usarse para saponificar las resinas fenólicas que contienen metilol esterificado que, por saponificación a temperatura ambiente, forman composiciones de resinas fenólicas curadas. Según se ha mencionado previamente, tales bases relativamente débiles no producen composiciones satisfactorias a temperatura ambiente cuando se usan en el curado con ésteres según la técnica anterior, de resinas fenólicas alcalinas. Puesto que estas bases relativamente débiles forman sales con el componente ácido de un éster liberado por saponificación del compuesto fenólico que contiene metilol esterificado, sales que son menos solubles que las correspondientes sales de sodio y potasio, el uso de bases relativamente débiles en la presente invención hace posible formar composiciones de resinas fenólicas que tienen una reducida 9 ES 2 059 792 T3 extraibilidad por agua. 5 10 15 20 25 30 35 40 45 50 55 60 En el primer aspecto de la invención descrito previamente, el compuesto fenólico esterificado se hace reaccionar con una composición de resina de resol fenólico no esterificada y una base en presencia de agua y/u otro disolvente polar. El compuesto fenólico esterificado se usará en la ejecución de este primer aspecto de la presente invención en una cantidad tı́picamente de 10 - 120% en peso, basado en el peso de la resina de resol fenólico no esterificada. Preferiblemente, la cantidad de compuesto fenólico esterificado usada será de 30 - 80% en peso de la resina de resol fenólico no esterificada. Resinas de resol se producen por reacción de un fenol y un exceso molar de un aldehı́do reactivo con fenoles, tı́picamente en presencia de un compuesto de metal alcalino o alcalino - térreo como catalizador. Los métodos para preparar resinas de resol fenólicas son bien conocidos y no es preciso describirlos aquı́ con detalle. Tı́picamente, la resina de resol será una resina de fenol - formaldehı́do, producida al hacer reaccionar fenol y formaldehı́do en una relación molar (fenol:formaldehı́do) en el intervalo de 1:1 a 1:3. La resina de resol fenólica no esterificada se usará usualmente en solución, especialmente como una solución acuosa de la sal de metal alcalino de la resina resol de fenol - formaldehı́do. Según los diversos aspectos y realizaciones de la invención, también pueden incorporarse otros aditivos con el compuesto fenólico esterificado, el material básico y/o con el disolvente acuoso o polar. Particularmente útiles son soluciones de materiales que podrı́an co - reaccionar con los compuestos fenólicos que contienen metilol esterificado o con los materiales fenólicos resultantes de la saponificación de los ésteres. Además de las soluciones acuosas de sales de metales alcalinos de resinas de resol fenólico ya mencionadas, se podrı́a incorporar ventajosamente con los otros componentes un material polı́mero, tal como poli(alcohol vinı́lico), celulosa y caseı́na. Además, también puede incorporarse un silano, tal como gamma - aminopropiltrietoxisilano, para fomentar la adhesión, particularmente en aplicaciones tales como la producción de moldes y machos de fundición, en los que la resina fenólica se usa como un aglutinante para un material refractario granular. Todavı́a en una realización adicional de la invención, un resol fenólico no esterificado puede combinarse con álcali y agua y mezclarse con una resina fenólica que tiene metilol esterificado en el momento de usarlos. Un proceso de este tipo puede dar lugar a una gelificación casi instantánea, incluso a temperatura ambiente. Consiguientemente, este proceso puede emplearse convenientemente en procedimientos tales como el denominado “procedimiento de aplicación por separado” para unir superficies. En este procedimiento, un primer componente de un sistema que comprende dos ingredientes mutuamente reactivos, se aplica en forma de una pelı́cula fina a una de las superficies a unir, en tanto que el segundo componente se aplica a la otra cara a unir. La adhesión se efectúa reuniendo rápidamente las dos superficies con presión. Este procedimiento tiene la ventaja de que se superan las restricciones en cuanto a la duración en el tiempo de manipulación al tiempo que se conservan tiempos de endurecimiento cortos a bajas temperaturas. En la anterior realización según la invención, el segundo componente es convenientemente una solución acuosa alcalina de una resina resol de fenol - formaldehı́do, preferiblemente en forma de una solución acuosa de hidróxido potásico o sódico. Como es bien conocido en la técnica de las resinas fenólicas, en algunas aplicaciones el curado rápido de una resina fenólica puede ser una desventaja y se realizan etapas para rebajar y controlar la velocidad de curado de la resina fenólica. Por ejemplo, en la producción de moldes y machos de fundición a partir de una composición de arena para fundición que contiene un aglutinante de resina y un agente de curado para la resina, la composición de arena debe tener una vida en el banco de trabajo suficientemente larga, es decir, debe permanecer manipulable durante un tiempo suficientemente largo para permitir la fabricación de los moldes o machos. Sin embargo, puede darse el caso de que una resina de resol fenólico que contiene metilol esterificado cure demasiado rápidamente en presencia de una base y agua u otro disolvente polar, para que sea manipulable durante un tiempo suficientemente largo para algunas de tales aplicaciones. Este problema puede superarse utilizando una combinación de una resina resol fenólica que contiene metilol esterificado y un agente de curado tipo éster convencional para curar en condiciones alcalinas, una resina resol de fenol - formaldehı́do no esterificada. Parece ser que la velocidad de curado de la resina de resol no esterificada por el éster fenólico puede ser rebajada y, por tanto, ser controlada por el uso simultáneo de agentes de curado tipo éster convencionales, tales como diacetina, triacetina, diacetato de etilenglicol, diacetato de propilenglicol, acetato de butilenglicol, carbonatos orgánicos (por ejemplo, carbonato de propileno) y lactonas (por ejemplo propiolactona, butirolactona, valerolactona y caprolactona). Con objeto de asegurar la homogeneidad de la mezcla de reacción, la resina fenólica que contiene metilol esterificado deberı́a añadirse a la mezcla en forma de una solución en el agente de curado tipo éster convencional. Además de la notable velocidad de reacción que se puede lograr usando las resinas fenólicas que contienen metilol esterificado y de su capacidad de gelificar a temperatura ambiente en presencia de bases más débiles que las requeridas por los resoles fenólicos curados con ésteres independientes de la técnica anterior, las composiciones según la invención tienen un cierto numero de otras propiedades que las distinguen claramente de las composiciones conocidas hasta ahora. 10 ES 2 059 792 T3 5 10 15 20 25 30 35 40 45 Los productos conocidos preparados al emplear un éster independiente para curar resoles fenólicos alcalinos son invariablemente de un color rojo oscuro. Usando el procedimiento de la invención pueden prepararse productos casi incoloros o blancos o ligeramente coloreados. Esto es importante en determinadas aplicaciones de la presente invención en las que se exige que los productos tengan una estética atractiva, por ejemplo en muchas aplicaciones de revestimiento de superficies, coladas decorativas, adhesivos para estratificados y aplicaciones de adhesivos en las que existe la posibilidad de “sangrar” una superficie visible. Aunque previamente se han producido resinas fenólicas ácidas de color tenue, con las limitaciones que ello conlleva, los autores de esta invención suponen que esta propiedad no se ha obtenido anteriormente con resinas fenólicas alcalinas. Los ésteres de resinas fenólicas que contiene grupos metilol son generalmente insolubles en agua. Sin embargo, los autores de esta invención han descubierto que la reacción de curado con bases no se produce o se produce menos rápidamente o de forma menos completa en ausencia de agua u otro disolvente polar que es necesario para la etapa de saponificación inicial. Ası́, según otra realización, la invención proporciona una composición que comprende una resina fenólica que contiene metilol esterificado, en condiciones esencialmente anhidras, y una base esencialmente anhidra, tal como óxido cálcico u óxido magnésico, composición que es capaz de formar una composición de resina fenólica curada cuando se pone en contacto con agua. Poniendo en contacto la mezcla anhidra con agua puede iniciarse una reacción rápida. Este contacto con agua puede efectuarse utilizando aire húmedo o vapor de agua. Por tanto, se entenderá que esto constituye la base de una técnica de curado con un gas o con vapor para el curado de composiciones de resinas fenólicas. Esta realización tiene una aplicación práctica en la producción de revestimientos superficiales curables en húmedo. Una aplicación adicional de la presente invención que hace uso de la capacidad de una composición que comprende una mezcla de una resina fenólica que contiene grupos metilol esterificados, en estado anhidro, y una base anhidra para formar una resina fenólica curada cuando se pone en contacto con vapor de agua o vapor, es en la producción de moldes y machos de fundición. Ası́, según todavı́a una realización adicional, la presente invención proporciona un método para producir moldes y machos de fundición, que comprende mezclar un material refractario granular que no contiene sustancialmente humedad, con una cantidad eficaz para unir dicho material refractario granular de una resina fenólica anhidra que contiene metilol esterificado y con una cantidad eficaz para saponificar dicha resina fenólica que contiene metilol esterificado, de una base anhidra, dar a la mezcla la forma deseada y luego hacer pasar vapor de agua y/o vapor a través de la mezcla conformada, con lo que la base y la resina fenólica que contiene metilol esterificado reaccionan entre sı́ en presencia de humedad para formar una resina fenólica curada que une el material refractario granular. En esta realización, el material refractario granular es tı́picamente una arena para fundición que se deshidrata sustancialmente antes de mezclarla con los otros componentes. Muchos tipos de arena usados convencionalmente en la producción de moldes y machos de fundición son básicos de por sı́ y, si tales arenas alcalinas se usan en la realización de la presente invención antes descrita, en la mezcla usada para hacer el molde y macho de fundición puede omitirse la adición de una base anhidra por separado. Según se ha indicado anteriormente, para efectuar el curado de la resina fenólica, la mezcla se gasifica con vapor de agua y/o vapor. La gasificación se logrará tı́picamente aspirando el vapor y/o vapor de agua obtenido a partir de un generador de vapor a través de la mezcla conformada de arena, resina esterificada y base en una caja de machos provista de placas perforadas, mediante la aplicación de un vacı́o en una de las placas perforadas. Al contrario que en otras técnicas de curado por gases, usadas en la producción de moldes y machos de fundición, la realización de la presente invención descrita precedentemente evita el uso de catalizadores de gasificación nocivos, inflamables y relativamente caros, para efectuar el curado del aglutinante de resina fenólica. 50 Las composiciones de la invención, según se describen anteriormente, tienen muchas y diversas aplicaciones que incluyen revestimientos, coladas, aglutinantes para uso en fundición, aglutinantes refractarios y adhesivos para madera y componentes metálicos. Además, las composiciones pueden ser espumadas según técnicas conocidas por la técnica. 55 En el caso de la fabricación de moldes y machos de fundición, una cantidad principal de un material refractario granular, tal como arena, puede ser mezclada con una cantidad secundaria de una resina de resol fenólico no esterificada y un compuesto fenólico esterificado según se describe aquı́, en presencia de una base y agua y/u otro disolvente polar, con lo que la resina de resol fenólico no esterificada y el compuesto fenólico esterificado reaccionan para producir una composición de resina fenólica curada que une el material refractario granular. Tı́picamente, aunque no esencialmente, la cantidad de resina de resol fenólico no esterificado usada estará en el intervalo de 0,1 a 10% en peso, basado en el peso del material refractario granular y la cantidad de compuesto fenólico esterificado usada estará en el intervalo 60 11 ES 2 059 792 T3 5 10 de 10 a 120% en peso, basada en el peso de la resina de resol fenólico. Cuando el compuesto fenólico esterificado es un derivado, que contiene grupos metilol esterificados, de un producto de condensación di - o poli - nuclear de un fenol y un aldehı́do o cetona reactivos con fenol, es posible hacer moldes o machos de fundición según lo anterior sin necesidad de una resina de resol fenólico no esterificada. En tal caso, la cantidad de compuesto fenólico esterificado usado, en general pero no esencialmente, estará en el intervalo de 0,1 a 10% en peso, basada en el peso del material refractario granular. Se apreciará que la cantidad real de resina fenólica (ya sea no esterificada o con contenido de grupos metilol esterificados), requerida para añadir al material refractario granular, dependerá de un cierto número de factores que incluyen el peso molecular de la resina, la naturaleza del compuesto fenólico esterificado y el tipo y la cantidad de la base. Para usarlos en la ilustración de la invención, se prepararon los ésteres siguientes: Los productos A a E son compuestos y resinas de fenol - formaldehı́do que contienen grupos metilol. 15 Los productos I a XI son ejemplos de ésteres fabricados a partir de compuestos que llevan grupos metilol usando diversos reactivos y procesos. 20 Los Ejemplos 1 a 12 y los Ejemplos de Aplicación 1 a 8 ilustran la invención y ejemplifican la polimerización de los ésteres fenólicos en presencia de materiales alcalinos. Preparación de los productos que contienen grupos metilol para la esterificación Producto A 25 Saligenina Saligenina (ortometilolfenol, 2 - (hidroximetil)fenol) 30 Este producto se usó tal y como se adquirió de Aldrich Chemical Company Producto B Resol de fenol - formaldehido (relación molar F:P = 1,6:1; Sólidos = 70%) 35 40 45 Fenol (1 mol) y formalina al 50% (0,6 moles) se cargaron en un recipiente de reacción y la temperatura se mantuvo por debajo de 40◦ C al tiempo que se añadı́a hidróxido sódico (0,004 moles). A continuación, se elevó la temperatura hasta 80◦ C. La temperatura se mantuvo a 80◦ C mientras se añadı́a lentamente una segunda carga de formalina al 50% (1,0 mol) a lo largo de 30 minutos y la temperatura se mantuvo a 80◦ C durante 15 minutos más. Luego se mantuvo la mezcla a 70◦C durante 30 minutos más. El pH se ajustó con una solución de ácido p - toluensulfónico a 4,0 +/ - 0,2 y los componentes volátiles se separaron por destilación en vacı́o a 70◦C hasta una viscosidad de 80 centistokes a 25◦ C. Se enfrió la resina hasta 60◦C, se ajustó el pH a 6,2 +/ - 0,2 con hidróxido sódico, se añadieron 0,027 moles de urea y después se concentró adicionalmente el producto hasta una viscosidad final de 500 cP a 25◦ C, se enfrió y se descargó. Producto C Resol de fenol - formaldehido (relación molar F:P = 2,5:1; Sólidos = 77%) 50 55 Fenol (1 mol) y de formaldehı́do al 50% (0,6 moles) se cargaron en un recipiente de reacción y se mantuvo la temperatura por debajo de 40◦C al tiempo que se añadı́a óxido magnésico (0,03 moles) y se dispersaba bien. Luego se dejó que la temperatura se elevara a 70◦ C a lo largo de 30 minutos y se mantuvo a esta temperatura mientras se añadı́a lentamente una segunda carga de formaldehı́do al 60% (1,9 moles) a lo largo de una hora y luego se la mantuvo durante 30 minutos más. A continuación, se bajó la temperatura hasta 55◦C y se inició la destilación en vacı́o hasta que se obtuvo una viscosidad de 85 cSt a 25◦C, luego se elevó la temperatura de nuevo a 80◦ C y se mantuvo durante una hora, se enfrió luego la resina a 65◦C y se mantuvo hasta que la dilución en agua era de 1:4 a 25◦ C. A continuación, se enfrió el producto a temperatura ambiente y se descargó . 60 12 ES 2 059 792 T3 Producto D Resol de fenol - formaldehido (relación molar F:P = 2,0:1; Sólidos = 65%) 5 10 Fenol (1,0 mol) y una solución de formaldehı́do al 50% (0,6 moles) se cargaron en un recipiente de reacción y se mantuvo la temperatura a 44◦C mientras que se añadı́a hidróxido sódico al 50% (0,04 moles). Luego se calentó la mezcla a 80◦ C y lentamente se añadió una segunda carga de solución de formaldehı́do al 50% (1,4 moles) a lo largo de 25 minutos. A continuación, se mantuvo la mezcla a 80◦ C hasta que la viscosidad alcanzó 550 cP (alrededor de 6 horas). Finalmente, se enfrió el producto a temperatura ambiente y se descargó. Producto E fenol - formaldehido resol Relación molar f:p = 1,81:1; sólidos = 60,5%) 15 20 25 Un reactor se cargó con 1.061,9 g (11,30 moles) de fenol y 95,55 g (0,768 moles) de una solución acuosa al 45% de hidróxido potásico. Esta mezcla se calentó a 60◦ C, luego se añadieron 1.225,7 g (20,43 moles) de una solución acuosa caliente de formaldehı́do al 50%, a lo largo de 30 minutos, mientras que la temperatura de la mezcla de reacción se elevaba a 105◦C. A continuación, se enfrió la mezcla de reacción y se mantuvo a 75◦C - 80◦C hasta que se alcanzó una viscosidad Gardner (25◦C) de T - U (aproximadamente 600 centistokes). Luego, la solución de resinas se enfrió rápidamente a temperatura ambiente. El rendimiento de la solución de resinas era 2.263 g. El contenido de agua, determinado por la titulación de Karl Fisher, resultó ser 32,1%. El contenido de fenol libre era 2,3%. El contenido de sólidos, determinado por secado en estufa a 135◦C, era 60,5%. EL producto era un resol hecho a partir de una mezcla de reacción que tenı́a una relación molar F:P de 1,81:1 y una relación molar de potasio: fenol (K:P) de 0,068:1. Esterificación de los compuestos fenólicos con grupos metilol 30 Producto I Monoacetato de saligenina 35 40 Anhı́drido acético (59 g, 0,58 moles) se mezcló con piridina (50 g) y el Producto A (72 g, 0,58 moles) se añadió lentamente con agitación y enfriando para prevenir que la temperatura excediera de 50◦ C. Se permitió que la mezcla reposara durante una noche a temperatura ambiente y después se vertió en un gran exceso de agua frı́a. Se añadió dietiléter y el producto de reacción extraı́do se lavó luego con agua, ácido clorhı́drico al 1% y de nuevo con agua. Se secó la capa orgánica y el éter se separó en vacı́o dejando un aceite amarillo pálido. Producto II Metacrilato de saligenina 45 50 El producto A (13,5 g, 0,11 moles) se disolvió en piridina (8,6 g) y diclorometano (200 ml). Cloruro de metacriloı́lo (11,4 g, 0,11 moles) en diclorometano (50 ml) se añadió lentamente con agitación, mientras que la temperatura se mantenı́a por debajo de 40◦C. La mezcla se dejó reposar durante una hora más y luego se sometió a reflujo durante 20 minutos. El producto se enfrió, se lavó con agua, ácido diluido y de nuevo con agua, se secó sobre sulfato sódico anhidro y se evaporó en vacı́o para separar el disolvente. Producto III Producto B formilado 55 60 Acido fórmico (46 g) y anhı́drido acético (102 g) se mezclaron lentamente mientras que la temperatura se mantenı́a por debajo de 45◦ C. Se dejó reposar la mezcla durante una hora a 45◦C y a continuación se añadió con precaución a una mezcla del producto B (100 g) más piridina (7,9 g) mientras estaba sumergida en un baño de hielo/agua para mantener la temperatura por debajo de 20◦C. Después, se dejó que la mezcla reposara durante una noche a temperatura ambiente. A continuación, se añadió acetato de etilo a la mezcla, que se lavó varias veces con agua, luego con ácido diluido y finalmente de nuevo con agua, se secó la fase orgánica, se filtró y se evaporó hasta sequedad. Se obtuvo un lı́quido viscoso, de 13 ES 2 059 792 T3 color pajizo (formiato del Producto B). Producto IVa 5 10 Producto C parcialmente acetilado El producto C (50 g) y piridina (75 g) se mezclaron y se añadió con cuidado anhı́drido acético (25 g) con agitación, manteniendo la temperatura por debajo de 40◦ C. Se dejó reposar la mezcla durante una noche y después se vertió en un gran exceso de agua helada. Se añadió acetato de etilo y el producto se extrajo, se lavó varias veces con agua, ácido diluido y finalmente con agua de nuevo. La capa orgánica se secó y el disolvente se separó en vacı́o. Producto IVb 15 Producto C muy acetilado Se repitió el proceso descrito para la preparación del Producto IVa, pero usando el Producto C (50 g), piridina (75 g) y anhı́drido acético (50 g). 20 Producto IVc Producto C acetilado (usando cetena) 25 El producto C (resol de fenol - formaldehı́do de una relación molar F:P de 2,5:1) (400 g) se disolvió en acetona (100 ml) y se agitó continuamente mientras que cetena, generada in situ con una bombona de cetena, se hacı́a pasar durante 6 horas a 0,5 moles por hora. El producto se extrajo en acetato de etilo, se lavó varias veces con agua, luego con ácido diluido y finalmente con agua de nuevo. La capa orgánica se secó y el disolvente se separó en vacı́o. Se obtuvo un ı́ndice de saponificación de 6,3 x 10−3 moles por gramo. 30 Producto V Producto C formilado 35 Se siguió el proceso descrito para la preparación del Producto III, excepto que se usó el Producto C (200 g) en lugar del Producto B. Producto VI 40 45 Producto D acetilado (usando cetena) El producto D (90 g) se disolvió en acetona (100 ml) y se agitó continuamente mientras que cetena (generada in situ usando una bombona de cetena) se hacı́a pasar durante 2 horas a una velocidad de 0,5 moles por hora. El producto se extrajo en acetato de etilo, se lavó varias veces con agua, luego se lavó con ácido diluido y luego se lavó nuevamente con agua. A continuación, se secó la capa orgánica y el disolvente se separó en vacı́o. Producto VII 50 55 60 Salicilato de saligenina Cloruro de tionilo ( 1 mol) en diclorometano (400 ml) se añadió gota a gota y con agitación constante a una dispersión de salicilato sódico (1 mol) en diclorometano (800 ml). Se agitó la mezcla durante una hora más, luego se dejó enfriar a temperatura ambiente, teniendo cuidado de evitar la absorción de la humedad atmosférica. Esta solución se añadió luego gota a gota y con agitación vigorosa a una solución del Producto A (1 mol) y piridina (2 moles) en diclorometano (1.200 ml). Después de completada la adición, se calentó la mezcla a 40◦C, se mantuvo a esta temperatura durante 10 minutos y después se dejó enfriar. Luego la mezcla de reacción se lavó varias veces con agua y ácido diluido hasta que no quedaron trazas de piridina. Luego la fase orgánica se secó sobre sulfato sódico anhidro, se filtró y se eliminó el disolvente para obtener salicilato de saligenina con unrendimiento de 60%. 14 ES 2 059 792 T3 Producto VIII Diacetato de saligenina 5 10 Anhı́drido acético (82,3 g, 0,806 moles) se mezcló con piridina (130 g) y se añadió Producto A (50 g, 0,403 moles) lentamente con agitación y enfriando para evitar que la temperatura excediera de 50◦ C. Se dejó reposar la mezcla durante una noche a temperatura ambiente y después se vertió en un gran exceso de agua frı́a. Se añadió dietiléter y el producto de reacción se extrajo, se lavó con agua, luego se lavó con ácido clorhı́drico al 1% y luego se lavó de nuevo con agua. Se secó la capa orgánica y el éter se separó en vacı́o dejando un aceite amarillo pálido. Producto IX Diacetato de 2,6 - dimetilol - p - cresol 15 El diacetato de 2,6 - dimetilol - p - cresol (DMPC) se preparó haciendo reaccionar 3,4 g del dimetilolcresol con 4,8 g de anhı́drido acético en presencia de 7,8 g de tetrahidrofurano. 20 Después de 66 horas a temperatura ambiente, la solución de reacción se diluyó con 5 g de dicloruro de metileno, luego se lavó varias veces con 15 ml de agua frı́a. Una capa orgánica de aproximadamente 10 g se secó con 2 g de sulfato sódico anhidro. Producto X 25 30 Diacetoacetato de 2,6 - dimetilol - para cresol (DMPC) utilizando dicetena Un recipiente de reacción se cargó con 3,4 g (0,02 moles) de DMPC en 5 g de tetrahidrofurano y 0,1 g de acetato sódico anhidro. Después de que estos ingredientes se cargaron en el reactor, se añadieron 3,4 g (0,04 moles) de dicetena. Esta mezcla se agitó mientras se mantenı́a a 25◦ - 35◦ C mediante un baño de agua, durante unas 4 horas. Al cabo de este tiempo, la mezcla de reacción era esencialmente homogénea. El producto resultante era el éster di(acetoacético) de DMPC. Producto XI 35 40 45 Formiato de saligenina El formiato de saligenina se producı́a por reacción de saligenina con formiato de metilo. Ası́, 5,0 g de saligenina y 20 g de formiato de metilo, junto con 0,1 g de imidazol, se cargaron en un matraz de reactor que estaba provisto de una varilla de agitación. Se permitió que la mezcla reposara durante dos dı́as a temperatura ambiente. A la mezcla de reacción se aplicó después un vacı́o suave a temperatura ambiente, mientras que la mezcla se agitaba usando la varilla de agitación, para eliminar los componentes volátiles. El rendimiento del producto no volátil era 6,3 g, una ganancia de 1,3 g si se compara con la ganancia teórica posible de 2,5 g. El formiato de metilo recuperado se devolvió al matraz y el contenido del reactor se dejó reposar durante tres dı́as a temperatura ambiente. A continuación, se eliminaron los componentes volátiles hasta que el peso del matraz permanecı́a constante. EL rendimiento del producto sólido húmedo, no volátil era 6,8 g, con una ganancia total de 1,8 g. Suponiendo que no hubo reacciones secundarias, esto representaba una conversión de 70% aproximadamente. 50 Mediante tratamiento de una muestra con sosa cáustica al 20% en N,N - dimetilacetamida, la muestra de producto se hizo heterogénea y eventualmente se separó en dos capas. La capa superior tenı́a un ligero color ámbar y tenı́a un volumen aproximadamente el doble que el de la capa inferior. La capa inferior era casi incolora. La capa superior tenı́a una consistencia similar a la de un almı́bar medio para tortas. 55 Ejemplos de composiciones segun la invención 60 En los ejemplos que siguen, en los que se toma la dureza Shore D del gel, ésta se midió utilizando un durómetro Shore D de Bareiss (Bareiss AG,, 7938 Oberdisdingen, Alemania) según se describe en la norma DIN 53 505 (ISO Standard R 868). Se obtuvo un tiempo de gelificación aproximado mezclando 4,0 gramos del compuesto fenólico esterificado con cantidades apropiadas de material alcalino y agua (cuando habı́a de usarse) y observando el tiempo transcurrido para formar un gel. La observación se realizó, a no 15 ES 2 059 792 T3 ser que se indique otra cosa, a una temperatura ambiente de 20◦C aproximadamente. Ejemplo 1 5 10 15 10 g del Producto IVa (Producto C acetilado) se mezclaron con 5 ml de solución de hidróxido potásico al 45%. Esto daba un tiempo de gelificación de 30 segundos y una dureza después de 26 horas a 20◦ C de 45 - 50. Con fines comparativos, 10,0 g del Producto C que contenı́an 1,8 g de agua, se mezclaron con 3,2 ml de solución acuosa de hidróxido potásico al 70% y 3 g de triacetina. Esto daba un tiempo de gelificación de aproximadamente 24 horas y una dureza de menos de 10 después de 170 horas. El tiempo de gelificación más rápido y la dureza incrementada del éster de acetato del Producto C con respecto al Producto C con éster independiente demuestra las ventajas del producto según la invención con respecto al producto según la técnica anterior. Ejemplo 2 20 4,0 g del éster acetato del Producto C (Producto IVa), mezclados con 1,04 g de óxido cálcico y 1 g de agua, dieron un tiempo de gelificación de 30 segundos y una dureza de 75 después de 170 horas a 20◦ C. Por comparación, era difı́cil agitar el óxido cálcico en una mezcla del Producto C y triacetina, ya que se producı́an grumos pequeños. Se obtuvo un producto no homogéneo que contenı́a grumos de gel en la resina lı́quida. 25 30 La presente invención demuestra la ventaja que supone el uso de álcalis de metales alcalino - térreos para preparar productos útiles. De hecho, el material gelificado producido en este ejemplo demuestra una dureza mayor que la indicada en el Ejemplo I y se supone que esto es debido, en parte, a algún tipo de interacción electrónica entre el metal bivalente y los grupos hidroxi de los compuestos fenólicos. Esto parece inducir una copulación extra entre las moléculas de resina fenólica dando lugar con ello a un gel más duro. Ejemplo 3 35 40 4 g de monoacetato de saligenina (Producto I) se mezclaron con 0,67 g de óxido cálcico y se añadieron 0,5 g de agua. Se obtuvo un tiempo de gelificación de 60 segundos y una dureza, después de 144 horas, de 34. Este compuesto modelo, debido a la baja relación F:P y al relativamente bajo peso molecular, no serı́a de esperar que formara un producto gelificado a través de las reacciones de los grupos metilol solos. Utilizando óxido cálcico como el agente de curado alcalino se obtiene una considerable resistencia del gel, ilustrando una vez más la ventaja de emplear álcalis de metales bivalentes. Ejemplo 4 45 4,0 g de éster acetato del Producto C (Producto IVa), mezclados con 0,77 g de óxido magnésico y 1 g de agua, daban un tiempo de gelificación de 10 - 12 horas, pero tenı́a una dureza de 65 - 70 después de 170 horas a 20◦ C. 50 La elevada dureza del producto indica de nuevo la contribución, por interacciones electrónicas, del metal bivalente y los grupos hidroxi de los materiales fenólicos. Los ejemplos 2 y 4 ilustran una importante caracterı́stica de la invención, que es la capacidad para ajustar la reactividad del sistema empleando álcalis diferentes como agentes de curado, al tiempo que se conserva un producto de dureza útil. 55 Ejemplo 5 4 g de éster formiato del Producto C (Producto V), mezclados con 0,75 g de óxido cálcico y 0,5 g de agua, daban un tiempo de gelificación de 1 minuto y una dureza de 75 - 80 después de 96 horas a 20◦C. 60 La comparación con el Ejemplo 2 demuestra que la función ácido del éster puede variarse sin comprometer la dureza del gel producido. 16 ES 2 059 792 T3 Ejemplo 6 4 g de éster acetato del Producto C (Producto IVc), mezclados con 1,5 g de óxido cálcico y cantidades variables de agua. 5 10 15 Agua añadida Tiempo de gelificacion 0,28 g 0,036 g 30 segundos 45 minutos La presente invención permite que se pueda variar la reactividad del sistema por adición de agua u otro disolvente polar adecuado. Ejemplo 7 20 25 4 g de éster formiato del Producto B (Producto III), mezclados con 1,5 g de 2,4,6 tri(dimetilaminometil)fenol, daban un tiempo de gelificación de 2 - 3 minutos y una dureza de 60 después de 72 horas. En un experimento diferente, 4 g del Producto III se mezclaron con 1,5 ml de una solución (acuosa) de amonı́aco al 35%. La mezcla de reacción solidificó en 1 minuto desde 20◦C con una reacción ligeramente exotérmica para formar un gel blando. Ejemplo 8 30 4 g de metacrilato de saligenina (Producto II), mezclados con 0,58 g de óxido cálcico seguidos por 0,5 g de agua, daban un tiempo de gelificación de 1 minuto y una dureza de 50 - 60 después de 24 horas. Ejemplo 9 35 4 g del Producto C, tomados con diferentes grados de acetilación (Productos IVa y IVb), cuando se mezclan con 0,75 g de óxido cálcico y 0,5 g de agua, daban tiempos de gelificación de 30 segundos y de 3 minutos, respectivamente. El grado de esterificación puede usarse para variar las propiedades del sistema cuando sea preciso. 40 Ejemplo 10 45 50 55 60 La Tabla 1 ilustra la mejora en la resistencia a la extracción por agua, obtenida a partir de la resina gelificada mediante el uso de las composiciones según la invención, según se ha contrastado con una resina de fenol - formaldehı́do alcalina de la técnica anterior, curada de una manera tı́pica con un éster convencional. En la realización de los ensayos, muestras de los materiales a ensayar se gelificaron y se dejaron curar durante 10 dı́as a 20◦ C, después de lo cual se molieron y se tamizaron para proporcionar polvos en el intervalo de 300 a 600 micrómetros. Luego, los polvos se agitaron en 100 ml de agua desionizada y se sometieron a reflujo durante 3 horas. Al cabo de este tiempo, se separó por filtración el material en polvo, se pesó en un crisol tarado de vidrio sinterizado y se secó hasta peso constante a 100◦C. A continuación, las muestras se extrajeron adicionalmente de manera similar, pero sustituyendo el agua por acetona. La resina 1 era un resol de fenol - formaldehı́do catalizado con KOH que tenı́a una relación molar F:P de 2,0:1, una relación molar K:P de 0,745:1 y un contenido de sólidos de 63,5% en peso. La primera anotación en la tabla que sigue tiene fines comparativos solamente y se emplea triacetina (30 gramos sobre 100 gramos de resina) como agente de curado. La segunda anotación demuestra la mejora conseguida empleando la misma resina según la invención, utilizando diacetato de saligenina en lugar de triacetina como agente de curado. 17 ES 2 059 792 T3 RESINA PESO BASE ESTER CANTIDAD DE % DE EXTRACTO % EXTRACTO ESTER EN AGUA EN ACETONA 5 10 15 20 RESINA 1 10 g KOH TRIACETINA 3g 60,2 5,3 (Tiempo de gelificación = 8 - 10 minutos, dureza = 50 - 55 después de 96 horas a 20◦ C) RESINA 1 10 g KOH DIACETATO DE 3g 55,6 4,0 SALIGENINA (Tiempo de gelificación = 10 minutos, dureza = 60 - 65 después de 240 horas a 20◦ C) RESINA 1 10 g KOH SALICILATO DE 4,1 g 48,1 sin resultados SALIGENINA (Tiempo de gelificación = 2 dı́as, dureza = 60 después de 240 horas a 20◦ C) Producto IVa 10 g CaO(4 g) 30,2 3,2 (Tiempo de gelificación = 10 segundos, dureza = 70 - 80 después de 96 horas a 20◦ C) Producto IVa 10 g CaO(3 g) 34,0 sin resultados (Tiempo de gelificación = 10 segundos, dureza = 70 - 80 después de 96 horas a 20◦ C) Producto VI 10 g CaO(4g) 42,2 3,1 (Tiempo de gelificación = 20 segundos, dureza = 70 - 80 después de 96 horas a 20◦ C). Ejemplo 11 25 30 En este ejemplo, el diéster, Producto IX, se evaluó como un reticulante de un resol fenólico alcalino. Demostró que es muy eficaz. Ası́, 3,4 g del Producto E de la resina se mezclaron con 1,0 g de agua y 0,6 g de una solución de KOH al 45%, y se enfrió a temperatura ambiente y luego se mezcló rápidamente con 1,0 g del Producto IX. Esta mezcla solidificó en aproximadamente 30 segundos, a temperatura ambiente. Ejemplo 12 35 40 Se preparó una resina de fenol - formaldehı́do alcalina según las enseñanzas del documento US 4.474.904. Esta resina se caracterizó por una relación molar de formaldehı́do/fenol de 1,8, una relación molar de potasio/fenol de 0,63 y un contenido en sólidos de 50% en peso. 0,6 g de la solución de diacetato de 2,6 - dimetilol - p - cresol, obtenida en el Producto IX, que tenı́a una concentración de aproximadamente 50% se evaporó con una corriente de aire para producir 0,3 g de un residuo oleoso. A este residuo se añadieron 1,2 g de la resina de fenol - formaldehı́do alcalina descrita precedentemente. La resina gelificó inmediatamente. Ejemplos de Aplicaciones 45 Ejemplo de aplicación 1 2 - Revestimiento de superficies de piezas 50 4,0 g del éster acetato del Producto C (Producto IVc) se mezcló con 0,77 g de óxido magnésico y 1 ml de agua y la mezcla se aplicó inmediatamente sobre superficies de madera y de acero dulce. El material residual no gelificó durante 10 horas a 20◦C, pero el revestimiento producido habı́a alcanzado una dureza de lápiz de 2B después de 24 horas y de HB después de una semana a 20◦C. Ejemplo de Aplicación 2 55 60 Revestimiento de superficies que cura con la humedad 4,0 g de éster acetato del Producto C (Producto IVc), que estaba sustancialmente deshidratado, se mezclaron con 0,75 g de óxido cálcico y se extendieron sobre superficies de madera y de acero dulce y se dejó reposar en una atmósfera con alto contenido de humedad a temperatura ambiente. Aunque el material a granel aún permanecı́a lı́quido al cabo de 3 dı́as, el revestimiento habı́a endurecido hasta tomar un acabado opaco brillante después de 10 horas a 20◦ C. Sobre la superficie de acero dulce, el revestimiento alcanzó una dureza de lápiz de HB después de 24 horas y sobrepasó el valor H después de 1 semana a 18 ES 2 059 792 T3 20◦C. Ejemplo de Aplicación 3 5 10 15 20 25 Machos de fundición que curan con la humedad 15 g del éster acetato del Producto D (sustancialmente deshidratado, pero conteniendo 18% de acetona) (Producto VI) se mezclaron con 1 kg de arena de sı́lice Chelford 50 en un mezclador de laboratorio Ridsdale de arena para machos durante 30 minutos. Se añadieron 4,5 g de óxido cálcico y se mezclaron durante 1 minuto. La mezcla se compactó en una caja AFS para machos por compresión en crudo, provista de placas perforadas. Se empleó un generador de vapor aplicando vacı́o a la placa del fondo para succionar vapor de agua a través del macho. Después de hacer pasar vapor durante 30 segundos, el macho habı́a endurecido lo suficiente para poderlo extraer del molde. El macho estaba caliente al tacto, por lo que el curado se aceleró también mediante calor. Después de permanecer durante 2 horas a 20◦ C, el macho tenı́a una resistencia a la compresión de 250 kN/m2 . Aunque se admite que la resistencia es deficiente con relación a patrones convencionales, es válida para ilustrar que el principio de curar con agua es un principio sólido, confirmado por el Ejemplo 6 y el revestimiento de superficies del Ejemplo 2. La mezcla se habı́a endurecido y secado después de 30 minutos a 20◦ C, de modo que ya no era posible volver a utilizarla, mayormente por la evaporación de la acetona. Un macho producido por esta técnica se sumergió en agua frı́a durante 1 hora. Aunque se ablandó ligeramente, retuvo su forma, indicando ası́ que se habı́a logrado un significativo grado de curado. Ejemplo de Aplicación 4 Unión refractaria 30 Las siguientes muestras de material gelificado se sometieron a un análisis termogravimétrico a 750◦C en atmósferas de aire y nitrógeno. Los resultados se incluyen en la Tabla siguiente. TGA a 750◦C 35 Composición % en aire Residuo inorgánico teórico, % % de Carbono que queda en el aire % de N2 25,9 17,6 8,3 43,3 25,7 42,3 9,1 33,2 45,3 36,2 16,1 12,0 4,1 51,9 39,9 22,0 11,1 10,9 54,4 31,1 40 45 50 55 60 Acetato del producto IVb KOH al 50% Acetato del Producto Ivb CaO Agua Formiato del Producto V CaO Agua Formiato del Producto V MgO Agua 4,0 g 1,4 g 4,0 g 0,4 g 0,5 g 4,0 g 0,75 g 0,5 g 4,0 g 0,5 g 0,5 g Rendimiento de Carbono en % Residuo teórico en N2 El éster - formiato se comparaba de la manera esperaba dando principalmente MgCO3 y CaO como residuos de cenizas cuando se pirolizó con aire. El éster acetato con CaO daba rendimientos de carbono similares con aire y con nitrógeno, lo que indica una mejor resistencia a la oxidación. Este factor es de gran importancia en la aplicación de la invención a la fabricación de materiales refractarios, electrodos 19 ES 2 059 792 T3 de carbono aglomerado, etc. Se preparó una mezcla usando: 85 g de magnesia 15 g de grafito 10 g del Producto IVb (éster - acetato) 5 10 15 y se moldeó por compresión en forma de un lingote cilı́ndrico con 30,9 MPa. A la pieza resultante se le permitió curar a temperatura ambiente durante 24 horas, luego se sometió a una etapa de post - curado en una estufa durante 66 horas a 100◦C, seguido de 24 horas a 150◦ C. A continuación, las muestras se calentaron en un horno de mufla a 850◦C durante 5 horas para obtener un material refractario. Las muestras tenı́an un aspecto similar a los lingotes hechos a partir de una solución de resina novolaca en etilenglicol mezclada con hexamina (hexametilentetramina) y curada con calor. La ventaja de los ésteres de resol fenólico de la invención es que el lingote en el estado no calcinado en la estufa, es más estable que uno basado en el sistema novolaca/glicol. 20 Ejemplo de Aplicación 4 Espuma 25 30 4,0 g del éster - formiato del Producto C se mezclaron con 0,5 g de óxido magnésico, 0,1 g de agente tensioactivo DC193 (un producto comercialmente disponible de Dow Corning Corporation que se supone que comprende un polı́mero de silicona - glicol) y 1 g de Arcton II (“Arcton” es una marca comercial registrada) que es un agente de soplado de cloro - fluorocarburo comercialmente disponible de ICI Chemicals & Polymers Ltd). Finalmente, se añadieron 0,5 g de agua. Después de aproximadamente 30 segundos se produjo una reacción exotérmica, la mezcla se cremó y se espumó y poco después gelificó. Después de reposar, se encontró que la espuma tenı́a una densidad de 200 kg/m3 , era resistente y contenı́a algunas celdillas cerradas. Ejemplo de Aplicación 6 35 40 Auto - curado Por colada se produjo una pequeña pieza cilı́ndrica a partir de la composición del Ejemplo 4 y se la dejó curar durante 6 semanas a 15 - 20◦ C. Dio una resistencia a la compresión de 68.200 kNm−2 cuando se ensayó en un tensiómetro Monsanto. El producto presentaba una buena estabilidad dimensional y es útil para aplicaciones de colada en las que comúnmente se usan compuestos fenólicos convencionales endurecidos con ácidos. Ejemplo de aplicación 7 45 50 55 Mezcla para Machos de Fundición 30 g de la Resina 1 (véase el Ejemplo 10 anterior) se mezclaron con 2.000 g de arena de sı́lice Chelford 50 (en donde 50 es el ı́ndice de finura AFS) a 18◦ C en un mezclador de alta velocidad Kenwood Chef, durante 60 segundos. 9 g de un Producto B muy acetilado (éste se habı́a preparado según el proceso establecido para el Producto IVb anterior, excepto que los reaccionantes usados eran el Producto B (135 g), piridina (22 ml) y anhı́drido acético (270 g)) se añadieron a la mezcla de arena/Resina 1 y se mezclaron durante 45 segundos. A continuación, se descargó la mezcla e inmediatamente se hicieron probetas de ensayo para compresión AFS, utilizando un pistón estándar y tubos calibrados. (Las probetas de ensayo son cilindros de 5,1 cm de diámetro y 5,1 cm de altura, comprimidos tres veces con un peso de 6,35 kg dejado caer desde 5,1 cm). Luego se almacenaron a 20◦ C/50% de humedad relativa y se midieron la resistencia a la compresión de las probetas de ensayo, al cabo de 1 hora y de 24 horas, obteniéndose 1.085 kNm−2 y 3.945 kNm−2 , respectivamente. 60 20 ES 2 059 792 T3 Ejemplo de Aplicación 8 Uso como Revestimiento de Refuerzo 10 Siguiendo generalmente el proceso para la preparación del Producto C, se preparó una resina con una viscosidad más alta que la del Producto C, con el objetivo de formar una resina que, una vez curada, tuviera un punto de fusión en el intervalo de 104◦ C a 116◦ C. Esta resina se convirtió luego en el éster de acetato y se deshidrató sustancialmente. La resina éster se mezcló luego durante aproximadamente 30 minutos con arena en la proporción de aproximadamente 2% en peso de la resina éster basado en la arena. 15 El producto era arena revestida con un aglutinante que podı́a ser activado por contacto con una solución alcalina. Es útil para mejorar las caracterı́stica de una formación subterránea con el propósito, por ejemplo, de aumentar su permeabilidad y, ası́, la productividad de un pozo situado en la formación subterránea. 5 20 En uso, la arena revestida se coloca en o próxima a la formación, y luego se provoca el curado. El curado se efectúa haciendo pasar en contacto con la arena revestida una solución de un material básico adecuado, tal como por ejemplo hidróxido sódico, hidróxido cálcico o similares. En lugar de gránulos de arena, el núcleo del refuerzo puede ser un material muy resistente a la compresión, tal como perlas de vidrio fabricadas especialmente para ese propósito. 25 30 35 40 45 50 55 60 21 ES 2 059 792 T3 REIVINDICACIONES 1. Una composición de resina fenólica que comprende 5 (1) un compuesto fenólico esterificado que contiene uno o más grupos hidroxilo fenólicos y/o uno o más grupos hidroxilo fenólicos esterificados y que contiene, además, uno o más grupos metilol esterificados que tienen la fórmula general R | - C - OH | H 10 15 en donde R es H, un hidrocarbilo alifático o aromático o un grupo heterocı́clico, en posición orto y/o para con respecto a un grupo fenólico o a un grupo hidroxilo fenólico esterificado, (2) una composición de resina de resol fenólico no esterificado, y 20 25 30 35 (3) una base. 2. Una composición según la reivindicación 1, en donde el compuesto fenólico esterificado es un fenol mononuclear que tiene un anillo aromático al que está unido por lo menos un grupo hidroxi fenólico y/o por lo menos un grupo hidroxi fenólico esterificado. 3. Una composición según la reivindicación 2, en donde el compuesto fenólico esterificado se deriva de fenol, o - cresol, m - cresol, p - cresol, 3,5 - xilen - 1 - ol, resorcinol, floroglucinol, pirogalol, y sus mezclas, y ésteres de éstos, en donde el grupo hidroxilo fenólico o por lo menos uno de los grupos hidroxilo fenólicos está esterificado. 4. Una composición según la reivindicación 3, en donde el compuesto fenólico esterificado se elige entre 2 - acetiloximetilfenol, 2 - metacriloiloximetilfenol, 2 - saliciloiloximetilfenol, 2 - acetiloximetilfenol - acetato, 2,6 - diacetiloximetil - p - cresol, 2,6 - diacetiloximetil - p - cresol acetato, 2,6 - diacetoacetiloximetil - p - cresol, 2,4,6 - triacetiloximetilfenol, 2,4,6 - triacetiloximetilfenol - acetato y 2,6 - diacetiloximetilfenol - acetato. 5. Una composición según la reivindicación 1, en donde el compuesto fenólico esterificado se deriva de Bisfenol A. 40 45 50 6. Una composición según la reivindicación 5, en donde el compuesto fenólico esterificado es 2,2’,6,6’ - tetraacetiloximetil Bisfenol A o 2,2’,6,6’ - tetraacetiloximetil Bisfenol A diacetato. 7. Una composición según la reivindicación 1, en donde el compuesto fenólico esterificado comprende un derivado de un producto de reacción de condensación, obtenido haciendo reaccionar dos o más moléculas de un fenol mononuclear con una o más moléculas de un aldehı́do o cetona reactivos con fenol. 8. Una composición según la reivindicación 7, en donde el compuesto fenólico esterificado es un derivado de un producto de reacción de condensación, obtenido haciendo reaccionar formaldehı́do y un fenol mononuclear elegido entre fenol, o - , m - , ó p - cresol, 3,5 - xilen - 1 - ol, resorcinol, floroglucinol, pirogalol o una de sus mezclas. 9. Una composición según la reivindicación 8, en donde el compuesto fenólico esterificado es una resina de resol de fenol - formaldehı́do esterificada o parcialmente esterificada. 55 60 10. Una composición según una cualquiera de las reivindicaciones 7 a 9, en donde el compuesto fenólico esterificado contiene uno o más grupos acetiloximetilo o grupos formiloximetilo en posición orto y/o para con respecto a un grupo hidroxilo fenólico o a un grupo hidroxilo fenólico esterificado. 11. Una composición según una cualquiera de las reivindicaciones 1 a 10, en donde la base es un álcali elegido entre los óxidos e hidróxidos de litio, sodio, potasio, calcio y magnesio. 12. Una composición de resina fenólica, que comprende 22 ES 2 059 792 T3 5 (1) un compuesto fenólico esterificado que comprende un derivado, que contiene grupos metilol esterificados, de un producto de reacción de condensación, obtenido haciendo reaccionar dos o más moléculas de un fenolmononuclear con una o más moléculas de un aldehı́do o cetona reactivos con fenol, en donde el citado derivado contiene uno o más grupos hidroxilo fenólicos y/o uno o más grupos hidroxilo fenólicos esterificados y contiene uno o más grupos metilol esterificados, que tiene la fórmula general R | - C - OH | H 10 15 en donde R es H, un hidrocarbilo alifático o aromático o un grupo heterocı́clico, en posición orto y/o para con respecto a un grupo hidroxilo fenólico o un grupo hidroxilo fenólico esterificado, y (2) una base. 20 13. Una composición según la reivindicación 12, en donde el compuesto fenólico esterificado comprende un derivado de un producto de reacción de condensación, obtenido haciendo reaccionar formaldehı́do y un fenol mononuclear elegido entre fenol, o - , m - , ó p - cresol, 3,5 - xilen - 1 - ol, resorcinol, floroglucinol y pirogalol o una de sus mezclas. 25 14. Una composición según la reivindicación 13, en donde el compuesto fenólico esterificado es una resina de un resol de fenol - formaldehı́do esterificada o parcialmente esterificada. 30 15. Una composición según una cualquiera de las reivindicaciones 12 a 14, en donde el compuesto fenólico esterificado contiene uno o más grupos acetiloximetilo o grupos formiloximetilo en posición orto y/o para con respecto a un grupo hidroxilo fenólico o un grupo hidroxilo fenólico esterificado. 16. Una composición según una cualquiera de las reivindicaciones 12 a 15, en donde la base se elige entre óxido cálcico, hidróxido cálcico, óxido magnésico e hidróxido magnésico. 35 40 17. Una composición según una cualquiera de las reivindicaciones 1 a 11, que adicionalmente contiene por lo menos un agente de curado de éster convencional. 18. Una composición según la reivindicación 17, en donde el agente de curado de éster convencional se elige entre diacetina, triacetina, etilenglicol diacetato, propilenglicol diacetato, butilenglicol diacetato, carbonato de propileno, propiolactona, butirolactona, valerolactona y caprolactona. 19. Una composición según una cualquiera de las reivindicaciones 1 a 18, que adicionalmente contiene un agente de soplado o de formación de espuma. 45 50 55 60 20. Una composición para moldeo de fundición, que comprende una mezcla de una cantidad principal de un material refractario granular y una cantidad secundaria eficaz para unir el material refractario granular de una composición de resina fenólica según una cualquiera de las reivindicaciones 1 a 18. 21. Una composición según la reivindicación 20, que adicionalmente contiene un agente de copulación de silano. 22. Un método para hacer una composición de resina fenólica curada, que comprende hacer reaccionar una composición según una cualquiera de las reivindicaciones 1 a 19 en presencia de agua y/u otro disolvente polar. 23. Un método según la reivindicación 22, en el que una base sustancialmente anhidra y un compuesto fenólico esterificado sustancialmente anhidro se mezclan entre sı́ para formar una mezcla según las reivindicaciones 12 a 16, que se hace reaccionar para formar una composición de resina fenólica curada por tratamiento posterior de la misma con humedad. 24. Un método según la reivindicación 22, que comprende formar una mezcla de un material refractario granular y un compuesto fenólico esterificado esencialmente anhidro y luego tratar la mezcla 23 ES 2 059 792 T3 resultante con una solución acuosa de la base, después de lo cual el compuesto fenólico esterificado y la base reaccionan entre sı́ para formar una composición de una resina fenólica curada que une el material refractario granular. 5 10 25. Un método para hacer un molde o macho de fundición, que comprende formar una composición según la reivindicación 20 o la reivindicación 21, con la forma deseada y permitir que el aglutinante se endurezca en presencia de agua y/u otro disolvente polar. 26. Un método según la reivindicación 25, en el que se prepara una mezcla homogénea sustancialmente anhidra de material refractario granular, una base y un compuesto fenólico esterificado, se conforma en una caja molde o macho en comunicación con la atmósfera y luego se hace pasar vapor de agua por el interior de la mezcla conformada en la caja molde o macho, con lo que la base y el compuesto fenólico esterificado reaccionan entre sı́ para formar una resina fenólica curada que une el material refractario granular. 15 20 27. Un método según la reivindicación 22, en el que una mezcla homogénea sustancialmente anhidra de una base y un compuesto fenólico esterificado se aplica, como revestimiento, sobre un sustrato y el sustrato revestido se deja reposar en una atmósfera húmeda durante un perı́odo suficiente para permitir que la base y el compuesto fenólico esterificado reaccionen en presencia de humedad para producir una composición de resina fenólica curada. 28. Un método según la reivindicación 22, en el que se prepara una mezcla, según se describe en la reivindicación 19, de base, compuesto fenólico esterificado y agente de soplado, luego se añade agua a la mezcla y luego se espuma la mezcla para producir una espuma fenólica curada. 25 29. El uso, como precursor quı́mico de una resina fenólica, de un fenol mononuclear esterificado o un éster fenol que contiene uno o más grupos hidroxilo fenólicos o grupos hidroxilo fenólicos esterificados y que contiene uno o más grupos metilol esterificados que tienen la fórmula general 30 R | - C - OH | H 35 en donde R es H, un grupo hidrocarbilo alifático o aromático o un grupo heterocı́clico en posición orto y/o para con respecto a un grupo hidroxilo fenólico o un grupo hidroxilo fenólico esterificado, formando el citado fenol mononuclear esterificado o el éster fenol una resina fenólica por reacción con un compuesto básico de metal alcalino - térreo en presencia de agua y/u otrodisolvente polar. 40 45 50 55 60 30. Uso según la reivindicación 29, en donde el compuesto básico de metal alcalino - térreo se elige entre óxido cálcico, hidróxido cálcico, óxido magnésico e hidróxido magnésico. 31. Un método para hacer una composición de resina fenólica curada que tiene un contenido reducido de iones inorgánicos, que comprende hacer reaccionar (1) un compuesto fenólico esterificado que comprende un derivado que contiene grupos metilol esterificados de un producto de reacción de condensación, obtenido haciendo reaccionar dos o más moléculas de un fenol mononuclear con una o más moléculas de un aldehı́do o cetona reactivos con fenol, en donde el citado derivado contiene uno o más grupos hidroxilo fenólicos y/o uno o más grupos hidroxilo fenólicos esterificados y contiene uno o más grupos metilol esterificados que tienen la fórmula general R | - C - OH | H en donde R es H, un grupo hidrocarbilo alifático o aromático o un grupo heterocı́clico en posición orto y/o para con respecto a un grupo hidroxilo fenólico o un grupo hidroxilo fenólico esterificado, y 24 ES 2 059 792 T3 (2) una base de Mannich. 32. Un método según la reivindicación 31, en el que la base de Mannich es 2,4,6 - tri(dimetilaminometil)fenol. 5 10 33. Un método según la reivindicación 31 o la reivindicación 32, en el que el compuesto fenólico esterificado es una resina de resol de fenol - formaldehı́do por lo menos parcialmente acetilada o por lo menos parcialmente formilada. 34. Un derivado de un producto de reacción de condensación, obtenido haciendo reaccionar dos o más moléculas de un fenol mononuclear elegido entre fenol, o - cresol, m - cresol, p - cresol, 3,5 - xilen - 1 ol, resorcinol, floroglucinol y pirogalol, con una o más moléculas de un aldehı́do o cetona reactivos con fenol, derivado que contiene uno o más grupos hidroxilo fenólicos y/o uno o más grupos hidroxilo fenólicos esterificados y contiene también uno o más grupos metilol esterificados que tiene la fórmula general 15 20 25 R | - C - OH | H en donde R es H, un grupo hidrocarbilo alifático o aromático o un grupo heterocı́clico unido en posición orto y/o para con respecto a un grupo fenólico, en donde uno o más de los grupos metilol esterificados contiene un grupo éster de ácido carboxı́lico elegido entre formiato, acetato, acetoacetato, acrilato, propionato, lactato, crotonato, metacrilato, butirato, isobutirato, caproato, caprilato, benzoato, toluato, p - aminobenzoato, cinamato, laurato, miristato, oxalato, sucinato, fumarato, maleato, adipato, azelato, sebacato, o un grupo de la fórmula 30 35 40 en donde R es un grupo alquileno de 1 - 4 C, x = 0 o 1, y = 1 a 3 y z = 1 o 2, de modo que cuando x = 0, z = 1, derivado que experimenta reticulación por reacción con una base en presencia de agua y/u otro disolvente polar. 45 50 55 60 NOTA INFORMATIVA: Conforme a la reserva del art. 167.2 del Convenio de Patentes Europeas (CPE) y a la Disposición Transitoria del RD 2424/1986, de 10 de octubre, relativo a la aplicación del Convenio de Patente Europea, las patentes europeas que designen a España y solicitadas antes del 7-10-1992, no producirán ningún efecto en España en la medida en que confieran protección a productos quı́micos y farmacéuticos como tales. Esta información no prejuzga que la patente esté o no incluı́da en la mencionada reserva. 25