CAPITULO 6º: HORMONAS Y SEXO - PsiqueUned. Psicología. UNED
Anuncio

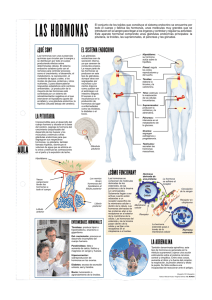
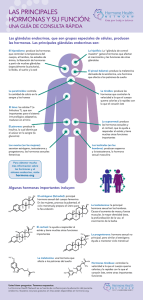
PF C_6º Página 1 de 17 CAPITULO 6º: HORMONAS Y SEXO Las hormonas influyen sobre el sexo de dos maneras: a través de la influencia sobre el desarrollo y al activar el comportamiento relacionado con la reproducción de adultos maduros sexualmente. La actitud de “los hombres son hombres” y “las mujeres son mujeres”. Desgraciadamente es completamente errónea. Esta actitud consiste en la tendencia a considerar la masculinidad y la feminidad como categorías discretas, mutuamente excluyentes y complementarias. 1. EL SISTEMA NEUROENDOCRINO. 1.1 Glándulas. Existen dos tipos de glándulas, las exocrinas y las endocrinas. Las glándulas exocrinas liberan sus sustancias químicas en conductos que los llevan hasta su blanco de acción, en su mayoría sobre la superficie del cuerpo. Las glándulas endocrinas liberan sus sustancias químicas, que son hormonas, directamente al sistema circulatorio. Una vez liberada la hormona es transportada por el sistema circulatorio hasta alcanzar el objetivo sobre el que ejerce su efecto. Por convención, solo se definen como glándulas endocrinas aquellos órganos cuya función principal es la de liberar hormonas. Aunque también otros órganos liberan hormonas al sistema circulatorio, y por tanto también forman parte del sistema endocrino. 1.2 Hormonas. La mayoría de las hormonas entran dentro de una de las tres categorías siguientes: - derivados de aminoácidos, - péptidos y proteínas, y - esteroides. Las hormonas derivadas de aminoácidos son hormonas sintetizadas en unos cuantos pasos sencillos a partir de una molécula de aminoácido. Las hormonas peptídicas y las proteínicas son cadenas de aminoácidos, las peptídicas son cadenas cortas y las proteínicas son cadenas largas. Las hormonas esteroides son hormonas sintetizadas a partir del colesterol, un tipo de molécula grasa. Son las hormonas esteroides las que desempeñan el papel fundamental en el desarrollo sexual y del comportamiento, y por tanto son las hormonas esteroides sobre las que nos vamos a centrar. prosado@teleline.es PF C_6º Página 2 de 17 La mayoría de las otras hormonas ejercen sus efectos únicamente al unirse a receptores en las membranas celulares. Los esteroides también pueden ejercer su acción de esta manera, pero, dado que son moléculas pequeñas y solubles en grasas, atraviesan fácilmente las membranas celulares. Una vez en el interior celular, pueden unirse a receptores en el citoplasma o el núcleo, e influir sobre la expresión genética. Las hormonas esteroides ejercen una acción particularmente variada y de larga duración sobre la función celular. 1.3 Gónadas. Las gónadas, los testículos masculinos y los ovarios femeninos, constituyen la parte central de cualquier estudio acerca de las hormonas y el sexo. La principal función de los testículos y de los ovarios es la producción de esperma y óvulos. Tras la cópula una única célula espermática puede combinarse con un óvulo para formar una célula, llamada cigoto, que contiene toda la información necesaria para el desarrollo normal de un organismo adulto completo en su ambiente natural. Con la excepción del óvulo y las células espermáticas, cada célula del organismo humano tiene 23 pares de cromosomas. El óvulo y las células espermáticas contienen sólo la mitad. Por tanto, cuando u espermatozoide fertiliza a un óvulo, el cigoto resultante acaba poseyendo el conjunto completo de 23 pares de cromosomas, la mitad del padre y la mitad de la madre. Resulta de especial interés, el par de cromosomas conocido como cromosomas sexuales, porque contienen el programa genético que dirige el desarrollo sexual. Las células de las hembras contienen dos grandes cromosomas X, y en los varones uno es X y el otro un pequeño cromosoma X llamado Y. El cromosoma sexual de cada óvulo es un cromosoma X, mientras que la mitad de las células espermáticas llevan uno X y la otra mitad Y. 1.4 Esteroides sexuales. Las gónadas hacen más que generar esperma y óvulos, también producen y liberan hormonas. Los testículos y los ovarios liberan las mismas hormonas. Las dos principales clases de hormonas gonadales son los andrógenos y los estrógenos. La testosterona es el andrógeno más común, y el estradiol es el estrógeno más común. El hecho de que los ovarios tienden a liberar más estrógenos que andrógenos y que los testículos liberan más andrógenos que estrógenos ha llevado a la práctica común, pero engañosa, de considerar los andrógenos como las hormonas sexuales masculinas y los estrógenos las femeninas, pero no es así. Los ovarios y los testículos también liberan un tipo de hormonas llamadas progestinas. La más común es la progesterona, que en las hembras prepara el útero y las mamas para el embarazo. Su papel en los varones no está claro. prosado@teleline.es PF C_6º Página 3 de 17 La principal función de la corteza adrenal, la capa externa de la glándula adrenal, es la regulación de los niveles de glucosa y de sal en sangre, pero además de sus principales hormonas esteroides, libera en pequeñas cantidades todos los esteroides sexuales liberados por las gónadas. 1.5 Hormonas de la pituitaria. La glándula pituitaria o hipófisis se conoce a menudo como la glándula maestra, porque la mayor parte de sus hormonas son hormonas trópicas. Estas son hormonas cuya función principal es influir sobre la liberación de hormonas por parte de otras glándulas. La glándula pituitaria consta en realidad de dos glándulas, la pituitaria posterior y la anterior, que se fusionan en el transcurso del desarrollo embriológico. La pituitaria posterior se desarrolla a partir de una pequeña excrecencia de tejido hipotalámico que cuelga del hipotálamo en el extremo del tallo pituitario. La pituitaria anterior o adenohipófisis, que comienza formando parte del mismo tejido embrionario que evoluciona hacia el velo del paladar, se descuelga durante el desarrollo y migra hacia su posición junto a la pituitaria posterior. Es la pituitaria anterior la que libera las hormonas trópicas, así que es esta en realidad la glándula principal. 1.6 Los niveles de las hormonas gonadales femeninas son cíclicos; los niveles de las hormonas gonadales masculinas son estables. La diferencia principal entre la función endocrina en mujeres y hombres es que en las mujeres los niveles de hormonas gonadales y gonadotrópicas atraviesan un ciclo que se repite más o menos cada 28 días. Son estas fluctuaciones hormonales las que controlan el ciclo menstrual femenino. Por el contrario, los varones son criaturas monótonas, desde un punto de vista neuroendocrino. Los niveles de sus hormonas gonadales y gonadotrópicas cambian poco día a día. Debido a que la pituitaria anterior es la glándula maestra, muchos investigadores dieron por cierto que la base de la diferencia entre los patrones de liberación hormonal gonadotrópica y gonadal estribaba en una diferencia inherente entre la pituitaria anterior masculina y femenina. Pero, esta hipótesis fue desechada por una serie de interesantes estudios sobre transplantes en la década de 1950. Lo que estos estudios demostraron fue que la pituitaria anterior no es inherentemente femenina o masculina. Sus patrones de liberación hormonal están regulados por otras zonas del cuerpo. 1.7 Control nervioso de la pituitaria. El sistema nervioso fue relacionado con el control de la pituitaria anterior tras los estudios sobre el comportamiento en pájaros y otros animales que crían durante una época determinada del año. prosado@teleline.es PF C_6º Página 4 de 17 De alguna forma, la entrada de señales visuales al sistema nervioso controla la liberación de hormonas trópicas desde la pituitaria anterior. La búsqueda de la estructura neurológica concreta que controla la pituitaria anterior se dirigió hacia el hipotálamo. La estimulación del hipotálamo y estudios sobre lesiones establecieron rápidamente que el hipotálamo regula la pituitaria anterior, pero la forma en que lo hace siguió siendo un misterio. La pituitaria anterior no recibe señales nerviosas del hipotálamo ni de cualquier otra estructura neurológica. 1.8 Control de la pituitaria anterior y posterior por parte del hipotálamo. Existen dos mecanismos distintos por los que el hipotálamo controla la pituitaria: uno para la pituitaria posterior y otro para la anterior. Las dos hormonas principales de la pituitaria posterior, la vasopresina y la oxitocina, son hormonas peptídicas sintetizadas en los corpúsculos celulares de las neuronas del núcleo paraventricular y del núcleo supraóptico del hipotálamo. Seguidamente, son transportadas por os axones de estas neuronas hacia sus terminales en la pituitaria posterior, donde son almacenas hasta que la llegada de un potencial de acción provoca su liberación al torrente sanguíneo. Las neuronas que liberan hormonas al sistema circulatorio general se conocen como células neurosecretoras. La oxitocina estimula las contracciones uterinas durante el parto y la expulsión de leche durante la succión. La vasopresina facilita la reabsorción de agua por parte de los riñones. Los medios por los cuales el hipotálamo controla la liberación de hormonas desde la pituitaria anterior, carente de neuronas, fueron más difíciles de explicar. Harris sugirió que esta liberación hormonal está regulada a su vez por hormonas liberadas del hipotálamo. Dos hallazgos apoyaron esta teoría. El primero fue el descubrimiento de una red vascular, el sistema portal hipotalamopituitario, que era capaz de transportar hormonas desde el hipotálamo a la pituitaria anterior. El segundo hallazgo fue el descubrimiento de que al cortar las venas portales del tallo pituitario se interrumpe la liberación de hormonas hasta que el daño sea reparado. 1.9 Descubrimiento de las hormonas hipotalámicas liberadoras de hormonas. Se pensó que la liberación de cada hormona de la pituitaria anterior está controlada por una hormona hipotalámica diferente. Las supuestas hormonas hipotalámicas putativas (hipotéticas) se llamaron factores de liberación. Aquellas que se pensaba que inhibían la liberación de las hormonas de la pituitaria anterior se llamaron factores de inhibición. prosado@teleline.es PF C_6º Página 5 de 17 Guilleman y sus colaboradores aislaron la hormona liberadora de tirotropina del hipotálamo de oveja, y Schally y sus colaboradores aislaron la misma hormona del hipotálamo del cerdo. La hormona liberadora de tirotropina desencadena la liberación de tirotropina desde la pituitaria anterior, lo que a su vez estimula la liberación de hormonas desde la glándula tiroides. Es difícil apreciar el esfuerzo llevado a cabo para aislar la hormona liberadora de tirotropina. ¿Por qué se dedicaron dos equipos de investigación durante más de una década a acumular una cantidad mínima de hormona liberadora de tirotropina?. La razón es que eso permitió tanto a Guilleman como a Schally determinar la composición química de la hormona liberadora de tirotropina y desarrollar métodos para sintetizar mayores cantidades de la hormona para usos clínico y de investigación. El aislamiento de la hormona liberadora de tirotropina por parte de Schally y de Guilleman confirmó que las hormonas liberadoras hipotalámicas controlan la liberación hormonal desde la pituitaria anterior y proporcionan así un mayor estímulo para el aislamiento y la síntesis de otras hormonas liberadoras. El aislamiento de la hormona liberadora de gonadotropina, fue de especial relevancia para el estudio de las hormonas sexuales. Esta hormona liberadora estimula la liberación de las dos gonadotropinas de la pituitaria anterior: la hormona foliculoestimulante (FSH) y la hormona luteizante (LH). Todas las hormonas liberadoras, la igual que todas las hormonas trópicas, han resultado ser péptidos. 1.10 Retroalimentación en el sistema neuroendocrino. El hipotálamo controla la pituitaria anterior, y la pituitaria anterior, controla a su vez a otras glándulas endocrinas. Pero la regulación neuroendocrina no es una vía de una sola dirección. La mayor parte de la retroalimentación en el sistema neuroendocrino es una retroalimentación negativa, cuya función es el mantenimiento de la estabilidad.. Aunque la retroalimentación negativa es la regla del sistema neuroendocrino, también puede tener lugar la retroalimentación positiva. Se ha sugerido que el paso de una retroalimentación negativa a una positiva podría ser el factor clave del incremento del nivel sanguíneo de progesterona y estradiol en las hembras, que es el responsable de la puesta en marcha de la ovulación. Se ha propuesto un mecanismo similar para explicar la aparición de las hormonas gonadales que tiene lugar tanto en machos como en hembras durante la pubertad. 1.11 Liberación hormonal pulsátil. Las hormonas suelen ser liberadas por pulsos, varias veces al día y en grandes picos que no suelen durar más que unos pocos minutos. Los niveles hormonales en sangre son regulados por cambios de la frecuencia y la duración de los pulsos hormonales. Una consecuencia de la liberación hormonal prosado@teleline.es PF C_6º Página 6 de 17 pulsátil es que a menudo hay grandes fluctuaciones minuto a minuto en los niveles hormonales circundantes. 1.12 Modelo resumen de la regulación endocrina gonadal. Un modelo resumido de la regulación de las hormonas gonadales es que según este modelo el cerebro controla la liberación de la hormona liberadora de gonadotropina desde el hipotálamo hacia el sistema portal hipotalamopituitario, que la conduce a la pituitaria anterior. En ella, la hormona liberadora de gonadotropina estimula la liberación de gonadotropinas, que son conducidas a las gónadas por el sistema circulatorio. En respuesta a las gonadotropinas, las gónadas liberan andrógenos, estrógenos y progestinas, que ejercen un efecto de retroalimentación sobre el hipotálamo y la pituitaria con el fin de regular subsiguientes liberaciones hormonales gonadales. 2. HORMONAS Y DESARROLLO SEXUAL. La diferenciación sexual en los mamíferos empieza en el momento de la fertilización, con la producción de uno de los dos tipos diferentes de cigotos: con un par de cromosomas sexuales XX o con un par XY. No hay que empezar por asumir el hecho de que existen dos programas genéticos paralelos de desarrollo sexual, uno del desarrollo femenino y otro del masculino. Estamos genéticamente programados para desarrollar cuerpos femeninos. Los varones genéticos desarrollan cuerpos masculinos únicamente porque su programa de desarrollo fundamental, femenino, resulta anulado. 2.1 Las hormonas fetales y el desarrollo de órganos reproductores. Gónadas. A las seis semanas después de la fertilización aparecen las gónadas, es en este estadio del desarrollo donde cada feto, independientemente de su sexo genético, presenta el mismo par de estructuras llamadas gónadas primordiales. Cada gónada primordial presenta una cubierta externa o corteza, que tiene la capacidad de desarrollarse en un ovario, y un núcleo interno o médula, que tiene la capacidad de desarrollarse en un testículo. Seis semanas después de la concepción, el cromosoma Y de los varones desencadena la síntesis del antígeno H-Y y esta proteína provoca el crecimiento de la médula de cada gónada primordial para que se desarrolle y forme un testículo. No existe una contrapartida femenina al antígeno H-Y. En ausencia del antígeno H-Y, las células corticales de las gónadas primordiales se desarrollan automáticamente y forman ovarios. prosado@teleline.es PF C_6º Página 7 de 17 Conductos reproductores internos. Seis semanas después de la fertilización, tanto los varones como las hembras presentan dos juegos completos de conductos reproductores. Tienen un sistema de Wolff masculino, con capacidad para desarrollarse y formar conductos reproductores masculinos, y también un sistema de Müller femenino, que presenta la capacidad para desarrollarse y convertirse en conductos femeninos. Durante el tercer mes de desarrollo masculino o femenino, los testículos segregan testosterona u una sustancia inhibitoria del conducto de Müller. La testosterona estimula el desarrollo del sistema de Wolf y la sustancia inhibidora del conducto de Müller provoca la degeneración del sistema de Müller y el descenso de los testículos hasta el escroto. Dado que es la testosterona, y no los cromosomas sexuales, lo que dispara el desarrollo del conducto de Wolf, las hembras genéticas inyectadas con testosterona durante el período fetal adecuado desarrollan conductos reproductores masculinos junto con los femeninos. La diferenciación de los conductos internos del sistema reproductor femenino no está bajo el control de las hormonas ováricas. El desarrollo del sistema de Müller tiene lugar en cualquier feto no expuesto a testosterona durante el período fetal crítico. La ovariectomía es la extirpación de los ovarios, y la orquidectomía la de los testículos. La gonadectomía o castración, es la extirpación quirúrgica de las gónadas, ya sean ovarios o testículos. Órganos reproductores externos. Existe una diferencia básica entre la diferenciación de los órganos reproductores externos y la diferenciación de los órganos reproductores internos. Todo feto normal desarrolla por separado precursores para las gónadas masculina (médula) y femenina (corteza) y para los conductos reproductores masculino y femenino. Los genitales masculino y femenino se desarrollan a partir del mismo precursor. En el transcurso del segundo mes de gestación, el precursor bipotencial de los órganos reproductores externos consta de cuatro partes; el glande, los pliegues uretrales, los cuerpos laterales y los abultamientos labioescrotales. Entonces empieza la diferenciación. El glande crece hasta formar la cabeza del pene en levaron o el clítoris en la hembra. Los pliegues uretrales se fusionan en el varón o se alargan hasta convertirse en los labios menores en la hembra. Los cuerpos laterales forman el tallo del pene en los varones o la caperuza del clítoris en las hembras, y los abultamientos labioescrotales forman el escroto en los varones o los labios mayores en las hembras. El desarrollo de los genitales externos está controlado por la presencia o la ausencia de testosterona. Si la testosterona está presente en el momento prosado@teleline.es PF C_6º Página 8 de 17 adecuado del desarrollo fetal, se desarrollan genitales externos masculinos a partir del precursor bipotencial. Si la testosterona no está presente, se desarrollan genitales externos femeninos. 2.2 Desarrollo de diferencias sexuales en el cerebro. Los cerebros femenino y masculino son similares, pero no idénticos. Los cerebros masculinos tienden a ser un 15% más grandes que los femeninos. Se ha documentado una serie de diferencias anatómicas más sutiles. La tomografía de emisión de positrones (PET) ha puesto de manifiesto diferencias sexuales en la función cerebral. Posiblemente, algunas de estas diferencias estén relacionadas con diferencias en la función cognitiva y emocional. LA mayoría de nuestros conocimientos actuales sobre la diferenciación sexual del cerebro humano viene de experimentos realizados con ratas. Así es fácil estudiar los efectos que ejercen las hormonas sobre el desarrollo cerebral sin peligro de confundirnos con los efectos sobre el desarrollo genital. Andrógenos perinatales y diferenciación cerebral. La mayoría de los primeros estudios acerca del desarrollo de las diferencias sexuales se centraron en los factores que controlan el desarrollo de los patrones de liberación, estable y cíclico, de las gonadotropinas en varones y hembras, respectivamente. Los primeros experimentos fueron por Pfeiffer en 1936. Observó que la gonadectomía de las ratas neonatales de cualquiera de los sexos genéticos las convertía en adultos con patrones cíclicos femeninos en cuanto a la liberación de gonadotropinas. El transplante de testículos en ratas neonatales femeninas, gonadectomizadas o intactas, las convertía en adultos machos en cuanto al patrón de liberación de gonadotropinas. El transplante de ovarios no ejerció ningún efecto sobre el patrón de liberación hormonal. Concluyo que el patrón cíclico femenino de liberación de gonadotropinas es el que se desarrolla, a no ser que este patrón preprogramado sea anulado por la testosterona durante el desarrollo perinatal. Concluyó erróneamente que la presencia o ausencia de hormonas testiculares en las ratas neonatales influye sobre el desarrollo dela pituitaria, porque no sabía que la liberación de gonadotropinas desde la pituitaria anterior está controlada por el hipotálamo. Varias otras diferencias entre los cerebros masculino y femenino están bajo control hormonal parecido. La presencia de testosterona perinatal lleva al desarrollo de un cerebro de características masculinas, independientemente del sexo genético. prosado@teleline.es PF C_6º Página 9 de 17 Aromatización y diferenciación cerebral. Todas las hormonas gonadales y adrenales sexuales son hormonas esteroides, derivadas del colesterol. Presentan estructuras similares, se convierten rápidamente unas en otras. Existen pruebas de que la aromatización constituye un paso crítico en el proceso de masculinización del cerebro por la acción de la testosterona en algunas especies. Según esta teoría, la testosterona perinatal no masculiniza directamente el cerebro. El cerebro se masculiniza por la acción del estradiol, que ha sido aromatizado a partir de la testosterona masculina. ¿Cómo pueden las hembras genéticas de especies, cuyos cerebros pueden ser masculinizados por el estradiol, evitar ser masculinizadas por el estradiol materno que circula en la sangre fetal?. En la rata, la respuesta es la alfa fetoproteína, esta está presente en la sangre de las ratas durante el período perinatal, y desactiva el estradiol circulante por medio de uniones con el mismo. Así, ¿de qué manera masculiniza el estradiol de los fetos masculinos en presencia de los efectos desactivadores de la alfa fetoproteína?. La testosterona es inmune a la alfa fetoproteína, puede ser transportada desde los testículos al cerebro, donde entra en las células para convertirse en estradiol. El estradiol no se descompone en el cerebro porque la alfa fetoproteína no atraviesa la barrera hematoencefálica con facilidad. En los seres humanos, los fetos femeninos están protegidos contra los efectos masculinizantes de los estrógenos maternos por la barrera placentaria. Esta barrera no resulta tan eficaz contra los estrógenos sintéticos, como el dietilstilbestrol, como resultado la descendencia femenina de madres expuestas a estrógenos sintéticos durante el embarazo muestra múltiples características masculinas. 2.3 Hormonas perinatales y desarrollo del comportamiento. Las hormonas perinatales afectan al desarrollo del cerebro, no debería sorprendernos que también influyan sobre el desarrollo del comportamiento. Phoenix y sus colaboradores fueron los primeros en demostrar que la inyección perinatal de testosterona masculiniza y desfeminiza el comportamiento copulatorio de un adulto genéticamente femenino. En un estudio complementario al de este autor, Grady, Phoenix y Young vieron que la ausencia de una exposición temprana de ratas macho a testosterona desmasculiniza y feminiza su comportamiento copulatorio adulto. La aromatización de la testosterona y su conversión en estradiol parece ser importante tanto para la desfeminización como para la masculinización del comportamiento copulatorio de los roedores. La mayor parte de la investigación sobre las hormonas y el desarrollo de l comportamiento se ha centrado en la cópula misma. Sabemos relativamente poco acerca del papel de las hormonas en el desarrollo de comportamientos proceptivos prosado@teleline.es PF C_6º Página 10 de 17 y en el desarrollo de comportamientos relacionados con el género que no están directamente vinculados a la reproducción. Al pensar en las hormonas y el comportamiento, es importante recordar que los efectos feminizantes y desmaculinizantes no van siempre juntos, al igual que los efectos desfeminizantes y masculinizantes. Los tratamientos hormonales pueden aumentar o alterar el comportamiento femenino sin alterar el comportamiento masculino y viceversa. 2.4 Pubertad, hormonas y desarrollo de las características sexuales secundarias. A lo largo de la niñez, los niveles circulantes de las hormonas gonadales son bajos, los órganos reproductores son inmaduros y los varones y las hembras difieren poco en su apariencia general. Este período finaliza de golpe en la pubertad, el período de transición entre la niñez y la madurez, durante la cual se alcanza el estado de fertilidad, el estirón del adolescente y el desarrollo de las características sexuales secundarias. Las características sexuales secundarias son aquellos aspectos que distinguen a los hombres sexualmente maduros de las mujeres. La pubertad se asocia con un aumento de la liberación hormonal por parte de la pituitaria anterior. El aumento en la liberación de la hormona de crecimiento, la única hormona de la pituitaria anterior que no tiene como diana principal una glándula endocrina, actúa directamente sobre el hueso y el tejido muscular y produce el estirón del crecimiento corporal. Los incrementos en la liberación de la hormona gonadotrópica y la adrenocorticotrópica provocan la liberación de las hormonas gonadales y adrenales, las cuales a su vez inician la maduración de los genitales y el desarrollo de los caracteres sexuales secundarios. El principio general es simple: en los varones púberes, los niveles de andrógenos son más elevados que los de estrógenos, lo que resulta en una masculinización. En las hembras púberes, predominan los estrógenos y el resultado es una feminización. Incluso durante la pubertad, el concepto de los hombres son hombres y las mujeres son mujeres se tambalea. La androstendiona es una andrógeno liberado principalmente por la corteza adrenal, normalmente responsable del crecimiento del vello púbico y del de las axilas en las mujeres. Es difícil considerar los andrógenos como hormonas masculinas cuando una de ellas es responsable del crecimiento del vello púbico femenino. El aspecto masculino es piramidal y el femenino es el de una pirámide invertida. 2.5 Tres casos de desarrollo sexual humano excepcional. Veremos tres excepciones: prosado@teleline.es PF C_6º • • • Página 11 de 17 CASO 1. Síndrome de la insensibilidad androgénica: El caso de Anne S. Todos los síntomas vienen del hecho de que su cuerpo carece de la capacidad para responder ante los andrógenos. Al parecer, en ausencia de los efectos masculinizantes de los andrógenos, los niños que parecen hembras son criados como hembras y acaban pensando y actuando como hembras, aunque genéticamente sena varones. CASO 2. Síndrome adrenogenital. Es un trastorno del desarrollo sexual provocado por una hiperplasia adrenal congénita, una deficiencia congénita de la liberación de la hormona cortisol por parte de la corteza adrenal, lo que da como resultado una hiperactividad adrenal compensatoria y un exceso de liberación de andrógenos adrenales. Esto tiene poco efecto en el desarrollo de varones, pero no en el de las hembras genéticas. Estas suelen nacer con un clítoris agrandado y los labios especialmente fusionados, sus conductos internos suelen ser normales. Si este síndrome se diagnostica en el momento del nacimiento de la niña, las anormalidades de los genitales externos pueden ser corregidas por medio de cirugía y cortisol. Tras el tratamiento precoz, las hembras crecen físicamente normales, salvo por el hecho de que la llegada de la menstruación suele producirse más tarde de lo normal. CASO 3. Reasignación del sexo de un gemelo con ablación del pene. Uno de los casos más famosos publicados sobre el desarrollo sexual es el de un gemelo idéntico varón cuyo pene fue accidentalmente destruido durante una circuncisión a la edad de 7 meses. Al no existir ninguna manera de reemplazar el pene, Money recomendó la castración del niño, que se le creara una vagina artificial y que fuese criado como niña y que se le administraran estrógenos al llegar a la pubertad. Así fue. La disponibilidad de un sujeto de control genéticamente idéntico, el hermano gemelo, aumentó el interés del caso. Según Money, el desenlace de este caso cae claramente del lado de la teoría del aprendizaje social de la identidad sexual. Money informó que cuando el paciente tenía 12 años, que ella se había desarrollado como una hembra normal, con lo cual se confirmaba su predicción. Sin embargo, un seguimiento a largo plazo publicado por varios expertos independientes de los que habían prescrito el tratamiento, cuentan una historia diferente. Aparentemente, el órgano que determina el curso del desarrollo psicológico es el cerebro y no los genitales. 3. EFECTOS DE LAS HORMONAS GONADALES SOBRE LOS ADULTOS. Una vez que el individuo ha alcanzado la madurez sexual, las hormonas gonadales empiezan a desempeñar un papel en la activación del comportamiento reproductor. prosado@teleline.es PF C_6º 3.1 Página 12 de 17 El comportamiento masculino relacionado con la reproducción y la testosterona. El importante papel que desempeñan las hormonas gonadales en la activación del comportamiento sexual masculino ha sido claramente probado por los efectos asexualizantes de la orquidectomía. Se pueden extraer dos generalizaciones importantes del estudio de Bremer. La primera es que la orquidectomía conduce a la reducción del interés y del comportamiento sexual. La segunda es que el ritmo u grado de pérdida es variable. ¿Por qué algunos hombres permanecen sexualmente activos durante meses tras una orquidectomía, a pesar del hecho de que las hormonas testiculares son eliminadas de su organismo en cuestión de días?. Se ha sugerido que los andrógenos adrenales pueden tener algún papel en el mantenimiento de la actividad sexual de algunos hombres castrados, pero no existe una prueba directa. La orquidectomía retira de un solo tajo un par de glándulas que liberan muchas hormonas. Como la testosterona es la principal hormona testicular, los principales síntomas de la orquidectomía se han atribuido generalmente a la pérdida de testosterona. Los efectos terapéuticos de las inyecciones de sustitución de testosterona han confirmado esta suposición. La testosterona, sin embargo, no elimina la esterilidad de los varones carentes de testículos funcionales. El hecho de que la testosterona sea necesaria para el comportamiento sexual masculino ha llevado a dos suposiciones: primero, que el nivel de la sexualidad masculina es función de la cantidad de testosterona en sangre, y segundo, que el impulso sexual de un hombre puede aumentar si se aumentan sus niveles de testosterona. Ambas suposiciones son incorrectas. El impulso sexual y los niveles de testosterona no están correlacionados en hombres sanos, y las inyecciones de testosterona no aumentan su impulso sexual. Parece ser que los hombres sanos tienen mucha más testosterona de la necesaria para activar los circuitos nerviosos que provocan su comportamiento sexual. En lo que se refiere a los efectos de la testosterona sobre el comportamiento sexual, más no significa necesariamente mejor. La dihidrotestosterona, andrógeno no aromatizable, ha sido incapaz de reactivar el comportamiento copulador de ratas macho castradas. Sin embargo, la dihidrotestosterona se ha mostrado eficaz para activar el comportamiento sexual en primates orquidectomizados. 3.2 El comportamiento femenino relacionado con la reproducción y las hormonas gonadales. Las ratas y conejillos de Indias hembras sexualmente maduras muestran ciclos de 4 días de liberación hormonal. Hay un incremento gradual en la secreción de estrógenos en desarrollo en el transcurso de los dos días anteriores a la ovulación, prosado@teleline.es PF C_6º Página 13 de 17 seguido de un repentino aumento en el nivel de progesterona al desprenderse el óvulo. Estos picos de estrógeno y de progesterona inician el estro, un período de 12 a 18 horas durante las cuales la hembra es fértil, receptiva, proceptiva y sexualmente atractiva. La estrecha relación entre el ciclo de liberación hormonal y el ciclo del estro, ciclo de la receptividad sexual, en hembras de ratas, conejillos de Indias y muchos otros mamíferos, sugiere que el comportamiento sexual femenino está bajo control hormonal. Los efectos de la ovariectomía confirman esta conclusión. Las mujeres no se parecen en nada a las hembras de las ratas en lo referente al control hormonal de su comportamiento sexual. La principal consecuencia de la ovariectomía, además de la esterilidad, es un descenso de la lubricación vaginal. Existen pruebas de que el impulso sexual en las mujeres está bajo control de andrógenos y no de estrógenos. El apoyo a la teoría viene de tres fuentes: 1. Experimentos en hembras no humanas de primates. 2. Estudios de correlación en mujeres sanas. 3. Estudios clínicos en mujeres tras ovariectomía y adrenalectomía. 3.3 Abuso de esteroides anabolizantes. Los esteroides anabolizantes son esteroides que ejercen un efecto anabolizante (estimulan el crecimiento). La testosterona no es muy útil por sí misma como droga anabolizante. Así que los químicos han conseguido sintetizar un número de potentes esteroides anabolizantes de efecto prolongado, pero no han conseguido sintetizar alguno que no contenga efectos secundarios. En la actualidad nos encontramos inmersos en una epidemia de abuso de los esteroides anabolizantes. En los últimos años, el uso cosmético de los esteroides ha alcanzado proporciones preocupantes. ¿Los esteroides anabolizantes aumentan de verdad la musculatura y la fuerza de los atletas que los utilizan? Los datos científicos no son uniformes. La incapacidad de la ciencia para confirmar los beneficios que al parecer experimentan los atletas deriva de dos puntos flacos de la investigación científica. En primer lugar, los estudios experimentales tienden a emplear dosis de esteroides más bajas que las usadas por atletas. En segundo lugar, los estudios experimentales a menudo se llevan a cabo en sujetos que no intervienen en un entrenamiento anabolizante intenso. Los efectos secundarios relacionados con el sexo derivados del uso de esteriodes anabolizantes resulta difícil de documentar. En hombres, la retroalimentación negativa ante los altos niveles de esteroides anabolizantes reduce la liberación de gonadotropina. Esto conduce a una disminución de la actividad testicular, lo que puede derivar en una atrofia ginecomastia (crecimiento de las mamas en los hombres). En las mujeres puede producir amenorrea, esterilidad, hirsutismo (crecimiento excesivo del bello corporal), crecimiento del clítoris, calvicie ... prosado@teleline.es PF C_6º Página 14 de 17 Muchos de los efectos relacionados con el sexo en las mujeres parecen ser irreversibles. Tanto los hombres como las mujeres que utilizan esteroides anabolizantes pueden sufrir espasmos musculares, dolor muscular, sangre en la orina, acné, inflamación debida a la retención de líquidos, hemorragias en la lengua, náuseas, vómitos y una variedad de comportamientos psicóticos que incluyen fases de depresión e ira. Los esteroides anabolizantes orales producen tumores cancerosos del hígado. Los efectos secundarios del abuso de esteroides anabolizantes establecen dos aspectos importantes. El primero es que las sustancias similares a la testosterona no provocan aumentos en al motivación sexual o el comportamiento en personas con niveles normales de testosterona. El segundo es que los efectos de las hormonas en la estructura del cuerpo humano no se restringen a los períodos críticos prenatales y de la pubertad. 4. EL HIPOTÁLAMO Y EL COMPORTAMIENTO SEXUAL. Muchas partes del cerebro intervienen en el comportamiento sexual de los mamíferos. El descubrimiento de que la liberación de gonadotropina está controlada por el hipotálamo centró los estudios sobre las bases neurológicas del comportamiento sexual en esta estructura. 4.1 Diferencias estructurales entre el hipotálamo masculino y el femenino. El hipotálamo masculino y el femenino son funcionalmente distintos en su control sobre las hormonas de la pituitaria anterior. En los años 70 se descubrieron diferencias estructurales entre los hipotálamos masculinos y femeninos en ratas. Gorski y sus colaboradores descubrieron un núcleo en el área preóptica medial del hipotálamo de la rata, que era más grande en machos. Fue llamado el núcleo sexualmente dimórfico. El crecimiento de los núcleos sexualmente dimórficos se dispara por la acción del estradiol, aromatizado a partir de testosterona. Según esto, la castración de un macho de un día de vida reduce de manera significativa el tamaño de sus núcleos sexuales dimórficos adultos, mientras que la inyección de testosterona en ratas hembra recién nacidas lo aumenta significativamente. Aunque el tamaño de los núcleos sexualmente dimórficos disminuye sólo ligeramente e los machos castrados en la edad adulta, determinadas zonas del núcleo sí muestran una degeneración significativa. El tamaño de los núcleos sexualmente dimórficos de ratas macho correlaciona con sus niveles de testosterona y con diversos aspectos de su actividad sexual. Sin embargo, es probable que aún no se haya establecido la función específica de este núcleo. Desde el descubrimiento se han identificado otras diferencias sexuales en ratas y en otras especies. En humanos, existen núcleos en las regiones preóptica, supraquiasmática y anterior del hipotálamo que son sensiblemente más grandes en prosado@teleline.es PF C_6º Página 15 de 17 varones que en hembras. Las diferencias entre géneros en la anatomía cerebral depende de la edad. 4.2 El hipotálamo y el comportamiento sexual masculino. La región preóptica medial del hipotálamo desempeña un papel clave en el comportamiento sexual masculino. LA destrucción de esta región anula el comportamiento sexual en los machos de muchas especies, y la destrucción selectiva de los núcleos sexualmente dimórficos reduce el comportamiento sexual de ratas macho. Las lesiones de la región preóptica medial no producen ningún efecto sobre el comportamiento sexual femenino, aunque limitan el comportamiento de monta masculina que se observa a menudo en ratas hembras. Así pues, las lesiones bilaterales preópticas mediales parecen anular el comportamiento copulador en ambos sexos. La estimulación eléctrica de la región preóptica medial estimula el comportamiento copulador en ratas macho y el comportamiento copulador puede restaurarse en ratas macho castradas por implantes de testosterona en la región preóptica medial. No está claro por qué los machos con lesiones preópticas mediales dejan de copular. La región preóptica medial presenta una gran cantidad de receptores del neuropéptido galanina. Las microinyecciones de galanina en la región preóptica medial de los machos estimula el comportamiento copulador. Las microinyecciones de endorfina en la misma zona bloquea el comportamiento copulador. La región preóptica medial parece controlar el comportamiento sexual masculino a través de una vía que se proyecta a una región del encéfalo medio llamado campo tegmental lateral. La destrucción de esta vía altera el comportamiento sexual de las ratas macho. 4.3 El hipotálamo y el comportamiento sexual femenino. El núcleo ventromedial (NVM) del hipotálamo contiene circuitos que son esenciales para el comportamiento sexual femenino. La estimulación eléctrica del núcleo ventromedial facilita el comportamiento sexual de las ratas hembra, las lesiones del NVM la reducen. Una inyección de progesterona lleva al estro a una hembra ovariectomizada que haya recibido una inyección de estradiol 48 horas antes. El estradiol debe estimular de alguna manera el sistema nervioso para que la progesterona ejerza su efecto. Este efecto estimulante parece estar mediado por el gran aumento en el número de receptores de progesterona que se encuentra en el NVM y sus alrededores. Existen pruebas de que el mecanismo del núcleo ventromedial que desempeña un papel en el comportamiento sexual de las hembras de ratas es noradrenérgico. prosado@teleline.es PF C_6º Página 16 de 17 La influencia del NVM sobre el comportamiento sexual de las hembras de rata parece estar regulada por una vía que desciende hasta la sustancia gris periacueductal del tegmento. La destrucción de esta vía suprime el comportamiento sexual femenino al igual que las lesiones de la propia sustancia gris periacueductal. En resumen, las investigaciones sobre roedores sugieren que las vías que van del hipotálamo al mesencéfalo tienen un papel importante en el comportamiento sexual. El comportamiento sexual masculino está influido por una vía que va desde la región preóptica medial hasta el campo tegmental lateral, y el comportamiento sexual femenino está influenciado por un conducto que va desde el núcleo ventromedial a la sustancia gris periacueductal. 5. ORIENTACIÓN SEXUAL, LAS HORMONAS Y EL CEREBRO. Algunas personas son heterosexuales, algunas homosexuales y algunas bisexuales. 5.1 Orientación sexual, genes y hormonas. La investigación ha demostrado que las diferencias en la orientación sexual tienen una base genética. Se ha localizado un gen que parece desempeñar un papel importante en la orientación sexual de los varones. Este gen está cerca de uno de los extremos del cromosoma X. Es importante no exagerar estas pruebas genéticas. 5.2 Orientación sexual y hormonas precoces. Muchas personas dan por hecho erróneamente que los homosexuales tienen un nivel más bajo de hormonas sexuales. No es así. Los homosexuales y los heterosexuales no difieren en cuanto a sus niveles de hormonas circulantes. Los esfuerzos para determinar si los niveles hormonales perinatales influyen sobre el desarrollo de la inclinación sexual se ha centrado en especies no humanas. En ratas, hámster, hurones, cerdos, cebras, pinzones y perros, la castración perinatal de los machos, o el tratamiento de las hembras con testosterona, han demostrado inducir preferencia sexual por el mismo sexo. Es necesario ser prudente a la hora de aplicar los resultados de los experimentos de laboratorio al desarrollo de las preferencias sexuales en humanos. Sería una equivocación ignorar los profundos componentes cognitivos y emocionales de la sexualidad humana. También sería un error pensar que un patrón de resultados tan coherente en numerosos mamíferos no tenga importancia alguna en humanos. ¿influyen las hormonas perinatales en la inclinación sexual de humanos adultos?. Hay indicaciones de que la respuesta es que sí. El apoyo más firme a este punto de vista viene del estudio cuasi experimental de Ehrhardt y sus colaboradores. prosado@teleline.es PF C_6º 5.3 Página 17 de 17 ¿Qué provoca el desarrollo de la atracción sexual?. Las pruebas indican que la mayoría de las niñas y de los niños que viven en países occidentales experimentan sus primeras sensaciones de atracción sexual hacia la edad de 10 años. McClintock y Herdt han sugerido que la aparición de la atracción sexual puede ser estimulada por los esteroides de la corteza adrenal. La maduración adrenal tiene lugar durante la niñez hacia la edad de 10 años. 5.4 ¿Existen diferencias entre los cerebros de homosexuales y de heterosexuales?. Existen diversos informes sobre las diferencias en la respuesta neuroanatómica, neuropsicológica y hormonal entre homosexuales y heterosexuales. La mayoría de los estudios han comparado varones homosexuales y heterosexuales. En muchos casos los varones homosexuales presentan una estructura cerebral a medio camino entre las hembras y los varones heterosexuales. Los informes de las diferencias que había entre géneros en las regiones anterior y preóptica del hipotálamo de varias especies, humanos incluidos, centraron las investigaciones de LeVay en estas regiones. LeVay confirmó un resultado anterior que el tercer núcleo intersticial del hipotálamo anterior (INAH 3) es más de dos veces más grande en hombres heterosexuales que en mujeres. Además encontró, que es más de dos veces más grande en hombres heterosexuales que en uno homosexual. Ser homosexual puede dar lugar a INAH 3 pequeños, más que a la inversa, incluso puede existir un tercer factor sin identificar que afecte a la correlación sea responsable de ella. LeVay consideró un tercer factor que podría conducir a la correlación, pero lo desechó por la posibilidad de que el SIDA fuese el responsable. Aun cuando LeVay tomó en consideración únicamente los sujetos muertos por causas ajenas al SIDA, seguía existiendo una débil correlación entre la inclinación sexual y el tamaño del INAH 3. prosado@teleline.es