el tracto gastrointestinal - Universidad Centroccidental "Lisandro
Anuncio

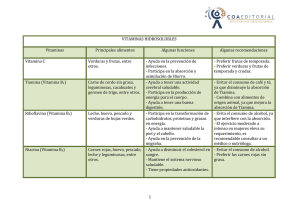
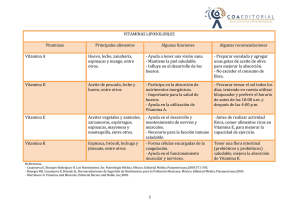
UNIVERSIDAD CENTROCCIDENTAL “LISANDRO ALVARADO” DECANATO DE CIENCIAS DE LA SALUD “DR. PABLO ACOSTA ORTIZ” DEPARTAMENTO DE CIENCIAS FUNCIONALES SECCION DE FISIOLOGIA FISIOLOGÍA II (V SEMESTRE) CAPITULO: FISIOLOGIA DIGESTIVA DIGESTION Y ABSORCION INTESTINAL DE NUTRIENTES Ramfis Enrique Nieto Martínez MD, MSc Profesor Asociado de Fisiología Humana. Enero 2013 Comentario [RR1]: CONTENIDO. Pag. I. INTRODUCCION.......................................................................... 1 II. INTEGRACION DEL TRACTO GASTROINTESTINAL CON OTROS ORGANOS.............................................................. 2 Higado........................................................................................... 2 Pancreas........................................................................................ 3 Cerebro........................................................................................... 3 Sistema inmunológico...................................................................... 4 III. FUNCIONES DEL TRACTO GASTROINTESTINAL...................... 5 3.1. Transporte de membrana........................................................... 5 3.1.1. Transporte pasivo....................................................................... 5 3.1.2. Transporte activo........................................................................ 7 3.2. Digestión de carbohidratos, proteínas y lípidos........................ 11 Carbohidratos................................................................................... 11 Proteínas.......................................................................................... 12 Lípidos.............................................................................................. 13 3.3. Función absortiva del tracto gastrointestinal............................. 16 Carbohidratos................................................................................... 16 Péptidos y aminoácidos..................................................................... 17 Grasa................................................................................................. 18 Iones y agua....................................................................................... 18 Vitaminas hidrosolubles...................................................................... 19 Vitaminas liposolubles......................................................................... 22 Minerales............................................................................................. 25 IV. ABSORCIÓN DE IONES Y AGUA...................................................... 31 4.1. Soluciones de rehidratación oral (SRO) ....................................... 33 4.2. Guías para el uso de las SRO.......................................................... 34 2 V. FACTORES QUE AFECTAN LA FUNCION GASTROINTESTINAL..... 36 5.1. Maduración....................................................................................... 37 5.2. Vejez.................................................................................................. 38 5.3. Adaptación........................................................................................ 39 5.4. Nutrición............................................................................................ 40 VI. BIBLIOGRAFIA.................................................................................... 43 INTRODUCCIÓN El tracto gastrointestinal es un sistema complejo de órganos cuya función principal es llevar a cabo la digestión y absorción de los nutrientes, y simultáneamente proteger al organismo de microorganismos y substancias nocivas ingeridas. Después de la ingestión, el alimento es reducido mecánicamente, mezclado con enzimas digestivas y transformado en partículas absorbibles. Posteriormente, los nutrientes son absorbidos a través de una mucosa especializada, y lo que no se absorbe es eliminado. Mas del 95% de los carbohidratos, lípidos y proteínas ingeridos son absorbidos durante su paso a través de un tracto gastrointestinal que funcione normalmente. Sin embargo, la absorción de algunas vitaminas, minerales y elementos traza puede ser menos eficiente. La protección contra las sustancias nocivas ingeridas comienza con el proceso de selección y preparación de los alimentos antes de la ingestión; y en cierto grado, por la discriminación sensorial en el momento de la ingestión. La acción química de la saliva; así como la producción de moco, ácido gástrico y enzimas digestivas, pueden proteger al organismo de estas substancias nocivas. El sistema 3 inmunológico, que incluye la producción de anticuerpos luminales para neutralizar parásitos, bacterias y virus ingeridos, también ofrece una protección adicional. Del mismo modo, el vómito y la diarrea son mecanismos adicionales de defensa. Las protaglandinas parecen contribuir a esta función protectora modulando la actividad motora y secretoria del intestino. Así, la inhibición de la síntesis de prostaglandinas por agentes como los analgésicos antiinflamatorios no esteroideos, afecta la integridad de la mucosa grastroduodenal y predispone a la formación de ulceras. OBJETIVOS Al finalizar esta actividad el estudiante estará en capacidad de: 1. Explicar la integración del tracto gastrointestinal con otros organos (higado, pancreas, cerebro y sistema inmunolóigico) 2. Enumerar las funciones del tracto gastrointestinal 3. Describir los mecanismos de transporte a traves de la membrana: Transporte activo y transporte pasivo 4. Describir los mecanismos de digestión y absorción de los macronutrientes (Carbohidratos, lipidos y proteinas) y micronutrientes (vitaminas y minerales) 5. Describir los mecanismos de absorción del agua y electrolitos 6. Explicar algunos factores que afectan la función gastrointestinal (maduración, vejez, adaptación, nutrición) 4 - Comentario [RR2]: I. INTRODUCCIÓN El tracto gastrointestinal es un sistema complejo de órganos cuya función principal es llevar a cabo la digestión y absorción de los nutrientes, y simultáneamente proteger al organismo de microorganismos y substancias nocivas ingeridas. Después de la ingestión, el alimento es reducido mecánicamente, mezclado con enzimas digestivas y transformado en partículas absorbibles. Posteriormente, los nutrientes son absorbidos a través de una mucosa especializada, y lo que no se absorbe es eliminado. Mas del 95% de los carbohidratos, lípidos y proteínas ingeridos son absorbidos durante su paso a través de un tracto gastrointestinal que funcione normalmente. Sin embargo, la absorción de algunas vitaminas, minerales y elementos traza puede ser menos eficiente. La protección contra las sustancias nocivas ingeridas comienza con el proceso de selección y preparación de los alimentos antes de la ingestión; y en cierto grado, por la discriminación sensorial en el momento de la ingestión. La acción química de la saliva; así como la producción de moco, ácido gástrico y enzimas digestivas, pueden proteger al organismo de estas substancias nocivas. El sistema inmunológico, que incluye la producción de anticuerpos luminales para neutralizar parásitos, bacterias y virus ingeridos, también ofrece una protección adicional. Del mismo modo, el vómito y la diarrea son mecanismos adicionales de defensa. Las protaglandinas parecen contribuir a esta función protectora modulando la actividad motora y secretoria del intestino. Así, la inhibición de la síntesis de prostaglandinas por agentes como los analgésicos antiinflamatorios no 5 esteroideos, afecta la integridad de la mucosa grastroduodenal y predispone a la formación de ulceras. II. INTEGRACIÓN DEL TRACTO GASTROINTESTINAL CON OTROS ÓRGANOS. El tracto gastrointestinal es un órgano muy activo metabólicamente. Sin embargo, aunque contiene la mayoría de las enzimas presentes en el hígado, las vías metabólicas son menos activas que en el hígado. Sus funciones metabólicas están dirigidas principalmente a soportar la digestión y a entregar los nutrientes absorbidos al hígado para su posterior procesamiento. Esta función demanda cantidades substanciales de energía y un aumento del riego sanguíneo del tracto gastrointestinal en el período postabsortivo. En ese período, el tracto gastrointestinal consume alrededor de 30% del gasto cardíaco para obtener esa energía. Hígado. El hígado es el órgano que tiene la mayor responsabilidad en la homeostasis metabólica de los nutrientes ingeridos. El hígado participa en la absorción de lípidos a través de la secreción de bilis, y en la modulación del nivel sanguíneo de nutrientes, a través de la captación de los nutrientes absorbidos provenientes de la vena porta y su posterior liberación a la vena hepática. Otras funciones hepáticas incluyen la destoxificación de drogas y químicos nocivos, modulación de ciertas hormonas circulantes, y eliminación de organismos patógenos. 6 La sangre venosa proveniente del tracto gastrointestinal es llevada al hígado por la vena porta. Con excepción de los quilomicrones intestinales que entran a los linfáticos, todos los productos absorbidos se dirigen inicialmente al hígado donde, en la mayoría de los casos, son extraídos y modificados antes de llegar a la circulación sistémica. Muchos nutrientes y drogas tienen una circulación enterohepática por su excreción en la bilis y su posterior reabsorción a nivel del intestino delgado. La interrupción de éste ciclo, debido a problemas biliares o dificultades en la reabsorción, ocasiona deficiencias nutricionales específicas. Entre las sustancias que tienen circulación enterohepática se incluyen las sales biliares, vitamina D, vitamina B12, folato, colesterol y drogas como el metrotexate. La circulación enterohepática del metrotexate (droga inmunosupresora), expone mas a estos dos órganos a la droga, y aumenta su tendencia a producir toxicidad intestinal y hepática. Páncreas. La actividad endocrina y exocrina del páncreas está íntimamente relacionada con la captación hepática y gastrointestinal de nutrientes. La insulina es liberada por las células beta del páncreas en respuesta a un aumento en la glucosa o aminoácidos plasmáticos, estimulación vagal, o un aumento en la circulación de gastrina, colecistoquinina o secretina. Todos estos signos postprandiales parece que se originan en el intestino. Por otro lado, la función exocrina pancreática, la cual es estimulada por hormonas liberadas por la mucosa del intestino delgado en respuesta a los nutrientes intraluminales, contribuye a la digestión y absorción de los alimentos. De manera recíproca, el páncreas produce 7 somatostatina, la cual parece modular la actividad funcional y metabólica del intestino. Cerebro. La relación entre el cerebro y el tracto gastrointestinal es mas compleja de lo que se suponía inicialmente. Se han descrito mas de 15 péptidos que se localizan tanto en el cerebro como en el intestino. Además de las funciones hormonales y neurotransmisoras en el intestino, algunos de esos péptidos muestran actividad paracrina sobre las células adyacentes. Muchos de esos mismos péptidos también parecen actuar como neurotransmisores en los ganglios nerviosos centrales. Se ha creado un nuevo termino que describe éste sistema de transmisión común en el cerebro y el tracto gastrointestinal - el “sistema nervioso peptidérgico”-. Entre estos péptidos se encuentran el péptido intestinal vasoactivo (VIP), motilina, colecistoquinina (CCK) y somatostatina. Además, muchos péptidos opiáceos y endorfinas se encuentran también tanto en el cerebro como en la mucosa intestinal. En el cerebro, estos neurotransmisores pudieran modular el dolor; mientras que en el intestino, parecen inhibir la secreción y motilidad gastrointestinal. Por otro lado, el apetito juega un rol principal en la conducta orientada a la búsqueda de alimento. Aunque el mecanismo no esta completamente claro, el apetito parece estar regulado por el sistema nervioso central, particularmente el hipotálamo. Existen estudios que postulan la relación entre la regulación del apetito y los péptidos transmisores mencionados anteriormente. 8 Sistema inmunológico. El intestino es una barrera importante entre el ambiente externo e interno. Para defender al organismo de substancias nocivas, el sistema inmune puede influenciar favorablemente la absorción de ciertos nutrientes; de manera inversa, la malnutrición o ciertas toxinas en la dieta, pueden afectar la función inmunológica. El sistema inmune puede reducir la cantidad de antígeno absorbido por el intestino. Un daño en el sistema inmune ha sido implicado en la génesis de algunas patologías que afectan la función intestinal y el estado nutricional. Entre estas patologías se incluyen la enteropatía sensible al gluten, alergias alimentarias, síndromes de inmunodeficiencia, y posiblemente, la enfermedad inflamatoria intestinal. III. FUNCIONES DEL TRACTO GASTROINTESTINAL. Después de la ingestión, el alimento es masticado y deglutido. Subsecuentemente, la integración entre la motilidad y la secreción incrementan la digestión y el contacto con la mucosa, para ser finalmente absorbido. Tanto la secreción como la motilidad están sujetas a control exógeno llevado a cabo principalmente por los sistemas autónomos intrínsecos tanto nervioso como hormonal. De las funciones del tracto gastrointestinal, se hará énfasis en los procesos de digestión y absorción de nutrientes, así como en el transporte de membrana. 9 3.1. Transporte de membrana. Las substancias pueden ser transportadas a través del epitelio intestinal por transporte pasivo (mediado por gradientes electroquímicos) o por transporte activo (mediado por mecanismos dependientes de energía). El transporte difusional (pasivo) depende del tamaño de la substancia, así como de su solubilidad en los lípidos. Los transportadores de membrana incrementan la capacidad de transporte de algunos substratos. 3.1.1. Transporte pasivo. La permeabilidad de la mucosa gastrointestinal es el factor determinante del transporte pasivo. La principal fuerza que conduce el transporte pasivo de agua y solutos es el gradiente de concentración o electroquímico que se establece a través de la mucosa gastrointestinal. Tomando en cuenta que las membranas está compuestas por una doble capa de lípidos, la mayor solubilidad en lípidos facilita el transporte pasivo de solutos. El movimiento de partículas con carga eléctrica a través de las membranas presenta problemas especiales. Estas partículas cargadas generalmente son insolubles en grasas y solo pueden atravesar la membrana a través de canales acuosos. La distribución pasiva de las partículas cargadas a ambos lados de la membrana depende de la diferencia química y eléctrica predominante. La tasa de transporte pasivo de un soluto con carga eléctrica depende del tamaño, así como de la carga del canal acuoso. El tamaño de los canales acuosos oscila entre, alrededor de 15 nm en el yeyuno hasta sólo 4 nm en la parte del 10 colon menos permeable. La carga neta dentro del canal depende de la relación entre los grupos amino y carboxilo de las proteínas del canal. Por ejemplo, el numero de grupos anionicos carboxilo en la vesícula biliar, sobrepasa el numero de grupos cationicos amino, esto hace que los canales presenten una carga neta negativa. Esto hace que la vesícula biliar sea mas permeable a los cationes, ya que las cargas opuestas se atraen unas a otras. En el estómago, ocurre lo contrario. Otra particularidad del tracto gastrointestinal, es el microambiente inmediatamente adyacente a la membrana luminal. Esta capa de fluido no es idéntica a la que se encuentra en el centro de la luz intestinal, y como ningún movimiento peristaltico puede afectarla, ha sido llamada “capa de agua no agitada”. Su presencia tiene dos consecuencias importantes: (1) Por su carácter acuoso, representa la principal barrera a la absorción de lípidos; (2) considerando que posee grupos ácidos en el glucocalix, el pH bajo de la capa de agua no agitada influye sobre la absorción de electrolitos débiles, incluyendo muchas drogas. Finalmente, cuando se considera el transporte pasivo en el tracto gastrointestinal, debe destacarse que existen vías de permeabilidad entre una célula epitelial y otra. Estas vías intercelulares o paracelulares tienen particular importancia en el transporte de pequeños electrolitos y el agua. El cemento proteico de las uniones celulares sirve como un canal alterno para la difusión pasiva. En el íleon, 4 veces mas cantidad de agua y electrolitos atraviesan las vías paracelulares que las propias membranas celulares. En la vesícula biliar esta relación es de 20 veces. 11 En resumen, muchos factores pueden influenciar la permeabilidad y por tanto el transporte pasivo del agua y substratos a través del epitelio gastrointestinal. Estos factores se ilustran en la figura 1. Concentración y gradiente eléctrico Transporte pasivo Capa de agua no agitada Tamaño y carga del poro Carga del soluto Vías paracelulares Solubilidad en lípidos Figura 1. Factores que influyen en la permeabilidad y el transporte pasivo de agua y substratos a través del epitelio gastrointestinal (Reproducido de Shils, 1994). 3.1.2. Transporte activo. En el transporte activo existe la interacción de la substancia transportada con uno de los componentes proteicos de la membrana. Esta interacción reúne todas las características de la interacción entre una enzima y un substrato: la reacción es saturable, existe competencia entre substratos estructuralmente similares, tiene especificidad para los esteroisómeros de los substratos, y puede ser inhibida por inhibidores metabólicos. Así, la proteína “transportadora” que moviliza al substrato de un lado a otro de la membrana, puede ser considerada como una enzima especializada de membrana. Este tipo de transporte es llamado “mediado por transportador”. El transporte mediado por transportador viene a llenar la necesidad de la célula gastrointestinal de 12 permitir que substancias hidrosolubles grandes crucen la membrana, y hace que substratos esenciales puedan movilizarse en contra de fuerzas generadas por gradientes químicos o eléctricos. Por el contrario, la difusión facilitada es un tipo de transporte pasivo, mediado por un transportador especifico que facilita la difusión de la substancia al otro lado, sin necesidad de energía. Si el transporte mediado por transportador utiliza energía y opera en contra de un gradiente, es llamado transporte “activo” (transporte activo primario). La energía metabólica para éste movimiento de substancias a través de la membrana es el adenosin trifosfato (ATP). La liberación de energía es provocada por una ATPasa que hidroliza el fosfato terminal del ATP para formar adenosin difosfato (ADP). Así, cada proceso de transporte activo es conducido por la actividad de una ATPasa de membrana. Las ATPasas no necesariamente son específicas para la substancia que es transportada. Por ejemplo, el transporte activo de azúcares y aminoácidos carece de ATPasas específicas, y su transferencia activa se produce por el acoplamiento al transporte activo de Na+ (transporte activo secundario o acoplado). Así, la proteína transportadora de azúcares y aminoácidos tiene sitios específicos para glucosa (o aminoácidos), y también para el Na+. La unión de Na+ y azúcar, o Na+ y aminoácido, ocurre en el lado luminal de la membrana, desde donde ellos difunden al lado intracelular para ser liberados (figura 2). Los requerimientos de energía metabólica de éste proceso se originan en el lado opuesto de la célula en la membrana basolateral. Aquí, el Na+ es sacado activamente de la célula por la bomba Na+/K+ , la cual conserva el gradiente de Na+ a través de la membrana mucosal. El 13 movimiento de azúcar y aminoácidos hacia afuera a través de la membrana basolateral es energéticamente favorable y pudiera ocurrir por difusión facilitada. Membrana mucosal Transportador lado seroso ? Sitio Azúcar T1 Difusión facilitada Sitio 2 Na+ 2 Na+ (50 mEq/L) ATP Na+ ADP T2 Na+ (140 mEq/L) Figura 2. Diagrama del mecanismo propuesto para el transporte activo acoplado de azúcares y aminoácidos con Na+. T1, transportador 1 para el transporte acoplado al interior de la célula; T2, transportador 2 para el transporte de Na+ fuera de la célula. (Reproducido de Shils, 1994). Virtualmente todas las substancias entran o salen de la células del tracto gastrointestinal total o parcialmente por transporte pasivo simple (difusión simple). Muchas substancias son transportadas en ausencia de acoplamiento con sodio, y algunas son transportadas en mas de una 14 forma. No es correcto asignar a cada nutriente un mecanismo de absorción único. El mecanismo de transporte de un nutriente puede ser diferente en la membrana apical, o basolateral del enterocito, y variar de acuerdo al estado fisiológico del individuo. Los distintos tipos de transporte utilizados en la transferencia de substancias a través de las membranas intestinales son enumerados en la tabla 1. La tabla 1 muestra que las proteínas totales pueden ser transportadas por pinocitosis. Este proceso puede ser importante en la absorción de pequeñas cantidades de inmunoglobulinas de la leche materna, y es activo porque requiere de energía. Tabla 1. Tipos de transporte a través de las membranas intestinales *. TRANSPORTE PASIVO SIMPLE Agua Lípidos Drogas Electrolitos Azucares Aminoácidos Vitaminas Esteroles FACILITADO Azúcares Aminoácidos Electrolitos TRASPORTE ACTIVO ACTIVO Electrolitos Azucares Aminoácidos Dipéptidos Vitaminas Acidos biliares ACTIVO ACOPLADO Electrolitos Azúcares Aminoácidos Vitaminas PINOCITOSIS Proteínas * Reproducido de Shils, 1994. 15 3.2. Digestión de carbohidratos, proteínas y lípidos. Las secreciones provenientes de la boca, estómago, intestino delgado, hígado y páncreas son mezcladas con los alimentos. En consecuencia, las moléculas complejas son hidrolizadas a componentes simples que pueden ser absorbidos. Carbohidratos. La principal forma dietaria de los carbohidratos son los polisacáridos (almidones y componentes de la fibra dietaria), disacáridos (sucrosa y lactosa), y monosacáridos (glucosa y fructosa). La digestión y absorción de los carbohidratos ocurre en la boca, estómago e intestino delgado (figura 3). En humanos, la fermentación bacteriana de los carbohidratos que no son absorbidos en el intestino delgado sólo provee una cantidad insignificante de energía. Los azúcares simples (glucosa, fructosa y galactosa) son absorbidos por procesos saturables mediados por proteínas transportadoras. La deficiencia de las enzimas del borde en cepillo (lactasa, maltasa, sucrasa etc.) puede producir malabsorción de carbohidratos. Esta malabsorción puede causar diarrea, acompañada frecuentemente de flatulencia. La diarrea y la flatulencia son producto de la fermentación bacteriana en el ciego de los disacáridos no absorbidos, produciéndose gas y partículas osmóticamente activas. La fibra dietaria, compuesta predominantemente por carbohidratos, es resistente a las enzimas digestivas humanas, pero es desdoblada por las bacterias. Esto produce un incremento en el volumen y contenido acuoso de las heces. 16 El consumo de fibra en exceso, también puede causar diarrea con flatulencia. BOCA ESTOMAGO INTESTINO LUMEN CELULA EPITELIAL Borde en Citosol cepillo PT galactosa galactosa LACTOSA (0-100% de los CHO dietarios en la infancia) Lactosa Lactasa Na+ glucosa PT Na+ glucosa Transporte activo ALMIDON (60-70% de los CHO dietarios despues de la infancia) Amilasa alfadextrinas maltotriosa HCl dextrinasa isomaltasa dextrinasa Amilasa pancreática maltosa Glucosa PT Na+ maltasa Dextrinas SUCROSA (20-30% de los CHO dietarios despues de la infancia) fructosa glucosa Glucosa Difusión facilitada sucrasa Fructosa PT Na+ Figura 3. Digestión de los carbohidratos (Reproducido de Shils, 1994). 17 Proteínas La digestión de las proteínas ocurre en el estómago y en el intestino delgado. Los productos finales son aminoácidos, dipéptidos y tripéptidos. Las activación de las diferentes enzimas que intervienen en la digestión de las proteínas se esquematiza en la figura 4. ESTOMAGO INTESTINO AMINOACIDOS Exopeptidasas Carboxipeptidasas Procarboxipeptidasa PEPTIDOS Pepsina + HCL PROTEINAS Elastasa Endopeptidasas Quimiotripsina Proelestasa Quimiotripsin ó-geno + Pepsinógeno Tripsina Tripsinógeno + Enteroquinasa Figura 4. Relación entre las enzimas que intervienen en la digestión de las proteínas. En el estómago, las pepsinas activadas hidrolizan las proteínas a polipéptidos de diversos tamaños. Dentro del intestino delgado, las endopeptidasas pancreáticas (tripsina, quimiotripsina y elastasa) rompen los enlaces peptídicos internos de las proteínas para producir péptidos mas pequeños. Las exopeptidasas (carboxipeptidasa A y B) clivan los enlaces terminales de los péptidos grandes para producir aminoácidos libres y fragmentos de péptidos. Estas enzimas tienen un pH óptimo de 8,0, y la hipersecreción de ácido gástrico puede dañar su 18 función. Las peptidasas del borde en cepillo y citosólicas hidrolizan los péptidos pequeños para producir aminoácidos. La digestión de las proteínas se resume en la figura 5. Lípidos Los principales lípidos en la dieta son los triglicéridos, fosfolípidos, colesterol y ésteres de colesterol (figura 6). La lipasa lingual, producida en las glándulas linguales, hidroliza algunos triglicéridos dentro del estómago a ácidos grasos y diglicéridos. Dentro del intestino delgado, la lipasa pancreática continúa la hidrólisis de éstos últimos, para producir ácidos grasos libres y glicerol. La colipasa es un polipéptido pancreático que proviene de la activación de la procolipasa por parte de la tripsina y actúa como cofactor para la lipasa pancreática. La colipasa se une a la interfase sales biliares-triglicéridos-agua mejorando la actividad de la lipasa. También ha sido identificada una lipasa intestinal pero no se conoce su función precisa. 19 BOCA ESTOMAGO INTESTINO LUMEN PROTEINA CELULA EPITELIAL Borde en Citosol Proteína de leche (60-100% de la proteína dietaria en la infancia) Renina Lactalbumina cepillo cuajo globulinas algunas proteínas son absorbidas caseína catepsina pepsinógeno Vena porta pepsina HCl aa ácidos PT Na+ pepsina aminoácidos aa PROTEINA HCl Aminoácidos aa neutros péptidos PT Na+ aa básicos Péptidos Tripsina proelastasa quimiotripsinógeno procarboxipeptidasa PT peptidasas peptidasas PT Na+ péptidos Na+ enteroquinasa Tripsinógeno Figura 5. Digestión de las proteínas (Reproducido de Shils, 1994). 20 BOCA ESTOMAGO INTESTINO LUMEN CELULA EPITELIAL Borde en Citosol cepillo GRASA a los linfáticos Lipasa pancreática Triglicérido Quilomicrones Colipasa TCL (> 12 C) AG libres Glicerol di y monoglicéridos apoproteína Lipasa lingual fosfolípidos colina colesterol ácidos grasos di y monoglicéridos + Micelas lípidos dietaácidos grasos (AG) rios ( > 12 C) vitaminas A,K, D y E. sales biliares TCM (<12C) TCM lipasa di y monoglicéridos monoglicéridos AG < 12 C Vena Porta Figura 6. Digestión de los lípidos (Reproducido de Shils, 1994). 21 Las sales biliares, las cuales tienen terminaciones tanto hidrofílicas como hidrofóbicas, forman micelas. Las micelas tienen una capa hidrofílica externa (hidrosoluble), lo cual facilita la absorción de su contenido liposoluble (ácidos grasos, colesterol y vitaminas liposolubles). Los triglicéridos que contienen ácidos grasos de menos de 12 átomos de carbono pueden ser absorbidos directamente sin necesidad de hidrólisis. Es posible que la absorción de triglicéridos de cadena media no sea cuantitativamente importante, ya que se ha observado que los infantes con déficit de lipasa-colipasa responden mejor a los extractos de enzimas pancreáticas que a las fórmulas de triglicéridos de cadena media. 3.3. Función absortiva del tracto gastrointestinal. Aunque la glucosa, el etanol, la aspirina y el agua pueden ser absorbidos a través de la mucosa oral y gástrica, los nutrientes y la mayoría de las drogas se absorben en el intestino delgado. El colon absorbe principalmente agua y electrolitos. Para la mayoría de los nutrientes el gradiente de absorción es descendente, con una mayor absorción en los primeros 120 centímetros de intestino en un humano adulto normal. Las substancias que son transportadas activamente, se absorben principalmente en el yeyuno. 22 Carbohidratos. Como fue discutido anteriormente, la entrada de sodio desde el lado luminal de la célula intestinal proporciona la fuerza necesaria para la transferencia de carbohidratos. Así, la glucosa es cotransportada al interior de la célula en contra de un gradiente de concentración (figura 2). Una vez que la glucosa es liberada de la proteína transportadora, se acumula en el enterocito y establece un gradiente de concentración para su difusión facilitada a través de la membrana basolateral hacia el interior de los espacios intercelulares, y finalmente a la sangre. Entre los substratos orgánicos hidrosolubles que son transportados de forma similar por acoplamiento con un gradiente dependiente de sodio, se incluyen aminoácidos, di- y tripeptidos, ácido ascórbico (vitamina C), sulfatos, fosfatos, sales biliares, bilirrubina y riboflavina (vitamina B2). Este mecanismo de transporte parece estar presente en muchas especies del reino animal y vegetal. Los aminoácidos y la glucosa pueden inhibir de forma recíproca su absorción, al competir por un aporte limitado de energía proveniente de este gradiente electroquímico. Un aumento en la concentración luminal de sodio, mejora la absorción de aminoácidos y glucosa, y viceversa. El conocimiento de este fenómeno ha permitido la utilización de soluciones de sodio-glucosa (soluciones de rehidratación oral) para contribuir al manejo de pacientes con síndromes diarreicos agudos. Péptidos y aminoácidos. Del mismo modo como ocurre con la absorción de glucosa, la absorción de aminoácidos es un proceso dependiente de sodio, 23 mediado por transportador y saturable. Los di-péptidos, y en algún grado, los tripéptidos, pueden ser absorbidos intactos. Sin embargo, las peptidasas citoplasmáticas hidrolizan los di- y tripéptidos, y hacen que la proteína dietaria que llega al hígado sea principalmente en forma de aminoácidos libres. Los aminoácidos libres son transportados a través de la membrana basolateral tanto por difusión pasiva, como por difusión mediada por transportador (difusión facilitada). Grasa. La absorción de las grasas generalmente es un proceso pasivo. Los ácidos grasos y triglicéridos con menos de 12 átomos de carbono (triglicéridos de cadena corta y media), pueden pasar directamente a la circulación portal. Los ácidos grasos y triglicéridos de cadena larga (mas de 12 átomos de carbono), requieren ser digeridos a ácidos grasos y monogliceridos para su solubilización micelar y una absorción eficiente. Aunque la bilis y las enzimas pancreáticas facilitan en gran medida la absorción de grasas, la lipasa del borde en cepillo y la difusión simple por sí solos permiten la absorción de una porción considerable de la grasa ingerida en un intestino sano. Además, en circunstancias fisiológicas a mayor cantidad de grasa ingerida, mayor cantidad será absorbida. Las grasas insaturadas son absorbidas mas fácilmente que las grasas saturadas. Una vez dentro del enterocito, los ácidos grasos y otras partículas de lipidos provenientes del interior de la micela, son empacados y liberados en los linfáticos como quilomicrones. 24 Iones y agua. + La bomba Na -K + dependiente de ATPasa, localizada en la membrana basolateral, saca sodio , manteniendo la electronegatividad intracelular. El sodio es absorbido por difusión pasiva desde la luz intestinal al interior del enterocito siguiendo el gradiente electroquímico creado por la ATPasa basolateral, y el cloro lo sigue pasivamente. Una pequeña cantidad de Cl HCO3 – – es reabsorbido activamente al intercambiarse con . El proceso descrito anteriormente ocurre principalmente en el íleon terminal y en el intestino grueso. El sodio intracelular es transportado activamente hacia al espacio extracelular. El agua se mueve pasivamente de acuerdo al gradiente osmótico prevalente y sigue al sodio hacia el espacio extracelular. El quimo permanece isotónico en todo su paso a través del intestino delgado y grueso. La liberación brusca de grandes cantidades de fluidos hipertónicos en el intestino delgado produce un flujo rápido de agua hacia la luz intestinal, lo cual puede conducir a hipovolemia y deshidratación. Vitaminas hidrosolubles. Las vitaminas hidrosolubles, cuando se consumen en cantidades fisiológicas, se absorben predominantemente por difusión pasiva o mediada por transportador. En la figura 7 se mencionan los mecanismos de absorción de algunas vitaminas hidrosolubles. Se ha sugerido que el ácido ascorbico (vitamina C), la riboflavina (vitamina B2) y la tiamina (vitamina B1) son absorbidas principalmente en el yeyuno por mecanismos dependientes de sodio. La vitamina B6, cuando es ingerida se encuentra principalmente en forma fosforilada. 25 Posteriormente en el intestino, las fosfatasas la transforman en piridoxal, piridoxina y piridoxamina, las cuales son absorbidas eficientemente (70 a 80%) por difusión pasiva en el yeyuno y en el íleon. La niacina (vitamina B3) en la dieta está presente en forma de nicotinamin-adenosin-dinucleotido y su forma fosforilada (NAD y NADP). Estas moléculas son hidrolizadas a niacinamida o acido nicotínico, los cuales son absorbidos por difusión simple (a concentraciones altas) o por difusión facilitada (a concentraciones bajas). La biotina (vitamina B8) en los alimentos está unida a proteínas por medio de un residuo de lisina (holocarboxilasa). En el intestino las proteasas separan a las proteínas (carboxilasas), quedando un compuesto que tiene la biotina unida a la lisina (biocitina). Posteriormente, una biocitidinasa separa a la biotina de la lisina, permitiendo su absorción. Sin embargo, no está claro si el mecanismo de absorción de la biotina es por difusión pasiva o mediante un transportador saturable. Por otro lado, el tetrahidrofolato-poliglutamato (ácido fólico) es 26 Acido ascórbico (Vitamina C) Riboflavina (Vitamina B2) Transporte activo acoplado con sodio Tiamina (Vitamina B1) Vitamina B6: Piridoxal-P Piridoxina-P Piridoxamina-P Fosfatasas Piridoxal Piridoxina Piridoxamina Difusión pasiva Niacina (Vitamina B3) Difusión: - Simple (Concentraciones altas) - Facilitada (Concentraciones bajas) NAD Niacinamida o NADP Acido nicotínico Glucohidrolasa Acido Fólico THF-Poliglutamato THF-Monoglutamato Conjugasa Transporte mediado por transportador Biotina (Vitamina B8) Biotina - C -N -Proteína O Lisina (Holocarboxilasa) Biotina - N- Lisina + Proteínas Proteasas Lisina + Biotina Biocitidinasa (Biocitina) (Carboxilasas) Difusión pasiva o Transportador saturable Figura 7. Mecanismos de absorción de algunas vitaminas hidrosolubles 27 hidrolizado a tetrahidrofolato-monoglutamato por una conjugasa dependiente de zinc que se encuentra en el borde en cepillo del epitelio intestinal. Posteriormente, es absorbido en el duodeno por un mecanismo mediado por transportador y dependiente del pH del medio. La cobalamina (vitamina B12) es absorbida por un mecanismo complejo con una eficiencia aproximada del 10% (figura 8). La vitamina B12 se une inicialmente a la proteína R (presente en la saliva y en el jugo gástrico), con la cual presenta una gran afinidad en el pH ácido del estomago. En el estomago, las endopeptidasas del jugo gástrico liberan a la vitamina B12 de otras proteínas, aumentando su afinidad con la proteína R. Posteriormente, en el duodeno, las enzimas proteolíticas secretadas por el páncreas, separan la vitamina B12 de la proteína R, y el pH alcalino (producto de la secreción de bicarbonato por el páncreas) favorece la unión de la vitamina B12 con el factor intrínseco (FI) secretado en la mucosa gástrica. Finalmente, el complejo vitamina B12FI es absorbido en sitios específicos (receptores) de las células del borde en cepillo del íleon distal. Aproximadamente el 99% de la absorción de vitamina B12-FI ocurre en el íleon distal, mientras que la absorción pasiva en el yeyuno e íleon proximal solo representa el 1%. Cualquier alteración en alguna de las estructuras involucradas en la absorción de la vitamina B12, puede disminuir su absorción y ocasionar una deficiencia clínica (anemia perniciosa). Estas alteraciones incluyen la resección o atrofia gástrica (por disminución del FI); sobrecrecimiento bacteriano o parasitario en el intestino delgado (por aumento en el consumo de vitamina B12 por parte de los microorganismos); daño del páncreas exocrino (por disminución de las enzimas y el bicarbonato); anticuerpos anti-FI (por aumento en la 28 destrucción del FI), y finalmente, enfermedad del íleon terminal (enteritis regional, resección ileal, o ausencia congénita de receptores ileales para vitamina B12 o FI). En caso de ausencia de FI o en B12 B12 - R ESTOMAGO - pH = 2 - Pepsina (Endopeptidasa) FI B12 = Vitamina B12 R = Proteína R. FI = Factor intrínseco PANCREAS - Enzimas - Bicarbonato DUODENO - pH = 7 a 8 B12 - FI ILEON Receptores para B12-FI Figura 8. Absorción de la vitamina B12. presencia de enfermedad del íleon terminal, con la administración de grandes dosis de vitamina B12 se pueden lograr una absorción adecuada, aunque es preferible el tratamiento parenteral. Vitaminas liposolubles. La absorción de la mayoría de las vitaminas liposolubles es por difusión pasiva y ocurre paralelamente a la absorción de grasas. En general, solamente alrededor del 50% de la dosis ingerida es retenida 29 (como es el caso de la vitamina D). Para casi todas las vitaminas liposolubles, es necesario que ocurra suficiente digestión por parte de las enzimas lipolíticas, formación de micelas lipídicas, difusión a través de la membrana del enterocito, y finalmente, transporte a los linfáticos (como quilomicrones) y en menor proporción a la circulación portal. La vitamina A es ingerida en la dieta en dos formas principales: vitamina A preformada (ésteres de retinol en alimentos de origen animal) o carotenoides provitamina A (en alimentos de origen vegetal)(figura 9). En el primer caso, los ésteres de retinol son hidrolizados por una lipasa pancreática no específica o colesterol esterasa en presencia de bilis con la formación de micelas. El retinol resultante es absorbido por difusión facilitada cuando está presente en la luz intestinal en concentraciones fisiológicas. Dentro del enterocito el retinol es reesterificado, y los ésteres de retinol resultantes son incorporados principalmente a los quilomicrones. La eficiencia de absorción de la vitamina A de la dieta, en personas sanas que consumen cantidades importantes de grasa (>10g/día), es mayor a 80%. En el caso de los carotenoides (betacaroteno principalmente), cuando se ingieren entre 1 y 3 mg diarios, la eficiencia de su absorción en humanos está alrededor del 40%. Es posible que exista un transportador de membrana o intracelular para carotenoides. Una vez dentro del enterocito, el betacaroteno es clivado por la 15, 15 dioxigenasa para ser transformado en 2 moléculas de retinal. Posteriormente, el retinal es convertido a retinol (vitamina A) por una deshidrogenasa; y finalmente, el retinol es esterificado e incorporado a los quilomicrones. Una parte del betacaroteno se incorpora directamente al quilomicrón y se absorbe intacto. 30 ESTERES DE RETINOL (ER) BETACAROTENO Sales biliares ER MICELA Difusión simple o transportador ? Lipasas - Esterasas RETINOL + ACIDO PALMITICO BETACAROTENO Difusión facilitada (Transportador) 15, 15 dioxigenasa 2 RETINAL RETINOL Ac. Palmitico BETACAROTENO Deshidrogenasa ENTEROCITO 2 RETINOL ER Acido palmitico ER QUILOMICRON ( LINFA ) ER BETACAROTENO Figura 9. Absorción de la vitamina A. El nivel de absorción de la vitamina K depende de la forma de esta vitamina presente en la dieta. La menadiona (vitamina K3, forma sintética), se absorbe en un 100% y pasa a la vena porta; mientras que la filoquinona (vitamina K1, de origen vegetal) y la menoquinona (vitamina K2, de origen animal o bacteriano) se absorben entre un 60 a 70%, pasando a los quilomicrones principalmente. La absorción ocurre mayormente por transporte activo (yeyuno); y por difusión pasiva (intestino distal y colon). La vitamina K producida por acción bacteriana (menoquinona), es absorbida en el colon. En el caso de la vitamina E, la absorción es facilitada por una esterasa luminal de origen pancreático y dependiente de sales biliares (figura 10). La absorción de todas las vitaminas liposolubles puede ser afectada por cualquier enfermedad que produzca malabsorción de grasas, tales como insuficiencia pancreática u obstrucción biliar. 31 VITAMINA K K1 FILOQUINONA: Origen vegetal Transporte activo (yeyuno) K2 MENOQUINONA : Origen animal o bacteriano Difusión simple (intestino distal y colon) K3 MENADIONA : Origen sintético VITAMINA E. ESTERES TOCOFEROL Difusión simple Esterasa Tocoferol acetato Tocoferol palmitato Figura 10. Absorción de las vitaminas K y E. Minerales. Calcio. La eficiencia relativa de absorción de calcio es baja (25 a 50 %), y es afectada por múltiples factores luminales y hormonales (altos niveles circulantes de cortisol, tiroxina y estrogeno). Aunque la acidez gástrica tiene poco efecto en la absorción del calcio proveniente de la dieta, la solubilidad de las sales de calcio presentes en los suplementos de calcio, se incrementa en el ambiente ácido del estomago. Por esa razón, es conveniente administrar los suplementos de calcio con las comidas, ya que el alimento estimula la secreción gástrica y retrasa su vaciamiento, permitiendo una mejor dispersión y disolución de las fuentes de calcio. 32 Por otro lado, cuando existe déficit de vitamina D, disminuye la absorción de calcio. Como mecanismo homeostático, para mantener el nivel de calcio circulante, se puede producir osteopenia (disminución de la masa ósea por resorción de calcio). La baja ingesta de calcio en forma crónica, produce una disminución sus niveles plasmáticos (hipocalcemia), lo cual estimula la producción de paratohormona, produciéndose un hiperparatiroidismo secundario (aumento de la actividad de la glándula paratiroides). La paratohormona estimula la secreción de 1,25 dihidroxicolecalciferol (metabolito de la vitamina D), quien incrementa la absorción de calcio en el intestino para compensar la hipocalcemia. Tanto la paratohormona, como el 1,25 dihidroxicolecalciferol, también aumentan la resorción ósea, para liberar calcio al plasma. Por lo tanto, si la ingesta insuficiente de calcio se prolonga en el tiempo, se produce osteopenia que puede manifestarse como osteomalacia (mineralización defectuosa) u osteoporosis (remodelamiento óseo anormal). Cuando el defecto de mineralización se produce en el cartílago epifisiario de los huesos en crecimiento se denomina raquitismo (figura 11). Los estrógenos aumentan la síntesis de 1,25 dihidroxicolecalciferol; la disminución de éstos en mujeres postmenopáusicas quizás explique su mayor predisposición a presentar osteoporosis. 33 HIPERPARATIROIDISMO ( PARATOHORMONA) DIETA BAJA EN CALCIO OSTEOPENIA 1,25 (OH) 2- COLECALCIFEROL Si se prolonga OSTEOMALACIA OSTEOPOROSIS RAQUITISMO Figura 11. Regulación de la absorción de calcio. En cuanto a los mecanismos de absorción (figura 12), existen dos rutas para la absorción de calcio en el intestino. Una es un proceso activo, saturable, transcelular que ocurre principalmente en el duodeno y yeyuno proximal. Este proceso es regulado por la vitamina D e involucra a una proteína fijadora de calcio dependiente de vitamina D (CaBP o calbidina). El calcio es bombeado fuera del enterocito a la sangre por una bomba de calcio dependiente de ATP. Esta absorción activa de calcio depende del estado fisiológico del sujeto. Por lo tanto, es afectada por el estado nutricional del calcio y la vitamina D, edad, embarazo y lactancia. 34 TRANSPORTE ACTIVO (transcelular) TRANSPORTE PASIVO (Paracelular) CALCIO CALCIO CaBP (Calbidina) Dependiente de vitamina D ENTEROCITO CALCIO Nucleo Bomba de calcio dependiente de ATP CALCIO LUGAR: Duodeno y yeyuno proximal DEPENDE DE: - Estado nutricional del calcio y vit. D. - Edad - Embarazo - Lactancia CALCIO LUGAR: Todo el intestino (+ en ileon) DEPENDE DE: - Cantidad y biodisponibilidad de calcio en la dieta. Figura 12. Mecanismos de absorción intestinal de calcio. La otra vía de absorción del calcio es la ruta paracelular, pasiva, no saturable, que es independiente de la regulación por parte de la vitamina D, y ocurre en todo el intestino delgado. La cantidad de calcio absorbida de esta forma, depende fundamentalmente de la cantidad y disponibilidad en la dieta. Cuando la ingesta de calcio en una comida es superior a 120 mg probablemente se absorbe por esta ruta. Aunque la velocidad de absorción del calcio en el íleon es mas lenta, la mayoría del calcio se absorbe a este nivel, donde el alimento permanece mas tiempo. Por lo tanto, la remoción del íleon afecta mas la absorción de calcio que la remoción del yeyuno. 35 Hierro. En personas sanas la pérdida de hierro del organismo es muy baja y el balance normal del hierro se mantiene por la regulación de la absorción. El hierro en la dieta se presenta principalmente como hierro no hemo (fuentes vegetales) o como hierro hemo (fuentes animales). El hierro hemo (orgánico) es ingerido en forma de hemoglobina y mioglobina, y se absorbe mejor que el hierro no hemo. Después que las enzimas proteolíticas separan la fracción proteica de la hemoglobina (globina), el hierro hemo se absorbe directamente e ingresa al plasma como Fe +++. Por otro lado, el hierro no hemo (inorgánico), es ionizado y solubilizado por el jugo gástrico, reducido a la forma ferrosa (Fe ++) y quelado. Los agentes quelantes como el ácido ascorbico, azúcares y aminoácidos; incrementan la absorción de hierro no hemo. Las secreciones gástricas normales contienen un factor estabilizante (quelante endógeno) , que disminuye la precipitación del hierro ingerido que ocurre bajo el pH alcalino del intestino delgado. La disminución de la absorción de hierro observada en pacientes con aclorhidria (disminución de la secreción de HCl del estomago) o gastrectomizados (resección parcial o total del estomago), puede ser debida a una menor solubilización o quelación del hierro. La forma ferrosa del hierro (Fe++) es mas soluble que la forma férrica (Fe+++), y por tanto, atraviesa la capa mucosa y alcanza el borde en cepillo mas rápido (figura 13). Una vez en el borde en cepillo, el Fe++ es oxidado a Fe+++, el cual es tomado por una proteína de membrana fijadora de hierro (MIBP=membrane iron binding protein) que lo 36 transfiere al interior de la célula. Del enterocito el hierro pasa al plasma, donde es tomado por la transferrina (proteína transportadora de hierro en el plasma). La apotransferrina (forma de la transferrina no unida al hierro) que se encuentra en el citosol del enterocito, puede incrementar la absorción de hierro. Quizás por esa razón la cantidad de apotransferrina en la célula intestinal aumenta cuando las necesidades de hierro son mayores. Una vez superada la capacidad de transporte, la porción del hierro citosólico restante se combina con la apoferritina para formar ferritina (proteína que almacena hierro en los tejidos). La mayoría de la ferritina se pierde con la descamación de los enterocitos cada 2 a 3 días. Cuando el aporte de hierro es excesivo, la mucosa es capaz de incorporarlo a la ferritina, para ser eliminado posteriormente en las células descamadas; mientras que cuando el aporte es deficiente, la mayoría del hierro se une a la transferrina para ser transportado. Algunos autores han denominado éste fenómeno como “bloqueo mucoso” de la absorción de hierro. Por lo tanto, considerando el mecanismo de regulación anteriormente mencionado y los efectos colaterales de los suplementos de hierro en algunos pacientes, hay autores que proponen la administración oral de suplementos de hierro semanalmente y no diariamente. La absorción de hierro puede ocurrir en cualquier parte del intestino delgado, pero es mas eficiente en el duodeno. El mecanismo de absorción es pasivo y relativamente ineficiente, ya que solo se absorbe entre el 5 al 15% del hierro ingerido. La absorción del hierro no hemo es inhibida por algunos componentes: fitatos (presentes en cereales y leguminosas), polifenoles (presentes en té y café), calcio, manganeso, zinc y fibra. Por el contrario, se ha observado que la reducción de los depósitos de hierro; así como el incremento en las necesidades 37 (eritropoyesis activa en caso de sangramiento o destrucción de eritrocitos), estimulan la absorción de hierro. Descamación celular Fe Fe VELLOSIDAD INTESTINAL Migración celular (Fe ++) Fe +++ Quelatos Fe Fe Fe - Transferrina Transferrina Fe hemo Fe + Hemo LUZ INTESTINAL SANGRE Ferritina Lisosoma CRIPTA Figura 13. Mecanismos de absorción de hierro (Tomado de Linder 1991). Zinc. El zinc es absorbido por difusión facilitada en todo el intestino delgado con una eficiencia del 20 al 40%. La absorción mejora cuando hay 38 deficiencia de zinc. El zinc orgánico es mejor absorbido que el zinc inorgánico, y éste ultimo es mas afectado por factores luminales tales como fitatos, fibra dietaria, fosfatos y otros cationes. La absorción de zinc es facilitada por ligandos que se unen al zinc que se encuentran tanto en la leche humana, como en las secreciones pancreáticas. Aunque 1 o 2 mg de zinc pueden ser secretados por el páncreas diariamente, éste es reabsorbido en el intestino delgado. Por lo tanto, los pacientes con enfermedades malabsortivas tienen mayor riesgo de presentar una deficiencia de zinc. Durante la absorción de zinc, la célula intestinal retiene grandes cantidades del zinc absorbido, el cual se une a una proteína intracelular llamada metalotioneina. El zinc unido a metalotioneina se puede perder en las heces por descamación celular. Por tanto, la metalotioneina puede contribuir a regular la absorción o retención de zinc. Otros minerales. Poco se conoce de la absorción de otros elementos traza como el yodo, cromo, manganeso, selenio y molibdeno. Cada uno de ellos parece ser absorbido pasivamente, con distintos grados de eficiencia. Excepto en áreas geográficas donde el suelo es muy deficiente el yodo o selenio, la deficiencia de estos minerales es extremadamente rara y generalmente se asocia con enfermedad intestinal severa y/o uso prolongado de nutrición parenteral total. El colon. El colon tiene una gran capacidad absortiva, particularmente de agua. El colon absorbe aproximadamente 850 ml de los 1000 ml de agua que 39 en promedio pasan la valvula ileocecal. La absorción colónica de glucosa, aminoácidos y vitaminas es baja, al contrario de los ácidos grasos de cadena corta (producto del metabolismo colonico bacteriano de los carbohidratos no absorbidos), los cuales son absorbidos principalmente en el colon. Además, la mucosa rectal proporciona una ruta para la administración de ciertas drogas, incluyendo sedantes, analgésicos, antipiréticos, y esteroides. IV. ABSORCIÓN DE IONES Y AGUA El epitelio gastrointestinal controla el intercambio de agua, electrolitos y otros compuestos hidrosolubles entre la luz intestinal y la circulación. La mucosa del intestino delgado es libremente permeable al agua, la cual sigue el movimiento de los electrolitos. El transporte de electrolitos también determina el paso de otras partículas hidrosolubles a través del epitelio intestinal, como es el caso del cotransporte sodioglucosa que mencionamos anteriormente. Este libre movimiento de fluidos y solutos hace que la presión osmótica del contenido yeyunal se equilibre con la del plasma. Es decir, los mecanismos de transporte pasivo en el intestino delgado son altamente capaces de equilibrar las diferencias creadas por los mecanismos de transporte activo de los electrolitos. Por lo tanto, es evidente la importancia que tiene el transporte activo de electrolitos desde el intestino al plasma en el mantenimiento del balance de fluidos y en la absorción de nutrientes. En contraste con el intestino delgado, el colon es menos permeable por mecanismos pasivos, pero mas activo en reabsorber los iones y el agua de la mucosa al plasma. Los iones Na+ y Cl- son absorbidos 40 activamente y el ion K+ es secretado en la luz del colon. Considerando que el epitelio del colon tiene una permeabilidad pasiva mas baja a los iones y al agua con respecto al intestino delgado, las diferencias de concentración creadas por los procesos de transporte activo no son fácilmente disipadas por los procesos de difusión simple de la mucosa. De éste modo, las concentraciones de electrolitos en las heces son diferentes a las concentraciones plasmáticas. A pesar de que las concentraciones de electrolitos en las heces son relativamente grandes, las cantidades perdidas son muy bajas considerando el pequeño volumen de las heces. Estas pequeñas perdidas, junto con la eficiente resorción renal de electrolitos, ayudan a explicar la capacidad de los humanos para sobrevivir a una ingesta extremadamente baja en sal. La regulación del transporte de iones influye en el movimiento de agua entre el medio ambiente y el organismo. El balance entre la secreción y absorción de agua es un proceso dinámico denominado ciclo enterosistémico del agua. Durante el ayuno, el agua que entra al lumen es reabsorbida después de la absorción de sodio. Por tanto, poca agua se pierde en las heces. Durante una comida, alrededor de 7 litros de agua pudieran entrar al lumen intestinal como consecuencia de las secreciones digestivas. El agua es reabsorbida durante la absorción de electrolitos y solutos, principalmente a través del sistema de cotransporte de sodio. 4.1. Soluciones de rehidratación oral (SRO) En el intestino se mantiene un proceso activo de absorción, que predomina en las células de la vellosidad intestinal; así como un 41 proceso activo de secreción, que ocurre principalmente en las células de la cripta de la mucosa intestinal. Además, la complejidad del funcionamiento intestinal aumenta, considerando que las células de la cripta se diferencian a células vellosas. El balance entre absorción y secreción depende tanto de la masa relativa de células vellosas respecto a las células de la cripta, como de la tasa de intercambio y diferenciación celular. Así, pueden existir patologías que afecten mas a las células de la cripta, lo cual fundamentalmente alterará la tasa de secreción; y patologías que afecten mas a las células vellosas mas maduras, lo cual afectará predominantemente la función absortiva. En ambos casos, las células vellosas remanentes pueden ser usadas para promover una máxima absorción del agua y de los solutos disponibles en la luz intestinal. El conocimiento de los mecanismos normales de absorción y secreción de fluidos, electrolitos y solutos; y de la forma como diversas enfermedades afectan estos procesos, han permitido el desarrollo de las soluciones orales diseñadas para aprovechar al máximo cualquier función absortiva remanente en el epitelio. Se ha documentado ampliamente los beneficios de las soluciones salinas de rehidratación oral (SRO) en el tratamiento de niños y adultos con deshidratación. La base fisiológica de la SRO es el transporte acoplado entre sodio y glucosa, u otra molécula orgánica pequeña transportada activamente. Para evitar la hipertonicidad (aumento de la osmolaridad en la luz intestinal), que pudiera inducir pérdidas adicionales de fluidos, estas soluciones están compuestas de concentraciones equimolares de glucosa y sodio. Las soluciones de rehidratación oral suplementadas con glucosa o aminoácidos, en general no disminuyen la diarrea, pero corrigen la deshidratación del paciente. Actualmente se están 42 investigando nuevas formulaciones en base a arroz, las cuales pudieran tener la ventaja adicional de disminuir la intensidad de la diarrea con respecto a las fórmulas utilizadas en la actualidad. 4.2. Guías para el uso de las SRO Los objetivos generales del uso óptimo de las SRO son: (1) corregir el déficit de agua y electrolitos existente, (2) reemplazar las pérdidas anormales de agua y electrolitos producidas por la diarrea, (3) proveer los requerimientos diarios de líquidos, y (4) permitir la alimentación temprana durante la terapia con fluidos. Generalmente con las SRO se logra rehidratar al paciente, excepto en aquellos casos de deshidratación severa, vómitos incontrolables, o presencia de una complicación seria, como la sepsis. Usualmente, las soluciones se dan por vía oral, aunque en algunos casos poco frecuentes, puede ser necesaria una infusión nasogastrica contínua. La Organización Mundial de la Salud (OMS) ha establecido recomendaciones generales para el uso de las SRO. Aunque su uso esta sometido a cambios constantes y las pautas en el futuro pueden variar en base a la nueva experiencia, a continuación se describen las recomendaciones actuales. Las SRO son usadas en dos fases: reemplazo inicial del déficit de líquidos y electrolitos (rehidratación) y subsecuentemente, reemplazo de las pérdidas (mantenimiento). Se ha documentado, la seguridad y eficacia de la fórmula de la OMS en ambas fases del tratamiento, aunque en un paciente con deshidratación leve se puede usar una solución que contenga menos sodio (70 meq/L) con respecto a las SRO. La tabla 2 muestra una lista de algunos de los principales fluidos utilizados para rehidratación oral. 43 El calculo de la dosis inicial de líquidos que requiere el paciente se basa en el grado de deshidratación estimada (Ej. un infante de 9 Kg con una deshidratación estimada en 10% requiere 1000 ml de SRO). La dosis debe ser administrada en 4 a 6 horas. A la cantidad total administrada se añaden las perdidas de líquidos en las heces. Después de las 4 a 6 horas de rehidratación, el paciente es examinado nuevamente, y pasado a la fase mantenimiento o sometido a un periodo adicional de rehidratación. En la fase de mantenimiento, una regla general es un niño requiere 4 ml/Kg por hora por los primeros 10 Kg de peso, 2 ml/Kg para los siguientes 10 Kg, y 1 ml/Kg por cada 10 Kg por encima de 20 (Ej. Un niño de 30 Kg requiere 40 + 20 + 10 ml/Kg por hora para mantenimiento). Se recomienda la incorporación temprana de una alimentación oral adecuada durante el tratamiento. Los 44 infantes alimentados con leche materna deben ser realimentados de esta forma durante la fase de mantenimiento; y los alimentados con fórmulas lácteas deberían volver a estas fórmulas cuando lo toleren. Tabla 2. Soluciones usadas comúnmente para el reemplazo de fluidos y electrolitos (Reproducido de Shils 1994) FLUIDO REHIDRATACION SRO OMS Rehidralite MANTENIMIENTO Pedialyte Ricelyte Jugo de manzana Gatorade CHO (g/L) NA+ K+ mEq/L* CL- BASE• 20 25 90 75 20 20 80 65 30 30 25 30 119 40 45 50 0.43 23.5 20 25 25 2.5 35 45 17 30 34 - Estos fluidos son de uso común para la rehidratación y mantenimiento en niños con diarrea y deshidratación. Las soluciones orales presentadas como Rehidratación también son usadas para el reeemplazo de pérdidas durante el mantenimiento, y proveen cantidad adecuada de fluido adicional cuando el niño recibe leche materna. El jugo de manzana y el Gatorade sólo se muestran para comparación, ninguno es recomendado durante la diarrea debido a su alta osmolaridad. • mEq potenciales de bicarbonato. Puede ser citrato o acetato. * Para Na+, K+ y Cl-, las unidades del Sistema internacional (mmol/L son equivalentes a mEq/L. Para las bases los mmol/L equivalen a 1/3 de los mEq/L (30 mEq/L = mmol/L). Son necesarios futuras investigaciones para diseñar nuevas SRO que puedan reducir el volumen y/o duración del episodio diarreico. Por ejemplo, el incremento de la concentración de glucosa pudiera incrementar la tasa de cotransporte de sal y agua; sin embargo, pueden aumentar la presión osmótica y esto promovería una mayor pérdida de agua por las heces. La idea de lograr un mayor contenido de glucosa sin incrementar la carga osmótica, pudiera lograrse usando polímeros de glucosa. Estudios recientes indican que polímeros basados en cereales (particularmente en arroz) promueven una reducción tanto del 45 volumen como de la duración de la diarrea, así como una recuperación rápida del apetito. Otros estudios tratan de evaluar el uso de otros sistemas de cotransporte con sodio, tales como aminoácidos, péptidos o proteínas pequeñas en el diseño de SRO. V. FACTORES QUE AFECTAN LA FUNCIÓN GASTROINTESTINAL Existen algunos factores capaces de afectar el funcionamiento del tracto gastrointestinal. Entre estos factores los mas importantes son los cambios fisiologicos en la diferentes etapas de la vida; así como el efecto de la presencia o ausencia de los nutrientes en el tubo digestivo. 5.1. Maduración. El tracto gastrointestinal del recién nacido experimenta muchos cambios madurativos durante los primeros 5 meses de vida. Hasta los 3 o 4 meses de edad, además del reflejo de succión, está presente el reflejo de extrusiòn, el cual protege al recién nacido contra la ingestión de sólidos potencialmente indigeribles. Aunque existe motilidad esofagica al nacimiento, la coordinación de las ondas propulsivas no se desarrolla hasta después de los 4 meses de vida postnatal. Entre los 3 y 6 meses de vida, la presión intragástrica normalmente excede la presión tanto del esofago como del esfinter esofagico inferior, lo cual provoca una alta incidencia de reflujo del contenido gastrico. Por otro lado, la coordinación de la motilidad gastrica es deficiente durante los primeros 3 o 4 meses de vida, lo cual hace insuficiente el mezclado de alimentos en el antro de estomago y la digestión de alimentos sólidos. A los 12 meses de edad, el tipo de peristalsis intestinal se hace similar 46 a la de niños mayores y adultos a los 12 meses de edad, pero es mas lenta. El tránsito lento puede servir para incrementar el tiempo de exposición del alimento a la mucosa intestinal y por tanto, mejorar la digestión y absorción de nutrientes. La función motora del intestino grueso parece estar madura al nacimiento. Durante el periodo neonatal la permeabilidad de la mucosa es máxima, y muchas moléculas grandes, incluyendo proteínas (inmunoglobulinas), tienden a ser absorbidas intactas. Este proceso provee mecanismos de transferencia pasiva de anticuerpos provenientes de la leche materna, pero también permite el paso de proteínas completas que potencialmente pueden provocar respuestas alérgicas. Las funciones secretorias y absortivas del intestino maduran durante los dos primeros años de vida. En general, los niños digieren y absorben mejor las grasas provenientes de aceites vegetales, que las grasas de origen animal. Las alfa-glucosidasas de la mucosa intestinal (sucrasa, maltasa e isomaltasa) están bien desarrolladas a las 32 semanas de gestación y al nacimiento sus niveles son cercanos a los del adulto. En contraste, la lactasa se desarrolla tardíamente en la vida fetal y no alcanza su maxima actividad hasta que comienza la alimentación del recién nacido. A pesar de que la actividad de la lactasa es relativa baja, las fórmulas que contienen lactosa son bien toleradas por los recién nacidos a término y por muchos recién nacidos de mas de 34 semanas. Los niños extremadamente prematuros (27 a 32 semanas), toleran mejor las fórmulas con menos de 60% del total de calorias carbohidratos provenientes de lactosa. 47 5.2. Vejez Los cambios de la función intestinal relacionados con la edad ocurren simultaneamente a la pérdida de masa magra (masa libre de grasa). En el anciano, además de afectarse la función gastrointestinal, también se altera la homeostasis de la glucosa, disminuye la depuraciòn de ciertas drogas, varia el control de la temperatura corporal, y se deteriora la función inmunológica. Otros cambios incluyen la pérdida de la dentición, disminución tanto del gusto como de la agudeza olfatoria, dismotilidad esofagica y retardo en el vaciamiento gastrico e hipoclorhidria (disminución de la secreción gastrica de HCl). Estos factores y el uso frecuente de medicamentos en ancianos, pueden contribuir al daño de la función del tracto gastrointestinal y a la mayor predisposición a presentar malnutrición. Muchos de los cambios fisiológicos observados en el envejecimiento (senescencia inmune, reducción en los niveles de proteína visceral, y la disminución en la masa magra), son similares a los observados cuando un sujeto joven está malnutrido. Sin embargo, el envejecimiento por sí solo parece que no afecta significativamente la absorción proteico-energética. En el anciano, la mayor lentitud en el vaciamiento gástrico y en el tránsito intestinal pudieran mejorar la eficiencia de absorción, particularmente de vitamina A. Sin embargo, la absorción de vitamina B12, calcio y zinc parece estar disminuída en la población anciana. 5.3. Adaptación El tracto gastrointestinal tiene una gran capacidad de adaptación, particularmente en niños. Cuando ocurre una resección intestinal extensa, el intestino residual es capaz de dilatarse considerablemente, 48 incrementar su rugosidad, e hipertrofiar sus vellosidades y microvellosidades; lo cual incrementa el área de superficie y la capacidad absortiva. Además, el recambio celular y la actividad enzimática también se incrementan. Estos cambios adaptativos pueden maximizarse por la exposición de la mucosa a nutrientes, secreciones biliares y pancreáticas y ciertos factores hormonales. La búsqueda de hormonas tróficas tiene implicaciones terapéuticas importantes, aunque hasta ahora ninguno de los factores estudiados ha mostrado estimular el crecimiento del intestino delgado. La acción trófica de la gastrina es ejercida principalmente sobre el esófago, estómago, colon y páncreas; y pudiera jugar algún rol en la adaptación del intestino delgado. La colecistoquinina tiene un efecto trófico moderado sobre el intestino delgado, aunque esto pudiera ser causado por su efecto estimulante de la secreción biliar y pancreática. Entre los factores que pueden limitar la adaptación intestinal se encuentran un aporte sanguíneo inadecuado, un estado nutricional deficiente, y la presencia de enfermedad residual. El íleon puede adaptarse mejor que el yeyuno, asumiendo ciertas funciones especializadas tales como la absorción activa de vitamina B12 y sales biliares. El tránsito mas lento en el íleon pudiera mejorar la capacidad absortiva, pero también proporciona un mejor ambiente para el sobrecrecimiento bacteriano. 5.4. Nutrición La función gastrointestinal es afectada por múltiples factores, algunos de los cuales responden a la dieta. Los alimentos parecen jugar un rol muy importante en el mantenimiento de la función gastrointestinal. 49 Ayuno y malnutrición Tanto el ayuno como la deficiencia de nutrientes específicos pueden afectar la función gastrointestinal. Se ha demostrado que acompañando a la malnutrición infantil y la diarrea prolongada generalmente se presenta esteatorrea e intolerancia a la glucosa. No se han evaluado los cambios que se producen en el intestino como consecuencia de una reducción de la ingesta dietética no asociada con malnutrición. Sin embargo, se reconoce que la restricción dietética con el objeto de perder peso, está asociada con síntomas gastrointestinales leves a moderados durante la realimentación. Estos síntomas resultan probablemente de una disminución, tanto en el contenido de enzimas de la mucosa; como de las secreciones gástrica, biliar, pancreática e intestinal por la restricción dietética. La deficiencia proteica severa predispone a una disfunción inmune que puede conducir a una diarrea prolongada, debido a la disminución de la capacidad inmunológica para responder a las bacterias ingeridas o al sobrecrecimiento bacteriano en el intestino delgado. Del mismo modo, se ha descrito que una deficiencia de vitamina A también puede prolongar un episodio diarreico. Entre las causas se señalan el defecto inmunológico causado por el déficit de vitamina A, un aumento en la actividad secretoria intestinal, el daño epitelial que disminuye tanto la absorción como la resistencia a las infecciones, y finalmente, la disminución en la proliferación celular intestinal. 50 Ausencia de ingesta enteral La exclusión de los alimentos por vía oral, a pesar del mantenimiento de una nutrición adecuada por alimentación parenteral, está asociada con cambios atróficos tanto en la capa muscular como en la mucosa del intestino. Cambios similares han sido descritos en aquellos segmentos de intestino sometidos a cortocircuito (procedimiento quirúrgico que hace que parte del intestino quede sin funcionamiento). Así, tanto la exposición a alimentos, como la presencia de secreciones gastrointestinales altas, son necesarias para mantener la morfología y la función gastrointestinal en condiciones óptimas. Glutamina como combustible intestinal La glutamina (aminoácido no esencial), ha sido estudiado por su papel en el mantenimiento del epitelio mucosal. Es posible que la glutamina sea el combustible preferido por las células que proliferan rápidamente, como el enterocito y los linfocitos. Algunas evidencias experimentales sugieren que durante una enfermedad crítica, la síntesis endógena de glutamina pudiera no satisfacer los requerimientos del organismo y pueden ser necesarios los suplementos de glutamina como una alternativa dentro del manejo médico. Adicionalmente, la administración de soluciones parenterales que contienen glutamina puede atenuar el grado usual de atrofia intestinal asociada con la nutrición parenteral. 51 Papel de la fibra en el mantenimiento de la función intestinal Es conocido que algunos tipos de fibra dietaria afectan la motilidad intestinal en el humano. Por ejemplo, las pectinas pueden retardar la tasa de vaciamiento gástrico; mientras que el salvado de trigo puede acelerar el transito en el colon. La adición de fibra a las dietas enterales, ha mostrado que mejora el crecimiento de la mucosa intestinal, la cicatrización de la anastomosis después de una resección del colon e incrementa la adaptación absortiva después de una resección masiva del intestino. Finalmente, es evidente que las funciones del tracto gastrointestinal son complejas y varían de acuerdo al estado fisiológico del individuo. Además, los factores que afectan su funcionamiento son múltiples. La intensa actividad metabólica del tracto gastrointestinal explica su comportamiento como un verdadero regulador de la digestión y absorción de nutrientes. Siempre que un tracto gastrointestinal funcione adecuadamente debe utilizarse para la nutrición de un paciente, ya que la colocación directa de los nutrientes en la sangre (nutrición parenteral), no garantizará en ningún momento las regulaciones fisiológicas para las cuales la evolución dotó a los seres vivos de un tracto gastrointestinal. 52 Bibliografía - Modern Nutrition in Health and Disease. Eighth edition (1994). Vol 1 & 2. Shils, M.E., Olson, J.A. y Shike, M. Edit. Lea & Febiger. Philadelphia. - Conocimientos actuales sobre nutrición. Sexta edición (1991). Organización Panamericana de la Salud (OPS) e Instituto Internacional de Ciencias de la Vida (ILSI). Washington, D.C. - Nutritional Biochemistry and Metabolism. Second Edition (1991). Maria C. Linder. Edit. Elsevier . New York. - Fisiología Medica. 12ª edición. (1990). William F. Ganong. Edit. El Manual Moderno. México, D.F. RENM/renm. 53 54