ESTADO SOLIDO Al contrario de lo que sucede con los
Anuncio

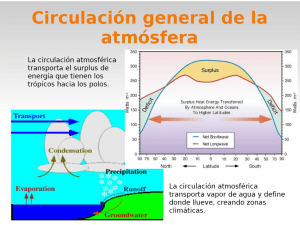
ESTADO SOLIDO Al contrario de lo que sucede con los estados líquido y gaseoso, una sustancia en estado sólido posee forma definida y rigidez. Por rigidez se entiende que la energía de las atracciones intermoleculares es mucho mayor que la energía cinética de las moléculas individuales. Los sólidos exhiben un amplio rango de propiedades; así una lámina delgada de hoja de aluminio es lo suficientemente flexible para utilizarse como envoltura, pero una lámina de vidrio de idéntico espesor no. Para organizar su estudio distinguiremos dos categorías de sólidos: los cristalinos y los amorfos. Un sólido cristalino es un sólido en el cual las unidades que constituyen la sustancia están dispuestas en una estructura regular que se manifiesta en toda la masa de la sustancia. Si se conocen las posiciones relativas de un pequeño número de unidades, se puede predecir con toda exactitud el lugar en donde se encuentran localizadas las restantes. En un sólido amorfo, por el contrario, no existe el orden de largo alcance característico de los sólidos cristalinos. Muchos de los sólidos amorfos están formados por moléculas de gran tamaño que en estado líquido presentan una viscosidad elevada. Cuando la temperatura del líquido disminuye, las moléculas de tamaño grande se mueven tan despacio que no les es posible organizarse de la forma ordenada que se requiere en el estado cristalino. El vidrio y la mayor parte de los plásticos pertenecen a este tipo de sustancias. Una característica que los diferencia de forma más marcada de los sólidos cristalinos es que su transición de sólido a líquido tiene lugar de forma gradual a lo largo de un amplio intervalo de temperatura. En lo que sigue, nuestra atención se va a centrar en el estudio de los sólidos cristalinos y, para ello, podemos clasificarlos de acuerdo con la naturaleza de las fuerzas que mantienen unidas entre sí sus partículas constituyentes. Este tipo de fuerzas con frecuencia reciben el nombre de fuerzas cristalinas. SOLIDOS MOLECULARES Las partículas que forman la estructura reticular de un sólido molecular son moléculas que se mantienen unidas entre sí por uno o más de los tres tipos de fuerzas cohesivas que existen entre especies eléctricamente neutras: dispersión, dipolo - dipolo y enlace de hidrógeno. Propiedades físicas tales como los puntos de fusión y dureza de los sólidos moleculares, como H2O, CO2 y I2, varían considerablemente dependiendo de las fortalezas de las interacciones intermoleculares. Los gases nobles están incluidos dentro de este grupo aunque están constituidos por átomos y no moléculas, en virtud de que sus fuerzas cohesivas son del tipo dispersión. Debido a que las fuerzas que mantienen unidas las moléculas entre sí son relativamente débiles, los sólidos moleculares tienen puntos de fusión bajos. Puesto que las fuerzas de dispersión aumentan con el tamaño de la molécula, los puntos de fusión de sólidos moleculares de sustancias semejantes aumentan con la masa molecular. SOLIDOS DE REDES COVALENTES En ciertos sólidos, los átomos están unidos entre sí a través de una red tridimensional de enlaces covalentes que abarca a todo el sólido cristalino y se denominan sólidos de redes covalentes. En estos casos, las fuerzas intra e intermoleculares no se diferencian, ya que todo el cristal es una red única de enlaces covalentes; donde cada muestra de sustancia sólida es una molécula gigante. El diamante es un ejemplo de sólido de red covalente; en él, cada átomo de carbono está unido covalentemente a otros cuatro átomos de carbono situados en los vértices de un tetraedro [Figura 12.22(a)]. Como los átomos están unidos en las tres dimensiones mediante enlaces covalentes fuertes, los sólidos de redes covalentes normalmente tienen puntos de fusión muy elevados y son materiales muy duros y el diamante es la sustancia más dura que se conoce. Otros ejemplos de cristales covalentes están representados por minerales en los que el silicio y el oxígeno están unidos mediante enlaces covalentes. El cuarzo y muchas arenas, por ejemplo, están formados prácticamente por sílice, SiO2 , puro, en donde cada átomo de Si está unido a cuatro átomos de oxígeno situados en los vértices de un tetraedro y cada átomo de oxígeno está unido a dos átomos de silicio. Cuando la sílice se calienta alrededor de los 1600 o C, se rompen muchos de sus enlaces Si—O transformándose de sólido cristalino a un líquido viscoso. Cuando este fluido se enfría, algunos de los enlaces Si—O vuelven a formarse sin ordenamiento alguno dando lugar a un sólido amorfo no cristalino denominado vidrio de cuarzo. Mezclándole aditivos adecuados antes de que se enfríe, se pueden preparar vidrios de características muy variadas. El vidrio común de ventana se prepara adicionando CaCO3. Mediante la adición de ciertos metales de transición se pueden preparar vidrios de colores variados, y la adición de B2O3 produce un vidrio boro silicato de elevado punto de fusión que se vende bajo el nombre comercial de Pyrex. El vidrio borosilicatado es muy útil para la fabricación de utensilios de cocina y material de laboratorio por su baja expansión cuando se calienta y su elevada resistencia al shock térmico. El grafito es otra forma cristalina del carbono, pero sus fuerzas cristalinas son de tipo covalente y de van der Waals [Figura 12.22(b)]. Los átomos de carbono con hibridación sp2 forman capas de átomos unidos entre sí mediante enlaces covalentes que mantienen unido al sólido en tan sólo dos dimensiones de las capas, mientras que las fuerzas de van del Waals más débiles mantienen unidas las capas entre sí. En contraste con el diamante, el grafito es blando debido a las débiles atracciones de van der Waals que permiten a las capas bidimensionales deslizarse entre sí. El grafito es la sustancia negra y resbaladiza utilizada como «mina» de los lápices, electrodos de baterías y lubricante de cerraduras. Todas estas aplicaciones derivan de su estructura en capas. A presiones normales es un material más estable que el diamante, pero puede convertirse en éste a elevadas presiones. En la actualidad se fabrican diamantes comprimiendo grafito a 150 000 atmósferas y temperaturas elevadas. http://www.youtube.com/watch?v=SjOXiUq6TME. Para designarlas dos o más formas moleculares o cristalinas que puede presentar un elemento en el mismo estado, pero que exhiben propiedades físicas y químicas diferentes, se utiliza el término alótropo. El diamante y grafito son alótropos, aunque no los únicos; el carbono; el azufre, fósforo y cinc son otros elementos que tienen formas alotrópicas en estado sólido, y O2 y O3 son ejemplos de alótropos gaseosos. Solidos Iónicos Formado por iones de carga opuesta que se mantienen unidos entre sí como consecuencia de atracciones electrostáticas. Las atracciones electrostáticas que mantienen a los iones en un cristal de un sólido iónico son relativamente muy intensas, comparables en fortaleza a los enlaces covalentes. Una característica propia de los compuestos iónicos es su elevado punto de fusión y, además, son sustancias relativamente duras y quebradizas. En estado sólido no pueden conducir la electricidad porque los iones están “fijos”, pero, una vez fundidos, son excelentes conductores porque los iones tienen libertad para moverse. Muchos de los compuestos binarios que se forman cuando reaccionan elementos metálicos con no metálicos, como, por ejemplo, NaCl o MgO, forman sólidos iónicos. En estas estructuras no existen moléculas como unidades individuales porque las uniones entre las partículas se extienden a lo largo y ancho de todo el cristal. Todos los compuestos iónicos forman sólidos cristalinos. Solidos Metálicos Están formados por átomos metálicos. Los elementos metálicos forman sólidos cristalinos que exhiben propiedades únicas tales como elevada conductividad térmica y eléctrica, brillo metálico, maleabilidad y ductilidad (formar laminas o alambres por presión). El enlace especial capaz de justificar estas propiedades se denomina enlace metálico y de él nos hemos ocupado ya en anteriores clases (11.11). Recordemos aquí tan sólo que un cristal metálico, es un conjunto de “iones positivos” dispuestos de forma regular en un «mar de electrones» que los mantienen unidos. Los electrones que forman la nube de carga negativa no pertenecen a ningún átomo específico y se mueven fácilmente a lo largo y ancho del cristal. Los metales tienen un rango muy amplio de sus puntos de fusión. El galio, funde a 29.78 oC, por debajo de la temperatura del cuerpo humano, y el mercurio permanece en forma líquida a temperaturas en las que el agua solidifica. Sin embargo, hay muchos metales que necesitan sobrepasar los 1000 oC para que fundan, llegando a 3410 oC en el tungsteno, el metal de punto de fusión más elevado. En la siguiente Tabla se resumen las características de los distintos sólidos que hemos tratado. MODELO DEL MAR DE ELECTRONES DEL ENLACE METALICO Estructuras Cristalinas Tal como hemos visto en la sección anterior, los sólidos se pueden clasificar tomando como criterio la naturaleza de sus fuerzas cohesivas; pero también, y en este caso solamente los sólidos cristalinos, se pueden clasificar basándonos en las características geométricas de sus retículos cristalinos. Dado que un cristal está formado por un número extraordinariamente grande de partículas de tamaño atómico, es posible describir la forma en que están dispuestas conociendo el lugar en donde se encuentran localizadas unas pocas en el interior del sólido. Las partículas microscópicas de un sólido cristalino (átomos, iones o moléculas) están situadas obedeciendo una estructura geométrica regular, por lo general de naturaleza sencilla. Aunque las partículas constituyentes del cristal pueden ser de considerable tamaño e incluso poliatómicas, como en el caso de los iones NO-2, generalmente es útil considerar a un cristal como un enrejado tridimensional de puntos o puntos reticulares, y la disposición geométrica de los mismos es lo que entendemos por retículo cristalino. El retículo cristalino es una abstracción deducida del cristal real para expresar el esquema de repetición que se manifiesta en dicho cristal. La visualización de los conceptos geométricos resulta más sencilla en dos que en tres dimensiones, por lo que, a modo de introducción, podemos fijar nuestra atención en los retículos bidimensionales de la Figura 12.23. Cada retículo se puede describir considerando que está constituido por un número determinado de celdas unidad idénticas, de forma similar a como un pavimento está formado por un cierto número de baldosas. Aunque una celda unidad se puede definir de formas muy distintas (Figura 12.23), lo más útil es hacerlo como el paralelogramo más pequeño posible que tiene la misma simetría que el retículo. El tamaño y la forma de la celda unidad bidimensional están definidas por los cuatro puntos del retículo situados en los vértices de la celda. En principio se puede proponer un retículo de cualquier tamaño alineando celdas unidad contiguas, de la misma forma que se puede cubrir un suelo de cualquier tamaño colocando un número determinado de baldosas adyacentes entre sí. Una celda que posee un punto reticular en su interior se denomina centrada, mientras que las que no contienen ningún grupo interior se llaman primitivas o simples. En el espacio no es de sorprender que existan más posibilidades. Para definir una celda unidad se necesitan ocho puntos, que son los vértices de la celda, y tienen que ser elegidos de tal forma que definan una caja que tenga tres pares de caras paralelas; las figuras sólidas de este tipo se denominan paralelepípedos. Cada celda unidad del cristal está formada por los mismos puntos del mismo tipo, en idénticos lugares y las mismas posiciones relativas. El contenido de la celda unidad es el motivo repetitivo del cual está constituido el cristal. Los lados y las aristas de la celda unidad pueden atravesar los puntos y, en ese caso, solamente las porciones de átomos situados en el interior de la celda unidad se cuentan como pertenecientes a la celda en cuestión. Los átomos situados en espacios fronterizos cuentan como compartidos. Las celdas unidad y los retículos cristalinos, que son el producto de la imaginación humana, permiten visualizar la estructura de un cristal como el resultado de apilar cuidadosamente (lado con lado, frente con espalda y suelo con techo) pequeños ladrillos. Una única celda unidad contiene toda la información estructural acerca del cristal, porque el cristal en principio podría construirse haciendo un número muy grande de copias del original de la celda unidad y apilarlas convenientemente (Figura 12.24) El tamaño y la forma de una celda unidad quedan completamente descritos una vez establecidas las longitudes de sus tres aristas (a, b y c) y la magnitud de sus tres ángulos (α, β y γ), que se denomina parámetros de celda o constantes de celda. Debido a las restricciones de tipo geométrico, sólo es posible un número limitado de retículos cristalinos, los cuales se pueden agrupar en siete sistemas, definidos por las longitudes relativas de las aristas y los ángulos entre las mismas de la celda unidad. En la Figura 12.25 y en la Tabla 12.10, se muestran las celdas unidad de cada uno de los sistemas cristalinos. El número de diferentes sistemas existentes es una limitación matemática que no tiene nada que ver con las propiedades físicas o químicas de las sustancias. Existe un sinfín de posibilidades a la hora de seleccionar la celda unidad de una estructura cristalina dada, por lo que es útil tener en cuenta algunas normas. 1. Respetar la simetría de la red cristalina teniendo en cuenta las condiciones que aparecen en la Tabla 12.10. 2. Encontrar la celda más pequeña que posee la simetría del retículo cristalino; no se obtiene ventaja alguna al utilizar celdas grandes si existen otras más pequeñas que pueden representar al cristal. Una celda de tamaño mínimo es primitiva y contiene tan sólo un punto reticular y puede compartir ocho puntos reticulares, uno por vértice, pero cada punto reticular está compartido con siete celdas vecinas con las que coincide en cada vértice. En realidad, tan sólo un octavo de cada uno de los ocho puntos reticulares pertenece a la celda unidad. Puesto que 1/8 x 8 = 1, los ocho puntos reticulares compartidos contribuyen siempre con un punto reticular a la celda unidad. En la Figura se muestran otras alternativas del número de celdas que pueden compartir un átomo. A veces la celda unidad más pequeña o primitiva no tiene la simetría completa del retículo cristalino y, es necesario elegir una celda de mayor tamaño que tenga la simetría característica. Las celdas de mayor tamaño son no primitivas (centradas) y se trazan sobre un retículo dado seleccionando los vértices de la celda unidad de forma que en ella queden incluidos otros puntos reticulares bien en el centro de la celda o en el centro de todas o algunas de sus caras. Si en el interior de la celda unidad existe un punto reticular extra, la celda es centrada en el cuerpo. Si existen puntos reticulares extras en los centros de sus caras en la celda unidad (pero no en el centro), la celda es centrada en las caras. Finalmente, si los puntos reticulares extras se encuentran en los centros de un solo par de caras paralelas de la celda unidad (y en ningún otro sitio), la celda es centrada en los extremos. Este tipo de celdas no primitivas se muestran en la Figura 12.27. En 1848, el físico francés Auguste Bravais demostró que sólo existen catorce redes cristalinas asociadas a los siete sistemas, que son las que se indican en la Tabla 12.10. Independientemente de cómo se seleccione una celda unidad, ésta contiene siempre un número entero de puntos reticulares. Una celda de dos puntos reticulares automáticamente ocupa un volumen doble que una celda unidad primitiva del mismo retículo. En lo que sigue centraremos nuestra atención en las celdas unidad cúbicas por ser las más sencillas de visualizar y, también, las que con más frecuencia se presentan en la naturaleza. En este sistema cúbico las tres simetrías existentes son la simple o primitiva, cúbica centrada en el cuerpo y cúbica centrada en las caras (Figura 12.28). Una norma elemental de la naturaleza es que las cosas se hacen siempre de la forma más eficaz posible. Si observamos los distintos retículos en función de la eficacia del empaquetamiento de los átomos o iones, nos encontramos con que la red cúbica centrada en las caras utiliza el 74% del espacio disponible en el cubo, mientras que las esferas empaquetadas en un celda cúbica primitiva utiliza tan sólo el 52% del espacio disponible, evidentemente mucho menos eficiente. La razón de estos hechos se puede empezar a comprender cuando observamos las dos formas básicas de empaquetamiento en dos dimensiones que pueden presentar las esferas (átomos o iones) (Figura 12.29). Como se puede ver en la parte a), las esferas están situadas en las esquinas de un cuadrado y cada una está en contacto con otras cuatro esferas. En la alternativa b), cada una de las esferas está en contacto con otras seis y se encuentra situada en los vértices de un hexágono. En cada uno de los ordenamientos existen espacios vacíos entre los átomos, mayores en (a) que en (b). El modo en que los átomos están dispuestos en las capas y éstas se superponen una sobre otra, son los factores determinantes del tipo de estructuras cristalinas que se forman. Un espacio tridimensional se llena cuando se apilan, una sobre otra, capas de átomos o iones. Si sobre una capa de ordenamiento cuadrado [Figura 12.29(a)] se sitúa otra idéntica directamente, la estructura que se obtiene es la de múltiples celdas cúbicas primarias en todas las direcciones del espacio. Sin embargo, como ya hemos indicado, existen formas de empaquetamiento más eficaz y cualquiera de ellas pasa por la utilización de las esferas que están dispuestas en forma hexagonal [Figura 12.29(b)]. Cualquiera que sea la forma en la que se superponen sucesivas capas hexagonales, las estructuras que se obtienen son de empaquetamiento compacto. Pero el agrupamiento compacto que se logra es distinto según que las esferas de una capa, al situarse sobre las depresiones disponibles de las otras, lo hagan en una u otra orientación (Figura 12.30). Existen dos posibilidades de ordenamiento, una de empaquetamiento cúbico compacto, que corresponde al retículo cúbico centrado en las caras ya mencionado, y otra estructura hexagonal de empaquetamiento compacto. Casi todos los elementos metálicos y muchos cristales moleculares presentan estructuras de estos dos tipos mencionados y hay algunas propiedades que son comunes. En ambos casos, las esferas ocupan el 74% del espacio disponible y, en cualquiera de las dos redes, cada esfera está en contacto directo con 12 de sus vecinas más próximas, seis que se encuentran en una capa y tres en cada una de las capas superior e inferior. Se denomina número de coordinación al número de átomos, iones o moléculas vecinas con los que está en contacto una especie en el sólido cristalino, y se ha visto que su valor máximo es 12. Las estructuras cristalinas son una expresión de algunas propiedades atómicas; así, por ejemplo, los radios de los átomos metálicos se determinan generalmente a partir de sus cristales. Conociendo la estructura cristalina y las dimensiones de la celda unidad, se puede calcular la densidad de un metal. Las densidades calculadas a partir de las estructuras de los cristales difieren ligeramente de las determinadas experimentalmente por los métodos convencionales debido a las (en mayor o menor grado) inevitables impurezas de los cristales. No obstante, los valores son siempre lo suficientemente concordantes para que sean útiles para la confirmación del tipo de celda determinado. A temperatura ambiente, el hierro forma cristales cúbicos centrados en el cuerpo con una longitud de celda unidad de 286.6 pm. ¿Cuál es la densidad del hierro a temperatura ambiente? ELABORO: VLADIMIR ARIAS RAMIREZ, DOCENTE ESCUELA DE QUIMICA UNIVERSIDAD TECNOLOGICA DE PEREIRA FUENTE: QUIMICA GENERAL RAYMOND CHANG 9ª EDICION. QUIMICA LA CIENCIA CENTRAL BROWN, LE MAY Y BURSTEN 9ª EDICION. QUIMICA LA CIENCIA BASICA M. D. REBOIRAS 1ª EDICION.