Detección del VHC, Diagnóstico y Tratamiento
Anuncio
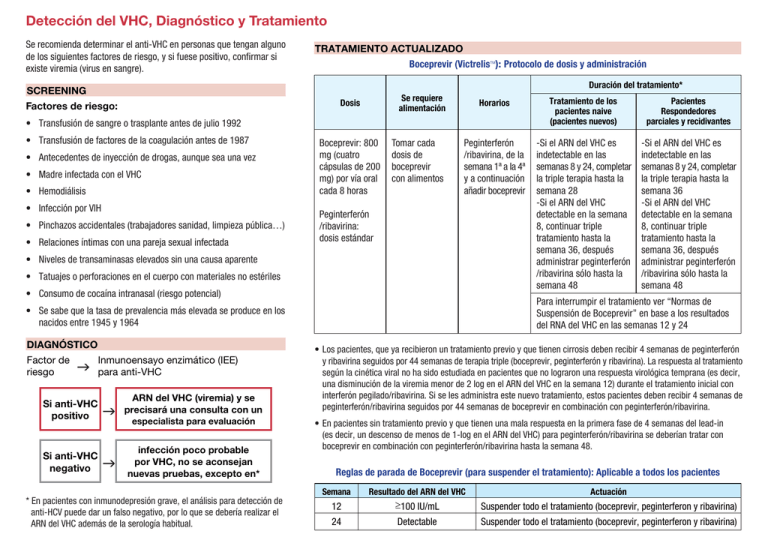
Detección del VHC, Diagnóstico y Tratamiento Se recomienda determinar el anti-VHC en personas que tengan alguno de los siguientes factores de riesgo, y si fuese positivo, confirmar si existe viremia (virus en sangre). TRATAMIENTO ACTUALIZADO Boceprevir (Victrelis ): Protocolo de dosis y administración TM Duración del tratamiento* SCREENING Se requiere alimentación Dosis Factores de riesgo: Horarios Tratamiento de los pacientes naive (pacientes nuevos) Pacientes Respondedores parciales y recidivantes Peginterferón /ribavirina, de la semana 1ª a la 4ª y a continuación añadir boceprevir -Si el ARN del VHC es indetectable en las semanas 8 y 24, completar la triple terapia hasta la semana 28 -Si el ARN del VHC detectable en la semana 8, continuar triple tratamiento hasta la semana 36, después administrar peginterferón /ribavirina sólo hasta la semana 48 -Si el ARN del VHC es indetectable en las semanas 8 y 24, completar la triple terapia hasta la semana 36 -Si el ARN del VHC detectable en la semana 8, continuar triple tratamiento hasta la semana 36, después administrar peginterferón /ribavirina sólo hasta la semana 48 • Transfusión de sangre o trasplante antes de julio 1992 • Transfusión de factores de la coagulación antes de 1987 • Antecedentes de inyección de drogas, aunque sea una vez • Madre infectada con el VHC • Hemodiálisis • Infección por VIH • Pinchazos accidentales (trabajadores sanidad, limpieza pública…) • Relaciones íntimas con una pareja sexual infectada Boceprevir: 800 mg (cuatro cápsulas de 200 mg) por vía oral cada 8 horas Tomar cada dosis de boceprevir con alimentos Peginterferón /ribavirina: dosis estándar • Niveles de transaminasas elevados sin una causa aparente • Tatuajes o perforaciones en el cuerpo con materiales no estériles • Consumo de cocaína intranasal (riesgo potencial) Para interrumpir el tratamiento ver “Normas de Suspensión de Boceprevir” en base a los resultados del RNA del VHC en las semanas 12 y 24 • Se sabe que la tasa de prevalencia más elevada se produce en los nacidos entre 1945 y 1964 DIAGNÓSTICO Factor de riesgo g Inmunoensayo enzimático (IEE) para anti-VHC Si anti-VHC positivo Si anti-VHC negativo g ARN del VHC (viremia) y se precisará una consulta con un especialista para evaluación g infección poco probable por VHC, no se aconsejan nuevas pruebas, excepto en* * En pacientes con inmunodepresión grave, el análisis para detección de anti-HCV puede dar un falso negativo, por lo que se debería realizar el ARN del VHC además de la serología habitual. • Los pacientes, que ya recibieron un tratamiento previo y que tienen cirrosis deben recibir 4 semanas de peginterferón y ribavirina seguidos por 44 semanas de terapia triple (boceprevir, peginterferón y ribavirina). La respuesta al tratamiento según la cinética viral no ha sido estudiada en pacientes que no lograron una respuesta virológica temprana (es decir, una disminución de la viremia menor de 2 log en el ARN del VHC en la semana 12) durante el tratamiento inicial con interferón pegilado/ribavirina. Si se les administra este nuevo tratamiento, estos pacientes deben recibir 4 semanas de peginterferón/ribavirina seguidos por 44 semanas de boceprevir en combinación con peginterferón/ribavirina. • En pacientes sin tratamiento previo y que tienen una mala respuesta en la primera fase de 4 semanas del lead-in (es decir, un descenso de menos de 1-log en el ARN del VHC) para peginterferón/ribavirina se deberían tratar con boceprevir en combinación con peginterferón/ribavirina hasta la semana 48. Reglas de parada de Boceprevir (para suspender el tratamiento): Aplicable a todos los pacientes Semana Resultado del ARN del VHC Actuación 12 ≥100 IU/mL Suspender todo el tratamiento (boceprevir, peginterferon y ribavirina) 24 Detectable Suspender todo el tratamiento (boceprevir, peginterferon y ribavirina) PUNTOS IMPORTANTES TRATAMIENTO Telaprevir (Incivek ): Protocolo de dosis y administración TM Duración del tratamiento Dosis Peginterferón/ ribavirina: dosis estándar con Telaprevir: 750 mg (dos tabletas de 375) cada 8 horas (se acepta tres tabletas cada 12 horas) Se requiere alimentación Horario de partida Tratamiento de los pacientes naive y recidivantes Pacientes respondedores parciales y respondedores nulos Tomar cada dosis de telaprevir con alimentos Telaprevir, peginterferón y ribavirina desde el primer día Si el ARN del VHC es indetectable en las semanas 4 y 12, continuar la terapia triple hasta la semana 12, luego administrar peginterferón /ribavirina sólo hasta la semana 24 * Continuar la terapia triple hasta la semana 12, después administrar peginterferón/ribavirina sólo hasta la semana 48 • El test del ARN del VHC debe hacerse para el boceprevir, al inicio del estudio y a las 4 y 8 semanas después de iniciar el tratamiento; para telaprevir debe hacerse el previo y a las 4 y 12 semanas; y para ambos, a las semanas 24 y 48, y después del tratamiento a las 24 semanas. Medida a tomar >1000 IU/mL Detener el tratamiento (telaprevir, peginterferón y ribavirina) 12 >1000 IU/mL Detener el tratamiento (telaprevir, peginterferón y ribavirina) 24 Detectable Detener el tratamiento (peginterferón y ribavirina) ® • Tanto boceprevir como telaprevir se asocian con interacciones entre fármacos que pueden ser graves o muy graves. Por este motivo los pacientes deben ser aconsejados en relación con estos riesgos, y las medicaciones o tratamientos concomitantes se deben suspender o ajustar las dosis, así como debe evitarse la automedicación. Ver “Normas de Suspensión de Telaprevir” para interrumpir el tratamiento en base a los resultados del RNA del VHC en las semanas 4, 12 y 24 4 Traducido y adaptado de: • Las modificaciones de dosis e interrupciones no están permitidas ni para boceprevir ni para telaprevir. Si se detiene el tratamiento, ya no se puede reiniciar. • La ribavirina es un teratógeno conocido. Tanto las pacientes como los pacientes varones con parejas femeninas, deben ser informados para evitar el embarazo durante todo el tratamiento antiviral y durante 6 meses después de la última dosis de la ribavirina. El paciente debe comprometerse a utilizar dos formas de métodos efectivos anticonceptivos no hormonales (por ejemplo, los métodos de barrera, dispositivos intrauterinos) durante el tratamiento y durante al menos 6 meses después de la última dosis de ribavirina. Reglas de parada de Telaprevir (para suspender el tratamiento): Aplicable a todos los pacientes Resultado del ARN del VHC • Boceprevir se inicia después de una fase de inducción (lead-in) de 4 semanas con peginterferón y ribavirina; telaprevir se inicia con peginterferón más ribavirina desde el primer día. Si el ARN del VHC detectable en las semanas 4, y / o 12, continuar la terapia triple hasta la semana 12, después administrar peginterferón/ribavirina sólo hasta la semana 48 * Pacientes con cirrosis y sin tratamiento previo y con ARN del VHC indetectable en las semanas 4 y 12 pueden beneficiarse de la continuación de peginterferón y ribavirina hasta la semana 48. Semana • Tanto boceprevir como telaprevir deben utilizarse en combinación con peginterferón y ribavirina. Nunca deben ser utilizados solos o únicamente en combinación con peginterferón. www.projectsinknowledge.com/VHC-CareandGuidance • Para controlar los posibles efectos adversos, se han de realizar análisis de sangre completos, hemograma y bioquímica en el momento basal y a las semanas 2, 4, 8 y 12 de tratamiento, y posteriormente de forma periódica, normalmente cada 4 semanas, o con más frecuencia, según criterio clínico. • Para mayor información sobre la prescripción de boceprevir y telaprevir se puede consultar la ficha técnica.











