HOJA DE PROBLEMAS 4 SOLUCIONES LA CONFORMACIÓN DE
Anuncio

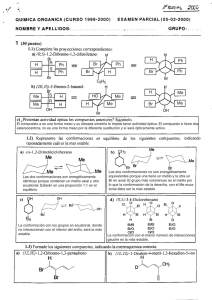
HOJA DE PROBLEMAS 4 SOLUCIONES LA CONFORMACIÓN DE LAS MOLÉCULAS. ESTUDIO PREVIO AL DE SU INFLUENCIA EN LA REACTIVIDAD 1. Al tratar la 2-terc-butil-6-etil-N-metil-anilina con cloruro de propionilo se obtienen dos isómeros que pueden separarse. ¿Puedes indicar de qué tipo de isómeros se trata?. La reacción que tiene lugar es la siguiente: CH3 t-Bu N H CH3 Et ClCOCH2CH3 N COCH2CH3 t-Bu Et base La amida formada tiene ciertas particularidades, debido a la presencia de los grupos sobre las posiciones 2 y 6 del anillo. En ausencia de esos sustituyentes voluminosos, el nitrógeno de la amida estaría conjugado con el anillo y tendría una disposición coplanar con él. En este caso esto no es posible y se produce el fenómeno denominado “inhibición estérica de la resonancia” o de la conjugación. Por tanto, se podrán tener dos disposiciones alrededor del enlace C(benc)-N: Ambas disposiciones resultan imágenes especulares y, por tanto, no separables en condiciones normales. Por tanto éste no puede ser el origen de la isomería observada. El enlace N-C(O) tiene cierto carácter doble porque se produce conjugación entre el par de electrones no compartido del nitrógeno (que reside en un orbital p) y el enlace π C=O. Su rotación está restringida. Pero en este caso la existencia de los sustituyentes en las posiciones 2 y 6 del anillo aun restrigen más este giro por impedimento estérico. Las siguientes figuras 1-3 ilustran este hecho. La diferencia de energía entre la configuración menos estable (1 según calcula el programa Hyperchem) y el hipotético estado de transición debe ser igual o superior a unas 20 kcal/mol para que los isómeros configuracionales puedan separarse por técnicas normales (cromatografía, cristalización, etc.). La interacción estérica del grupo metileno contiguo al carbonilo con el etilo de la posición 6 (átomos marcados en verde), al producirse el giro necesario para pasar del isómero Z al E, eleva la energía del estado de transición y dificulta la interconversión de los isómeros a temperatura ambiente. 2 1 3 Configuración Z El carbonilo está hacia dentro del anillo 1 Posible estado de transición en el giro del enlace N-C(O) 2 Configuración E El carbonilo está hacia fuera del anillo 3 2. Siguiendo principios de análisis conformacional, racionaliza las siguientes afirmaciones: a. Sólo el más estable de los dos isómeros del 1,2-dimetilciclohexano es capaz de mostrar actividad óptica. Isómero trans Isómero cis Este es el isómero más estable. De las dos conformaciones, una de ellas no tiene interacciones de grupos en posición axial. Ninguna de las dos conformaciones tiene simetría. Existen dos estereocentros y, por tanto, la molécula puede tener actividad óptica En este isómero las dos conformaciones son isoenergéticas y, por tanto, estarán en el equilibrio en igual proporción. Se da la paradoja de que una conformación es imagen especular de la otra. Por ello, el equilibrio conformacional produce inevitablemente la racemización del isómero cis y éste no puede tener nunca actividad óptica. b. Sólo el menos estable de los dos isómeros del 1,3-dimetilciclohexano es capaz de mostrar actividad óptica. Isómero cis Isómero trans Este es el isómero más estable. De las dos conformaciones, una de ellas no tiene interacciones de grupos en posición axial. Pero las dos conformaciones tienen un plano de simetría que las divide en dos En este isómero las dos conformaciones son isoenergéticas y, por partes, al modo como ocurre en una tanto, estarán en el equilibrio en igual proporción. En este caso forma meso. La molécula no puede tener los dos confórmeros son superponibles y por tanto no existe actividad óptica racemización provocada por el equilibrio conformacional. Podemos escribir equilibrios conformacionales independientes para cada enantiómero. Los enantiómeros podrían ser separables y, como no se equilibran entre sí, mostrarán actividad óptica c. El trans-cicloocteno puede presentar actividad óptica mientras que el trans-ciclodeceno no. Para interconvertir objeto e imagen en el trans-cicloocteno deberíamos retorcer los cuatro átomos de carbono consecutivos que contienen el doble enlace en el centro y eso haría que uno de los hidrógenos del doble enlace pasase por dentro del anillo, creando una enorme tensión. En un anillo de ocho átomos de carbono, la barrera de torsión es demasiado alta para poder sobrepasarse a temperatura ambiente, objeto e imagen no son interconvertibles, podrían separarse y una vez separados, mostrarían actividad óptica. Los valores indicados han sido calculados mediante mecánica molecular MM+, imponiendo las necesarias restricciones para simular el posible ET, en el que el plano del doble enlace es casi paralelo al plano medio del anillo. Para interconvertir objeto e imagen en el trans-ciclodeceno deberíamos retorcer los cuatro átomos de carbono consecutivos que contienen el doble enlace en el centro y eso haría que uno de los hidrógenos del doble enlace pasase por dentro del anillo, creando una relativa tensión. En un anillo de diez átomos de carbono, la barrera de torsión no es demasiado alta y se puede sobrepasar a temperatura ambiente. Por tanto, objeto e imagen son interconvertibles, no podrían separarse nunca y el trans-ciclodeceno no mostraría actividad óptica. Los valores indicados han sido calculados mediante mecánica molecular MM+, imponiendo las necesarias restricciones para simular el posible ET, en el que el plano del doble enlace es casi paralelo al plano medio del anillo. 3. Sugiere explicaciones para las observaciones siguientes, que se refieren a la preferencia ecuatorial de los sustituyentes en el ciclohexano: a. Los valores A de los grupos OH y NH2 son mayores en disolventes próticos. El valor A de un sustituyente se define como A = -RTlnK donde K = [axial]/[ecuatorial]. El valor A es positivo cuando predomina la conformación ecuatorial. Por tanto, valores A más grandes en disolventes próticos indican una mayor preferencia del ciclohexanol y la ciclohexilamina por la conformación ecuatorial en disolventes próticos. Desde un punto de vista estérico esto quiere decir que los grupos OH y NH2 son más “grandes” en disolventes próticos porque muestran más dificultad para estar en una disposición axial. Un disolvente prótico es aquél que es dador de hidrógeno en la formación de enlaces de hidrógeno. Los grupos OH y NH2 son buenos aceptores de enlace de hidrógeno. Al formar enlaces de hidrógeno con el disolvente prótico el tamaño de estos grupos aumenta y así lo hace la preferencia por la conformación ecuatorial, aumentando su valor A. b. El valor A del grupo carboxilato es mayor que el del grupo carboxilo. Es probable que la medida del valor A del grupo carboxilato de la base conjugada del ácido ciclohexanocarboxílico, haya que hacerla en un disolvente muy polar para promover su solubilidad. Esto quiere decir que el grupo carboxilato se tendrá que solvatar, formando probablemente enlaces de hidrógeno muy fuertes con el disolvente. La carga negativa formal del grupo carboxilato fomentará este hecho. De esta forma el grupo carboxilato solvatado tendrá un tamaño efectivo mayor que el grupo carboxilo, lo que nos permite explicar que tenga un valor A mayor. c. Los valores A de los halógenos son 0.15, 0.30, 0.38 y 0.43 para F, Cl, Br y I, respectivamente. Los radios covalentes de los halógenos aumentan de forma importante al descender en el sistema periódico. Sin embargo el aumento de tamaño no se refleja en un incremento importante de los valores A de los halógenos. Hay que tener en cuenta que el valor A está basado en el desplazamiento del equilibrio de los diferentes halociclohexanos y que estos equilibrios están condicionados por la interacción del sustituyente con los hidrógenos en disposición 1,3-sindiaxial. Un mayor radio covalente está acompañado por una mayor distancia de enlace C-X y una mayor distancia C-X alivia la interacción aludida. Por ello, a pesar de que los halógenos son cada vez más grandes, sus distancias al anillo son también cada vez mayores y los dos efectos se compensan, conduciendo a incrementos muy moderados de los valores A, a medida que descendemos en el sistema periódico. 4. Predice cuáles deben ser las conformaciones más pobladas, en disolventes no polares, de los siguientes compuestos: 2-bromociclohexanona, trans-1,2-dibromociclohexano, cis-1,3-dihidroxiciclohexano, y trans-1,3-di-t-butilciclohexano. ¿Como afectaría el tipo de disolvente a cada uno de los equilibrios conformacionales? 2-bromociclohexanona trans-1,2-dibromociclohexano O Br Br O Br Br Br Preferida en disolvente apolar Br El valor A de un Br es de 0.38 kcal/mol. Por tanto, no “cuesta” mucho tener un Br en posición axial en un ciclohexano. Si el Br está al lado de un grupo carbonilo, la conformación ecuatorial tendrá un momento dipolar muy grande, lo que inestabiliza a la molécula en un disolvente apolar. Por ello, puede ser posible que en un disolvente apolar, el Br prefiera la posición axial en la 2-bromociclohexanona. Valores de energía (kcal/mol) relativos calculados con el programa Hyperchem: Mecánica molecular: axial = 0; ecuatorial = +1.1 Semiempírico AM1: axial = 0; ecuatorial = +2.2 El programa predice que, en el estado gaseoso (“una única molécula”), la conformación predominante será la axial. Al cambiar a un disolvente polar la población de la conformación ecuatorial, más polar, aumentará. cis-1,3-dihidroxiciclohexano O H O La conformación daxial “cuesta” 2 x 0.38 = 0.76 kcal/mol, lo que no es una energía muy elevada. La conformación ecuatorial “cuesta” una interacción Br/Br gauche y una polaridad alta. En un disolvente apolar quizá la constante de equilibrio sea próxima a 1, es decir, ambas conformaciones tendrán una energía parecida. Valores de energía (kcal/mol) relativos calculados con el programa Hyperchem: Mecánica molecular: axial = 0; ecuatorial = +0.9 Semiempírico AM1: axial = 0; ecuatorial = -1.2 Según cual sea el método de cálculo empleado la conformación preferida difiere, señal de que ambas conformaciones deben estar próximas en energía, como habíamos predicho. Al cambiar a un disolvente polar la población de la conformación ecuatorial, más polar, aumentará. trans-1,3-di-t-butilciclohexano t-Bu H t-Bu OH HO La conformación biaxial “cuesta” 2 x 0.7 = 1.4 kcal/mol (los dos grupos OH en axial), una polaridad alta pero a cambio la estabilización por enlace de hidrógeno intramolecular. La conformación ecuatorial tiene mucha menos energía, baja polaridad t-Bu t-Bu El equilibrio conformacional es degenerado. Las dos conformaciones tienen idéntica energía y polaridad. La constante de equilibrio será 1 y no cambiará al variar la polaridad del disolvente. La única particularidad es que un grupo t-Bu en axial y, si la concentración es suficientemente alta, la deforma la silla del ciclohexano de forma muy posibilidad de tener enlaces de hidrógeno considerable: intermoleculares. Por ello es previsible que la conformación ecuatorial sea la preferida. Valores de energía (kcal/mol) relativos calculados con el programa Hyperchem: Mecánica molecular: axial = 0; ecuatorial = -1.2 Semiempírico AM1: axial = 0; ecuatorial = +1.1 Según cual sea el método de cálculo empleado la conformación preferida difiere, señal de que ambas conformaciones deben estar próximas en energía. Un disolvente polar hará que el tamaño aparente de los grupos OH aumente y por tanto la proporción de conformación ecuatorial aumentará. 5. Predice cuál de los isómeros cis o trans de la decalina es más estable. ¿Puedes estimar cuál es la diferencia de energía entre ellos? trans decalina cis decalina Un anillo parte del otro en disposición ecuatorial. No existen interacciones. Tomemos la trans decalina como referencia. La fusión de los anillos se produce de modo que uno de los metilenos está en axial respecto del otro anillo. Esto es análogo a la situación del metilciclohexano y, por tanto, la diferencia de energía entre trans y cis decalina debería ser similar al doble (hay dos anillos) de la que existe entre los confómeros axial y ecuatorial del metilciclohexano: 2 x 1.7 kcal/mol 6. Dibuja una estructura tridimensional de los perhidrofenantrenos que se indican. Utilizando principios de análisis conformacional predice cuál será más estable y haz una estimación semicuantitativa de la diferencia de energía entre ellos. Utilizando un programa de mecánica molecular, dibuja las estructuras apropiadas, minimiza sus geometrías y compara sus energías. trans-anti-trans trans-sin-trans E = 25.1 kcal/mol (Se señalan en verde los átomos en disposición sin) E = 17.7 kcal/mol Dibujar estas moléculas no es fácil. Pero enseguida se da uno cuenta de que el isómero trans-sin-trans debe adoptar una conformación en su anillo central que se aleja mucho de una silla. Las formas flexibles y bote del ciclohexano tienen una diferencia de energía con la forma silla de entre 5 a 10 kcal/mol. Por tanto, deberíamos esperar una diferencia de estabilidad entre los dos isómeros en ese intervalo. Las energías absolutas calculadas por el Hyperchem (o por cualquier otro programa de simulación molecular) no tienen significado en sí mismas. Pero la diferencia entre ellas sí, ya que estamos comparando dos moléculas isómeras, con exactamente el mismo número de átomos. Esta diferencia (7.4 kcal/mol) corresponde a la deformación del anillo central del isómero trans-sin-trans, que debe adoptar una conformación análoga a una forma flexible del ciclohexano para acomodar la disposición de los enlaces. El valor calculado por el Hyperchem se encuentra dentro de nuestras previsiones semicuantitativas. 7. Plantea el equilibrio conformacional del isómero cis del 3-hidroxitiano S-óxido y la ecuación correspondiente de ΔGº de equilibrio. La Figura muestra la variación experimental observada del valor de ΔGº en función de la concentración del compuesto en CD2Cl2. ¿Cuáles son las poblaciones de las dos conformaciones en equilibrio en los extremos del rango de concentraciones medidas ? ¿Puedes dar una explicación a la enorme variación observada? O H O S S O H O A altas concentraciones (aprox. 5M) en un disolvente relativamente apolar y aprótico, se observa un valor de ΔGº = -1.0, lo que indica que el equilibrio está muy desplazado hacia una de las dos conformaciones. A alta concentración, las moléculas tenderán a agregarse, interaccionando intermolecularmente por enlace de hidrógeno. Esto sucederá más fácilmente en la conformación ecuatorial. A muy baja concentración (aprox. 10-2.5) se observa un valor de ΔGº = 1.4, lo que indica que el equilibrio se ha desplazado casi totalmente hacia el lado contrario. Si nuestra hipótesis anterior es correcta, ahora la conformación preferida es la biaxial. Esto es razonable porque puede estabilizarse mediante enlace de hidrógeno intramolecular. 8. Predice la estereoquímica que debe obtenerse en el(los) producto(s) de las reacciones siguientes en función del estudio conformacional de los productos de partida. Me O OAc Me2CuLi (exceso) H O O Et2AlCl N O + Bn Me O Existen más hidrógenos sindiaxiales en la aproximación por la cara posterior que la impiden El grupo CH unido al grupo alcoxi de la lactona impide el ataque por la cara de abajo. H La cara posterior del alqueno está impedida por el grupo acetoxilo En este caso cabe preguntarse si el ataque a los dos dobles enlaces será simultáneo o no. Las implicaciones estereoquímicas pueden ser diferentes. endo-meta La aproximación para dar el producto “meta” está menos favorecida desde el punto de vista orbitálico pero la interacción estérica del caso anterior no existe. La aproximación endo es más favorable que la exo. Aproximación más probable El catalizador quiral se une momentáneamente a los dos carbonilos por el átomo de cobre, fijando su conformación y haciendo que el dienófilo sea más deficiente en electrones y más reactivo. Por tanto, las moléculas de tiazolidinona unidas al cobre serán las que reaccionen mucho más rápidamente porque el dienófilo está más activado. El cobre (en naranja en el modelo) tiene una disposición tetraédrica lo que hace que los planos medios de la tiazolidinona y del catalizador quiral sean perpendiculares. El catalizador tiene un eje de simetría C2 pero es quiral y ópticamente puro (si los dos grupos terc-butilo estuvieran hacia el mismo lado tendríamos una forma “meso” y no sería quiral). En principio, la tiazolidinona tendría dos posibles orientaciones respecto del catalizador: con la olefina hacia delante (modelo de la izquierda) y con ella hacia detrás (modelo de la derecha). Puede verse que si los “colgamos” de la parte superior y los giramos 180º (eje C2) son idénticos. Por tanto el ciclopentadieno sólo tiene una manera de aproximación en la que no interacciona con los grupos terc-butilo, dando lugar a una única estereoquímica del producto final. La reacción es completamente estereoselectiva, obteniéndose el enantiómero que se indica.