18 REACCIÓN DE GRIGNARD PREPARACIÓN DE TRIFENIL
Anuncio
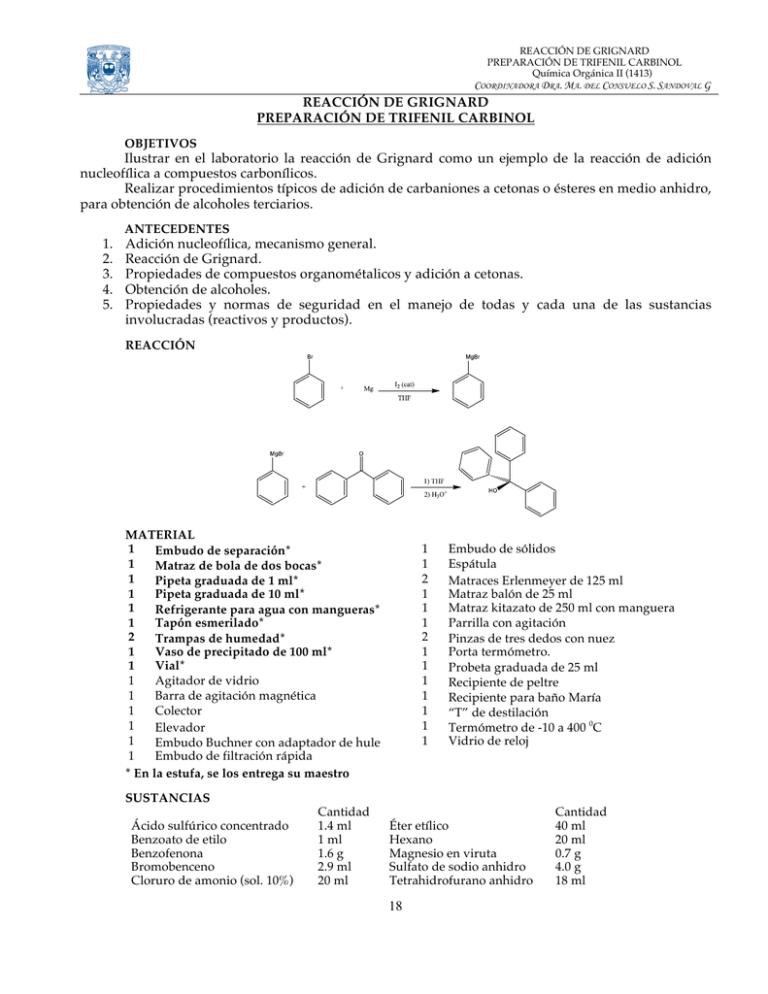
REACCIÓN DE GRIGNARD PREPARACIÓN DE TRIFENIL CARBINOL Química Orgánica II (1413) COORDINADORA DRA. MA. DEL CONSUELO S. SANDOVAL G REACCIÓN DE GRIGNARD PREPARACIÓN DE TRIFENIL CARBINOL OBJETIVOS Ilustrar en el laboratorio la reacción de Grignard como un ejemplo de la reacción de adición nucleofílica a compuestos carbonílicos. Realizar procedimientos típicos de adición de carbaniones a cetonas o ésteres en medio anhidro, para obtención de alcoholes terciarios. ANTECEDENTES 1. 2. 3. 4. 5. Adición nucleofílica, mecanismo general. Reacción de Grignard. Propiedades de compuestos organométalicos y adición a cetonas. Obtención de alcoholes. Propiedades y normas de seguridad en el manejo de todas y cada una de las sustancias involucradas (reactivos y productos). REACCIÓN MATERIAL 1 Embudo de separación* 1 Matraz de bola de dos bocas* 1 Pipeta graduada de 1 ml* 1 Pipeta graduada de 10 ml* 1 Refrigerante para agua con mangueras* 1 Tapón esmerilado* 2 Trampas de humedad* 1 Vaso de precipitado de 100 ml* 1 Vial* 1 Agitador de vidrio 1 Barra de agitación magnética 1 Colector 1 Elevador 1 Embudo Buchner con adaptador de hule 1 Embudo de filtración rápida * En la estufa, se los entrega su maestro SUSTANCIAS Ácido sulfúrico concentrado Benzoato de etilo Benzofenona Bromobenceno Cloruro de amonio (sol. 10%) Cantidad 1.4 ml 1 ml 1.6 g 2.9 ml 20 ml 1 1 2 1 1 1 2 1 1 1 1 1 1 1 Embudo de sólidos Espátula Matraces Erlenmeyer de 125 ml Matraz balón de 25 ml Matraz kitazato de 250 ml con manguera Parrilla con agitación Pinzas de tres dedos con nuez Porta termómetro. Probeta graduada de 25 ml Recipiente de peltre Recipiente para baño María “T” de destilación Termómetro de -10 a 400 0C Vidrio de reloj Éter etílico Hexano Magnesio en viruta Sulfato de sodio anhidro Tetrahidrofurano anhidro 18 Cantidad 40 ml 20 ml 0.7 g 4.0 g 18 ml REACCIÓN DE GRIGNARD PREPARACIÓN DE TRIFENIL CARBINOL Química Orgánica II (1413) Coordinadora Dra. Ma. del Consuelo S. Sandoval G Cloruro de calcio anhidro Cloruro de sodio 30 g 15 g Yodo 0.1 g PROCEDIMIENTO 1era Parte Secar el material perfectamente y preparar dos trampas de humedad con cloruro de calcio anhidro. I. Bromuro de fenil magnesio. En el matraz pera Quickfit de dos bocas colocar 0.3 g (0.0125 at. g.) de viruta de magnesio y un cristal de yodo, agregar 1 ml de Tetrahidrofurano (1) y adaptar el embudo de separación con la llave cerrada en la boca inclinada; en la otra boca del matraz colocar un refrigerante de agua en posición de reflujo y en la parte superior de éste un tubo con cloruro de calcio. En el embudo de separación colocar 1.3 ml (1.9 g, 0.0121 moles) de bromobenceno (de preferencia recién destilado) y tapar el embudo con el otro tubo de calcio y dejar gotear el matraz alrededor de 0.2 ml de bromobenceno, sin agitar, para tener una concentración local alta (2) una vez que la reacción se inicia, agregar 7 ml de THF seco en el embudo de adición (para diluir el bromobenceno restante), agitando continuamente, agregar el resto de esta solución gota a gota de tal forma de tener una ebullición suave y continua (2). Si la reacción no se inicia puede inducirse mediante: 1. Adición de otro cristal de yodo. 2. Calentamiento suave agitando continuamente, con un baño de agua a 50 oC. Si el color del yodo desaparece y la ebullición continúa una vez retirado el baño, la reacción se ha iniciado. 3. Adición de otro cristal de yodo y frotándolo sobre el magnesio contra la pared del matraz agitando con movimiento circular (sin romper el matraz) con una varilla seca. 4. Adición de unas gotas de reacción ya iniciada. 5. Adición de gotas de dibromoetano. No permitir que ésta se suspenda. Si la ebullición disminuye sensiblemente, calentar la mezcla de reacción suavemente con el baño de agua a 50 oC. La reacción termina cuando todo el magnesio se ha desintegrado y la solución adquiere turbidez de color café. Si es necesario, calentar a reflujo durante 10 minutos. II. a Adición de benzofenona (3). En el embudo separación colocar 1.2 g (0.007 moles) de benzofenona y disolver en 6 ml de THF seco, adicionar lentamente esta solución al reactivo de Grignard, agitando y enfriando solamente lo necesario para mantener una ebullición suave. Terminada la adición calentar a reflujo durante 20 minutos. Verter la mezcla de reacción en un vaso de precipitados de 150 ml con 10 g de hielo. Lavar el matraz de pera con 5 ml de éter común, y verterlo en el vaso. II. b Adición de benzoato de etilo (3). En el embudo de separación colocar 0.6 ml (0.62g, 0.004 moles) de benzoato de etilo y 5 ml de THF, adicionar lentamente y con agitación esta solución al reactivo de Grignard. Terminada la adición calentar a reflujo durante 20 minutos. Continuar con el procedimiento descrito en la alternativa II a. 19 REACCIÓN DE GRIGNARD PREPARACIÓN DE TRIFENIL CARBINOL Química Orgánica II (1413) COORDINADORA DRA. MA. DEL CONSUELO S. SANDOVAL G NOTAS: (1) El éter y el THF son muy inflamables debiendo evitarse la presencia de chispas, flamas de cigarrillos encendidos, sobrecalentamientos, etcétera. En su manejo se debe extremar las precauciones de seguridad y en esta práctica específicamente, mantener condiciones anhidras. (2) La reacción es difícil de iniciar en presencia de agua, oxígeno o alcohol y el rendimiento disminuye notablemente. (3) En la alternativa II a se utilizó una relación molecular de benzofenona a reactivo de Grignard 1:2. En la alternativa II b se utilizó una relación molecular de benzoato de etilo a reactivo de Grignard de 1:3. (4) El THF es soluble en agua acidulada. 2da Parte Para lograr la hidrólisis completa se agrega una solución de ácido sulfúrico al 5%, hasta disolver el sólido (4). La mezcla se transfiere a un embudo de separación, separando la fase orgánica (THF, éter y producto). La fase acuosa se somete a una extracción múltiple con éter etílico (2 x 7 ml). Se reúnen los extractos orgánicos, en el embudo de separación, y enseguida se lavan con 20 ml de una solución de cloruro de amonio al 10 % y después con una solución saturada de cloruro de sodio. Secar la fase orgánica con sulfato de sodio anhidro, filtrar y destilar el éter-THF casi a sequedad. El residuo se cristaliza vertiéndolo en 15 ml de hexano. El sólido formado se filtra y se determina su punto de fusión y rendimiento. CUESTIONARIO 1. Describa un método para eliminar el agua del éter etílico y tetrahidrofurano. 2. ¿Cuál es la evidencia que muestra que la reacción de Grignard ha terminado? 3. ¿Qué productos se formarán, si la benzofenona o el benzoato de etilo son adicionados al reactivo de Grignard con trazas de agua? 4. ¿Cómo se detienen la reacción? 5. ¿Por qué es necesario acidular? BIBLIOGRAFÍA Brewster, R. Q. y Vander, Werf C. A., Curso práctico de química orgánica, 2ª. Edición, Alambra, España, 1970. Morrison, R. T. y Boyd, R. N., Química Orgánica, Fondo Educativo Interamericano, México, 1976. Cremlyn, R. J. W. y Still, R. H., Named and Miscellaneus Reactions in Practical Organic Chemistry. Heineman Educational Books Ltd., London 1967, pag. 66 20 REACCIÓN DE GRIGNARD PREPARACIÓN DE TRIFENIL CARBINOL Química Orgánica II (1413) Coordinadora Dra. Ma. del Consuelo S. Sandoval G 21 REACCIÓN DE GRIGNARD PREPARACIÓN DE TRIFENIL CARBINOL Química Orgánica II (1413) COORDINADORA DRA. MA. DEL CONSUELO S. SANDOVAL G 22 OBTENCIÓN DE BUTIRALDEHIDO POR OXIDACIÓN DE n-BUTANOL Química Orgánica II (1413) Coordinadora Dra. Ma. del Consuelo S. Sandoval G OXIDACIÓN DE ALCOHOLES PRIMARIOS OBTENCIÓN DE BUTIRALDEHÍDO POR OXIDACIÓN DE n-BUTANOL. OBJETIVOS 1. Ejemplificar el método para obtener aldehídos alifáticos mediante la oxidación de 2. alcoholes. Formar un derivado sencillo del aldehído obtenido para caracterizarlo. ANTECEDENTES 1. Métodos de obtención de aldehídos y cetonas. 2. ¿Cómo se obtiene el butiraldehído industrialmente; para qué se usa; que importancias 3. 4. 5. económica tiene este aldehído? Diferentes oxidantes, ventajas y desventajas de cada uno de ellos. ¿Qué tipo de aldehídos se pueden obtener por el método de oxidación directa? Reacciones de identificación de aldehídos. REACCIÓN MATERIAL 1 Anillo metálico 1 Buchner con alargadera 1 Colector 1 Columna Vigreaux 1 Embudo de separación con tapón 1 Embudo de vidrio 1 Espátula 1 Kitasato de 250 ml con manguera 1 Matraz Erlenmeyer de 125 ml 1 Matraz Erlenmeyer de 50 ml 1 Matraz pera de dos bocas 1 Mechero con manguera 2 1 1 1 1 1 1 1 2 1 1 1 SUSTANCIAS Cantidad 3.8 g Dicromato de potasio 4.0 ml H2SO4 concentrado 3.2 ml n-Butanol 0.5 ml Reactivo de 2,4- Dinitrofenilhidrazina INFORMACIÓN 23 Pinzas de tres dedos con nuez Porta termómetro Probeta graduada de 25 ml Recipiente para baño María Refrigerante para agua con mangueras T de destilación Tela de alambre con asbesto Termómetro -10 a 400 oC Tubos de ensayo Vaso de precipitados de 150 ml Vaso de precipitados de 400 ml Vidrio de reloj OBTENCIÓN DE BUTIRALDEHIDO POR OXIDACIÓN DE n-BUTANOL Química Orgánica II (1413) Coordinadora Dra. Ma. del Consuelo S. Sandoval G Un método para obtener aldehídos es por oxidación de alcoholes. Los aldehídos se oxidan fácilmente. Los aldehídos son compuestos con punto de ebullición menor que el de los alcoholes y de los ácidos carboxílicos con peso molecular semejante. 4. Los aldehídos forman compuestos sólidos con la 2,4- dinitrofenilhidrazina que se les conoce como 2,4- dinitrofenilhidrazonas y cuyos puntos de fusión permiten caracterizar a los aldehídos. 1. 2. 3. PROCEDIMIENTO A un matraz de 2 bocas se le adapta, por una de ellas, un embudo de adición con la llave cerrada y por la otra un sistema de destilación fraccionada. Colocando una columna Vigreaux en posición vertical. En un vaso de precipitados de 125 ml disolver 3.8 g de dicromato de potasio dihidratado en 12.5 ml de agua, añadir cuidadosamente y con agitación 2.5 ml de ácido sulfúrico concentrado (1). En el matraz de destilación colocar 3.2 ml de n-butanol y unas piedras de ebullición. En el embudo de separación colocar la solución de dicromato de potasio-ácido sulfúrico. Calentar el n-butanol a ebullición con flama suave de tal forma que los vapores del alcohol lleguen a la columna de fraccionamiento. Agregar entonces gota a gota la solución de dicromato de potasio-ácido sulfúrico en un lapso de 15 minutos (2) de tal forma que la temperatura en la parte superior de la columna no pase de 80-85 o C (3). Cuando se ha añadido todo el agente oxidante continuar calentando la mezcla suavemente por 15 minutos más y colectar la fracción que destila debajo de 90 oC (4). Pasar el destilado a un embudo de separación (limpio), decantar la fase acuosa y medir el volumen de butiraldehído obtenido para calcular el rendimiento. Agregar 2 gotas del producto a 0.5 ml del reactivo de 2,4-dinitrofenilhidrazina en un tubo de ensayo y agitar vigorosamente; al dejar reposar precipita el derivado del aldehído el cual se puede purificar por cristalización de etanol-agua. El punto de fusión reportado para la 2,4dinitrofenilhidrazona del butiraldehído es de 122 o C. NOTAS: (1) ¡Precaución! La reacción es exotérmica. Si al dejar enfriar la solución, cristaliza el dicromato, caliente suavemente con flama y pásela al embudo de separación en caliente. Continúe con la práctica. (2) Más o menos dos gotas por segundo. (3) La oxidación del alcohol se efectúa con producción de calor pero puede ser necesario calentar la mezcla de vez en cuando para que la temperatura no baje de 75 oC. (4) La probeta en la que se recibe el destilado debe estar en baño de hielo. CUESTIONARIO 1. ¿Qué sucedería si al efectuar la oxidación del n-butiraldehído no se controla la temperatura de destilación? ¿Este método se puede aplicar a todos los alcoholes? ¿Qué destila antes de 80 oC?, ¿Qué destila arriba de 90 oC? ¿Cómo logra identificar el producto obtenido?, ¿Esta forma de identificación se puede aplicar a todos los aldehídos?, ¿Es especifica para aldehídos? 5. ¿Si no se controla bien la reacción y se forma el ácido carboxílico correspondiente, en donde lo podría encontrar, y como lo identificaría? 6. ¿Si al destilar el aldehído, también destilara parte del alcohol sin reaccionar, como comprobaría su presencia? 7. ¿Es tóxico el CrVI?, ¿Es tóxico el CrIII?, Se puede tirar al drenaje. 2. 3. 4. BIBLIOGRAFÍA 1. Vogel, A. I. Text Book Practical Organic Chemistry, 3ª. Edición, Editorial Longmans, Londres (1961), Páginas: 320-322. 24 OBTENCIÓN DE BUTIRALDEHIDO POR OXIDACIÓN DE n-BUTANOL Química Orgánica II (1413) Coordinadora Dra. Ma. del Consuelo S. Sandoval G 2. Morrison, R. T. y Boyd, R. N., Organic Chemistry. 2ª Allyn and Bacon Inc., Boston (1966) 3. Brieger, G., Química Orgánica Moderna, Curso Práctico de Laboratorio, Ediciones del Castillo, S.A., Madrid (1970). Obtención de n-butiraldehído partiendo de n-butanol n-butanol 1) Calentar a ebullición K2Cr2O7/H2SO4 (Goteo) D1 Mezcla de reacción 2) Destilar T < 90°C Destilado Residuo Cr3+, H2SO4 Ácido butírico, n-Butanol Butiraldehído H2O 3) Separar Fase Acuosa Fase Orgánica H2O Butiraldehído D2 4) Tomar muestra + 2,4-Dinitrofenilhidrazina 2,4-Dinitrofenilhidrazona del butiraldehído D3 D1: Agregar bisulfito de sodio, para pasar todo el Cr6+ a Cr3+ (Hacer esto en la campana). Precipitar con lejía de sosa. Filtrar el precipitado Cr(OH)3. Repetir la operación hasta no obtener precipitado. La solución debe neutralizarse para ser desechado por el drenaje. El hidróxido debe mandarse a confinamiento controlado. D2: Deséchese por el drenaje. D3: Filtrar. Mandar sólidos a incinerar. Tratar el líquido con carbón activado hasta la eliminación del color naranja. 25





