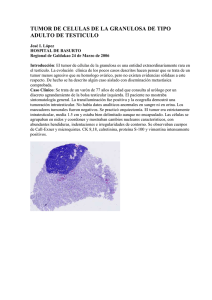
TUMOR DESMOPLÁSICO DE CÉLULAS PEQUEÑAS REDONDAS
Anuncio

Rev Cubana Oncol 1999;15(1):43-8 TEMAS DE REVISIÓN Instituto Nacional de Oncología y Radiobiología TUMOR DESMOPLÁSICO DE CÉLULAS PEQUEÑAS REDONDAS Dra. María del C. Barroso Álvarez1 y Dra. Iraida Caballero Aguirrechu2 RESUMEN Los tumores de células redondas pequeñas son un grupo heterogéneo de neoplasias propias de la niñez y la adolescencia, constituidos por una extensa lista no sólo de entidades clásicas, sino también por una recientemente descrita, a la que se llamó tumor desmoplásico abdominal de células pequeñas y redondas, cuyo diagnóstico positivo se sustenta en estudios inmunohistoquímicos y microscopía electrónica. La edad promedio descrita es de 22 años, y es más frecuente en el sexo masculino, con marcaje inmunohistoquímico epitelial, muscular y neural, que se plantea como una coexpresión epitelial (keratina, antígeno de membrana epitelial) mesenquinal muscular (desmina y vimentina) y neural (neuroenolasa específica), además de una traslocación +(11;22)(p13;q12). Los enfermos se presentan con enfermedad diseminada y su tratamiento multidisciplinario combina la cirugía y la quimioterapia agresiva, incluye trasplante de médula ósea o de células progenitoras periféricas y radiaciones ionizantes. Hasta el momento la sobrevida reportada es de 4 años. Descriptores DeCS: NEOPLASMAS DE TEJIDO CONJUNTIVO/diagnóstico; NEOPLASMAS DE TEJIDO CONJUNTIVO/terapia; NEOPLASMAS ABDOMINALES/diagnóstico; NEOPLASMAS ABDOMINALES/terapia. El término tumor de células pequeñas y redondas (TCPR) de partes blandas ha sido empleado tradicionalmente para designar un grupo heterogéneo de neoplasias que aparecen sobre todo en la niñez y la adolescencia. A pesar de su diferente origen tisular y diferenciación histotípica, estos tumores malignos comportan aspectos morfológicos semejantes, que coexis1 2 ten en una densa proliferación de células pequeñas redondas de aspecto muy primitivo e indiferenciado. Por esta razón, el término TCPR no es aceptable como categoría diagnóstica y sólo representa una definición provisional que debe llegar a un diagnóstico preciso.1-6 La extensa lista que debe considerarse en el diagnóstico diferencial de un TCPR Especialista de II Grado en Oncología. Profesora Agregada. Especialista en Medicina General Integral, Residente de 4to. Año de Oncología. 43 comprende no sólo las entidades clásicas (rabdomiosarcoma, tumor neuroectodérmico periférico primitivo y linfomas), sino también tumores metastásicos y 2 entidades recientemente descritas: el tumor desmoplásico de células pequeñas y redondas (TDCPR) y los tumores rabdoides de partes blandas1,7,8 que se describen a continuación: TCPR CLÁSICOS - Neuroepitelioma periférico - Sarcoma de Ewing extraóseo - Neuroblastoma metastásico - Rabdomiosarcoma - Linfomas malignos no hodgkinianos/ leucemia NUEVAS ENTIDADES - Tumor desmoplásico de células pequeñas redondas - Tumor rabdoide de partes blandas DIAGNOSTICO DIFERENCIAL - Tumor metastásico de Wilms; tumor extrarrenal de Wilms - Ectomesenquimoma maligno - Sarcoma sinovial poco diferenciado - Osteosarcoma de células pequeñas - Condrosarcoma mesenquimal La información clínica y los exámenes histopatológicos de rutina como la hematoxilina-eosina, la coloración de reticulina y la coloración de glucógeno, deben ser suplementadas con estudios inmunohistoquímicos para establecer un correcto diagnóstico, aunque en un considerable número de casos, los aspectos 44 morfológicos por sí solos, sugieren fuertemente algunos de estos diagnósticos. En algunos TCPR menos diferenciados el examen por microscopia electrónica puede ofrecer datos adicionales de indudable utilidad.9-11 El diagnóstico preciso tiene una importancia clínica y pronóstica porque los esquemas terapéuticos son diferentes, aún en subgrupos de tumores de la misma línea de diferenciación, como por ejemplo sucede entre el rabdomiosarcoma alveolar y el embrionario, y los resultados van desde excelentes, como los que se alcanzan en pacientes pediátricos con linfomas no hodgkinianos/leucemias, hasta los muy graves, como son los tumores rabdoides y el TDCRP que es un tumor indiferenciado, asociado a las superficies serosas, especialmente del peritoneo.1,4-8 Éste es un tumor infrecuente, descrito por primera vez por Gerald en 19899, y hasta enero de 1998 se habían descrito 60 pacientes en la literatura médica. Generalmente, al momento del diagnóstico es un tumor diseminado, con toma ganglionar extensa, hígado y pulmón y raras veces metastiza médula ósea y huesos. Se comporta como un tumor agresivo, con compresión de las estructuras vecinas (gastrointestinal o genitourinaria principalmente), aunque también se puede encontrar en localización paratesticular y en el tórax. La sintomatología clínica estará en dependencia de las estructuras tomadas y el tamaño o volumen tumoral y también se pueden presentar sudoraciones nocturnas, pérdida de peso, dolor, constipación y hematuria, entre otros. Se encuentra, sobre todo en adolescentes y adultos jóvenes, entre los 8 y los 38 años de edad con una edad promedio de 22 años. Es más frecuente en el sexo masculino con una relación de 4:1.8-12 Desde el punto de vista histopatológico este tumor está caracterizado por presentar grupos compactos de células neoplásicas de tamaño variable y bien delimitadas, separadas por bandas gruesas de estroma desmoplásico. Este patrón lobular puede ser sólo focal y las células tumorales a veces están agrupadas en cordones pequeños trabeculados que de manera alterna pueden formar grandes islas sólidas neoplásicas, rodeados por delgados tabiques de estroma fibrovascular, por lo que su aspecto recuerda a los tumores carcinoides. Con menos frecuencia puede haber un patrón pseudoalveolar focal, y áreas sólidas de crecimiento difuso. También pueden observarse, aunque no es frecuente, estructuras parecidas a las rosetas que recuerdan a los neuroblastomas y los tumores neuroectodérmicos primitivos con tendencia a la formación tubular. También se ha descrito necrosis de los nidos celulares y calcificaciones.1,3-5,9-13 El estroma desmoplásico colágeno tiene un componente celular importante, de miofibroblastos elongados y una rica vascularización que incluye capilares y grandes vasos de paredes engrosadas. Las células neoplásicas son pequeñas y redondas, con un citoplasma escaso o moderado, usualmente eosinófilo y a veces vacuolados y claros. La coloración de PAS puede revelar una pequeña cantidad de glucógeno. El núcleo tiene condensaciones citoplasmáticas, parecidas a inclusiones eosinofílicas que se asemeja a los tumores rabdoides y que están presentes en algunas células. Los núcleos son monomórficos, con cromatina fina y con 1 a 3 nucléolos, cercanos a la membrana nuclear. Hay una marcada actividad mitótica. En el 10 % de los casos hay células grandes con pleomorfismo nuclear. Sólo en casos raros se observan células alargadas. Este estroma lo distingue del resto de los TCPR. Se sugiere que este estroma es una reacción intrínseca a las células tumorales y esta ca- racterística también está presente en las metástasis.2, 5-13 El perfil inmunohistoquímico (tabla) expresa los marcadores polifenotípicos con una coexpresión epitelial (keratina, antígeno de membrana epitelial) mesenquinal muscular (desmina y vimentina) y neural (neuroenolasa específica). Este perfil antigénico, distingue esta entidad de otros TCPRA que se ven en este grupo de edades. La diferenciación de tipo epitelial de éste se plantea por la presencia de anticuerpos antiqueratina de bajo peso molecular y de antígenos de membrana epitelial. La desmina es casi siempre intensamente positiva, y se observa como puntos, en más del 50 % de los casos. Otros marcadores musculares como la actina α músculo-específica (HHF-35) y las actinas α de músculo liso son negativos, así como la expresión de MyoD1. Estos hallazgos sugieren que la positividad a la desmina, probablemente no indica una verdadera diferenciación muscular, sino que es el resultado de una expresión neoplásica aberrante. La vimentina también está presente, pero toma la apariencia globoide paranuclear con menos frecuencia que la desmina y usualmente en un número menor de células,1,2,6-10 otro aspecto de este tumor es su parcial diferenciación neuroectodérmica y se detecta neuroenolasa específica (NSE), Leu-7 y la sinaptofisina en más del 50 % de los casos, en células aisladas o agrupadas. La positividad a la cromogranina es discutible, y ha sido descrita sólo por algunos autores. Usualmente son negativas las reacciones a neurofilamentos, GFAP y a la proteína S-100. Se puede encontrar actividad focal, en algunos casos de anticuerpos al antígeno p30/32MIC2, aunque la coloración tiene una distribución citoplásmica difusa y no en la membrana, como se ve en el sarcoma de Ewing y los neuroepiteliomas periféricos. 45 Las técnicas de inmunohistoquímica son importantes en el diagnóstico diferencial con otros tumores de la familia de células pequeñas y redondas, como son los tumores carcinoides metastásicos y el tumor extrarrenal de Wilms. También debe tenerse en cuenta el mesotelioma de células pequeñas, pero este tumor aparece en edades más tardías y no muestran la diferenciación polifenotípica de la familia de los TCPR.1 Tabla. Perfil inmunohistoquímico típico del TDCPR Positiva Keratina EMA Desmina* Vimentina Positiva/negativa NSE Leu-7 Syn Chr Negativa HHF 35 a-sma Myo D1 NF GFPA S-100 Leyenda: EMA: antígeno de membrana epitelial; a-sma: actina α de músculo liso; chr: cromogranina; HHF5: actina antimúsculo específica al monoclonal HHF5; Myo D1 anticuerpo 5,8 A anti Myo D1; NF: neurofilamento; Syn: sinaptofisina; S-100: proteína 100; * positividad en puntos paranucleares En ocasiones la desmina y la keratina son negativas con una positividad al MIC2 (anticuerpo monoclonal anti p30/32MIC2), lo que puede llevar a errores diagnósticos, sobre todo si el tumor tiene un patrón pseudoalveolar y estructuras parecidas a rosetas, aun en presencia de grupos celulares separados por gruesas bandas de estroma desmoplásico y presencia de inclusiones citoplasmáticas. Los estudios citogenéticos muestran una traslocación t(11;22) (p13;q12) que difiere de las encontradas en el tumor de Ewing, y parece ser específica de éstos. En esta traslocación están involucrados los genes WT1 y EWS. El análisis de la reacción en cadena de la polimerasa de la 46 transcriptasa reversa del tumor fresco confirma la transcripción característica EWSWT1.2,7,8,14-16 En el diagnóstico de estos tumores, se realizan con frecuencia estudios de microscopia electrónica que señala células tumorales indiferenciadas uniformes y empaquetadas; en la interfase en el estroma, pueden formar una lámina basal discontínua. En el citoplasma se pueden observar filamentos intermediarios. En algunas células, el núcleo está desplazado por grandes agregados de filamentos que corresponden a los puntos citoplasmáticos positivos a la desmina y a la vimentina. En casos raros, pueden encontrarse un número pequeño de gránulos intracitoplasmáticos de núcleo denso.8,12,17 En los tumores abdominales, es esencial el diagnóstico por laparotomía pues ni siquiera la tomografía axial computarizada (TAC) evalúa de forma adecuada la extensión de la enfermedad y aunque la biopsia por aspiración con aguja fina, hace el diagnóstico, el material no se considera suficiente para el diagnóstico preciso. Esta lapatoromía diagnóstica permite evaluar la extensión de la enfermedad y realizar una citorreducción, siempre que sea posible.3-6,10,18 y 19 En cuanto al tratamiento no hay definiciones del mejor esquema terapéutico y como en todos los tumores, estará en dependencia del estado del paciente y de los parámetros de laboratorio. El tratamiento ideal es la quimioterapia agresiva, seguida de trasplante de médula ósea de células progenitoras periféricas, la cirugía de evaluación de respuesta (con o sin braquiterapia intraoperatoria y la criocirugía de nódulos peritoneales).19-21 Como la mayoría de los pacientes se presentan con una enfermedad localmente avanzada o con metástasis a distancia, la quimioterapia es el tratamiento inicial de elección, aunque algunos de estos tumores responden poco a este tratamiento. Se prefiere el empleo de dosis altas de quimioterapia para obtener una remisión, consolidar la remisión con radiaciones o con quimioterapia mieloablativa y trasplante de médula ósea o de células progenitoras. Los citostáticos más empleados son la adriamicina, la vincristina, la ciclofosfamida y el platino. La experiencia de la literatura señala que el empleo de altas dosis de quimioterapia con esquemas tales como el PAVEP (ciclofosfamida/vepesid/adriamicina/ cisplatino) o PEVEP (donde se sustituye la adriamicina por la epirrubicina) por 4 ciclos más carboplatino/vepesid/ifosfamida), con trasplante de células periféricas progenitoras, producen remisiones completas estables. Otros esquemas asociados o remisiones completas son: adriamicina/ciclofosfamida/vincristina/platino, o altas dosis de ciclofosfamida/ adriamicina/vincristina. También se ha publicado el empleo de esquemas alternos, consistente en la administración de regímenes de multiagentes sin resistencia cruzada conocida, como la cisplatino/vepesid/adriamicina/bleomici- na,gemcitabina/ifosfamida/acarbazina y methotrexate/5fluoroura-cilo/ácido folínico.18-21 Después de la quimioterapia de inducción se debe realizar una cirugía, considerada como agresiva, de las lesiones abdominales visibles y hay quienes preconizan el tratamiento con radiaciones ionizantes intraoperatorio con altas tasas de dosis hasta administrar 1 200 cGy o el empleo de criocirugía de los nódulos peritoneales. La utilidad de la teleterapia es discutible por la poca tolerancia de las vísceras abdominales. No obstante, se han reportado sobrevidas prolongadas en pacientes que han recibido radioterapia sobre el abdomen. La sobrevida reportada en la literatura médica no es mucho mayor de 4 años. Se han reportado remisiones completas estables en muchos pacientes con una duración media entre 6 y 48 meses, pero la remisión parcial es la más frecuente. La causa de muerte más frecuente, además de la diseminación del tumor, es la sepsis secundaria al tratamiento. Se describió un paciente en remisión completa constatada en la necropsia que falleció por un síndrome de Budd-Chiari. SUMMARY The tumors of the small round cells are a heterogeneous group of neoplasias characteristic of childhood and adulthood that is composed of a long list including not only classical entities but also a recently described one called abdominal desmoplastic tumor of small round cells whose positive diagnosis is based on immunohistochemical studies and electronic microscopy. Average age is 22 and it is more frequent among males with epithelial, muscular and neural immunohistochemical marking that is stated as an epithelial (keratin, antigen of epithelial membrane), muscular mesenchymal (desmin and vimentin), and neural coexpression (specific phosphopyruvate hydratase), in addition to a traslocation + (11;22) (p13;q12). The patients present themselves with a disseminated disease and their multidisciplinary treatment combines surgery and aggresive chemotherapy, including the transplant of bone marrow or of peripheral progenitor cells and ionizing radiations. Up to now, a 4 year survival has been reported. Subject headings: NEOPLASMS, CONNECTIVE TISSUE/diagnosis; NEOPLASMS, CONNECTIVE TISSUE/ therapy; ABDOMINAL NEOPLASMS/therapy. 47 REFERENCIAS BIBLIOGRÁFICAS 1. Amore ESG, Ninfo V. Soft tissue round cell tumors: morphological parameters. Semin Diag Pathol 1996;13(3):184-203. 2. Mitelman F, Johansson B, Mandahl N, Mertens F. Clinical significance of cytogenetic findings in solid tumors. Cancer Genet Cytogenet 1997;95(1):1-8. 3. Crombleholme TM. The desmoplastic round cell tumor: a new solid tumor of childhood. Oncolink [Disponible en:] http;///www.intap.net-dsret/farhat.html. 4. Gerald WL, miller HK, Battifora H. Intra-abdominal desmoplastic small-round cell. Report of 19 cases. Am J Surg Pathol 1991;15:499-513. 5. Prat J, Matias-Guiu X, Algaba F. Desmoplastic round cell tumor. Am J Surg Pathol 1992;16:306-7. 6. Farhat F, Culine S, Lhomme C, Duvillard P. Desmoplastic small round cell tumor in adults: a new entity. Bull Cancer 1995;82(8):665-73. 7. Quiel V. Desmoplastic small round cell tumor with multiple phenotype differentiation. Zentralb Gynacol 1995;117(7):375-7. 8. Winters JL, Geil JD, OConnor WN. Immunohistology, cytogenetics, and molecular studies of small round cell tumors of childhood. Ann Clin Lab Sci 1995;25(1):66-78. 9. Gerald WL, Rosai J. Desmoplastic small cell tumor with divergent differentiation. Pediatr Pathol 1989;9:177-83. 10. González-Cruzzi F, Susan E, Crawford SE. Intra-abdominal desmoplastic small-round cell with divergent differentiation. Observation of three cases of childhood. Am J Surg Pathol 1990;14:633-42. 11. Parkash B, Gerald WL, Parma A. Desmoplastic small round cell tumor of the pleura. Am J Surg Pathol 1995;19:659-65. 12. Ordoñez NG, Zirkin R, Bloom RE. Malignant small cell epithelial tumor of the peritoneum coexpresing mesenchymal-type intermediate filaments. AM J Surg Pathol 1989;13:413-21. 13. El Kattan I, Redline RW, Naggar AK, Grimes MC, Abdul Karim FW. Cytologic features of intraabdominal desmoplastic small round cell tumors. Acta Cytol 1995;39(3):514-20. 14. Whang-Peng J, Triche TJ, Knutsen. Cytogenetic characterization of selected small round cell tumors of childhood. Cancer Gen Citogen 1986;21(3):185-208. 15. Ladanyi M, Gerald W. Fusion of the EWS and WT1 genes in the desmoplastic small round cell tumor. Can Res 1994;54:2837-40. 16. De Alava E, Ladanyi M, Rosai J, Gerald WL. Detection of chimeric transcriptase polimerase chain reaction. A specific diagnostic assay. Am J Pathol 1995;147(6):1584-91. 17. Mink KW. Uselfulness of electron microscopy in the diagnosis of small round cell tumors of the sinonasal region. Ultrastruct Pathol 1995;19(5):347-63. 18. Cummings OW, Ulbrigth TM, Young RH, Del Tos AP, Fletcher CD, Hull MT. Desmoplastic small round cell tumor of the paratesticular region. A report of six cases. Am J Surg Pathol 1997;21(2):219-25. 19. Kushner BH, LaQuaglia MP, Wollner N, Meyers PA, Lindsley KL. Desmoplastic small round-cell tumor: prolonged progression free survival with aggressive multimodality therapy. J Clin Oncol 1996;4:1526-31. 20. De Lena M, Caruso ML, Marzullo F, Mancarella S. Complete response chemotherapy in intraabdominal desmoplastic small round cell carcinoma. Tumori 1998;84(3):412-6. 21. Mazurick M, Paterson AH, Temple W, Arthur K. Benefit of aggressive multimodally therapy with autologous stem cell support for intraabdominal desmoplastic small round cell tumor. Bone Marrow Transplant 1998;21(9):961-3. Recibido: 2 de noviembre de 1998. Aprobado: 6 de noviembre de 1998. Dra. María del C. Barroso Álvarez. Instituto Nacional de Oncología y Radiobiología. Calle 29 esquina a E, El Vedado, Ciudad de La Habana, Cuba. 48