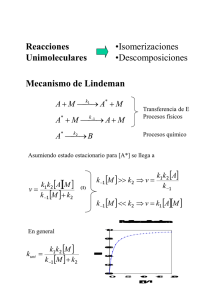
Reacciones en cadena 2 H Br HBr + →
Anuncio

1/30/2014 Reacciones en cadena Mecanismo: Christiansen, Herzefeld y Polanyi H 2 Br2 2 HBr Propagación Inhibición Iniciación Ley de rapidez : 1 d HBr k r H 2 Br2 2 Terminación 2 dt 1 k r' HBr Br2 1 P Propagación ió 1 1/30/2014 Ejemplo de reacción en cadena H2 Br2 2 HBr Ley de rapidez : 2 1 d HBr kr H 2 Br2 2 dt 1 kr' HBr Br 1 0 2 El producto está actuando como inhibidor en etapas lejos de t 0. En t 0, el orden, n (3/2) Mecanismo M + Br2 Br + H2 H + Br2 HB + H HBr M + 2Br k1 k2 k3 k4 k5 2 Br + M iniciación HBr + H propagación HBr + Br B Br + H2 Br2 + M propagación i hibi ió inhibición terminación 2 1/30/2014 M + Br2 Mecanismo Br + H2 H + Br2 rapidez de reacción neta rformación rdesaparición H 2 Br2 2 HBr HBr + H M + 2Br k1 2 Br + M k2 HBr + H k3 k4 k5 1 d HBr k 2 Br H 2 k 3 H Br2 k 4 H HBr dt 2 HBr + Br Br + H2 Br2 + M (1) Estado estacionario para intermediarios que no pueden determinarse experimentalmente d H dt d Br dt 0 k 2 Br H 2 k3 H Br2 k 4 H HBr (2) 0 2 k1 Br2 M k 2 Br H 2 k3 H Br2 (3) k 4 H HBr 2 k5 Br M 2 Rapidez de reacción neta 1 d HBr k 2 Br H 2 k 3 H Br2 k 4 H HBr dt 2 (1) Sumando las ecuaciones de los intermediarios d H dt d Br dt 0 k 2 Br H 2 k3 H Br2 k 4 H HBr (2) 0 2 k1 Br2 M k 2 Br H 2 k 3 H Br2 (3) k 4 H HBr HB 2 k 5 B Br M 2 0 2k1 Br2 M 2k5 Br M 2 2k5 Br M 2k1 Br2 M 2 (4) 3 1/30/2014 Concentración de Br• estacionaria Sumando (2) y (3) : 2k5 Br M 2k1 Br2 M (4) k Br 1 Br2 es k5 (5) 0 k 2 Br H 2 k 3 H Br2 k 4 H HBr (6) k 2 Br H 2 H k 3 Br2 k 4 HBr (7) 2 De la ecuación (2) : Sustituyendo (5) en (7) : H k2 Br H k1 k2 2 2 (8) k 3 Br2 k 4 HBr Ley del rapidez del producto según mecanismo 1 d HBr k Br H k H Br k 2 2 dt Sustituyendo (8) y (5) en (1) : 1 d HBr k2 2 dt B Br k1 k2 2 k4 HBr k2 2 3 2 4 H HBr (1) k1 k k Br H Br 3 2 k2 2 2 2 H2 k3 Br2 k4 HBr Br H k1 k2 2 2 (9) k3 Br2 k4 HBr Sacando denominador común y luego factor común, combinando y luego dividiendo entre k4[Br2] toda la expresión arriba y abajo: 2 k k 1 d HBr 2k2 3 k4 1 k5 H 2 Br2 2 dt k3 k4 HBr Br 1 1 2 2 (10) 4 1/30/2014 Comparación con Ecuación experimental k k 1 d HBr 2 k 2 3 k 4 1 k5 H 2 Br2 dt 2 k3 k4 HBr Br 1 2 2 2 k 1 d HBr 2k2 1 k5 H 2 Br2 2 dt 1 k4 k3 HBr Br2 Si : kr 2k2 k1 k5 2 (10) : k3 k4 1 2 1 2 dividiendo 10 arriba y abajo por 1 1 kr' k4 k3 y 2 1 d HBr kr H 2 Br2 2 dt 1 kr' HBr Br (11) (12) 1 2 (13) Aproximación del paso lento o determinante de reacción 5 1/30/2014 Reacción y mecanismo a I OCl Cl OI Ley de rapidez experimental: d I dt k OCl I Mecanismo : OH 1 OCl H 2O HClO OH k k K1 1 k2 HClO I HIO Cl paso lento HIO OH OI H 2O k k3 (1) (2) (3) 3 k3 k2 Mecanismo : Aproximación paso lento 1 OCl H2O HClO OH k k 1 d I (1) (2) 3 HIO OH OI H2O k (3) k k2 HOCl I K1 HClO I HIO Cl paso lento k2 3 (b) dt del paso 1 en el mecanismo : HOCl K1 OCl OH (c ) S tit Sustituyendo d (c) en b : d I dt OCl I OCl I k2 K1 k' OH OH 6