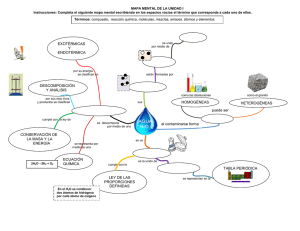
Clase Isósteros Archivo
Anuncio
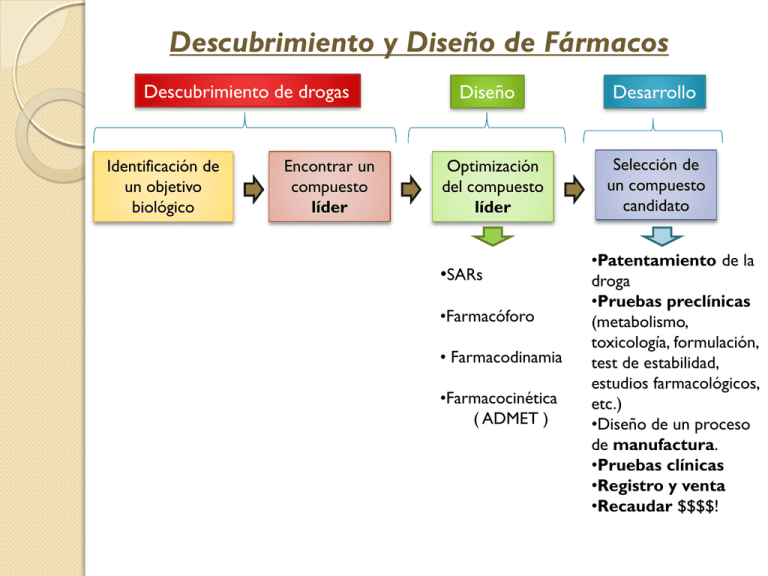
Descubrimiento y Diseño de Fármacos Descubrimiento de drogas Identificación de un objetivo biológico Encontrar un compuesto líder Diseño Optimización del compuesto líder •SARs •Farmacóforo • Farmacodinamia •Farmacocinética ( ADMET ) Desarrollo Selección de un compuesto candidato •Patentamiento de la droga •Pruebas preclínicas (metabolismo, toxicología, formulación, test de estabilidad, estudios farmacológicos, etc.) •Diseño de un proceso de manufactura. •Pruebas clínicas •Registro y venta •Recaudar $$$$! Optimización del compuesto líder • Identificar las relaciones de estructura-actividad (SARs). • Identificar el farmacóforo (atomos o grupos funcionales requeridos para una específica actividad farmacológica, y sus posiciones relativas en el espacio). • Mejorar la interacción con su objetivo biológico (Farmacodinamia) – Unión al receptor, efectos en el organismo, ventana terapéutica, efectos indeseables. • Mejorar las propiedades farmacocinéticas – ADME T Variación de los sustituyentes Extensión de la estructura Extensión o contracción de cadenas o anillos Variaciones de anillos Fusiones de anillos ReemplazosIsóstericos Isóstericos y bioisóstericos Reemplazos y bioisostéricos Simplificación de la estructura Rigidización de la estructura Variaciones moleculares basadas en reemplazos iso-bioistéricos ISÓSTEROS: átomos o grupos de átomos que presentan características electrónicas y estéricas similares Isósteros bivalentes BIOISÓSTEROS: (isósteros no clásicos) átomos o grupos de átomos que presentan propiedades biológicas similares (aunque la semejanza fisicoquímica sea vaga) Reemplazos Isostéricos: • Mejorar la interacción con su objetivo biológico (Farmacodinamia) – Unión al receptor, efectos en el organismo, ventana terapéutica, efectos indeseables. • Mejorar las propiedades farmacocinéticas – Absorción Distribución Metabolismo Excreción Optimización de propiedades : Hidro/lipofílicas (LogP) interacción con receptores, paso a través de las membranas Polaridad Pka Modificaciones que afecten la metabolización Reemplazos isostéricos Clasificación: Átomos o grupos univalentes Átomos o grupos divalentes Átomos o grupos trivalentes Anillos equivalentes Grupos con efectos polares similares: Biosisot. de ácidos carboxílicos Biosisot. de ésteres carboxílicos Bioisost. del enlace carboxamida Biosisot. de urea Biosisot. de fenol Biosisot. de catecol Biosisot. de sulfonamida Inversión de grupos funcionales Reemplazos isostéricos Clasificación: Átomos o grupos univalentes Metabolic product Anti tumor agents Reemplazos isostéricos Clasificación: Átomos o grupos divalentes Reemplazos isostéricos Clasificación: Átomos o grupos divalentes Reemplazos isostéricos Clasificación: Átomos o grupos divalentes Reemplazos isostéricos: Átomos o grupos univalentes Átomos o grupos divalentes Átomos o grupos trivalentes Anillos equivalentes Grupos con efectos polares similares: Biosisot. de ácidos carboxílicos Biosisot. de ésteres carboxílicos Bioisost. del enlace carboxamida Biosisot. de urea, Biosisot. de fenol Biosisot. de catecol Biosisot. de sulfonamida Inversión de grupos funcionales Anillos equivalentes Inhibidor de Acetilcolinesterasa Anillos equivalentes Reemplazos isostéricos: Átomos o grupos univalentes Átomos o grupos divalentes Átomos o grupos trivalentes Anillos equivalentes Grupos con efectos polares similares: Biosisot. de ácidos carboxílicos Biosisot. de ésteres carboxílicos Bioisost. del enlace carboxamida Biosisot. de urea, Biosisot. de fenol Biosisot. de catecol Biosisot. de sulfonamida Inversión de grupos funcionales Biosisot. de ésteres carboxílicos Molécula con una mayor estabilidad metabólica, (t1/2= 61 h) Reemplazos isostéricos: Átomos o grupos univalentes Átomos o grupos divalentes Átomos o grupos trivalentes Anillos equivalentes Grupos con efectos polares similares: Biosisot. de ácidos carboxílicos Biosisot. de ésteres carboxílicos Bioisost. del enlace carboxamida Biosisot. de urea, Biosisot. de fenol Biosisot. de catecol Biosisot. de sulfonamida Inversión de grupos funcionales Bioisost. del enlace carboxamida : clásicos Bioisost. del enlace carboxamida: no clásicos Los que más se aproximan en el reemplazo del enlace peptídico Biosisósteros de urea tiourea cianoguanidina diaminonitroetileno Inversión de grupos funcionales Generalmente usado en química de péptidos Similares valores de inhibición de endopeptidasa neutral y de termolisina . Diferencias en la inhibicion de la Enz. Convertidora de angiotensina. Inversión de grupos funcionales No peptídicos y… suerte! Antihistamínico Hipnótico Sedante antihemético antidepresivo antipsicótico Metabolismo: Conversión química o transformación, de fármacos o sustancias endógenas en compuestos más fáciles de eliminar. metabolitos activos metabolitos inactivos productos metabólicos con menor, mayor o distinta actividad farmacológica. Metabolismo: Glucurónidos Acetatos Sulfatos Oxidaciones: Cit P450 Oxidaciones: Cit P450 Hidrólisis: Amidas se hidrolizan más lento que los ésteres Modificaciones que hacen a las drogas más resistentes al metabolismo Remoción, reemplazo de grupos metabólicamente susceptibles: Grupo Protector estérico: Bioisósteros de grupos polares: Bloqueadores de metabolismo: Remoción o reemplazo de grupos metabólicamente lábiles: Variación de anillos o sustituyentes de anillos: Imidazol es más susceptible a metabolización que el triazol. Modificaciones que hacen a las drogas menos resistentes al metabolismo Introducción de grupos metabólicamente lábiles: Prodrogas Ésteres: Compuestos inactivos por sí mismos, pero que son convertidos a moléculas activas en el organismo, generalmente mediante una reacción enzimática. Análisis de las Modificaciones Isostéricas: compuesto líder compuesto modificado Aumento, disminución o anulación de: Actividad Potencia Selectividad ADME Toxicidad Efectos indeseables