Descargar
Anuncio

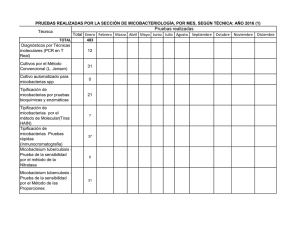
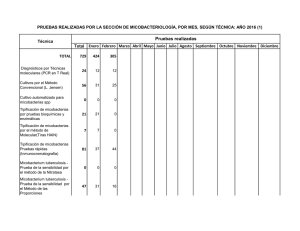
SUSCEPTIBILIDAD A INFECCIONES POR MICOBACTERIAS Vía IFN-γ/IL-12 Bioq. M. Mercedes Gallinger Bioq. Javier Jimenez Residencia de Inmunología para Bioquímicos Hospital de Pediatría “J. P. Garrahan” COREBIO 2006 MEDIO AMBIENTE Factores de exposición Factores micobacterianos FENOTIPOS INMUNOLÓ INMUNOLÓGICOS EXPOSICIÓ EXPOSICIÓN A MICOBACTERIA INFECCIÓ INFECCIÓN Inmunidad innata INFECCIÓ INFECCIÓN Inmunidad adaptativa FENOTIPOS CLÍ CLÍNICOS Factores Factores gené éticos gen ticos HUÉSPED Factores no genéticos IFNγ e IL12 fundamentales en la defensa contra microorganismos intracelulares. IFNγ Producido por células NK, Li Th1, Li T CD8 Li Tγδ. + y Activa fagocitos mononucleares y Neutrófilos. Favorece la diferenciación Li T CD4+ a Li Th1 inhibiendo la diferenciación a Li Th2. IL-12 Producida por subpoblaciones de macrófagos y células dendríticas activadas. Estimula cél. NK. Favorece la diferenciación Li T CD4+ a Li Th1 y estimula su proliferación. Puede ser inducida por exposición de MN a microorganismos o sus productos como LPS. MECANISMO DE DEFENSA CONTRA MICOBACTERIAS: Vía IFN-γ/IL-12 bacteria DCDC-sign R Toll/CD14 Toll/CD14 IL-12 IFNIFN-α ILIL-12R R de manosa β1 β2 fagosoma muerte bacteriana IFN-γ quemoquinas TNFTNF-α R1 R2 IFNIFN-γR TNFTNF-αR Li Th1/cél. NK FAGOCITO MN TNFTNF-α IL-12R IL-12p70 p40 Tyk2 Jak2 p35 Li Th1/cél. NK activadas IL-12Rβ1 IL-12Rβ2 Li Th1/cél. NK activadas P P STATSTAT-4 P P P P STATSTAT-4 -4-P STATSTAT- 4- P - 4 STAT STAT STAT STAT STATSTAT-4 P P STATSTAT-4-P STATSTAT-4-P Núcleo IFN-γR Jak1 Jak2 IFN-γ Fagocito MN IFN-γR2 IFN-γR2 IFN-γR1 IFN-γR1 IFN-γR1 Ubicua, en todas las células nucleadas. Pobremente inducible. Cadena que une IFN-γ. IFN-γR2 Bajo nivel de expresión. Inducible, finamente regulada limitante para la respuesta a IFN-γ. No une IFN-γ. Cadena transductora de señales. Estabiliza el complejo IFN-γ /IFN-γR1. Fagocito MN P P P P P STATSTAT-1 P STATSTAT-1-P P STATSTAT-1-P STATSTAT-1 P STATSTAT-1-P STATSTAT-1-P STATSTAT-1-P STATSTAT-1-P P P Núcleo P P SUSCEPTIBILIDAD MENDELIANA A INFECCIONES POR MICOBACTERIAS 1996: defectos hereditarios en la inmunidad mediada por IFNγ/L12 susceptibles a infecciones por micobacterias ambientales no tuberculosas o el bacilo de la vacuna BCG. IL-12Rβ1 IL-12p40 Incapacidad de sus IFN-γR1 células de producir o IFN-γR2 responder a IFN-γ. STAT-1 SUSCEPTIBILIDAD MENDELIANA A INFECCIONES POR MICOBACTERIAS 1996: defectos hereditarios en la inmunidad mediada por IFNγ/L12 susceptibles a infecciones por micobacterias ambientales no tuberculosas o el bacilo de la vacuna BCG. IL-12Rβ1 IL-12p40 IFN-γR1 IFN-γR2 STAT-1 MECANISMO DE DEFENSA CONTRA MICOBACTERIAS: Vía IFN-γ/IL-12 bacteria DCDC-sign R Toll/CD14 Toll/CD14 IL-12 IFNIFN-α R de manosa r ILIL-12R β1 β2 fagosoma muerte bacteriana IFN-γ quemoquinas TNFTNF-α R1 R2 IFNIFN-γR TNFTNF-αR Li Th1/cél. NK FAGOCITO MN TNFTNF-α Deficiencia de IL-12Rβ1 Herencia: AR. Patógenos más frecuentes: BCG, Salmonella spp. Deficiencia: - completa (58) fenotipo clínico más severo - parcial (1) Receptores mutantes WT IL-12Rβ1 EC TM IC AR AR AR Expresión en superficie - + + Unión a IL12 - - +/- Defectos en señalización completo completo parcial Herencia SUSCEPTIBILIDAD MENDELIANA A INFECCIONES POR MICOBACTERIAS 1996: defectos hereditarios en la inmunidad mediada por IFNγ/L12 susceptibles a infecciones por micobacterias ambientales no tuberculosas o el bacilo de la vacuna BCG. IL-12Rβ1 IL-12p40 IFN-γR1 IFN-γR2 STAT-1 MECANISMO DE DEFENSA CONTRA MICOBACTERIAS: Vía IFN-γ/IL-12 bacteria DCDC-sign r R Toll/CD14 Toll/CD14 IL-12 IFNIFN-α ILIL-12R β1 β2 R de manosa fagosoma muerte bacteriana IFN-γ quemoquinas TNFTNF-α R1 R2 IFNIFN-γR TNFTNF-αR Li Th1/cél. NK FAGOCITO MN TNFTNF-α Deficiencia de IL-12p40 Herencia: AR Ausencia de producción de IL12p70. Infecciones: la mayoría por M bovis BCG y en menor frecuencia Salmonella spp. Evolución clínica: variable, de infección local y curable (n=10) a severa y fatal (n=6). Mayor tasa de muerte (6 de 16) que deficiencia de IL-12Rβ1 (6 de 59). SUSCEPTIBILIDAD MENDELIANA A INFECCIONES POR MICOBACTERIAS 1996: defectos hereditarios en la inmunidad mediada por IFNγ/L12 susceptibles a infecciones por micobacterias ambientales no tuberculosas o el bacilo de la vacuna BCG. IL-12Rβ1 IL-12p40 IFN-γR1 IFN-γR2 STAT-1 MECANISMO DE DEFENSA CONTRA MICOBACTERIAS: Vía IFN-γ/IL-12 bacteria DCDC-sign R Toll/CD14 Toll/CD14 IL-12 IFNIFN-α ILIL-12R R de manosa β1 β2 fagosoma muerte bacteriana IFN-γ quemoquinas TNFTNF-α r R1 R2 IFNIFN-γR TNFTNF-αR Li Th1/cél. NK FAGOCITO MN TNFTNF-α Deficiencia de IFN-γR1/2 Herencia: AR y AD, dependiendo del defecto. Patógenos más frecuentes: BCG, micobacterias ambientales. Deficiencia: - completa fenotipo clínico más severo (comienzo más temprano, mayor número y severidad de infecciones, menor sobrevida). infecciones resistentes a quimioterapia antimicobacteriana intensa. - parcial DP-IFNγR1: mayor frecuencia de osteomielitis por micobacterias con buena respuesta al tratamiento. Receptores mutantes WT IFN-γR1 EC TM IC AR AR AR AD Expresión en superficie - + + +++ Unión a IFNγ - - +/-? + Defectos en señalización completo completo parcial parcial Herencia Receptores mutantes WT IFN-γR2 EC TM IC AR AR Expresión en superficie - + Unión a IFNγ +? + Defectos en señalización completo parcial Herencia SUSCEPTIBILIDAD MENDELIANA A INFECCIONES POR MICOBACTERIAS 1996: defectos hereditarios en la inmunidad mediada por IFNγ/L12 susceptibles a infecciones por micobacterias ambientales no tuberculosas o el bacilo de la vacuna BCG. IFN-γR1 IFN-γR2 IL-12Rβ1 IL-12p40 STAT-1 MECANISMO DE DEFENSA CONTRA MICOBACTERIAS: Vía IFN-γ/IL-12 bacteria DCDC-sign R Toll/CD14 Toll/CD14 IL-12 IFNIFN-α ILIL-12R R de manosa β1 β2 fagosoma muerte bacteriana IFN-γ quemoquinas TNFTNF-α R1 R2 r IFNIFN-γR TNFTNF-αR Li Th1/cél. NK FAGOCITO MN TNFTNF-α Deficiencia de STAT-1 Deficiencia: - completa (2) AR BCGitis diseminada tratada exitosamente con drogas anti-micobacterianas. Muerieron por infección viral severa. - parcial (3) AD Gen IL12B (p40) IL12RB1 (IL12Rβ (IL12Rβ1) Herencia Pacientes reportados N° (%) muertes < 11 años Completo AR 16 5 (31%) Completo AR 58 6 (10%) Parcial AR 1 - Completo AR 26 7 (27%) AR 2 - M bovis BCG (1) Salmonella (1) M tuberculosis (1) AD 46 - MNT (30) M bovis BCG (14) M tuberculosis (1) Salmonella (3) Completo AR 3 - MNT (3) M bovis BCG (1) Parcial AR 1 - M bovis BCG (1) Completo AR 2 2 (100%) inf. viral Parcial AD 3 - Defecto IFNGR1 (IFNγ (IFNγR1) Parcial IFNGR2 (IFNγ (IFNγR2) STAT1 Principales infecciones (n°) M bovis BCG (12) M tuberculosis (1) Salmonella spp (5) M bovis BCG (27) MNT (12) M tuberculosis (3) Salmonella spp (29) M bovis BCG (1) MNT(22) M bovis BCG (11) M tuberculosis (1) Salmonella (1) M bovis BCG (2) Viral (2) M bovis BCG (1) MNT (1) Tratamiento Deficiencia de IL12Rβ1 o IL12p40: quimioterapia ATB intensa a largo plazo, IFNγr dependiendo el caso. Deficiencia parcial de IFNγR: quimioterapia ATB intensa a largo plazo, IFNγr a mayores dosis. Deficiencia completa de refractarias a ATB, TMO. IFNγR: usualmente Deficiencia de STAT-1 parcial: quimioterapia ATB. Deficiencia de STAT-1 completa: quimioterapia ATB. P1 P2 P3 Edad / Sexo 4 años/ fem Presentación Enf. Regional 1 mes 6 meses 3 meses Infección diseminada 8 meses 2 años 17 meses Ganglio regional Ganglio distal Secr. bronquial Biopsia axilar, Lav. gástrico Ganglio distal Aislamiento Biopsia axilar, hemocultivo, coprocultivo Lav. gástrico Ganglio distal 15 años/masc 3 años/ fem Tratamiento Anti TBC IFNγr Anti TBC IFNγr Anti TBC IFNγr Evolución Sin enfermedad Infecció Infección persistente por 13 añ años. Actualmente sin enfermedad Infección persistente Evaluaci ón de ón yy funcionalidad éculas Evaluación de la la expresi expresión funcionalidad de de mol moléculas de ía IFN γ/IL12 por ía de de la la vvía IFNγ/IL12 por citometr citometría de flujo. flujo. ón de γR1 en Expresi Expresión de IFN IFNγR1 en monocitos. monocitos. ón de γ rr en Fosforilaci Fosforilación de STAT1 STAT1 mediada mediada por por IFN IFNγ en monocitos. monocitos. ón de ática en en Producci Producción de IL12 IL12 (p40/p70) (p40/p70) citoplasm citoplasmática monocitos monocitos activados activados con con LPS LPS ee IFN IFN γγ.. ón de 1 del Expresi Expresión de la la cadena cadena ββ1 del receptor receptor de de IL12 IL12 en en CMT CMT activadas activadas con con PHA. PHA. ón de en Fosforilaci Fosforilación de STAT4 STAT4 mediada mediada por por IL12 IL12rr en CMT CMT previamente previamente estimuladas estimuladas con con PHA PHA ee IL2. IL2. Fosforilación de STAT1 mediada por IFNγ r en monocitos Paciente Control Normal 1x106 CMT RPMI 20%SBF IFNγ r (20UI) BASAL ESTIMULADO 10 min, 37°C Lavar Marcación i.c. con mAbs anti-STAT1 Y STAT1-P Análisis por CF en región monocítica Evaluación de la función del Receptor de IFNγ Fosforilación de STAT1 89% M1 Stat1 P basal R1 %Stat 1 P1 P2 P3 N 97 99 89 91 %Stat1P %Stat1P basal estimulada 0 0 0 0 70 90 70 80 Stat1 P est Producción de IL12 (p40/p70) citoplasmática % IL12 (monocitos) P1 P2 P3 N LPS 6 10 5 14 LPS/IFNγγ 12 35 18 33 Expresión de la Cadena β1 Rc. IL12 % Cadena β1 Rc. IL12 PHA PHA+IL2 Paciente %CD25 P1 0% 0% 80% P2 0% 3% 81% P3 0% 0% 81% N 51% 55% 83% paciente 0% normal 0% M1 Cadena β1 Rc IL12 51% 51% M1 Cadena β1 Rc IL12 Fosforilación de STAT4 mediada por IL12r en CMT previamente estimuladas con PHA e IL2. Paciente Control Normal PBS 2%SBF 1x106 CMT PHA IL-2r IFNα IFNαr ILIL-12r 20 min, 37°C Lavar Marcación i.c. con mAbs anti-STAT4 Y STAT4-P Análisis por CF en región linfoide Evaluaci ón de la funcionalidad del receptor de IL12 Evaluación fosforilaci ón de STAT 4 fosforilación paciente STAT 4 STAT 4-P con IL12 STAT 4-P con IFNα α normal 98% 70% M1 M1 34% neg M1 77% M1 80% M1 M1 Paciente 2 RNT PAEG Vacunado al nacer con BCG. 6 meses: BGCitis localizada/regional en brazo derecho. Durante los 2 primeros años: infección pulmonar recurrente. 2 años: aislamiento de M bovis-BCG de esputo y ganglio axilar. Durante los siguientes 13 años: múltiples tratamientos antimicobacterianos. Sin eliminación de la micobacteria ni mejoría clínica. 9 años: HIV (-), IDP(-). 14 años: Se constató deficiencia de IL-12Rβ1 por BM: Q542X, CF: función y expresión de IL-12Rβ1: ausente. 15 años: deterioro clínico importante a pesar de tto. Antimicobacteriano e IFNγr (40 µg/m2) Medición de actividad bactericida/bacteriostática del suero: ausente. Se constata enteropatía perdedora de proteínas y esteatorrea. Aumento de dosis de IFNγr (100 µg/m2) y cambio de antimicobacterianos. + 2 meses de tto.: negativiza el esputo. + 8 meses de tto.: neuropatía óptica y periférica (Estreptomicina, Linezolid). Tto. concluído al año. Profilaxis con acitromicina semanal. + 6 meses de profilaxis: continúa con cultivos (-), lesión torácica resuelta, neuropatía óptica y periférica: recuperación significativa. Inicio de tratamiento 6 meses 4 meses 9 meses GRACIAS POR SU ATENCIÓN!!!