Estereoquimica semestre 2-2012
Anuncio
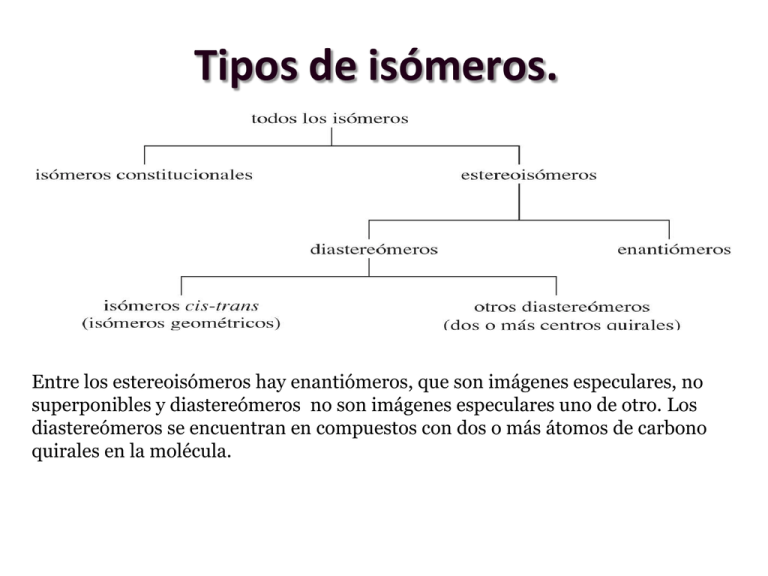
Tipos de isómeros. Entre los estereoisómeros hay enantiómeros, que son imágenes especulares, no superponibles y diastereómeros no son imágenes especulares uno de otro. Los diastereómeros se encuentran en compuestos con dos o más átomos de carbono quirales en la molécula. Moléculas con más de un centro quiral. Si una molécula tiene un único carbono quiral, sólo puede existir un par de enantiómeros. Si tiene dos carbonos quirales tiene un máximo de cuatro estereoisómeros (dos pares de enantiómeros). En general, una molécula con n carbonos quirales tiene un número máximo de 2n estereoisómeros posibles. Por ejemplo, el 3-bromo-2-butanol tiene dos carbonos quirales, por lo tanto, se esperaría 4 estereoisómeros. CH3 OH *CH *CH Br CH3 H HO CH3 H H3C C C C C Br CH3 H H3C (2S, 3R) Br H (2R, 3S) H H HO CH3 H Br OH H3C OH C C C C (2S, 3S) CH3 H3C (2R, 3R) H Br Flechas horizontales: Los estereoisómeros que no enantiómeros son imágenes especulares se denominan DIASTEREOISÓMEROS Flechas verticales y oblicuas: diastereoisómeros Moléculas con más de un centro quiral Una molécula con n estereocentros tiene un máximo de 2n estereoisómeros. Moléculas con más de un centro quiral. Acido 2-amino-3-hidroxibutanoico. Moléculas con más de un centro quiral. 1-bromo-2-chlorocyclopropane Enantiómeros Diasteroisómeros LA FORMA MESO ¿Por qué en el caso del ácido tartárico (ácido 2,3-dihidroxibutanodioico), con dos estereocentros, sólo se producen tres estereoisómeros? (+)-tartaric acid: [α]D = +12º m.p. 170 ºC (–)-tartaric acid: [α]D = –12º m.p. 170 ºC meso-tartaric acid: [α]D = 0º m.p. 140 ºC Compuestos meso. El 2,3-dibromobutano, ejemplo de un compuesto que tiene menos de 2n estereoisómeros, tiene dos carbonos asimétricos, C2 y C3, por lo que la regla 2n predice un máximo de cuatro estereoisómeros. Las cuatro permutaciones de las configuraciones (R) y (S) en C2 y C3 se representan a continuación. Compuestos meso. (+)-tartaric acid: [α]D = +12º m.p. 170 ºC (–)-tartaric acid: [α]D = –12º m.p. 170 ºC meso-tartaric acid: [α]D = 0º m.p. 140 ºC •Una forma meso es un compuesto que contiene dos o más estereocentros y es superponible con su imagen especular. •Los compuesto meso contienen un plano de simetría que divide la molécula en dos, de tal forma que una mitad es la imagen especular de la otra Compuestos meso. Compuestos meso. Ciclohexanos Disustituidos Ciclohexano Disustituidos, Aquirales, 1,1- y cis- 1,3- poseen elemento simetría Plano de simetría (entre C1 y C4) Plano de simetría (entre C2 y C5) Ciclohexanos Disustituidos Ciclohexano Disustituidos, Aquirales, cis y trnas -1,4- hay elemento simetría Plano de simetría (entre C1 y C4) Plano de simetría (entre C1 y C4) Ciclohexanos Disustituidos Ciclohexano disustituidos, Quirales, trans-1,3-sust. no hay elemento simetría No hay Plano de simetría Enantiómeros Compuestos quirales. Ciclohexanos Disustituidos Ciclohexano Disustituido, Quirales, 1,2 - no hay elemento simetría No hay Plano de simetría Enantiómeros Compuestos Aquirales. Ciclohexanos Disustituidos Ciclohexano Disustituido cis-1,2- son Opticamnete inactivo, hay racemización Ciclos Disustituidos Aquirales vs Quirales. Moléculas disimétricas. los términos eritro y treo se utilizan con moléculas disimétricas, cuyos extremos son diferentes Los términos meso y (+), (-), o (d),(l) se suelen utilizar con moléculas que poseen extremos iguales. Otros sistemas de Nomenclatura. Configuraciones D y L de los azúcares (R) (S) D y L son enantiómeros. La familia D de las aldosas Todos estos azúcares son naturales, excepto la treosa, lixoxa, alosa y gulosa. Clasificación de los monosacáridos • • A los azúcares con un grupo aldehído se les denomina aldosas y a los que tienen un grupo cetona, cetosas. La mayor parte de las cetosas tienen el grupo centona en C2, segundo átomo de carbono de la cadena. Clasificación de los monosacáridos Un azúcar generalmente tienen entre tres y siete átomos de carbono, denominándose triosa (tres carbonos), tetrosa (cuatro carbonos), pentosa (cinco carbonos), hexosa (seis carbonos) y heptosa (siete carbonos). Epímeros. Los azúcares que sólo difieren en la estereoquímica de un carbono se denominan epímeros y el átomo de carbono cuya configuración es opuesta generalmente se especifica. Si no se especifica el número de carbonos, se asume que es un C2. Conformaciones de la glucosa. La glucosa se presenta, casi completamente, en la forma hemiacetálica cíclica. La proyección de Haworth se utiliza mucho para representar los hemiacetales, aunque puede dar la impresión de que el anillo es plano. La conformación de silla es más real Anómeros de la glucosa En el anómero α, el grupo hidroxilo del carbono anomérico (hemiacetal) está hacia abajo (axial) y en el anómero β hacia arriba (ecuatorial). El anómero β de la glucosa tiene todos sus sustituyentes en posiciones ecuatoriales. El carbono hemiacetal se denomina carbono anomérico, que se identifica con facilidad como el único átomo de carbono unido a dos oxígenos. Mutarrotación. Una solución acuosa de D-glucosa contiene una mezcla en equilibrio de α-D-glucopiranosa, β-D-glucopiranosa, y un intermedio de cadena abierta. La cristalización por debajo de 98°C da el anómero alfa y la cristalización por encima de 98°C da el anómero beta. Repulsión eletrostática Otros Elementos Quirales. Aquiralidad debido a la inversión del Nitrógeno sp3 Al contrario que las aminas, las sales de amonio cuaternario, con cuatro sustituyentes distintos sobre el átomo de nitrógeno, no pueden interconvertirse y por tanto son ópticamente activas.