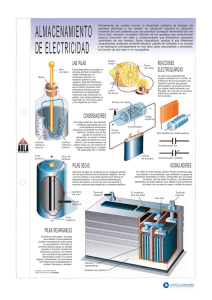
Los procesos redox en la vida cotidiana
Anuncio

Grupo Lentiscal Comentarios de textos redox COMENTARIO DE TEXTO Los tests de alcoholemia Las pruebas que realiza la policía de tráfico para detectar el posible consumo de alcohol etílico (etanol, CH3-CH2OH) por parte de los conductores, y en las que éstos deben soplar a través de un tubo que contiene pequeños cristales de color anaranjado que se vuelven verdes en caso de que la prueba resulte positiva, se basan en una reacción redox. Los cristales anaranjados del tubo son de dicromato de potasio, que oxida a etanal (CH3CHO) los vapores de etanol posiblemente contenidos en el aire espirado, reduciéndose él a una sal de cromo (III), de color verde. La reacción que tiene lugar es: K2Cr2O7 + 3 CH3-CH2OH+ 5 H2SO4 3 CH3-CHO + Cr2 (SO4)3 + 2 KHSO4+ 7 H2O (Anaranjado) (Verde) GUÍA DE LECTURA: 1. Explica en que consiste el test de alcoholemia. 2. ¿Qué sustancia es la oxidante y la reductora en dicho proceso? 3. ¿Cuáles son los pequeños cristales de color anaranjado? ¿Qué sustancia es la que se pone verde? 1 Grupo Lentiscal Comentarios de textos redox COMENTARIO DE TEXTO: OXIDACIÓN REDUCCIÓN ANTISÉPTICOS, BLANQUEADORES Y QUITAMANCHAS Muchos antisépticos de uso común (compuestos que se utilizan para destruir microorganismos o prevenir su crecimiento) son agentes oxidantes suaves. El peróxido de hidrógeno (H2O2), en disolución acuosa al 3%, se usa en medicina como antiséptico. El hipoclorito de sodio (NaCIO), disponible en el comercio en disolución acuosa para blanquear la ropa, se emplea como desinfectante y desodorante. Las disoluciones de ioduro se utilizan como antisépticos. El peróxido de benzoilo (C6H5COO)2O2 agente oxidante poderoso, se usó ampliamente al 5 y 10% en la preparación de cremas para tratamientos del acné. El Ca(CIO)2 se utiliza como desinfectante de la ropa y el cloro, como desinfectante del agua para beber. Las aguas residuales se tratan con cloro antes de ser devueltas a los ríos o lagos. Las piscinas se desinfectan generalmente por cloración que puede acidificar demasiado el agua por lo que debe reajustarse el pH añadiéndose Na2CO3. Las piscinas pequeñas se suelen clorar con Ca(CIO)2, esto puede provocar un exceso de basicidad del agua, en este caso debe reajustarse el pH añadiendo HCI. Los blanqueadores (compuestos que vuelven blancos los tejidos y otros materiales) son agentes oxidantes o reductores, los más familiares son el NaCIO y Ca(CIO)2. Otra sustancia blanqueante muy útil es el SO2, gas incoloro, tóxico y de olor sofocante. Diversos compuestos presentes en la lana, seda y papel se transforman en especies incoloras cuando son reducidas por el SO2. Estos compuestos reducidos (incoloros) pueden ser reoxidados para dar de nuevo los compuestos originales coloreados. El papel de periódico (hecho con pulpa de madera blanqueada) cuando se expone al Sol se oxida tomando un color amarillo. Algunos quitamanchas son también agentes oxidantes o reductores. El peróxido de hidrógeno en agua caliente quita las manchas de sangre en tejidos de algodón y lino. El permanganato de potasio elimina las manchas de tejidos blancos (excepto el rayón), y a su vez la mancha de permanganato se quita con ácido oxálico: 5 H2C2O4 + 2 MnO4- + 6 H+ Ö 10 CO2 + 2 Mn2+ + 8 H2O. GUÍA DE LECTURA: A.1 Realiza una lista de las sustancias oxidantes y reductoras de uso domestico que se utilizan en le hogar, señalando su principal utilización PAREJAS DE SUSTANCIAS DE LIMPIEZA QUE NUNCA DEBEN MEZCLARSE. La reacción del amoniaco con el hipoclorito presente en la lejía produce un gas muy tóxico, la cloroamina, [ClNH2(g):] NH3(aq) + ClO-(aq) Ö NH2Cl(g) + OH-(aq) Por otro lado, cuando el salfumant (ácido clorhídrico) se mezcla con lejía, se produce cloro, un gas muy venenoso: H+ (aq) + Cl- (aq) + ClO- (aq) Ö Cl2(g) + H2O(l) GUÍA DE LECTURA: A.1 Identifica los cambios en el número de oxidación que tienen lugar en cada uno de los procesos. 2 Grupo Lentiscal Comentarios de textos redox RESTAURACIÓN DE PINTURAS En las pinturas se utilizaban antiguamente pigmentos blancos que contenían compuestos de plomo. Estos pigmentos, con el paso del tiempo, experimentan la acción del sulfuro de hidrógeno existente en el aire, formándose monosulfuro de plomo, de color negro, con lo que la pintura pierde una gran parte de su estética original. La restauración del color blanco primitivo puede conseguirse por medio de una disolución de agua oxigenada, H2O2, que oxida el monosulfuro de plomo a sulfato de plomo (II), de color blanco: PbS + 4H2O2 PbSO4 + 4H2O En la actualidad, debido a su carácter venenoso, el uso de pigmentos de plomo en pinturas ha sido bastante restringido. GUÍA DE LECTURA: A.1 Explica cómo consigue el agua oxigenada restaurar las pinturas a su color blando original eliminado su color ennegrecido. COMENTARIO DE TEXTO “COMENTARIO DE TEXTO 2 TIPOS DE PILAS Las pilas alcalinas de "alta potencia" y larga vida son similares a la de Leclanché, pero en vez de cloruro de amonio llevan cloruro sódico o potásico. Duran más porque el cinc no está expuesto a un ambiente ácido como el que provocan los iones NH4+. Como los iones se mueven más fácilmente a través del electrólito, producen más potencia y una corriente más estable. Su mayor coste se deriva de la dificultad de sellar las pilas contra la fuga del hidróxido. Otra pila importante, aunque es más cara, es la de mercurio. Tiene múltiples aplicaciones, por ejemplo, en relojes y cámaras. El ánodo es de cinc, pero el cátodo es acero en contacto con una mezcla de óxido de mercurio (II), hidróxido de potasio e hidróxido de cinc. La ventaja de esta pila es que puede fabricarse en tamaños muy pequeños con un voltaje estable durante períodos largos (1,3 V). Las pilas de combustible son aquéllas en que los reactivos se suministran de forma continua a los electrodos. Las anguilas eléctricas son pilas de combustibles naturales. Generan su carga eléctrica en un "órgano eléctrico" una batería de pilas electroquímicas biológicas alimentadas con comida, que produce cada una unos 0,15 V. La cabeza de la anguila es un cátodo y la cola un ánodo. La mayoría de las pilas de uso doméstico contienen materiales contaminantes, como el mercurio, cadmio, plomo o litio, muy perjudiciales para la salud y el medio ambiente. Cuando se tira una pila a un basurero, estos metales, en especial el mercurio, se incorporan al ciclo del agua, a través de las lluvias o el gas producido en las incineradoras. Alrededor de 310 millones de pilas se utilizan anualmente en España, lo que significa 7,7 Tm de Hg y 0,92 Tm de Cd en los basureros. GUÍA DE LECTURA: 1. ¿Cómo se podría contribuir a la disminución de la contaminación generada por la utilización de las pilas? 3 Grupo Lentiscal Comentarios de textos redox COMENTARIO DE TEXTO “PROTECCIÓN FRENTE A LA CORROSIÓN La protección de los objetos metálicos frente a la corrosión se basa en evitar el contacto con el aire y el agua, lo que se consigue recubriendo la superficie con una capa protectora. Así, las puertas y ventanas de hierro suelen recubrirse de una sustancia de color naranja conocida como "minio" que es el óxido de plomo Pb3O4. También se puede recubrir la superficie del hierro o acero con una lámina de otro metal aplicada eléctricamente (galvanizado) o por inmersión a altas temperaturas. Los coches se recubren con una capa continua de cinc a través de un proceso de inmersión en el cinc fundido. Otra forma de evitar la corrosión es poner el objeto de hierro en contacto eléctrico con un metal más fácilmente oxidable (Mg o Zn). En estas condiciones, el hierro hace de cátodo y, por tanto, queda protegido contra la corrosión. Por ejemplo, si se conecta una barra de cinc a una conducción de acero será el cinc el que se oxide. El metal más fácilmente oxidable se denomina ánodo de sacrificio. Este procedimiento, es conocido como protección catódica y se utiliza para proteger objetos de acero tales como cables oleoductos, que están enterrados en el suelo o bajo el agua. También se emplea para proteger barcos y puentes, en estos casos se conecta un bloque de metal (como magnesio o cinc) a la estructura a proteger. De esta forma se consigue que sea el bloque, y no la estructura, quien ceda los electrones que necesita el oxígeno. El bloque (ánodo de sacrificio) se oxida, pero es mucho más barato de reemplazar que la estructura que protege. Protección catódica. Ánodo de magnesio: Mg Ö Mg2+ + 2eConducción de hierro: (cátodo) GUÍA DE LECTURA: 1. Se dispone de dos vasos con agua caliente que contienen unas gotas de fenolftaleína. Introducir un clavo de hierro en uno de ellos. Arrollar una cinta de magnesio a un clavo de hierro y colocarlo en el otro vaso. Observar el comportamiento del clavo en ambos casos y extraer conclusiones. 2. Explicar por qué la corrosión suele producirse de forma más rápida en el agua del mar que en agua dulce. 3. ¿Cuál de los siguientes metales podrían emplearse para proteger galvánicamente al hierro de la corrosión: cobre, níquel, magnesio, estaño, berilio, oro, platino, cinc y plomo’ [Se pueden emplear aquellos metales más activos que el hierro; es decir aquellos que posean un potencial de reducción mayor que él. Esto es: Mg, Be y Zn.] 4 Grupo Lentiscal Comentarios de textos redox COMENTARIO DE TEXTO “L A CONSERVACIÓN DE LAS CARNES El nitrito y nitrato de sodio se han utilizado desde hace tiempo para conservar carnes. La carne se oscurece cuando se almacena debido a la oxidación de la sangre. Ambas sales se reducen a NO por acción de algunos de los componentes de la carne. El NO se combina con la hemoglobina y retrasa su oxidación. De esta forma, la carne mantiene su apariencia fresca y un color rojo. Además, los nitratos también se añaden a las conservas para evitar el crecimiento de una bacteria que produce botulismo, una variedad peligrosa de envenenamiento de alimentos. Sin embargo, en los últimos años existe una cierta preocupación ante la posibilidad de que los nitritos reaccionen con ciertos compuestos de la carne formando nitrosaminas, compuestos altamente cancerígenos. Por otro lado, la presencia de nitritos conduce a la oxidación de la hemoglobina (Hb-Fe2+) a la metahemoglobina (Hb-Fe3+) de color marrón, que ya no es transportadora de O 2, originando la enfermedad llamada metahemoglobinemia. GUÍA DE LECTURA: 1. Realiza una lectura del y realiza un resumen del mismo. 2. Explica como actúan el nitrito y o el nitrato de sodio como conservantes de las canes. 3. Señala algunos peligros de añadirle a la carne nitritos o nitratos para su conservación. 5