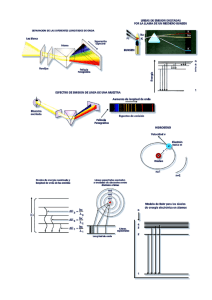
TEMA 6
Anuncio

REACCIONES CONCERTADAS: Transcurren en una única etapa elemental sin intermedios intermedios. REACCIONES PERICÍCLICAS: -Concertadas - Reorganización concertada de los enlaces a través de un estado de transición cíclico con escasa polarización - Controladas por la simetría y energía de orbitales (R l d (Reglas de Woodward-Hoffmann) W d d H ff ) -Controladas también por otros factores: Tensión angular Efectos estéricos Efectos de entropía - Presentan características estereoquímicas definidas 1 REACCIONES PERICICLICAS: 2 ESTRUCTURA Y ENLACE DESCRIPCIÓN DEL ENLACE Y DE LA ESTRUCTURA Ecuación de Schroedinger: H = E TEORÍA DEL ENLACE DE VALENCIA -Considera los enlaces formados p por p parejas j de electrones entre átomos. - Los electrones se encuentran asociados a orbitales atómicos en la moléculas. - Hibridación -Resonancia TEORÍA DE ORBITALES MOLECULARES - Considera los electrones situados en orbitales moleculares que se extienden por toda la molécula. - Combinación lineal de orbitales atómicos. - Métodos semi-empírics - Métodos Ab Initio 3 TEORIA DE ORBITALES MOLECULARES Matemáticamente la función de onda del orbital molecular (OM) se aproxima a una combinación lineal de la función f de onda de orbitales atómicos (OA). (O ) = c11+ c22+ C33+ ………..cnn En realidad existen tantos OM como OA se combinan: 1 = c1,11+ c1,22+ ………..c1,nn 2 = c2,11+ c2,22+ ………..c2,nn n i = ci,,j j j n = cn,11+ cn,22+ ………..cn,nn Los valores de ci,j no se conocen. Lo que se hace es partir de unos valores iniciales y se van modificando hasta encontrar aquellos valores de ci,j que minimizan la energía del orbital 4 TEORIA DE ORBITALES MOLECULARES 2 H = E2, E = (∫ H d)/ (∫ 2 d) La condición de mínimo de energía es: E/ ci = 0, La resolución de esta ecuación se hace por diferentes métodos (semiempíricos y Ab initio). Los resultados son ci,j y E. 2 indica i di lla probabilidad b bilid d d de encontrar t un electrón l tó d dell orbital bit l en un punto t determinado del espacio. E es la energía del orbital Los coeficientes ci,j dan la densidad electrónica sobre cada átomo: qr = nj c2j,r nj es el número de electrones en el orbital j y cj,r el coeficiente en el átomo r para cada orbital j 5 TEORÍA DE ORBITALES MOLECULARES (APLICACIÓN CUALITATIVA) DIAGRAMAS DE INTERACCIÓN DE ORBITALES El procedimiento por el que se obtienen las funciones de onda de un conjunto de OM a partir de un conjunto de OA es un proceso esencialmente matemático matemático. No obstante obstante, este proceso proceso, al menos para moléculas pequeñas puede hacerse de manera cualitativa sin necesidad de ningún input matemático. La herramienta gráfica por la que es posible construir OMs a partir de OAs (o de otros OM sencillos) son los diagramas de interacción de orbitales. Esta interacción está controlada por la simetría de los orbitales. orbitales Consideraciones sobre la simetría de los orbitales: 1. La simetría de un orbital depende no sólo de su forma sino también de la fase. Orbitales simétricos y antisimètricos (respecto a un elemento de simetría, C, σ, i) El orbital p es simétrico respecto σv y antisimétrico respecto σh 6 TEORÍA DE ORBITALES MOLECULARES (APLICACIÓN CUALITATIVA) DIAGRAMAS DE INTERACCIÓN DE ORBITALES Consideraciones sobre la simetría de los orbitales (2): 2. El solapamiento entre orbitales puede ser positivo (idéntica fase) o negativo (diferente fase). 3. El solapamiento entre orbitales sólo es efectivo si tienen la misma simetría (simétricos o antisimétricos) respecto a todos los elementos de simetría compartidos del sistema. La falta de concordancia respecto a un elemento resulta en un solapamiento cero. cero 7 TEORÍA DE ORBITALES MOLECULARES (APLICACIÓN CUALITATIVA) CONSTRUCCIÓN DE DIAGRAMAS DE INTERACCIÓN DE ORBITALES 1. El número de OM es igual al número de OA del conjunto a partir del cual se forman. 2. La interacción entre dos OA a y b da lugar a dos OMs: OM, el orbital enlazante (solapamiento en fase), y *OM, el orbital antienlazante (solapamiento fuera de fase). 3. El orbital enlazante es de energía inferior a los dos OA de los que deriva 4. El orbital antienlazante es de energía superior a los dos OA de los que deriva 5. Simplificación de Hückel (sistemas ): En sistemas planos el sistema de enlaces puede ser tratado independientemente del sistema de enlaces . El sistema propiedades químicas y espectroscópicas determina las 8 TEORÍA DE ORBITALES MOLECULARES (APLICACIÓN CUALITATIVA) CONSTRUCCIÓN DE DIAGRAMAS DE INTERACCIÓN DE ORBITALES Interacción entre dos OA degenerados: 1. La interacción entre dos OA a y b da lugar a dos OMs: OM, el orbital enlazante (solapamiento en fase), y *OM, el orbital antienlazante (solapamiento fuera de fase). 2. Las contribuciones de cada OA en los OM son idénticas (coeficientes orbitálicos idénticos). Los coeficientes son representados por el tamaño y la fase por el color (o signo) signo). 3. La energía de estabilización del orbital enlazante es igual a la energía de desestabilización del orbital antienlazante. 9 TEORÍA DE ORBITALES MOLECULARES (APLICACIÓN CUALITATIVA) CONSTRUCCIÓN Ó DE DIAGRAMAS DE INTERACCIÓN Ó DE ORBITALES Efecto de la ocupación electrónica: Les propiedades químicas del sistema dependen del número de electrones que ocupa el conjunto de OMs generado. El sistema con 1 electrón se ejemplifica con la especie+. El electrón ocupa 1 OM de baja energía, el enlace es relativamente débil y esto se refleja en una longitud de enlace relativamente larga (1.06 A). La introducción de un electrón adicional ((H2) tiene lugar g en el mismo OM enlazante provocando un incremento en la fuerza del enlace y una disminución en la longitud. La introducción de un tercer electrón (He2+) disminuye la fuerza del enlace ya que el electrón ocupa un orbital antienlazante de mayor energía que el OA. La introducción de un cuarto electrón conduce a una situación no enlazante ya que los dos electrones en OM antienlazantes anulan la estabilización debida a los dos electrones en el OM enlazante. enlazante 10 TEORÍA DE ORBITALES MOLECULARES (APLICACIÓN CUALITATIVA) CONSTRUCCIÓN DE DIAGRAMAS DE INTERACCIÓN DE ORBITALES Interacción entre dos OA no degenerados: 1. La interacción entre dos OA a y b da lugar a dos OMs: OM, el orbital enlazante (solapamiento en fase), y *OM, el orbital antienlazante (solapamiento fuera de fase). 2. Las contribuciones de cada OA en los OM son diferentes (coeficientes orbitálicos diferentes): El OM enlazante tiene mayor contribución del OA de menor energía y el OM antienlazante tiene mayor contribución del OA de mayor energía. 3. La energía del OM enlazante es próxima a la energía del OA de menor energía y la energía del OM antienlazante es próxima a la del OA de mayor energía 11 TEORÍA DE ORBITALES MOLECULARES (APLICACIÓN CUALITATIVA) CONSTRUCCIÓN DE DIAGRAMAS DE INTERACCIÓN DE ORBITALES ETILENO - Aplicamos la simplificación de Hückel El sistema del etileno se construye a partir de dos orbitales 2p de carbono. La combinación en fase conduce al orbital de baja energía (enlazante). La combinación fuera de fase conduce al orbital * de alta energía (antienlazante). Los dos electrones que inicialmente ocupan los OA se sitúan en el OM 12 TEORÍA DE ORBITALES MOLECULARES (APLICACIÓN CUALITATIVA) CONSTRUCCIÓN DE DIAGRAMAS DE INTERACCIÓN DE ORBITALES ALILO - Combinamos C bi 3 orbitales bi l p, resultan l 3 OM OM: 1 1 ((enlazante l sin i ningún i ú nodo), d ) 2 2 ((no enlazante l con un nodo) y 3 (antienlazante con dos nodos) 13 TEORÍA DE ORBITALES MOLECULARES (APLICACIÓN CUALITATIVA) CONSTRUCCIÓN DE DIAGRAMAS DE INTERACCIÓN DE ORBITALES 1. El orbital n tiene (n-1) nodos distribuidos alrededor de un punto central 2. Los orbitales son alternativamente simétricos y antisimétricos respecte un plano de simetría que contiene al punto central 3. Los orbitales son alternativamente antisimétricos y simétricos respecte a un eje de simetría binario que pasa por el punto central 14 TEORÍA DE ORBITALES MOLECULARES (APLICACIÓN CUALITATIVA) CONSTRUCCIÓN DE DIAGRAMAS DE INTERACCIÓN DE ORBITALES En sistemas con un número impar de átomos, el análisis anterior también es válido, pero existen OM no enlazantes que poseen nodos sobre alguno de los átomos. 15 TEORÍA DE ORBITALES MOLECULARES (APLICACIÓN CUALITATIVA) TEORÍA DE PERTURBACIONES Análisis de los OM en moléculas que interaccionan durante una reacción química. - Los OM de las dos especies reaccionantes se perturban mutuamente hasta convertirse en OM de una nueva especie química. - Orbitales frontera: Las interacciones más importantes se producen entre dos orbitales particulares, normalmente próximos en energía. HOMO (orbital ocupado de mayor energía) LUMO (orbital desocupado de menor energía) - Sólo orbitales que coinciden en simetría pueden interaccionar para formar p un enlace. La falta de concordancia en simetría resulta en un solapamiento cero. - Coeficientes: El solapamiento más fuerte se produce si los dos OM que grandes en los átomos entre los q que se interaccionan tienen coeficientes g forma el enlace. 16 TEORÍA DE ORBITALES MOLECULARES (APLICACIÓN CUALITATIVA) TEORÍA DE PERTURBACIONES Comparación de la reactividad entre etileno y formaldehído H2C CH2 En el etileno los coeficientes en los dos carbonos son iguales (sistema degenerado) H2C O En el formaldehido los coeficientes son diferentes: dif t LUMO -El orbital tiene mayor contribución del orbital p (O) HOMO LUMO HOMO -El El orbital bit l ** ti tiene mayor contribución del orbital p (C) La energía de los orbitales en el formaldehído es más baja j q que en el etileno debido a la presencia del oxígeno, electronegativo. 17 TEORÍA DE ORBITALES MOLECULARES (APLICACIÓN CUALITATIVA) TEORÍA DE PERTURBACIONES Comparación de la reactividad entre etileno y formaldehído (Interacción con un electrófilo) H2C CH2 E+ H2C O LUMO HOMO E1 E1 > E2 HOMO E2 La interacció principal es entre el LUMO del electrófilo y el HOMO del nucleòfilo. La energía del LUMO (E) es más baja que en el HOMO (etileno) pero mucho más alta que la del HOMO ((formaldehído). q ) La interacción es estabilizadora en la interacción Eetileno. En cambio, en la interacción E-formaldehído, la energía del orbital perturbado es casi igual a la del HOMO (formaldehído) y la interacción es poco 18 estabilizante. TEORÍA DE ORBITALES MOLECULARES (APLICACIÓN CUALITATIVA) TEORÍA DE PERTURBACIONES Comparación de la reactividad entre etileno y formaldehído (Interacción con un nucleófilo) H2C CH2 NuH2C O LUMO HOMO LUMO HOMO E1 E2 E1 < E2 HOMO La iinteracción L t ió principal i i l es entre t ell HOMO d dell nucleófilo l ófil y ell LUMO d dell electrófilo. l t ófil L La energía del LUMO (etileno) es mucho más alta que la del HOMO (Nu). El orbital perturbado tiene una energía muy próxima a la del HOMO (Nu) y apenas hay estabilización. Una p posible interacción HOMO(etileno)-HOMO(Nu) ( ) ( ) resultaría en una estabilización nula. La interacción entre el HOMO (Nu) y el LUMO (formaldehído) es 19 estabilizante. Además el nucleófilo ataca al carbono que es el átomo de mayor coeficiente en el LUMO. REACCIONES ELECTROCÍCLICAS -Formación de un enlace entre los extremos de un sistema lineal de electrones y también el proceso inverso (apertura del anillo). Isomerización ciclobuteno-butadieno (reacción térmica) -Energía de activación 30-35 Kcal/mol - La reacción está favorecida termodinámicamente en el sentido de apertura del anillo debido a la elevada tensión del anillo de ciclobuteno ciclobuteno. - Reacción altamente estereoespecífica: Los grupos unidos al enlace que se rompe (o los grupos en los extremos del sistema durante el proceso de ciclación) giran todos en el mismo sentido durante la reacción (PROCESO CONROTATORIO) H H Me calor Me Me pero no ni Me Me Me Me Me H H calor M Me pero no Me Me ni Me Me Me Me Me 20 REACCIONES ELECTROCÍCLICAS Isomerización entre 1,3,5-trienos y 1,3-ciclohexadienos (reacción térmica) -El cierre del anillo es normalmente la reacción favorecida termodinamicamente, debido a la mayor estabilidad del compuesto cíclico con 6 enlaces y dos enlaces frente a los 5 enlaces y 3 enlaces del compuesto acíclico - Reacción altamente estereoespecífica: Los grupos unidos al enlace que se rompe (o los grupos en los extremos del sistema durante el proceso de ciclación) giran en sentidos opuestos (PROCESO DISROTATORIO) 21 REACCIONES ELECTROCÍCLICAS La estereoquímica del proceso puede cambiar si la reacción se hace irradiando con luz (reacción fotoquímica) en vez de utilizando calor (reacción térmica). Por ejemplo: Reacción térmica: Proceso disrotatorio Reacción fotoquímica: Proceso conrotatorio 22 REACCIONES ELECTROCÍCLICAS Orbitales frontera: El argumento más sencillo considera exclusivamente el control de la reacción por parte del HOMO (Woodward y Hoffman) 23 REACCIONES ELECTROCÍCLICAS Orbitales frontera: El HOMO controla la reacción Isomerización entre 1,3,5-trienos y 1,3-ciclohexadienos (reacción térmica y fotoquímica) 24 REACCIONES ELECTROCÍCLICAS Reglas: Proceso térmico: Número de electrones = 4n + 2 Número de electrones = 4n proceso disrotatorio proceso conrotatorio Proceso fotoquímico Número de electrones = 4n + 2 Número de electrones = 4n proceso conrotatori p proceso disrotatorio 25 REACCIONES ELECTROCÍCLICAS Ejemplos: Síntesis y estabilidad del benceno de Dewar. El derivado del benceno de Dewar es estable. La estabilidad se atribuyó inicialmente a la presencia de los grupos terc-Bu. El benceno de Dewar no sustituido también es b t t estable bastante t bl (2 dí días a 25 °C). °C) H# = 25 Kcal/mol La descomposición térmica del benceno de Dewar es un proceso conrotatorio que no conduce inicialmente a benceno sino a un hexatrieno muy tensionado 26 REACCIONES ELECTROCÍCLICAS Ejemplos: Muy favorecida desde el punto de vista entrópico ya que los extremos del sistema se encuentran muy próximos. La reacción transcurre a T ambiente. conrot disrot Isomerización de 2,4,6,8decatetraenos 27 REACCIONES ELECTROCÍCLICAS Especies cargadas cargadas. Ejemplos: Les regles de Woodward y Hoffmann también se aplican a sistemas cargados. La conversión de un catión ciclopropílico en un catión alílico es un proceso electrocíclico con 2 electrones (4n +2), se trata por tanto de un proceso disrotatorio. La formación del catión es la etapa lenta (debido a la elevada tensión angular del catión resultante). En cis-dimetilciclopropanos p p la apertura p del anillo favorece la formación del catión en forma de W per razones estéricas. 28 REACCIONES ELECTROCÍCLICAS Especies cargadas cargadas. Conversión de un catión ciclopropílico en un catión alílico (cont). (cont) La velocidad de solvólisis depende de la sustitución y la estereoquímica del sustrato Esto se explica considerando que el proceso de ionización (formación del catión ciclopropilo) y la apertura del anillo ocurren de manera casi concertada. Los electrones del enlace C2-C3 se mueven hacia la cara opuesta al enlace C-OTs, asistiendo la ruptura de este enlace enlace. 29 REACCIONES ELECTROCÍCLICAS Especies cargadas cargadas. Otros ejemplos conrotatorio disrotatorio 30 TRANSPOSICIONES SIGMATRÓPICAS Implican una reorganización concertada de electrones π durante la cual un grupo unido por un enlace σ migra al extremo más distante del sistema π. Se clasifican según el número de átomos participantes en el fragmento que migra y en el sistema π. 31 TRANSPOSICIONES SIGMATRÓPICAS Reglas de selección: La migración de hidrógeno entre los extremos de un sistema alílico es el ejemplo más sencillo de transposición [1,3]. Desde el punto de vista estereoquímico existen dos posibles caminos, un de los cuales no está permitido por la simetría de los orbitales. Migración suprafacial: La ruptura y formación de los enlaces tienen lugar por la misma cara del plano que contiene al sistema Migración antarafacial: La ruptura p y formación de los enlaces tienen lugar por caras opuestas del plano que contiene al sistema 32 TRANSPOSICIONES SIGMATRÓPICAS Reglas de selección: migración [1,3] de hidrógeno (Proceso térmico) La migración [1,3] suprafacial de hidrógeno no está permitida por simetría de los orbitales. La migración [1 [1,3] 3] antarafacial si que lo está está, pero no se puede dar porque el protón no es suficientemente voluminoso para experimentar el proceso. NO HAY MIGRACIONES [1,3] DE HIDRÓGENO TÉRMICAS ¡¡¡¡¡ POM: Como modelo utilizamos el sistema formado por un protón (0 e, s, LUMO) y un 33 anión alilo (4e, 2, HOMO). TRANSPOSICIONES SIGMATRÓPICAS Reglas g de selección: migración g [1,3] [ ] de hidrógeno g ((Proceso fotoquímico) q ) Como es habitual, las reglas de selección se invierten al pasar del estado fundamental al estado excitado como ocurre en los procesos fotoquímicos.(el HOMO en el anión alilo ahora es el orbital 3). En procesos fotoquímicos la migración suprafacial está permitida por simetría y la antarafacial no llum HO D H D HO Migració [1,3] d'hidrogen suprafacial f i l 34 TRANSPOSICIONES SIGMATRÓPICAS Reglas g de selección: migración g [1,5] [ ] de hidrógeno g ((Proceso térmico)) Si extendemos el sistema con un doble enlace adicional también se produce un cambio en las reglas de selección. La migración [1,5] de hidrógeno suprafacial está permitida La migración [1 [1,5] 5] de hidrógeno antarafacial no está permitida 35 TRANSPOSICIONES SIGMATRÓPICAS Estereoquímica q del proceso p de migración g [1,5] [ ] de hidrógeno g ((Proceso térmico). ) Únicamente se observan los productos del proceso suprafacial. El producto mayoritario se forma a través de la conformación que sitúa el grupo Et hacia afuera, lejos del doble enlace. (Roth et al.) Estereoquímica de los productos esperados para un proceso antarafacial. (La formación de estos productos no se observa) 36 TRANSPOSICIONES SIGMATRÓPICAS Migración g [1,7] [ ] de hidrógeno g ((Proceso térmico). ) Proceso antarafacial. Ejemplos j p en vitamina D y análogos Prueba experimental para un proceso antarafacial en un análogo de la vitamina D 37 TRANSPOSICIONES SIGMATRÓPICAS Migración g [1,3] [ ] de carbono ((Proceso térmico). ) Cuando el g grupo p q que migra g es un g grupo p alquilo hay que considerar una característica estereoquímica adicional: La migración puede ocurrir con retención o inversión en la configuración del carbono que migra. Reglas de selección (proceso suprafacial): 3 sistema p alquilo 2 alílo p alquilo 1,3-suprafacial retenció (prohibit)) (p 1,3-suprafacial inversió (permés) 1,5-suprafacial retenció (permés) 1,5-suprafacial inversió (prohibit) 38 TRANSPOSICIONES SIGMATRÓPICAS Migración [1,3] i [1,5] de grupo alquilo (ejemplos). [1,3] suprafacial con inversión [1,3] [1 3] suprafacial con inversión [1,5] suprafacial con retención 39 TRANSPOSICIONES SIGMATRÓPICAS Transposición de Cope: Es la interconversión entre dos sistemas de 1,5-hexadieno Reglas de selección (proceso térmico): Hay que considerar la estereoquímica en los d ffragmento. dos t Existen E i t tres t posibilidades: ibilid d ((consideremos id lla iinteracción t ió entre t d dos orbitales bit l 2) Supra-supra permitido Antara-antara. Aunque q permitido por simetría orbitálica, el ET tiene una tensión muy alta y es menos probable que el proceso supra-supra 40 TRANSPOSICIONES SIGMATRÓPICAS Transposición de Cope Reglas de selección (proceso térmico, continuación) Supra-antara no permitido por simetría Reglas de selección (proceso fotoquímico): Se produce una inversión de las reglas como es habitual. (consideremos la interacción entre un orbital 2 i 3) Supra-antara permitido por simetría p 41 TRANSPOSICIONES SIGMATRÓPICAS Resumen reglas de selección para procesos sigmatròpicos térmicos 42 TRANSPOSICIONES SIGMATRÓPICAS [3,3] Transposición de Cope: La reacción es estereoespecífica y estereoselectiva. estereoselectiva El requerimiento supra-supra debido a la simetría de los orbitales hace que la reacción transcurra a través de un estado de transición en forma de silla de ciclohexano (al igual que todas las transposiciones [3,3]) favorable E,E mayor E,Z iguales desfavorable dl-estereoisómero Z,Z minor EZ E,Z meso-estereoisómero 43 TRANSPOSICIONES SIGMATRÓPICAS [3,3] Transposición de Cope (ejemplos): La transposición de Cope es un proceso reversible reversible. La posición final del equilibrio depende de la estabilidad relativa de los productos inicial y final. 44 TRANSPOSICIONES SIGMATRÓPICAS [3,3] Transposición de oxi oxi-Cope Cope y oxi oxi-Cope Cope aniónica (ejemplos): Si en la posición 3 del hexadieno hay un grupo hidroxilo, el producto resultante de la transposición es un enol que tautomeriza rápidamente al correspondiente compuesto carbonílico 5,6-insaturado y desplaza el equilibrio. La reacción transcurre en condiciones más suaves en medio básico (reacción aniónica) HO HO 2 O 3 6 4 5 La velocidad de la reacción de oxi-Cope aniónica depende del grado de coordinación del catión tió con ell alcóxido. l ó id Bu4N+> K+>Na+>Li+ 45 TRANSPOSICIONES SIGMATRÓPICAS [3,3] Transposición de Claisen: Es la transposición de un éter alil vinílico o alil fenólico fenólico. El producto resultante es un compuesto carbonílico 4,5-insaturado. La reacción suele estar favorecida en el sentido de formación del compuesto carbonílico. O 2 O 5 OH O O 3 4 CHO 195 oC 87% O OH (H3C)2C CH CH2 + H2C CH3 OCH3 H+ 125 oC H3 C O CH2 (H3C)2C CH CH2 (H3C)2C CH CH2CH2COCH3 94% 46 TRANSPOSICIONES SIGMATRÓPICAS [3,3] Variaciones de la transposición de Claisen: 47 TRANSPOSICIONES SIGMATRÓPICAS [3,3] 48 TRANSPOSICIONES SIGMATRÓPICAS [2,3] Transposición de sulfóxidos alílicos: Conducen a sulfenatos alílicos que posteriormente se pueden transformar en alcoholes alílicos O CH-CH2-SPh O-SPh CH CH2 PhS OH CH CH2 + PhSSPh 49 TRANSPOSICIONES SIGMATRÓPICAS [2,3] Transposición de Wittig: Es una transposición aniónica en la que un éter alílico se transforma en un -alil alcóxido (alcóxido homoalílico). Z es un grupo capaz de estabilizar el carbanión Ejemplos: 50 TRANSPOSICIONES SIGMATRÓPICAS [2,3] Otros ejemplos: Iluros de azufre: Iluros de amonio 51 TRANSPOSICIONES SIGMATRÓPICAS [1,2] Migración de C en carbocationes (Wagner-Meerwein) Permitida: Supra con retención 52 TRANSPOSICIONES SIGMATRÓPICAS [1,2] Migración en carbaniones No son posibles 53 REACCIONES DE CICLOADICIÓN Definición: Son reacciones en la que dos fragmentos moleculares (normalmente dos moléculas diferentes) se combinan para formar un anillo. REACCIÓN DE DIELS-ALDER Es la reacción entre un alqueno y un 1,3-butadieno para formar un anillo de ciclohexadieno. + La reacción de Diels-Alder se clasifica como una cicloadición [4 + 2], ya que un componente de la reacción aporta 4 electrones y el otro aporta 2. El componente 4 se denomina dieno El componente 2 se denomina dienófilo. Aparte de los alquenos, otros sistemas insaturados como alquinos o alenos pueden participar como dienófilos en la reacción. ió 54 REACCIONES DE DIELS-ALDER Reglas de selección: Las reglas de selección para la reacción térmica térmica, considerando la interacción más habitual entre el LUMO del dienófilo y el HOMO del dieno indican que la aproximación es supra-supra respecto ambos componentes de la reacción. 55 REACCIONES DE DIELS-ALDER. CARACTERÍSTICAS Estereoespecifidad. La reacción de Diels-Alder es normalmente estereospecífica s pra s pra respecte a los dos componentes supra-supra componentes. Esta propiedad está relacionada con el hecho que la reacción es concertada (proceso más o menos sincrónico). Esta estereoespecifidad se traduce en que la estereoquímica del dieno y del dienófilo se mantienen en el cicloaducto resultante X X X X + + Y Y Y Y X X X X + + Y Y Y Y 56 REACCIONES DE DIELS-ALDER. CARACTERÍSTICAS Estereoespecifidad. La mayor parte de las reacciones se consideran concertadas. Sin embargo en algunos embargo, alg nos casos la reacción p puede ede transc transcurrir rrir a tra través és de intermedios y se puede observar pérdida de estereoespecifidad. 57 REACCIONES DE DIELS-ALDER. CARACTERÍSTICAS Estereoselectividad. Con dienófilos sustituidos hay dos aproximaciones posibles diferentes compatibles con el req requerimiento erimiento ssupra-supra. pra s pra endo exo 58 REACCIONES DE DIELS-ALDER. CARACTERÍSTICAS Regla de Alder: Cuando el dienófilo presenta un sustituyente insaturado (carbonilo, éster, ciano etc.) se prefiere la aproximación endo de dicho sustituyente. Mayoritario La relación endo-exo depende de diferentes factores: Factores estéricos, interacciones dipolo-dipolo, interacciones secundarias entre orbitales. Hay muchas excepciones a la regla de Alder y en la mayoría de los casos la relación endo:exo no es muy elevada 59 REACCIONES DE DIELS-ALDER. CARACTERÍSTICAS Regla de Alder: La explicación comúnmente aceptada para la regla de Alder es la existencia de una interacción secundaria entre los orbitales del grupo insaturado (carbonilo) y los orbitales del dieno Estereoquímica de la reacció de Diels Diels-Alder Alder (Resumen) e i e i i e endo d exo endo exo + e i e do endo exo exo endo 60 REACCIONES DE DIELS-ALDER. CARACTERÍSTICAS Reactividad y regioselectividad: Existe una fuerte relación entre la naturaleza electrónica de los sustituyentes de dieno y dienófilo y la velocidad y regioselectividad de la reacción. La reacción es más rápida cuando dieno y dienófilo contienen sustituyentes con características electrónicas complementarias. EA ED ED EA 61 REACCIONES DE DIELS-ALDER. CARACTERÍSTICAS Reactividad y regioselectividad: Si dieno y dienófilo no son simétricos se pueden obtener diferentes regioisómeros. g En g general se observa la p preferencia de uno de ellos según g el siguiente esquema 62 REACCIONES DE DIELS-ALDER. CARACTERÍSTICAS Regioselectividad: La regioselectividad observada se explica teniendo en cuenta los coeficientes orbitálicos en los orbitales frontera de dieno y dienófilo 63 REACCIONES DE DIELS-ALDER. CARACTERÍSTICAS Regioselectividad: Consideremos una reacción de tipo A, con demanda electrónica normal y un n dieno sustituido s stit ido en el carbono C C-1. 1 El ma mayor or coeficiente del LUMO del dienófilo es el del C-1, mientras que en el dieno, el mayor coeficiente del HOMO corresponde a C-4. La interacción más favorable es aquella en la que ambos átomos de mayor coeficiente interaccionan,, obteniéndose el producto p “orto”. HOMO LUMO En cambio cambio, si el dieno está ssustituido stit ido en C C-2, 2 se obtiene el producto prod cto “para” HOMO LUMO 64 REACCIONES DE DIELS-ALDER. CARACTERÍSTICAS Efectos estéricos: La reacción de Diels-Alder es sensible a los efectos estéricos de los s stit entes sustituyentes: Por una parte, estos dificultan el acercamiento entre dieno y dienófilo. Reacción con anhídrido maleico. Sustituyentes voluminosos dificultan la reacción Por otra parte los sustituyentes en el dieno pueden favorecer o dificultar que éste adopte la conformación reactiva s-cis. Más reactivo que butadieno 65 REACCIONES DE DIELS-ALDER. CARACTERÍSTICAS Catálisis ácida. Los ácidos, especialmente los ácidos de Lewis aceleran la reacción e incrementan la estereoselectividad estereoselecti idad y regioselecti regioselectividad idad Me + CO2Me CO2Me Me CO2Me + Me Reacció no catalítica: 120 oC, 6h 70% 30% Reacció catalitzada amb AlCl3: 20 oC, 3h 95% 5% El ácido se coordina al carbonilo del dienófilo afectando tanto a su energía como al valor de sus coeficientes orbitálicos E LUMO 2,5 eV OR H LUMO HOMO -14,5 eV -7,0eV OR OR H O HOMO 23 5 eV -23,5 OR H O O El signo i de d las l fases f no se ha h tenido t id en cuenta en este dibujo 66 REACCIONES DE DIELS-ALDER. EJEMPLOS Dienófilos Dienos ( (funcionalizados) ) Danishefski 67 CICLOADICIONES 1,3-DIPOLARES Són cicloaddicions [4+2]. [4 2]. Síntesi de compostos heterocíclics a + b c a d b c e d e Molècula 1,3-dipolar: Isoelectrònica con el anión alilo. 4 e- deslocalitzados y al menos una forma resonante con dos cargas opuestas en posición 1,3 Òxids de nitril Diazoalcans Ilurs d’azometí Azides Nitrona Dipolarófilo: Especie insaturada: alqueno, alquino, compuestos con enlaces N=N, C=N etc.. 68 CICLOADICIONES 1,3-DIPOLARES. CARACTERÍSTICAS Estereoespecifidad y estereoselectividad: La estereoquímica de la reacción es análoga a la Diels-Alder. La adición es supra-supra. La estereoquímica del dipolarófilo se mantiene en el producto final También son posibles dos orientaciones entre dipolo y dipolarófilo equivalentes a la aproximación endo-exo. La estereoselectividad no siempre es elevada 69 CICLOADICIONES 1,3-DIPOLARES. CARACTERÍSTICAS Regioselectividad: Viene marcada por la complementariedad en las interacciones HOMO-LUMO entre dipolo y dipolarófilo. La iinteracción L t ió más á frecuente f t es LUMO (di (dipolarófilo)-HOMO l ófil ) HOMO (di (dipolo) l ) pero h hay muchas h excepciones. En algunos casos las dos interacciones HOMO-LUMO posibles son próximas en energía Coeficiente de los OF en algunos dipolos comunes 70 CICLOADICIONES 1,3-DIPOLARES. CARACTERÍSTICAS Regioselectividad Energías de los OF en algunos dipolos comunes Ejemplo de predicción de la regioselectividad 71 CICLOADICIONES 1,3-DIPOLARES. EJEMPLOS AZIDA DIAZOMETANO OXIDO DE NITRILO 72 CICLOADICIONES 1,3-DIPOLARES. EJEMPLOS NITRONA 73 CICLOADICIONES [2+2] Son reacciones en las que dos alquenos interaccionen para formar un anillo de ciclobutano. La simetría de los orbitales impone que la reacción sea supra respecto un doble enlace y antara respecto al otro + * 74 CICLOADICIONES [2+2] El requerimiento supra supra-antara antara conduce a ET muy tensionados tensionados. Hay pocos alquenos que puedan dar esta reacción. La mayoría de ejemplos de reacciones [2s + 2a] son con cetenas. Estas poseen un carbono con hibridación sp (lineal) que permite disminuir las interacciones etéricas en el ET Cicloadiciones 2s+2a con cetenas HOMO alqueno q LUMO cetena 75 CICLOADICIONES [2+2]. EJEMPLOS Las cetenas son inestables y suelen prepararse in situ . La forma más habitual es a 76 partir de un cloruro de ácido y una amina. CICLOADICIONES [2+2] FOTOQUÍMICAS Las cicloadiciones fotoquímicas proporcionan métodos complementarios a las cicloadiciones térmicas en lo que se refiere a la estereoquímica de los productos. Desde el punto de vista sintético las más interesantes son les cicloadiciones [2+2] fotoquímicas, para dar sistemas de ciclobutano. En muchos casos transcurren a través de radicales, de manera no concertada, y no siempre son estereoespecíficas. Sales de Cu (I) catalizan la reacción 77 CICLOADICIONES [2+2] FOTOQUÍMICAS Otro tipo de moléculas que experimentan cicloadiciones fotoquímicas son las enonas enonas, especialmente las cíclicas. O O X O X llum + + X Afavorit si X = ED Afavorit si X = EA Reacción de Paterno-Büchi: Es la reacción entre un aldehído o una cetona y un alqueno. C d Conducen a un sistema i t d de oxetano t (ét (éter cíclico í li d de4 4 miembros). i b ) L La reacción ió es estereoespecífica con algunas cetonas alifáticas y no estereoespecífica con cetonas aromáticas. O llum O + Ph Ph H Bz H Ph + O Ph llum Bz O Ph Ph 78 CICLOADICIONES. RESUMEN 79 REACCIONES QUELETRÓPICAS Son reacciones en las que se rompen dos enlaces sobre un mismo átomo. También se denominan reacciones de extrusión porque un fragmento molecular es eliminado de la molécula Extrusió de SO2 80 REACCIONES ÉNICAS Son reacciones en las que un alqueno con un hidrógeno alílico se adiciona a un doble enlace electrófilico (C=O o C=C) transifirendo el hidrógeno alílico al electrófilo + H EA H EA 81 REACCIONES ÉNICAS. EJEMPLOS 82