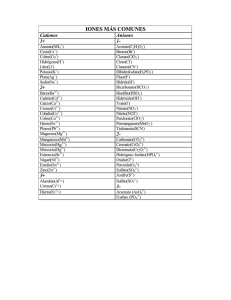
ANIONES COMUNES: Halogenuros: F Fluroruro Cl Cloruro Br
Anuncio

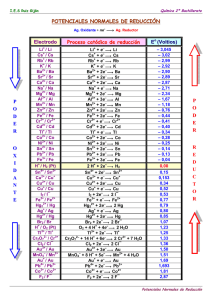
Química Inorgánica (Licenciatura) Dr. Juan Carlos Fierro González Departamento de Ingeniería Química Instituto Tecnológico de Celaya ANIONES COMUNES: Halogenuros: F– Cl– Br– I– Fluroruro Cloruro Bromuro Ioduro además Sulfuro S2– CN– Cianuro SCN– Tiocianato Radicales conteniendo oxígeno: ClO4– Perclorato ClO3– Clorato ClO2– Clorito ClO– Hipoclorito (las mismas reglas de nomenclatura se aplican para radicales con otros halógenos). NO3– NO2– SO42– SO32– HSO4– HSO3– Nitrato Nitrito Sulfato Sulfito Bisulfato Bisulfito CO32– Carbonato HCO3– Bicarbonato Fosfato PO43– HPO42– Bifosfato AsO43– Arsenato CrO42– Cromato Cr2O72– Dicromato MnO4– Permanganato CH3COO– Acetato OH– hidróxido (o ión hidroxilo). Química Inorgánica (Licenciatura) Dr. Juan Carlos Fierro González Departamento de Ingeniería Química Instituto Tecnológico de Celaya Iones positivos Todos los elementos del grupo 1 (IA) forman cationes con carga + Todos los elementos del grupo 2 (IIA) forman cationes con carga 2+ Al3+ Cd2+ Zn2+ Fe2+, Fe3+ Co2+, Co3+ Ni2+, Ni3+ Sn2+, Sn4+ Cr3+ Hg22+ Hg2+ Cu+, Cu2+ Au+, Au3+ NH4+ Amonio