problemas planteados
Anuncio

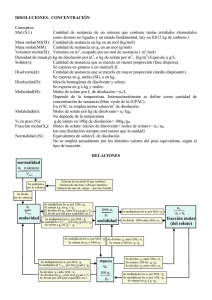
COLEGIO LOS PRÓCERES “Al rescate de los valores perdidos para vivir dignamente y convivir pacíficamente” “FORMAMOS LIDERES PARA LA SANA CONVIVENCIA” CUESTIONARIO DEL CUARTO PERIODO ESCOLAR PROBLEMAS PLANTEADOS Normalidad: Es la cantidad de equivalentes químicos de soluto por cada litro de solución. Como fórmula: CONCENTRACION: N = Normalidad. n eq. : Número de equivalentes del soluto. V: Volumen de la solución en litros. La concentración es la relación que existe entre la cantidad de soluto y la cantidad de solución o desolvente. Esta relación se puede expresar de ° muchas formas distintas. Una de ellas se refiere a los porcentajes. Porcentaje masa en masa o peso en peso, (%m/m):Es la cantidad en gramos de soluto por cada 100 gramos de solución. Ej: Una solución 12% m/m tiene 12 gramos de soluto en 100 gramos de solución. Como formula, podemos expresar esta relación así: %m/m = x 100 Porcentaje masa en volumen (%m/v): Es la cantidad en gramos de soluto por cada 100 ml de solución. Aquí como se observa se combina el volumen y la masa. Ej: Una solución que es 8% m/v tiene 8 gramos de soluto en 100 ml de solución. Fórmula: % m/v = x 100 Porcentaje volumen en volumen (%v/v): Es la cantidad de mililitros o centímetros cúbicos que hay en 100 mililitros o centímetros cúbicos de solución. Ej: Una solución 16% v/v tiene 16 ml de soluto por 100 ml de solución. Fórmula: % v/v = x 100 Otras formas son la Molaridad, la Normalidad y la Molalidad. Es bueno recordad antes el concepto de mol. El mol de una sustancia es el peso molecular de esa sustancia expresada en gramos. Estos datos se obtienen de la tabla periódica de los elementos. Sumando las masas de los elementos se obtiene la masa de la sustancia en cuestión. Molaridad: Es la cantidad de moles de soluto por cada litro de solución. Como fórmula: M = n/V M = M: Molaridad. n: Número de moles de soluto. V: Volumen de solución expresado en litros. N = n eq/V Molalidad: Es la cantidad de moles de soluto por cada 1000 gramos de solvente. En fórmula: m = n/kgs solvente m = Molalidad. n: Número de moles de soluto por Kg = 1000 gramos de solvente o 1 kg de solvente. Ejercicios: A continuación comenzaremos una guía de problemas donde pondremos en práctica a todas estas formulas. 1) Calcula el % m/m de una solución que tiene 6 gramos de soluto en 80 gramos de solución. Aplicamos la fórmula: % m/m = 6 grs x 100 / 80 grs % m/m = 7.5 2) Calcula el % m/m de una solución que tiene 10 grs. de soluto y 110 grs. de solvente. En este caso la masa de la solución es de 120 grs. ya que resulta de sumar los 10 grs. de soluto mas los 110 grs. de solvente. % m/m = 10 grs x 100 / 120 grs % m/m= 8.33. 3) Calcula la masa de soluto que tendría una solución de 220 grs. que es 4% m/m. En este caso podemos despejar la masa de soluto de la fórmula. Nos queda. masa de soluto = % m/m x masa solución / 100 masa de soluto = 4% x 220 grs / 100 Masa de soluto = 8.8 grs. 4) Cuantos grs. de soluto y solvente tendrán 320 grs. de solución cuya concentración es 5% m/m: 1 COORDINADORA RECTORA COLEGIO LOS PRÓCERES “Al rescate de los valores perdidos para vivir dignamente y convivir pacíficamente” “FORMAMOS LIDERES PARA LA SANA CONVIVENCIA” CUESTIONARIO DEL CUARTO PERIODO ESCOLAR % v/v = 4.76. masa de soluto = 5 % x 320 grs / 100 Masa de soluto = 16 grs. La masa de solvente es fácil obtenerla. Directamente le restamos a la masa de la solución la masa de soluto. ° Masa de solvente = 320 grs. – 16 grs. 8) Cuáles son los volúmenes del soluto y solvente de una solución de 2000 ml al 16 % v/v. Volúmen de soluto = ( % v/v sción x Volúmen sción ) Volúmen de soluto = ( % v/v sción x Volúmen sción ) / 100 Volúmen de soluto = (16 % x 2000 ml) / 100 Volumen de soluto = 320 ml. Volumen de solvente = 2000 ml – 320 ml. Masa de solvente = 304 grs. 5) Cuantos gramos de soluto tendrán 1200 ml de solución cuya concentración es de 6% m/v. De la fórmula: % m/v = masa de soluto x 100 / volúmen de sción despejamos la masa de soluto. masa de soluto = % m/V x volúmen de sción / 100 masa de soluto = 6 % m/v x 1200 ml / 100 Volumen de solvente = 1680 ml. Densidad: Con la densidad podemos transformar o pasar una cantidad de masa a su equivalente en volumen o viceversa. Densidad = masa / volumen Aquí les dejo 2 ejemplos. 1) Cuantos grs. habrán en un volumen de 12 ml de una solución que tiene una densidad de 1.84 gr/ml. V = 80 grs x 100 / (5 % m/v sción) Masa de soluto = 72 grs. Masa = Densidad x Volumen Masa = (1.84 gr./ml) x 12 ml. 6) Que volumen tendrá una solución al 5% m/v que contiene 80 grs. de soluto. De la misma fórmula utilizada en el anterior problema despejamos el volumen. Masa = 22.08 grs. 2) Que volumen tendrá una masa de 28 grs. de una solución cuya densidad es 1.76 gr./ml. V = ( masa de soluto x 100) / ( % m/v sción) De la fórmula anterior despejamos al volumen. V = 1600 ml. V = masa / densidad V = 28 grs / 1,76 grs/ml 7) Cuál será el % v/v en una solución que se preparo con 9 ml de soluto y 180 ml de solvente. V = 15.91 ml. El volumen de la solución lo obtenemos sumando a ambos volúmenes. Molaridad: % v/v = ( volúmen de soluto x 100 ) / ( volúmen de sción ) % v/v = (9 ml / 189 ml) x 100 1) Calcula la M de una solución que tiene 8 grs. de hidróxido de sodio (NaOH) en 680 ml de solución. 2 COORDINADORA RECTORA COLEGIO LOS PRÓCERES “Al rescate de los valores perdidos para vivir dignamente y convivir pacíficamente” “FORMAMOS LIDERES PARA LA SANA CONVIVENCIA” CUESTIONARIO DEL CUARTO PERIODO ESCOLAR Según la fórmula de Molaridad. M=n/V Para calcular la Molaridad hay que saber la cantidad de moles y el volumen expresado en litros. La cantidad de moles se calcula por ° n = masa / ( Peso molecular ) también de hidróxido de sodio cuya concentración es 1.8 M. Cuando se prepara una solución a partir de otra de mayor concentración lo que se hace es tomar una cantidad de la de mayor concentración y luego se la diluye con agua hasta llegar al volumen requerido de la de menor concentración. Para saber cuánto debemos tomar de la más concentrada usamos una fórmula. M1 x V1 = M2 x V2 n = 8 grs / 40 grs n = 0.2 moles. Los 680 ml pasados a litros son 0,68 lts. M = ( 0,2 moles ) / ( 0,68 lts ) Los subíndices numéricos se usan para diferenciar a las dos soluciones de distinta concentración. Llamamos 1 a la más concentrada y 2 a la más diluida. 1.8 M x V1 = 0.5 M x 2 lts. Molaridad = 0.294 M (molar). V1 = ( 0,5 M x 2 lts ) / ( 1,8 M ) V1 = 0.555 lts. 2) Cuantos moles de ácido clorhídrico (HCl) serán necesarios para hacer una solución 1,4M que tenga un volumen de 3.6 lts. Se toman 0.555 lts de la solución más concentrada o 555 ml y se disuelven hasta 2 litros. M=n/V Despejamos n de la fórmula quedando: n=MxV n = 1,4 M x 3.6 lts. n = 5.04 moles. 3) Que volumen tendrá una solución que es 2 M y contiene 18 grs. de hidróxido de potasio. (KOH). El volumen lo despejamos de la fórmula de molaridad. Y los 18 grs. de soluto lo pasamos a moles. M = n/V v = n/M n = masa/PM 5) Calcula la M de una solución de ácido sulfúrico (H2SO4) de densidad 1.82 gr/ml y de 94% de pureza. Sabemos que para calcular la molaridad tenemos que tener los datos de la cantidad de moles y el volumen expresado en litros. A partir de la densidad deducimos que en un ml de solución hay 1.82 grs. de masa de solución. Por lo tanto en 1 litro habrá 1820 gramos de solución. Ahora bien, de esos 1820 gramos solo el 94% es puro en el soluto que tenemos. Con un simple cálculo de porcentaje obtendremos la cantidad que realmente hay de soluto en esos 1820 gramos. 1820 grs. x 0.94 = 1710.80 grs. n = = 0.321 moles. V = ( 0,321 moles ) / 2 M V = 0.16 lts. A partir de esta masa sacamos la cantidad de moles. n = ( 1710,80 grs ) / ( 98 grs/mol ) 4) Como prepararía 2 lts. de una solución 0,5 M de hidróxido de sodio (NaOH) a partir de otra n = 17.457 moles. 3 COORDINADORA RECTORA COLEGIO LOS PRÓCERES “Al rescate de los valores perdidos para vivir dignamente y convivir pacíficamente” “FORMAMOS LIDERES PARA LA SANA CONVIVENCIA” CUESTIONARIO DEL CUARTO PERIODO ESCOLAR Estos cálculos se basaron al principio cuando usamos la densidad en un volumen de 1 litro. Por lo tanto si dividimos esta cantidad de moles por un litro obtenemos directamente la molaridad. Molaridad = 17.457 M (molar). dividiendo el peso molecular por la cantidad de hidrógenos que tiene la molécula. El ácido clorhídrico tiene un peso molecular de 36.5. Tiene un solo átomo de hidrógeno, por lo tanto su peso equivalente es el mismo. N de eq soluto = ( 6 grs ) / ( 36,5 grs/eq ) 6) Se dispone de un ácido nítrico comercial del 96,73% en peso y 1,5 gr/ml densidad ¿Cuántos ml ° de ácido concentrado serán necesarios para preparar 0,2 litros de disolución 1,5 molar de dicho ácido? Directamente lo podemos hacer cambiando las unidades con los factores de conversión hasta llegar a molaridad. Se van cancelando las unidades viejas y quedan solo las nuevas, es decir mol/litro que es M (molaridad): Primero usaremos el porcentaje de pureza, luego la densidad, los mililitros a litros y por último pasaremos la masa a moles. (96,73 grs soluto / 100 grs solución) x (1,5 grs soluc / 1 ml soluc) x (1000 ml soluc / 1 litro) x (1 mol acido nítrico / 63 grs soluto) = 23 M Ahora con la fórmula M1 x V1 = M2 x V2 calculamos el volumen del ácido concentrado que necesitarás. Podes llamar con el 1 a la solución concentrada y con el 2 a la nueva solución. V1 = M2 x V2 / M1 = 1.5 M x 0,2 lit / 23 M = 0.013 lit = 13 ml Entonces tomas 13 ml de la solución concentrada y le agregas agua hasta que llegues a los 200 ml o 0,2 litros que nos piden. 7) Cuál será la Normalidad de una solución de ácido clorhídrico que tiene 6 grs. de este en 1200 ml de volumen. A partir de la fórmula: N = N° de equivalentes de soluto / V (scion en lts) Tenemos que calcular el número de equivalentes de soluto y pasar a litros el volumen que ya tenemos de solución. En el caso de los ácidos el número de equivalentes se calcula dividiendo la masa de este por el peso del equivalente químico de este. El equivalente químico en el caso de los ácidos se calcula N de eq. Soluto = 0.164 equivalentes. Normalidad = (0,164 equiv) / ( 1,2 lts) Normalidad = 0.137. 8) A un recipiente que contiene 200 mL de solución acuosa 0.2 M de H2SO4 se le agregan 10 mL de H2SO4 puro (densidad=1.83 g/mL). Suponiendo volúmenes aditivos, calcular para la solución resultante normalidad Debemos calcular el número de moles totales y despues de equivalentes en este caso. Por ejemplo en la primera solución tenemos: Moles = 0,200 lts x 0,2M = 0,04 moles. Como el H2SO4 tiene 2 hidrógenos la cantidad de equivalentes es moles x 2 = 0,08 equivalentes. Ahora calculamos los equivalentes de la otra solución. Pero de la otra no tenemos la Molaridad, la debemos calcular de la densidad y del % de pureza que es del 100% por ser puro. M = 1,83 grs/ml x 1000 ml/litro x 1 mol/98 grs = 18.67 M (molar) por lo tanto tiene 18,67 M x 0,01 litros = 0,187 moles o sea, 0,374 equivalentes. Si sumamos tenemos 0,08 equivalentes + 0,374 equivalentes = 0,454 equivalentes en total al mezclar ambas soluciones. Entonces N = equiv/litros. N = 0,454 equiv / 0,21 litros = 2.16 N de la solución final. El volúmen de 0,21 litros se obtuvo sumando los volúmenes aditivos. 9) Que volumen tendrá una solución 2.6 N de hidróxido de calcio ( Ca(OH)2 ) si la cantidad de soluto usada fue de 4 moles. N = N° eq (st0) / V Despejamos el volumen: V = N° eq (st0) / N En este caso tenemos moles pero no equivalentes. Se puede pasar de una manera sencilla de moles a equivalentes. Teniendo en cuenta que para calcular 4 COORDINADORA RECTORA COLEGIO LOS PRÓCERES “Al rescate de los valores perdidos para vivir dignamente y convivir pacíficamente” “FORMAMOS LIDERES PARA LA SANA CONVIVENCIA” CUESTIONARIO DEL CUARTO PERIODO ESCOLAR el peso de un equivalente de un hidróxido se divide al peso molecular por la cantidad de grupos oxhidrilos. El peso del equivalente es el peso molecular dividido por 2. Ya que este hidróxido posee 2 grupos oxhidrilos. El peso molecular es 40. Por lo tanto el peso del equivalente de Ca(OH)2 es 20. Deducimos por lo tanto que en un mol de este compuesto hay 2 equivalentes. Como tenemos 4 moles del hidróxido tenemos 8 equivalentes. ° V = 8 eq / 2,6N V = 3.077 litros. 10) Calcula la Normalidad de: Una solución 4 M de NaOH. Una solución 6 M de Mg (OH)2 Una solución 0.5 M de H2SO4 Una solución 0.8 M de HNO3 En el caso del NaOH vemos que tiene un solo radical oxhidrilo, o sea que el peso molecular o el mol coincide con el peso de un equivalente químico. Por lo tanto si es 4 M también será 4 N. En el segundo caso, el Mg(OH)2, tiene 2 grupos oxhidrilos. El peso de un equivalente será la mitad del peso molecular. En un mol hay dos equivalentes. Entonces si es 6 M será 12 N. En el tercer caso, vemos que el ácido sulfúrico tiene 2 hidrógenos. O sea que el peso de su equivalente será la mitad de su mol o peso molecular. En un mol hay dos equivalentes. Asi que si es 0.5 M será 1 N. En el último caso, este ácido (ácido nítrico), tiene un solo hidrógeno. Asi que un mol equivale a un equivalente. Es igual su molaridad y su normalidad. Es 0.8 M y 0.8 N. 11) Calcula la molalidad de una solución que se prepara con 16 gramos de Hidróxido de Potasio (KOH) y 1600 gramos de agua. La fórmula es: n = 0.286 moles. Esta cantidad de moles está presente en 1600 gramos de agua. Por lo tanto en 1 kg de agua habrá. m = (0,286 moles) / (1,6 Kgs) 0,179 m (molal). 12) Cuantos gramos de soluto habrá en una solución 2.8 m de Li(OH), que se hizo con 500 ml de agua. En el caso del agua 1 gramo equivale a un ml. Por lo tanto aceptamos que 500 ml son 500 grs. Primero calcularemos la cantidad de moles de soluto. Despejando de la fórmula: m = n / kgs svte n = m x kg de svte. n = 2.8m x 0,5 kgs. n = 1.4 moles. Ahora el último paso es pasar esta cantidad de moles a gramos. La masa es igual al peso molecular por la cantidad de moles. Masa = 23.94 grs./mol x 1.4 moles. Masa = 33.52 gramos. 13) Calcula la masa de agua que se utilizó para preparar una solución 2,2 m si se utilizó 12 gramos de soluto (NaOH). Primero hay que saber la cantidad de moles de soluto. El peso molecular de NaOH es de 40. moles = 12 grs / (40 grs/mol) 0.3 moles. Luego de la fórmula de m: m = moles/kgs svte Kg svte = moles sto / m Kgs de solvente = 0,3 moles / 2,2 m 0.136 kilos o 136 gramos de agua. m = Moles (st0) / Kg svte Tenemos que transformar los 16 grs. del soluto a moles. n = (16 grs) / (56 grs / mol) 14) Calcula la M y N de una solución que se preparó con 28 gramos de Mg(OH)2 al 82 % de pureza en un volumen final de 1600 ml. 5 COORDINADORA RECTORA COLEGIO LOS PRÓCERES “Al rescate de los valores perdidos para vivir dignamente y convivir pacíficamente” “FORMAMOS LIDERES PARA LA SANA CONVIVENCIA” CUESTIONARIO DEL CUARTO PERIODO ESCOLAR Primero debemos corregir la masa de 28 gramos ya que al no ser 100% pura en realidad no hay 28 gramos sino que habrá algo menos. 8) Que m (molalidad) tendrá una solución que se preparo colocando 20 gramos de NaOH en 2200 ml de agua. 28grs. x 0.82 = 22.96 gramos. Rta: 0.227 molal. Estos gramos ahora lo pasaremos a moles. 9) Como prepararía 2 litros de una solución 0.4 M a partir de otra que es 4 M. Moles = 22,96 grs / (58,3 grs/mol) Moles = 0.39 moles. ° Molaridad = 0,39 moles / 1,6 lts Molaridad = 0.24 M (molar). Como este hidróxido tiene 2 radicales oxhidrilos. Por cada mol tenemos 2 equivalentes. Por lo tanto será 0.48 N (Normal). Rta: Tomamos 200 ml de la más concentrada y la diluimos hasta llegar a 2 litros de volumen. 10) Que molaridad tendrá una solución que fue preparada añadiendo 46 grs. de Ca(OH)2 al 79 % de pureza a cierta cantidad de agua obteniendo un volumen final de 4200 ml. Rta: 0.117M. Problemas para resolver: 1) Calcula el % v/v de una solución que tiene un volumen de 1400 ml y 980 ml de agua (solvente). Rta: 30% v/v. 2) Que masa de AgOH se necesitara para preparar 3 litros de una solución 0,4 M en este soluto. Se encuentran 117 g de cloruro de sodio en 2.5 litros de la solución. La molaridad de la solución es Rta: 148.8 grs. 3) Que densidad tendrá una solución de 1500 centímetros cúbicos y 1,9 kgs. Rta: 1.267 grs./ml. 4) Cuál será el volumen de una solución que tiene 20 gramos de soluto y una concentración de 6% m/v Na = 23 glmol A. 0.8 M B. 0.4 M Cl = 35.5 glmol C. 1 M D. 2 M Rta: 333.33 ml. 5) Que masa de solvente se necesitará para hacer 260 grs. de una solución al 4% m/m Rta: 249.6 grs. 6) Calcula la Normalidad de: HNO2 (2M) – KOH (0.4M) – H2SO3 (3M) – Al(OH)3 (1M) – Na3PO4(0.6M) – NaCl (2M). Rta: 2N – 0.4N – 6N – 3M – 1.8N – 2N. 7) Que volumen de solución ocuparan 3 equivalentes de soluto de una solución 4N. Rta: 0.75 litros. 8. La normalidad de la solución cuando disolvemos 294 g de K2Cr2O7 en 500 mL de solución es A. 1 N. B. 4 N. C. 1.5 N. D. 2 N. K = 39 glmol Cr = 52 glmol O= 16 g/mol 9. La molalidad de la solución cuando se disuelven 79 g de KmnO4 en 1000 mL de agua es A. 2m B. 3m C. 1 m 0.5 m K = 39 glmol Mn = 55 glmol O= 16 glmol 6 COORDINADORA RECTORA COLEGIO LOS PRÓCERES “Al rescate de los valores perdidos para vivir dignamente y convivir pacíficamente” “FORMAMOS LIDERES PARA LA SANA CONVIVENCIA” CUESTIONARIO DEL CUARTO PERIODO ESCOLAR B. 82,6 g 1. El peso de Na es 23 y el del Cl es 35,5 al combinar 36,5 de HCl con NaOH los grs. de NaOH que se obtienen son : C 41,3 g D. 123,9 g E. 20,15 g B. 76,5 ° 5.Se disuelven 8,5 g de ácido sulfúrico en 41,5 g de agua. Si la solución resulta con una densidad de 1,1 g/cm3 entonces la concentración es : C. 58.5 A. 17% por peso D. 81.5 B. 8,4 Normal E.23.0 C. 5,5 Molar A 36.5 D. 9,2 molal 2. “A temperatura constante el volumen ocupado por una cantidad definida de un gas es inversamente proporcional a las presiones que soporta". Lo anterior se expresa así : E. 5,5% por peso A. V1P2 = V2P1 A. 30,5 ml B. V1T2 = V2T1 B. 15,2 ml C. V1T1 = V2T2 C. 20 ml D. V1 / P1 = V2 / P2 D. 36,3 ml E. V1P1 = V2P2 E. 28,3 ml. 6. Una masa de Cl2 ocupa 38ml a 20°C. El volumen a 280°K, con presión constante es : 7. La ecuación de la reacción MnO2 + HCl → MnCl2 + H2O + Cl2 se balancea con los siguientes coeficientes : 3.Un gas ocupa un volumen V a una temperatura T y a una presión P. Si la presión se triplica y la temperatura se reduce a la mitad el volumen ocupado por el gas a estas condiciones es : A. 6V B. 2/3V C. 3/2V D. V/6 E. 5V 4. Dada la ecuación : PCl5 → PCl3 + Cl2, los gramos de Cl2 que pueden obtenerse por descomposición de 121,2 g de PCl5 , son : A. 355,9 A. 1,2,1,4,1 B. 1,4,1,2,1 C. 4,2,1,1,2 D. 1,2,1,1,2 E. 4,1,1,2,1 8.Todos los gases se pueden mezclar en cualquier proporción , siempre y cuando no reaccionen químicamente. En este caso se dice que los gases son : A. Compresibles B. Difusibles C. Expandibles 7 COORDINADORA RECTORA COLEGIO LOS PRÓCERES “Al rescate de los valores perdidos para vivir dignamente y convivir pacíficamente” “FORMAMOS LIDERES PARA LA SANA CONVIVENCIA” CUESTIONARIO DEL CUARTO PERIODO ESCOLAR D. Densos E. Miscibles 9. Para una muestra determinada de un gas ideal, si la temperatura se mantiene constante, el producto de la presión por el volumen : A. Varía con la temperatura absoluta 13. La siguiente tabla muestra la solubilidad ( g/L) para los solutos X y Y; SOLUTO molecular 20°C 40°C 60°C Masa X 90 g 93 g 95 g 140 g/mol Y 70 g 68 g 65 g 30 g/mol B. Varía con la presión ° C. Es igual a 22,4 litros D. Es una constante E. Es igual a 1 atmósfera 10. La variación del volumen de un gas por un cambio simultáneo de la presión y de la temperatura se puede calcular aplicando : 14- Con respecto a la solubilidad de las anteriores sustancias se puede afirmar que : 28. Cuantos gramos de Ca(OH)2 hay 100 ml de una solución 5 N ( Ca= 40 , O=16g/mol y H= 1g/mol) A. Las dos sustancias presentan la misma solubilidad B. La solubilidad de Y aumenta con la temperatura A. Ley de Boyle B. Ley de Charles C. Constante universal de los gases C. La solubilidad de X disminuye con la temperatura D. La solubilidad de X aumenta con la temperatura D. Ley combinada de los gases E. La teoría cinética 11. La solución donde se llega al limite en la proporción del soluto que puede disolver en una cantidad de solvente se conoce como: A. Diluida B. Saturada C. Sobresaturada 12.En las condiciones normales, 22,4 litros de todos los gases tienen el mismo número de :27. Cual es el pH de 200 ml de solución que contienen 0.036 g de HCL( H=1 g/mol y Cl = 35.5 g/mol) A. Iones B. Átomos 15. Una muestra del gas Cl2 que ocupa un volumen de 0,50 litros a 20°C y 760 torr, tiene una masa igual a : 29. La densidad del oxígeno gaseoso en g/l a las condiciones normales es : A. 14,8 g l B. 0,148 g C. 0,296 g D. 1,48 g 5. Cuantos gramos de NaOH están presentes en 500 ml de solución con un pH de 10 ( Na= 23 g/mol, O= 16 g/mol,H= 1g/mol) C Moléculas D Electrones E. Enlaces 15. Cuantos gramos de NaOH están presentes en 500 ml de solución con un pH de 10 ( Na= 23 g/mol, O= 16 g/mol,H= 1g/mol) 8 COORDINADORA RECTORA COLEGIO LOS PRÓCERES “Al rescate de los valores perdidos para vivir dignamente y convivir pacíficamente” “FORMAMOS LIDERES PARA LA SANA CONVIVENCIA” CUESTIONARIO DEL CUARTO PERIODO ESCOLAR A. 0.2 g D.0,474 N B. 0.002 g E.0,632 N. C. 0.0002 g 20. Los volúmenes iguales de todos los gases, bajo las mismas condiciones de temperatura y presión, contienen igual número de moléculas. Este enunciado corresponde a: D. 0.02 g 16. Una solución 1M de H3PO4 es también : ° A.Ley de Gay Lussac A. 1N B.Ley de Graham B. 0.33 N C.Ley de Boyle C. 3N D.Principio de Avogadro D. N/3 E.Ley de Charles E.Ninguna de las anteriores. 21. Si tenemos la distribución electrónica de un elemento no podemos predecir: 17. Los gramos de NaOH que se requieren para neutralizar 9,12g de HCl son : A Número de protones en el núcleo A.9,12 g B. Peso atómico B.1g C. Período al que pertenece C. 0,1g D. Grupo al que pertenece D.100g E. Número atómico E.10g 22. A una temperatura de 20°C y una presión de 70 mm Hg, la densidad de un gas desconocido es 2,25g/l. Su masa molecular es : 18. Una masa de gas nitrógeno a una presión de 760 mm Hg y a una temperatura de 77°C, ocupa un volumen de 12,31. El volumen de dicho gas cuando su temperatura es de 27°C es : A. 70,20 g B. 55,51 g A.18,45 l C. 80,40 g B.8,20 l D. 27,30 g C.4,10 l E. 30,50 g D.36,90 l 23. Una presión de 800 mm de Hg es equivalente a : E.Ninguna de las anteriores A. 800/760atm 19. En la titulación de 30 ml de HCl se gastaron 47,5 ml de NaOH 0,1 N La Normalidad del HCl es : B. 800/76atm A.0,158 N B.0,014N C.0,316 N C. 800/7,6atm D. La presión a nivel del mar E. 14,7 lbs/pulg2 9 COORDINADORA RECTORA COLEGIO LOS PRÓCERES “Al rescate de los valores perdidos para vivir dignamente y convivir pacíficamente” “FORMAMOS LIDERES PARA LA SANA CONVIVENCIA” CUESTIONARIO DEL CUARTO PERIODO ESCOLAR 24. Las condiciones normales se definen como: C. 112 litros A. 0°K y 1 atm D. 21,1 litros B. 0°C y 76 mmHg E. 11,2 litros C. 100°C y 760 mm de presión 28. Cuantos gramos de Ca(OH)2 hay 100 ml de una solución 5 N ( Ca= 40 , O=16g/mol y H= 1g/mol) D. 273°K y 760 g de presión E. 0°C y 760 mm de presión ° 25. El cero absoluto es : A. La temperatura a la cual todos los gases se licúan B. La temperatura a la cual el vapor de agua solidifica A. 36 B. 1.8 C. 3.6 D. 18 C. °C + 273°K 29. La densidad del oxígeno gaseoso en g/l a las condiciones normales es : D. -273°C A. 14,29g/l E. 283°C B. 32,0 g 26 Que una solución sea normal 0.5 normal significa que: C. 1,429 g/l A. La solubilidad del soluto es del 50% D. 22,4 l B. Su volumen total s de 1/2 de litro 30. A temperatura constante, si la presión de un gas se duplica, su volumen: C. Contiene la mitad de moles que debería contener A. Se duplica D. Soluble B. Se reduce a la mitad E. Insoluble C. Se triplica 27. Cual es el pH de 200 ml de solución que contienen 0.036 g de HCL( H=1 g/mol y Cl = 35.5 g/mol) D. Disminuye 1/3 parte A.3 B. 3.3 C. 2 D. 2.3 E. 5 27. De acuerdo con la reacción; 2H2 (g) + O2 (g) → 2H2O (l) .El volumen de oxígeno gaseoso necesario para que reaccione con mol de hidrógeno, completamente, es: A. 1,12 litros B. 1 litro 10 COORDINADORA RECTORA





![guíasoluciones[2][1]](http://s2.studylib.es/store/data/004409996_1-4c22b608b62968c9dca601aaf9328ec2-300x300.png)