Determinación de la fórmula y constante de inestabilidad de un
Anuncio

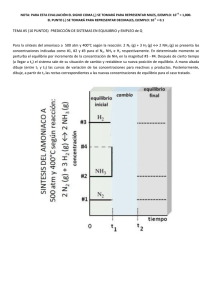
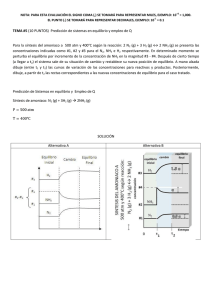
QUÍMICA INORGÁNICA II – 2011 Trabajo Práctico: DETERMINACIÓN DE LA FÓRMULA Y LA CONSTANTE DE ESTABILIDAD DE UN COMPLEJO POR VOLUMETRÍA DE PRECIPITACIÓN Objetivo del trabajo: Determinación experimental de la fórmula y de la constante de inestabilidad (Ki) de un complejo de coordinación formado por amoníaco y plata. [Ag(NH3)x]+ ↔ Ag+ + xNH3 Ki=[Ag+][NH3]/[ Ag(NH3)x+] 1- Material a utilizar Cuatro erlenmeyers, bureta y pipeta limpios y enjuagados con agua bi-destilada. Solución de nitrato de plata y de bromuro de potasio ambas 0,01 M y solución de amoníaco 2 M. Para preparar la solución de amoníaco se deberá utilizar la medida de la densidad de la solución comercial y determinar la concentración para luego calcular la dilución necesaria. Para evaluar la ausencia de Cl- en el agua bi-destilada se debe probar la ausencia de opalescencia al agregar una gota de solución de nitrato de plata a un tubo de ensayo con agua. Ag+ + Cl- ↔ AgCl KpsAgCl= 2,0 . 10-10 2- Técnica Se vierten en los cuatro erlenmeyers 20 ml de solución de [AgNO3]=0,01M y en cada uno de ellos volúmenes crecientes de solución de amoníaco completando con agua bi-destilada hasta un volumen final de 100 ml, a saber: abcd- 10 ml 15 ml 20 ml 30 ml Determinar desde bureta el volumen de solución de [KBr]=0,01 M necesario para producir una ligera opalescencia (punto final) debida a la aparición de AgBr como precipitado. IMPORTANTE: Observar sobre fondo negro para detectar fácilmente el punto final. Tomando como base los volúmenes utilizados en las titulaciones anteriores procede a una segunda serie de determinaciones. Se repiten las preparaciones con los mismos volúmenes de AgNO3 y NH3 pero ahora se utilizan volúmenes de agua ajustados de modo que el volumen final incluyendo el agregado de BrK de la titulación sea de aproximadamente 100ml. Si en esta segunda serie de titulaciones alguno de los volúmenes finales se aparte del valor buscado de 100 ml en más de 2 ml deberá realizarse una tercera determinación variando el volumen de agua según convenga. Con los datos obtenidos calcular la fórmula del ión complejo y su constante de inestabilidad. 3- Cálculos Considerar las siguientes aproximaciones: La solución amoniacal compuesta por la base débil y su anión conjugado se considerará a los fines prácticos como compuesta solamente por la especie NH3. Debido a la diferencia entre las concentraciones de la solución de AgNO3 y de NH3, se considerará al catión Ag+ como totalmente complejado. La disminución de la concentración de NH3 debido a la formación del complejo es despreciable. Teniendo en cuenta lo anterior, en la ecuación de la constante de inestabilidad del complejo sólo es incógnita la concentración de equilibrio del catión Ag+ en equilibrio con el complejo. Esa concentración puede calcularse a partir de los resultados de las titulaciones y del conocimiento del Kps del bromuro de plata. Ag+ + Br- ↔ AgBr KpsAgBr= 5,4 . 10-13 Puede llegarse entonces a la siguiente expresión para el cálculo de la estequiometria del complejo y de la constante de inestabilidad del complejo: log([Br-])= log (KpsAgBr/ Ki. [ Ag(NH3)x+]) + x log ([NH3]) Como el volumen final de las soluciones debe ser igual o muy próximo a 100 ml, la concentración del complejo en todas ellas será la misma, ya que siempre se utilizan 20 ml de AgNO3 0,01 M. Resulta así, que en la relación anterior, el primer término del segundo miembro es aproximadamente constante, por ello si se representan en un gráfico las magnitudes log([Br-]) vs log ([NH3]) , se obtendrán puntos situados en una recta que puede ser aproximada por el método de los cuadrados mínimos. De esta recta pueden calcularse los valores de la pendiente y la ordenada al origen que permitirán a su vez obtener los valores del coeficiente x en la fórmula del complejo y de la constante de inestabilidad (Ki). 4- Resultados Completar en la siguiente tabla los valores obtenidos en la primera titulación. Vol. de NH3 (ml) Vol. de H2O (ml) 10 15 20 30 70 65 60 50 Vol. de KBr (ml) Vol. de AgNO3 (ml) 20 20 20 20 Vol. Total (ml) Completar en la siguiente tabla los valores obtenidos en la segunda titulación. Vol. de NH3 (ml) Vol. de H2O (ml) Vol. de KBr (ml) 10 15 20 30 Vol. de AgNO3 (ml) 20 20 20 20 Vol. Total (ml) Si el valor de Vol. Total llega a diferir en más de 2 ml a los 100 ml buscados se deberá repetir la experiencia modificando el volumen de agua agregado de manera conveniente. Completar la siguiente tabla con los valores calculados para aplicar cuadrados mínimos a los resultados experimentales, calcular Ki y x. log([Br-]) log ([NH3]) 5- Comentarios y discusión del TP ¿Cómo afecta a los cálculos realizados la suposición de que la única especie presente en el sistema por agregado de amoníaco es el NH3? ¿Por qué es apropiado suponer que la totalidad del ión Ag+ se encuentra complejado para el cálculo de la concentración en equilibrio del complejo? ¿Utiliza la misma suposición para el cálculo de todas las magnitudes del TP? ¿Por qué utiliza agua bi-destilada en el TP? Dado el valor del KpsAgCl= 2,0 . 10-10, discuta la importancia de este valor respecto del dado antes para el AgBr en cuanto a las reacciones utilizadas. Deducir la ecuación utilizada para el cálculo de las magnitudes determinadas en el TP. ¿Cómo calcula el error asociado a las magnitudes determinadas y de qué depende? Detallar las aproximaciones realizadas.