Caso 6 Fracaso renal agudo en paciente con bicitopenia
Anuncio
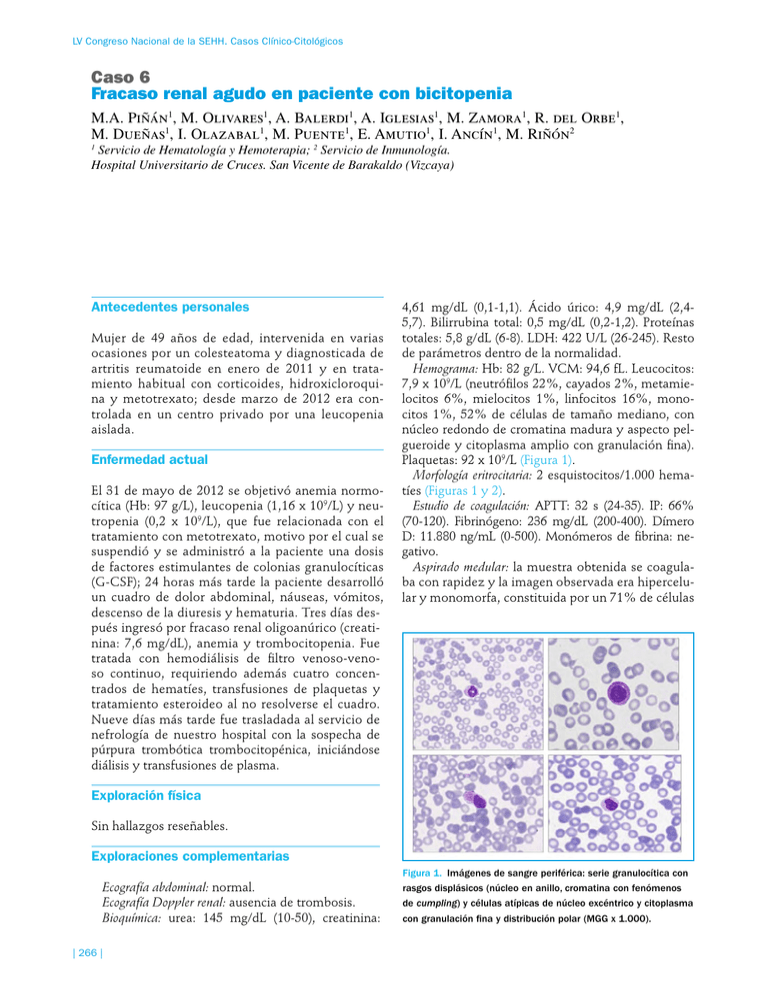
LV Congreso Nacional de la SEHH. Casos Clínico-Citológicos Caso 6 Fracaso renal agudo en paciente con bicitopenia M.A. Piñán1, M. Olivares1, A. Balerdi1, A. Iglesias1, M. Zamora1, R. del Orbe1, M. Dueñas1, I. Olazabal1, M. Puente1, E. Amutio1, I. Ancín1, M. Riñón2 Servicio de Hematología y Hemoterapia; 2 Servicio de Inmunología. Hospital Universitario de Cruces. San Vicente de Barakaldo (Vizcaya) 1 Antecedentes personales Mujer de 49 años de edad, intervenida en varias ocasiones por un colesteatoma y diagnosticada de artritis reumatoide en enero de 2011 y en tratamiento habitual con corticoides, hidroxicloroquina y metotrexato; desde marzo de 2012 era controlada en un centro privado por una leucopenia aislada. Enfermedad actual El 31 de mayo de 2012 se objetivó anemia normocítica (Hb: 97 g/L), leucopenia (1,16 x 109/L) y neutropenia (0,2 x 109/L), que fue relacionada con el tratamiento con metotrexato, motivo por el cual se suspendió y se administró a la paciente una dosis de factores estimulantes de colonias granulocíticas (G-CSF); 24 horas más tarde la paciente desarrolló un cuadro de dolor abdominal, náuseas, vómitos, descenso de la diuresis y hematuria. Tres días después ingresó por fracaso renal oligoanúrico (creatinina: 7,6 mg/dL), anemia y trombocitopenia. Fue tratada con hemodiálisis de filtro venoso-venoso continuo, requiriendo además cuatro concentrados de hematíes, transfusiones de plaquetas y tratamiento esteroideo al no resolverse el cuadro. Nueve días más tarde fue trasladada al servicio de nefrología de nuestro hospital con la sospecha de púrpura trombótica trombocitopénica, iniciándose diálisis y transfusiones de plasma. 4,61 mg/dL (0,1-1,1). Ácido úrico: 4,9 mg/dL (2,45,7). Bilirrubina total: 0,5 mg/dL (0,2-1,2). Proteínas totales: 5,8 g/dL (6-8). LDH: 422 U/L (26-245). Resto de parámetros dentro de la normalidad. Hemograma: Hb: 82 g/L. VCM: 94,6 fL. Leucocitos: 7,9 x 109/L (neutrófilos 22%, cayados 2%, metamielocitos 6%, mielocitos 1%, linfocitos 16%, monocitos 1%, 52% de células de tamaño mediano, con núcleo redondo de cromatina madura y aspecto pelgueroide y citoplasma amplio con granulación fina). Plaquetas: 92 x 109/L (Figura 1). Morfología eritrocitaria: 2 esquistocitos/1.000 hematíes (Figuras 1 y 2). Estudio de coagulación: APTT: 32 s (24-35). IP: 66% (70-120). Fibrinógeno: 236 mg/dL (200-400). Dímero D: 11.880 ng/mL (0-500). Monómeros de fibrina: negativo. Aspirado medular: la muestra obtenida se coagulaba con rapidez y la imagen observada era hipercelular y monomorfa, constituida por un 71% de células Exploración física Sin hallazgos reseñables. Exploraciones complementarias Figura 1. Imágenes de sangre periférica: serie granulocítica con Ecografía abdominal: normal. Ecografía Doppler renal: ausencia de trombosis. Bioquímica: urea: 145 mg/dL (10-50), creatinina: | 266 | rasgos displásicos (núcleo en anillo, cromatina con fenómenos de cumpling) y células atípicas de núcleo excéntrico y citoplasma con granulación fina y distribución polar (MGG x 1.000). LV Congreso Nacional de la SEHH. Casos Clínico-Citológicos Figura 2. Sangre periférica: blastos granulares y esquistocitos aislados (MGG x 1.000). de tamaño mediano a pequeño, en cuyo contorno se observaban con alguna frecuencia blebs; los núcleos eran redondos, excéntricos, sin indentaciones, con una cromatina de aspecto maduro y pelgueroide; los citoplasma eran abundantes y granulares; esta granulación era fina y a veces mostraba una disposición polar; no se vieron astillas ni bastones de Auer y la reacción citoquímica para la peroxidasa fue intensamente positiva. La serie granulocítica residual era muy dismórfica y los megacariocitos estaban en cantidad suficiente y tenían morfología normal; la serie roja estaba escasamente representada (Figura 3-9). Inmunofenotipo: el 84% de las células de la médula ósea tenían un fenotipo compatible con leucemia aguda promielocítica (LPA): CD45+, CD13+, CD33+, CD117+ (64%), DR-, CD56+, CD11c+, CD32+, CD64+, CD38+, MPO+, CD34-, CD11b-, CD16-, CD14-, CD4- (Figura 10). Figura 3. Aspirado medular en el que se observa una imagen hipercelular y monomorfa, constituida por una población blástica de tamaño mediano, con un núcleo redondo y excéntrico y un citoplasma amplio con granulación fina, sin Figura 4. Aspirado medular: blastosis de estirpe granulocítica bastones de Auer (MGG x 200). (MGG x 1.000). | 267 | LV Congreso Nacional de la SEHH. Casos Clínico-Citológicos Figura 5. Aspirado medular: blastos granulares con presencia Figura 6. Aspirado medular: blastos de núcleo con apariencia de blebs en su contorno (MGG x 1.000). madura y gran fragilidad (MGG x 1.000). Figura 8. Aspirado medular: blasto con blebs y probable Figura 7. Aspirado medular: blastosis y un eritroblasto con elemento de serie granulocítica desgranulado (MGG x 1.000). cromatina deslustrada (MGG x 1.000). Los estudios citogenéticos y moleculares realizados en médula ósea fueron: • Reordenamiento PML-RARα t(15;17)(q22;q21) (RTPCR): negativo. • FISH: nuc ish 15q22 (PMLx2), 17q21 (RARax3) [23/100] (Figura 11). • Citogenética: 46, XX, del(5)(q13q31), t(11;17) (q23;q21) [20/30] / 46,XX [10/30] (Figura 12). • Reordenamiento PLZF-RARα positivo (RT-PCR) (Figura 13). • Reordenamiento RARα-PLZF positivo (RT-PCR). Diagnóstico Figura 9. Aspirado medular: reacción muy intensa de los blastos con la peroxidasa (P x 1.000). | 268 | LPA con translocación variante RARα (según la clasificación de la Organización Mundial de la Salud [OMS]). LV Congreso Nacional de la SEHH. Casos Clínico-Citológicos Figura 10. Inmunofenotipo de la médula ósea: la población blástica estaba caracterizada por los marcadores CD45+, CD13+, CD33+, CD117+ (64%), DR-, CD56+, CD11c+, CD32+, CD64+, CD38+, MPO+, CD34-, CD11b-, CD16-, CD14-, CD4-. Figura 11. Técnica de FISH en el aspirado medular donde se observa una señal en el cromosoma 11. Cortesía de la Dra. Calasanz. Universidad de Navarra. Pamplona. Figura 12. Citogenética de médula ósea en la que se confirma la t(11;17)(q23;q21), además de una del(5q)(q13q31) en 20/30 metafases. Cortesía de la Dra. Calasanz. Universidad de Navarra. Pamplona. Evolución Figura 13. Reordenamiento PLZF-RARa que demuestra la presencia de una banda de 269 pb; C-: control negativo; MPM: marcador de pesos moleculares (RTPCR); P: paciente. | 269 | El 28/6/2013 la paciente fue trasladada a nuestro servicio e inició tratamiento quimioterápico de inducción según esquema IDICE (idarrubicina: 12 mg/m2/día los días 1, 3 y 5; Ara-C: 500 mg/m2/12 h, días, 1, 3, 5 y 7; y etopósido: 100 mg/m2/día, los días 1, 2 y 3) + ácido transretinoico (ATRA), 45 mg/m2/día repartido en 2 dosis, hasta alcanzar remisión completa y ajustando las dosis a la insuficiencia renal durante los primeros días y a dosis plenas 9 días más tarde, una vez resuelto este problema. LV Congreso Nacional de la SEHH. Casos Clínico-Citológicos El aspirado medular en el día +37 postinducción mostró un 3% de células blásticas, una enfermedad residual (EMR) por citometría de flujo de un 0,4% y un cariotipo: 46,XX,del(5)(q13q31),t(11;17)(q23;q21) [4/50] / 46,XX [46/50]; el reordenamiento PLZFRARα era positivo. Se inició tratamiento de consolidación (2 ciclos de Ara-C: 500 mg/m2/12 h, días 1 a 6; mitoxantrone: 12 mg/m2/día los días 4, 5 y 6; y ATRA: 45 mg/m2/día repartido en dos dosis, días 1 a 15), tras los cuales se normalizó el cariotipo. La EMR fue en ese momento de 0,072%, y los estudios moleculares para PLZFRARα y RARα-PLZF se negativizaron. Durante el ingreso, previo al tratamiento quimioterápico, y como consecuencia de la colocación de un catéter de vía central para la diálisis, la paciente desarrolló un gran hematoma pectoral derecho con sangrado a través del orificio de entrada, que fue imposible de controlar con medidas físicas y obligó a retirar esa vía. En febrero de 2013 se efectuó trasplante alogénico de precursores hematopoyéticos con acondicionamiento mieloablativo y progenitores obtenidos a partir de la sangre periférica de su hermana, sin que sufriese complicaciones significativas. Discusión La LPA se incluye entre las leucemias agudas con anomalías citogenéticas recurrentes y se caracteriza por presentar la translocación t(15;17)(q22;q12) PML-RARα. Sin embargo, en un 10% de los casos no se detecta esta alteración por técnicas citogenéticas, ya sea por problemas técnicos, inserciones cromosómicas submicroscópicas o reodenamientos más complejos. A pesar de ello podremos hacer un diagnóstico certero ya que el estudio molecular del tránscrito PMLRARα será positivo. Por otro lado, aproximadamente un 2% de los casos de LPA portan un gen de fusión alternativo al PML (PLZF con la t(11;17)(q23q21), NPM1 con la t(5;17), NuMA con la t(11;17(q13q21), FIPIL1 con la t(4;17), BCOR con la t(X;17), STAT5b y PRKAR1A con reordenamientos de 17q); el más frecuente de todos ellos es el PLZF (promielocytic zinc finger)(1); este gen, también conocido como Zbtb16, fue descrito por primera vez en 1993 en un paciente chino que padecía de una LPA atípica; está localizado en el cromosoma 11q23, entre un cluster de genes de la familia zinc finger, codificantes de unas proteínas con gran contenido en cisteínas e histidinas que requieren una o más uniones de zinc para estabilizar su estructura(2); tiene una alta capacidad represora de la transcripción, y su nivel de expresión es muy alto en la célula madre y progenitora, pero disminuye a medida que la célula madura. | 270 | La importancia clínica de estas variantes de LPA estriba, sin duda, en la diferente respuesta al tratamiento con ATRA y trióxido de arsénico, ya que todas son sensibles, a excepción de las portadoras de los genes PLZF y STAB5b. En el caso de la LPA con t(11;17) (q23q21) hay evidencia de esta resistencia tanto in vivo como in vitro, particularmente en aquellos pacientes que tienen el reordenamiento inverso RARα-PLZF, cuyo producto jugaría un papel importante en la mediación de la resistencia al ácido retinoico(1,3). Desde el año 1993 se han comunicado aproximadamente 16 casos más de pacientes con esta translocación variante(4-7), con una incidencia muy baja en la mujer (14 hombres versus 2 mujeres), frecuente coagulopatía (11 pacientes) y en todos ellos se detectó la t(11;17), ya fuera por citogenética convencional o por FISH; ocurrió lo mismo con los reodenamientos PLZF-RARα y RARα-PLZF en aquellos pacientes en los que se realizó el estudio molecular por PCR; respecto al tratamiento, 13 recibieron quimioterapia según diferentes esquemas, y en 14 se adicionó ATRA; 4 se sometieron a alotrasplante y 1 a autotrasplante de progenitores hematopoyéticos, consiguiendo respuestas de duración variable en todos los pacientes. En nuestro caso la forma de debut de la enfermedad fue peculiar, por la presentación “subaguda”, la ausencia de clínica hemorrágica espontánea y el fracaso renal. La relación causa-efecto entre el tratamiento con factores madurativos y el daño renal nos lleva a pensar que los efectos proinflamatorios o trombogénicos de los G-CSF podrían jugar algún papel; sin embargo, no se demostró la existencia de una trombosis renal, ni de datos que apoyaran un daño endotelial evidente; por otro lado, uno de los casos descritos en la literatura fue tratado con la asociación de ATRA más G-CSF con buenos resultados(8) y nuestra paciente resolvió la insuficiencia renal con el tratamiento quimioterápico. Hay que recordar también que durante los 15 días previos al diagnóstico recibió múltiples transfusiones de plasma y se había sometido a diálisis, lo que bien pudiera haber enmascarado las alteraciones de la hemostasia habituales en este tipo de leucemia; aún así, en los días previos al tratamiento detectamos signos de fibrinolisis. El antecedente de una artritis reumatoide tratada con metotrexato y la presencia de una del 5q en el cariotipo nos permiten especular con la posible existencia de una mielodisplasia previa al desarrollo de la leucemia o relacionar ambas enfermedades. En este sentido, no tenemos datos que demuestren la primera posibilidad y, por otra parte, la mayoría de los estudios que han investigado la asociación de enfermedades autoinmunes y sus tratamientos con la leucemia mieloide aguda han descrito un incremento del riesgo de desarrollarla que, sin embargo, no alcanza significación estadística, por lo que etiquetar a estas leucemias como leucemia mie- LV Congreso Nacional de la SEHH. Casos Clínico-Citológicos loide aguda relacionada con terapia (t-LMA) no parece, de momento, apropiado(9). El diagnóstico morfológico de la LPA de morfología variante es siempre complejo, y en la literatura muchos de los casos fueron descritos como intermedios entre LMA-M2 y M3 de la clasificación FAB(7) y los blastos, definidos como células bloqueadas en un estadio intermedio promielocito-mielocito, con un núcleo de apariencia madura y cromatina condensada, así como presencia de rasgos displásicos asociados (hipogranulación, hiposegmentación del núcleo); la descripción de los blastos que hace la clasificación de la OMS de 2008 no difiere mucho de esas descripciones iniciales(10). Sin embargo, el perfil inmunofenotípico de la LPA es independiente de las variaciones citogenéticas subyacentes, de manera que es una herramienta rápida e imprescindible para el diagnóstico(11), que por supuesto se debe completar con los estudios citogenéticos y moleculares. Para recordar • Las leucemias promielocíticas agudas con t(11;17) (q23;q21) son poco frecuentes. Su morfología es muy peculiar y ha sido descrita como intermedia entre LMA M2 y M3 con rasgos displásicos severos. Su fenotipo, sin embargo, es indistinguible de la LPA con t(15;17). • Las técnicas citogenéticas y moleculares son imprescindibles para poder llevar a cabo correctamente el diagnóstico. • La experiencia terapéutica en esta entidad es escasa. Bibliografía 1. Jovanovic JV, Rennie K, Culligan D, Peniket A, Lennard A, Harrison J, et al. Development of real-time quantitative poly- | 271 | merase chain reaction assays to track treatment response in retinoid resistant acute promyelocytic leukemia. Frontiers in oncology 2011; 35: 1-8. 2. Suliman BA, Xu D, Williams BR. The promyelocytic leukemia zinc finger protein: two decades of molecular oncology. Front Oncol 2012; 2: 74. 3. Guidez F, Parks S, Wong H, Jovanovic JV, Mays A, Gilkes AF, et al. RAR-PLZF overcomes PLZF-mediated repression of CRABPI, contributing to retinoid resistance in t(11;17) acute promyelocytic leukemia. PNAS 2007; 20: 18694-99. 4. Grimwade D, Biondi A, Mozziconacci MJ, Hagemeijer A, Berger R, Neat M, et al.; on behalf of Groupe Francais de Cytogénétique Hematologique, Groupe Francais d’Hematologie Cellulaire, UK Cancer Cytogenetics Group, and BIOMED 1 European Community-Concerted. Action “Molecular Cytogenetic Diagnosis in Haematological Malignancies” Characterization of acute promyelocytic leukemia cases lacking the classic t(15;17): results of the European Working Party. Blood 2000; 96: 1297-308. 5. Rohr SS, Flores Pelloso LA, Borgo A, De Nadai LC, Yamamoto M, Rego EM, et al. Acute promyelocytic leukemia associated with the PLZF-RARA fusion gene: two additional cases with clinical and laboratorial peculiar presentations. Med Oncol 2011; DOI10.1007/s12032-011-0147-y 6. 6. Cassinat B, Guillemot I, Moluçon-Chabrot C, Zassadowski F, Fenaux P, Tournilhac O, Chomienne C. Favourable outcome in an APL patient with PLZF/RARalpha fusion gene: quantitative real-time RT-PCR confirms molecular response. Haematologica 2006; 91: e158-e159. 7. Licht JD, Chomienne C, Goy A, Chen A, Scott AA, Head DR, et al. Clinical and molecular characterization of a rare syndrome of acute promyelocytic leukemia associated with translocation (11; 17). Blood 1995; 85: 1083-94. 8. Jansen JH, de Ridder MC, Geertsma MC, Erpelinck CA, van Lom K, Smit EM, et al. Complete remission of t(11;17) positive acute promyelocytic leukemia induced by all-trans retinoic acid and granulocyte colony-stimulating factor. Blood 1999; 94: 39-45. 9. Ramadan SM, Fouad TM, Summa V, Hasan SK, Lo-Coco F. Acute myeloid leukemia developing in patients with autoimmune diseases. Haematologica 2012; 97: 805-17. 10. Swerdlow SH, Campo E, Harris NL, Jaffe ES, Pileri SA, Stein H, et al. World Health Organization Classification of Tumours of Haematopoietic and Lymphoid Tissues. Vol 2. Geneva (Switzerland) WHO Press; 2008. 11. Dong HY, Kung JX, Bhardwaj V, McGill J. Flow cytometry rapidly identifies all acute promyelocytic leukemias with high specificity independent of underlying cytogenetic abnormalities. Am J Pathol 2011; 135: 76-84.