PATOLOGÍA DEL SISTEMA RESPIRATORIO Dr. Alfonso López
Anuncio

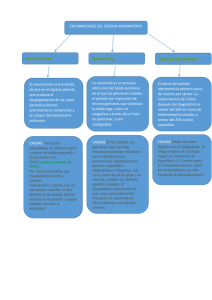
PATOLOGÍA DEL SISTEMA RESPIRATORIO Dr. Alfonso López Mayagoitia Atlantic Veterinary College Versión: Marzo 30, 2006 Referencias: Pathology of Domestic Animals, Jubb, Kennedy, Palmer, Academic Press, 1993 Thomson’s Special Veterinary Pathology, Mosby, 2000 Applied Veterinary Histology, Banks WJ. Williams Wilkins second ed. 1986 Correo electrónico: lopez@upei.ca Pagina Web: http://people.upei.ca/lopez/ MORFOFISIOLOGIA Para facilitar la comprensión de la fisiología y patología, el sistema respiratorio se divide en tres sistemas o componentes estructurales: 1 • • • • • 2 Sistema de Conducción: Cavidad nasal Senos paranasales Laringe Tráquea Bronquios. Sistema de transición: • Bronquiolos. 3. Sistema de intercambio: • Alvéolos A parte del intercambio gaseoso, el sistema respiratorio tiene como funciones importantes la voz, regulación de temperatura, controles del pH, de la presión sanguínea, de la destoxificación, metabolismo (serotonina, epinefrina, leucotrienos), etc. Una o mas de estas funciones pueden estar alteradas como resultado de enfermedades respiratorias . FLORA NORMAL DEL APARATO RESPIRATORIO Como cualquier otra membrana mucosa que está en contacto directo con el medio ambiente, el aparato respiratorio tiene su propia flora normal bacteriana. Si se introduce un hisopo en condiciones asépticas hasta las partes profundas de la cavidad nasal y se siembra en medios de cultivo apropiados, diferentes géneros y especies de bacteria crecerán abundantemente. Esta población mixta de microorganismos constituye la flora nasal bacteriana el aparato respiratorio. La flora respiratoria está restringida únicamente a la porción proximal del sistema de conducción (cavidad nasal, nasofaringe y laringe) mientras que las porciones distales del sistema de conducción (traquea y bronquios), el sistema de transición (bronquiolos) y el sistema de intercambio (alvéolos) son membranas esencialmente estériles. Los tipos de bacterias (aerobias y anaerobias) presentes en la flora nasal varían considerablemente en las especies animales, así como también, varían de acuerdo al medio ambiente en el que se crían los animales. Es importante destacar que ciertas bacterias de la flora normal son capaces de producir severas infecciones respiratorias. Por ejemplo, Pasteurella multocida es un habitante de la mucosa nasal normal de los porcinos pero también es el agente infeccioso causante de neumonía en cerdos. Estudios experimentales en animales domésticos y de laboratorio han demostrado que las bacterias de la flora nasal son acarreadas constantemente a los pulmones en el aire inspirado. Los pulmones permanecen estériles gracias a sus eficientes mecanismos de defensa a pesar de este constante acarreo de bacterias en el aire inspirado. MECANISMOS DE DEFENSA DEL APARATO RESPIRATORIO El sistema respiratorio está constantemente bombardeado por partículas (microorganismos, polvo, fibras), gases tóxicos (SO2, NO2, H2S, ozono) y vapores (amoniaco, formaldehído, acetona, gasolina). En condiciones normales, los gases inhalados son destoxificados, las toxinas son neutralizadas; las partículas son atrapadas y eliminadas, y los microorganismos son atrapados, destruidos y eliminados. Cada región anatómica-histológica del aparato respiratorio tiene su propio mecanismo de defensa. En otras palabras, el sistema de conducción (de nariz a bronquios), sistema de transición (bronquiolos) y sistema de intercambio (alvéolos) tiene cada uno un mecanismo diferente de defensa. • Sistema de Conducción (Conchas nasales, traquea, bronquios). La carpeta mucociliar es el principal mecanismo de defensa del sistema de conducción, que incluye desde las fosas nasales hasta los bronquios. Todas estas estructuras están recubiertas por la llamada carpeta mucociliar (escalera mucociliar). Esta carpetaestá formada por el epitelio pseudo-estratificado ciliar y las secreciones de las células caliciformes (moco). Cada célula ciliar del sistema de conducción tiene alrededor de 250 cilios los cuales producen alrededor de mil pulsaciones por minuto (1,000/minuto) con un movimiento longitudinal promedio de 20 mm por minuto. Existen mecanismos auxiliares que facilitan el atrapamiento de partículas, vapores y gases por la carpeta mucociliar. Por ejemplo, la generación de turbulencias de aire dentro de la cavidad nasal hace que las partículas mayores de 10 μm sean atrapadas en el moco que recubre las conchas (cornetes) nasales. Las partículas de tamaño entre 3-10μm son atrapadas principalmente en las bifurcaciones de los bronquios en donde se originan fuerzas centrifugas en al aire inspirado al cambiar su dirección súbitamente. En síntesis, las partículas suspendidas en el aire de un tamaño de 3-10 μm son atrapadas en le moco de la carpeta mucociliar (deposición) y de aquí son rápidamente eliminadas por el movimiento del moco hacia la faringe en donde son finalmente deglutidas. El moco que recubre la carpeta mucociliar juega también un papel preponderante y muchas veces ignorado en los mecanismos de defensa en contra de gases tóxicos. Algunos de estos gases (hidrosolubles) se disuelven en el moco reduciéndose de esta manera la concentración tóxica del gas que llega a las partes profundas del pulmón. La IgA es la inmunoglobulina más abundante en el moco y una de sus funciones principales es inhibir la adherencia de patógenos a las células ciliadas. • Sistema de transición (bronquiolos). Sólo aquellas partículas de tamaño menor a las dos micras (<2μ) logran penetrar hasta los bronquiolos y alvéolos. En estas regiones profundas del pulmón, las partículas pequeñas se depositan en la membrana respiratoria mediante sedimentación o movimiento browniano. Los mecanismos de defensa de los bronquiolos son una combinación de los encontrados en los sistemas de conducción y de intercambio, mas secreciones locales principalmente producidas por las llamadas células Clara. • Sistema de intercambio (alvéolos). Los alvéolos carecen de cilios y moco por lo que en esta región pulmonar tiene un mecanismo de defensa especializado para protegerse de las partículas y patógenos inhalados. El principal mecanismo de defensa en el alveolo lo constituyen los macrófagos alveolares. Estas células altamente fagocíticas se originan en la médula ósea de donde pasa a la sangre como monocitos sanguíneos para después llegar al pulmón en donde pasan un tiempo de “maduración” en el intersticio pulmonar. Durante el transito en el intersticio pulmonar adquieren la capacidad de fagocitar en un medio aeróbico. El número de macrófagos alveolares es proporcional al número de partículas respirables que llegan al pulmón; o sea que en un animal expuesto a un número mas alto de partículas tendrá mayor número de macrófagos en los alvéolos. La IgG / IgM son las inmunoglobulina preponderantes en las secreciones alveolares y estos anticuerpos juegan un papel importante en la opsonización y fagocitosis por macrófagos alveolares. Las secreciones alveolares, particularmente el surfactante producido por los neumocitos tipo II, también contienen substancias que favorecen la fagocitosis y actúan como antioxidantes para previenen daño celular causado por el estrés oxidativo. En conjunto, los mecanismos de defensa del aparato respiratorio son extremadamente eficientes en atrapar, destruir, eliminar, detoxificar agentes patógenos y gases tóxicos. Estudios experimentales con aerosoles han mostrado que en condiciones normales es posible someter animales a dosis masivas de bacterias patógenas (3x106 bacterias/gr de pulmón) sin que estas logren colonizar el pulmón y causar enfermedad. Sin embargo, cuando estos mecanismos de defensa son deprimidos, las bacterias inhaladas colonizan fácilmente el pulmón causando infecciones respiratorias. De la misma manera, cuando gases, vapores o partículas tóxicas y agentes oxidantes sobrepasan los mecanismos de defensa, las células pulmonares son fácilmente daZadas causando considerables alteraciones pulmonares. Entre los factores externos que mas frecuentes inhiben los mecanismos de defensa figuran las infecciones virales, el edema pulmonar, uremia, alcohol, amoniaco, deshidratación y estrés entre otros muchos. Por lo extenso del tema, no es posible discutir en detalle cada factor que está involucrado en la depresión de los mecanismos de defensa del pulmón. Solo se utilizará a las infecciones virales como un ejemplo característico de estos mecanismos inhibidores de las defensas pulmonares. Durante años se ha reportado que en algunas de las epidemias de influenza muchas personas pueden morir de neumonía secundaria bacteriana. Esto mismo sucede en animales domésticos durante brotes de infecciones virales respiratorias como influenza porcina, PRRS (Síndrome Disgenésico y Porcino) y Circovirus porcino-2 (PCV-2), virus de la peste porcina clásica y pseudo-rabia entre otros muchos. Estudios experimentales con aerosoles han demostrado que las curvas de eliminación bacteriana están notablemente reducidas de 5 a 7 días después de una infección viral. Una vez deprimidos los mecanismos de defensa, bacterias presentes en la flora nasal o en le medio ambiente fácilmente colonizan el pulmón. Las infecciones mixtas virales y bacterianas se presentan frecuentemente como resultado del llamado sinergismo virus-bacteria. Mediante este las lesiones pulmonares son mucho mas severas que la simple suma de las lesiones causadas por cada uno de estos organismos. Es importante enfatizar que la mayoría de las infecciones virales respiratorias solo causan una una “bronconeumonía intersticial” leve, transitoria y raramente fatal. Por razones todavía obscuras sólo algunos animales mueren debido a la infección viral primaria. La mayoría de los animales mueren de una neumonía bacteriana secundaria El edema pulmonar es otro factor importante que deprime los mecanismos de defensa y predisponen al pulmón a infecciones bacterianas secundarias. La deshidratación también produce alteraciones importantes en los mecanismos de defensa del pulmón. Se ha postulado que un aumento en la viscosidad del moco en animales deshidratados (diarreas, vómito) interfiere con el movimiento de la carpeta mucociliar. De la misma forma, se conoce que la uremia puede predisponer a perros y gatos a neumonías bacterianas secundarias. Otros factores importantes incluyen a la anestesia, hipoxia, acidosis y estrés. EXAMEN DEL APARATO RESPIRATORIO EN LA NECROPSIA La cavidad nasal se puede evaluar mediante cortes transversales o longitudinales; la laringe, tráquea y bronquios deben ser abiertos longitudinalmente con cuchillos o tijeras. La mucosa debe ser cuidadosamente observada para determinar la presencia de exudados, parásitos, erosiones, úlceras, o presencia de fluido, espuma, material aspirado, etc. La presión negativa en la cavidad torácica se investiga mediante una punción del diafragma antes de haberse abierto el tórax. Observar la retracción del diafragma y escuchar el silbido ocasionado al entrar el aire a la cavidad torácica son dos elementos que permiten establecer la existencia de presión negativa en el tórax. La falta de retracción diafragmática indica lesiones pulmonares (inflamación, edema, enfisema) empiema pleural, etc. En ausencia de estas lesiones, la falta de retracción del diafragma es indicativa de neumotórax. Observar y palpar los pulmones revisando la textura (elasticidad, consolidación, nódulos, crepitación). Siempre se debe incluir en el reporte de una necropsia la siguiente información 1.- La distribución de la lesión (focal, lobar, difusa, localmente extensiva). 2.- La magnitud of de la lesión pulmonar expresada en forma de porcentaje (%). Por ejemplo, consolidación difusa de los lóbulos apicales, cardíacos y la parte anterior de los diafragmáticos afectando el 65% del parénquima pulmonar. Examinar los vasos sanguíneos pulmonares, investigar la posible presencia de trombos, parásitos. Inspeccionar otros órganos especialmente corazón, riñones, hígado y cerebro. Para histopatología es recomendable mandar muestras de pulmón anormal al igual que normal. No debe olvidarse que es imperativo especificar en el reporte de necropsias la magnitud de la lesión pulmonar expresada en por ciento (%). Es importante que la fijación de tejidos para histopatología sea correcta debiéndose utilizar suficiente fijado (1:10 volúmenes de tijido:formol). Se recomienda NO dejar los tejidos en formol por más de 72 horas pues esto dificulta la inmunohistoquímica. Es bueno congelar muestras de pulmón si se sospecha de infecciones virales (aislamiento de virus, anticuerpos fluorescentes). Enviar muestras frescas o refrigeradas para bacteriología cuando sea necesario. Los resultados microbiológicos siempre se deben interpretar cuidadosamente tomando en cuenta la historia clínica y los hallazgos a la necropsia; Por ejemplo, aislamientos de Pasteurellae o Mannheimia pueden ser de la flora normal. Errores de interpretación son tan frecuentes como los errores en el diagnóstico morfológico. CAVIDAD NASAL Y SENOS PARANASALES Las conchas (cornetes) se dividen anatómicamente en: i. Nasales, ii. Maxilares y iii. Etmoidales. Los espacios que existen entre las conchas son muy estrechos y de acuerdo a su posición se denominan meato dorsal medio y ventral. Las conchas están cubiertas por tres diferentes tipos de epitelio: 1. -escamoso, 2. - ciliado y 3- olfatorio. La mucosa nasal tiene también abundantes glándulas y numerosos vasos sanguíneos. Alteraciones Circulatorias Congestión, Hiperemia, y hemorragias: Congestión o hiperemia de la mucosa nasal son cambios frecuentemente observados en animales domésticos debido a la gran vascularización de estas estructuras. Estos cambios vasculares están frecuentemente asociados a timpanismo en rumiantes, toxemia, rinitis aguda, trauma, agonía (falla circulatoria), e inhalación de gases irritantes. Epistaxis (hemorragia nasal) es una secuela común a neoplasias nasales, inflamación, trauma, o presencia de cuerpo extraño. Recordar que a diferencia del aparato digestivo en el cual se puede situar aproximadamente el origen de la hemorragia de acuerdo al color de las heces fecales, en le aparato respiratorio la apariencia de la sangre es la mismas trátese de hemorragia nasal o de hemorragia pulmonar. Epistaxis se observa comúnmente en caballos con hemorragia pulmonar inducido por ejercicio, micosis de bolsas guturales, y hematomas etmoidales. Hemoptisis en ganado bovino está generalmente asociada a la ruptura de vasos pulmonares como secuela a abscesos pulmonares o casos severos de ruptura de abscesos hepáticos hacia la vena cava. Cuidadosa revisión de los vasos pulmonares durante la necropsia es necesaria para lograr determinar el origen preciso de una hemorragia pulmonar. Inflamación- Rinitis y Sinusitis Las rinitis virales son muy comunes en los animales domésticos. La mayoría de las rinitis virales son transitorias a menos que se compliquen con infecciones bacterianas secundarias. LESIONES MACROSCÓPICAS son generalmente mínimas y solo se aparecen como una hiperemia severa de la mucosa nasal. Ejemplos importantes de rinitis viral en animales domésticos incluyen: Rinotraqueitis infecciosa bovina (IBR/HVB-1), Influenza Porcina, Rinitis por cuerpos de inclusión en lechones (Virus Herpes / Cytomegalovirus), etc. Nota: Las lesiones y los estadios de reparación son prácticamente las mismas en las infecciones virales y en daño tóxico o traumático. Las lesiones en cavidad nasal, en tráquea y en bronquios son similares pues todas estas estructuras están cubiertas por el mismo tipo de epitelio (ciliar con células caliciformes). Daño crónico a la mucosa del sistema de conducción (nasal traqueal, bronquial) causa hiperplasia de las células caliciformes y abundante secreción de moco; en casos persistentes metaplasia escamosa o fibrosis con pérdida de función ciliar Rinitis y Sinusitis: Etiologías: virus, bacteria, hongos, trauma, irritantes, alergias. De acuerdo al tipo de exudado, las rinitis y sinusitis pueden ser serosas, catarrales, fibrinosas (diftéricas / fibrinonecróticas), purulentas, o granulomatosa. De acuerdo a la apariencia de la inflamación, estas pueden ser también ulcerativas, necróticas, o polipoides. Los senos paranasales tienen un drenaje deficiente y por lo tanto en casos crónicos van frecuentemente acompañadas por una notable acumulación de moco (mucocele) o exudado purulento (empiema). IMPORTANTES RINITS Y SINUSITIS BACTERIANAS, MICOTICAS Y PARASITARIAS Rinitis por Cuerpos de Inclusión: Enfermedad contagiosa común causada por un citomegalovirus (virus Herpes) la cual pasa generalmente desapercibida en la granja. Esta enfermedad causa una rinitis transitoria, con epifora (lagrimeo) en lechones menores de 2 semanas de edad. LESIONES MACROSCÓPICAS: Nada espectacular, solo hiperemia de la mucosa nasal y en algunos casos discretas estrías de exudado. HISTOPATOLOGÍA: Necrosis del epitelio, infamación, pero lo más notable es una megalocitosis con prominentes inclusiones intranucleares. No hay mortalidad excepto en lechones inmunosuprimidos los cuales desarrollan un infección diseminada casi siempre fatal. En estos casos los cuerpos de inclusión están presentes en la mayoría de los órganos internos (riñón, hígado, cerebro. etc.) Rinitis Atrófica: Enfermedad muy importante de los porcinos con distribución mundial. La etiología es todavía de motivo de controversia: ¿bacteriana? (Pasteurella multocida, Bordetella bronchiseptica , Mycoplasma spp); viral? (rinitis por cuerpos de inclusión); nutricional (Vitamina D, Calcio, Fósforo); ¿Genética?; ¿Medio ambiental (humedad, temperatura, etc.)? La literatura actual sugiere que la rinitis atrófica es una infección mixta con cepas toxigénicas de Pasteurella multocida y de Bordetella bronchiseptica. El verdadero efecto de la rinitis atrófica en la tasa de crecimiento del cerdo y en la prevalencia de neumonías es todavía tema de discusión. La revisión de la cavidad nasal durante el examen postmortem se lleva a cabo mediante un corte transversal a nivel del 1er y 2ndo premolares; LESIONES MACROSCÓPICAS: Atrofia progresiva de las conchas con varios grados de severidad lo cual puede causar ensanchamiento de los meatos nasales. Hay poco o nada de exudado en la cavidad nasal. En casos severos se presenta una marcada deformación facial. Rinitis Necrótica (nariz de toro): Enfermedad esporádica en cerdos causada por Fusobacterium necrophorum. Siempre es una infección secundaria precedida por trauma, periodontitis, etc. LESIONES MACROSCÓPICAS: Rinitis y osteomielitis necrótica la cual ocasiona una deformidad marcada de los huesos nasales (Inflamación crónica proliferativa). ENFERMEDADES NEOPLASTICAS DE LA CAVIDAD NASAL Y SENUS PARANASALES Aspectos Generales: Las neoplasias de la cavidad nasal son generalmente raras en cerdos. Laringitis Necrótica (difteria de los terneros y lechones): Importante infección secundaria causada por Fusobacterium necrophorum la cual generalmente es precedida por trauma o infección viral en la mucosa de la laringe como en el caso de IBR o excesiva vocalización. La patogénesis es similar a la necrobacilosis oral. LESIONES: Exuberantes placas de exudado fibrino-necrótico con ulceración de la mucosa. El exudado a veces es aspirado por el becerro causando una neumonía por aspiración o la infección puede diseminarse causando toxemia o fusobacteremia. TRAQUEA Y BRONQUIOS Aspectos Generales: La tráquea está formada por cartílago hialino y cubierta por epitelio respiratorio ciliado (pseudoestratificado ciliar + células serosas y caliciformes). Superficialmente, la mucosa traqueal tiene una doble capa de moco. La submucosa esta altamente vascularizada y contiene numerosas glándulas túbuloalveolares. PULMONES Aspectos Generales: Existen notables diferencias en la morfología pulmonar entre las diferentes especies de animales domésticos. Los equinos por ejemplo, tienen lóbulos pulmonares muy poco definidos en comparación a los bovinos y a los caninos. ! Lóbulos Pulmonares se dividen en: lóbulos craneales (antes denominados apicales), lóbulos medios (antes denominados cardíacos / intermedios y los lóbulos caudales (antes denominados diafragmáticos). ! Lobulillos Pulmonares son pequeñas separaciones en el pulmón delineadas por tejido conectivo (septos interlobulillares). Estos lobulillos son particularmente notables en los bovinos y cerdos; poco definidos en equinos, y en los humanos; ausentes en perros y gatos. Histología Normal del Pulmón: Bronquios (cartílago), bronquiolos (sin cartílago), alvéolos. El epitelio pseudo estratificado gradualmente baja en altura y pierde los cilios en los bronquiolos. La pared alveolar está recubierta por una capa celular muy fina formada por los neumocitos tipo 1 (membranosos); los neumocitos tipo 2 (granulares) están interpuestos esporádicamente entre los neumocitos tipo 1. Los neumocitos tipo 2 son de forma cuboidal, sintetizan y secretan un fosfolípido importante llamado surfactante pulmonar. La barrera neumo-hemática (aire-sangre [blood-air barrier]) está formada por tres capas en forma de sándwich (emparedado): 1.2.3.- Endotelio Vascular Membrana Basal Neumocitos tipo 1. Los pulmones contienen abundantes vasos linfáticos y tejido linfoide asociado a las paredes de bronquios (BALT) y en algunos casos a los grandes vasos sanguíneos (manojos broncovasculares). Los espacio broncoalveolares contienen células libres en aproximadamente la siguiente proporción: Macrófagos .90%; linfocitos .5%; neutrófilos .2% y el .3 de otras células. Las células del espacio broncoalveolar pueden recolectar fácilmente mediante el uso del lavado broncoalveolar (lavado transtraqueal). Alteraciones en los valores absolutos, relativos y en la citomorfología son de gran utilidad en el diagnóstico de enfermedades respiratorias. Anomalías Congénitas de los Pulmones: Las anomalías congénitas de pulmón son raras como por ejemplo la hipoplasia o hamartoma pulmonar. La melanosis pulmonar es un hallazgo incidental en el cual no hay cambio en la textura del pulmón. ALTERACIONES CIRCULATORIAS Hiperemia (activa): Se ve generalmente en pulmones con inflamación (p.e daño pulmonar 6 mediadores de la inflamación 6 vasodilatación + exudación). LESIONES: los pulmones toman un color rojo intenso. Congestión (acumulación pasiva de sangre): Está generalmente asociada a falla cardiaca congestiva (lado izquierdo, no-compensada). Puede progresar a edema pulmonar con hemorragias intra-alveolares lo cual resulta en eritrofagocitosis ("células de falla cardiaca"). LESIONES: “Pulmones húmedos" con focos de decoloración. Hemorragia Pulmonar: Causas comunes de hemorragia en los pulmones incluyen: Falla cardiaca congestiva (ver congestión), trauma (penetración o laceración pulmonar), coagulopatías (p.e intoxicación con dicumarol), trombo embolismos pulmonares (p.e. septicemias, Coagulación Diseminada Intravascular (CID), embolismos, ruptura de vasos sanguíneos (p.e. aneurismas pulmonares). Hemorragia pulmonar 6 siderófagos + elimincaión de eritrocytoos y siderófagos mediante el escalador mucociliar 6 epistaxis. LESIONES: Dependiendio de la magnitud, las hemorragias varían de petequiales a focales, a áreas localmente extensivas de coloración rojiza. Una forma especial de hemorragia pulmonar en caballos es la llamada ("Hemorragia Pulmonar Inducida por Ejercicio".) Tromboembolismos pulmonares: Raramente tiene importancia clínica. Causas comunes de tromboembolismos pulmonares incluyen: endocarditis (lado derecho del corazón). Infartos Pulmonares son muy raros debido a la doble circulación del pulmón (pulmonar y bronquial) y por regla general no son fatales. LESIONES: Muy pocas veces se encuentran en la necropsia pero aparecen como focos rojo oscuro / hemorragia principalmente en los márgenes del pulmón. Edema Pulmonar: Lesión muy frecuente y algunas veces importante caracterizada por acumulación de líquido en el intersticio pulmonar o alvéolos. PATOGÉNESIS: En condiciones normales los pulmones producen trasudados (líquido bajo en proteína) el cual es absorbido por los vasos linfáticos. Si la producción de líquido excede la remoción, ya sea por exceso en producción o por falla en la absorción, el líquido se acumula causando edema pulmonar. El edema pulmonar es causa común de muerte en muchos animales, sin embargo, en algunos casos, el edema es puramente una lesión terminal que se desarrolla durante la agonía. Como en cualquier otro tejido, cambios en la ecuación de Starlyng aplican al edema pulmonar. Principales mecanismos involucrados en edema pulmonar: • Aumento en la presión hidrostática (edema pulmonar cardiogénico) Falla cardiaca, o sobre carga iatrogénica de líquidos por vía intravenosa. Falla cardiaca (no compensada) en el lado izquierdo del corazón 6 congestión pulmonar, edema, "células de falla cardiaca " en el pulmón ("edema pulmonar cardiogénico"). También puede ser el resultado de daño agudo en el sistema nervioso central 6 edema pulmonar neurogénico . El líquido edematoso en edema de tipo hidrostático tiene un bajo contenido de proteína. • Aumento en la permeabilidad capilar (edema pulmonar permeable) p.e daño a la barrera neumo-hemática (aire-sangre), gases tóxicos, alergias, inflamación, pancreatitis. El líquido edematoso en edema pulmonar de tipo permeable tiene típicamente un contenido alto de proteína. • Obstrucción de drenaje linfático (edema pulmonar obstructivo) p.e. Causas comunes incluyen neoplasia que involucren la obstrucción linfática. El líquido edematoso tiene un contenido variable de proteína. LESIONES MACROSCÓPICAS DE EDEMA PULMONAR: Espuma en la vías aéreas (bronquios y tráquea). Si no hay espuma en bronquios no se puede hacer el diagnóstico de edema pulmonar como causa de muerte. Los pulmones no colapsan al abrirse el tórax, se ven húmedos, están pesados y los espacios intersticiales están ensanchados lo que acentúa el patrón lobulillar (>bovinos, porcinos); Cuidado: el edema pulmonar agudo se puede confundir con neumonía. HISTOPATOLOGÍA: Líquido en los alvéolos, ensanchamiento de vasos linfáticos y de los septos interlobulillares. La cantidad de proteína se puede apreciar subjetivamente de acuerdo al grado de eosinofilia del líquido. Revisar las paredes de los vasos y los manojos broncovasculares. Presencia de siderófagos (células de falla cardiaca) es un hallazgo común en edema pulmonar de origen cardiogénico. A veces se requiere de tincion de azul de Prusia para evidenciar la hemosiderina en las macrófagos alveolares. ALTERACIONES EN EL INFLADO DE LOS PULMONES ATELECTASIA Expansión incompleta de los pulmones o de una porción del pulmón. Atelectasia: (del Griego atelesincompleto; ectasis-expansión). • Fetal; Atelectasia Neonatal (obstrucción de las vías aéreas al momento de nacer por obstrucción con moco, aspiración de meconeo; falta de surfactante en el Síndrome de "distress" respiratorio (enfermedad de las membranas hialinas) Este últimos síndrome es muy común en humanos mientras que en animales es relativamente raro (potros>lechones>otros). LESIONES MACROSCÓPICAS: Falta de distensión alveolar en forma de "parches". • Atelectasia adquirida: Compresiva, Obstructiva. LESIONES MACRORSCÓPICAS: pulmón colapsado, obscuro en color, firme en textura. La atalectasia comúnmente es confundida con neumonía, aunque desde luego, atelecatasia y neumonías tienden a presentarse juntas (causa-efecto). HISTOPATOLOGÍA: alvéolos colapsados (paredes alveolares en forma paralela), pérdida de espacio alveolar. Atelectasia A. Alvéolo normal. B. Atelectasia alveolar por obstrucción de vías aéreas. Causas comunes de obstrucción son meconeo, exudado, parásitos o cualquier material aspirado. C. Atelectasia por compresión. Note compresión de las paredes alveolares causando colapso alveolar. Abscesos, neoplasias, efusiones plurales son varias de las causas mas comunes de atelectasia por compresión. Enfisema Pulmonar Ensanchamiento anormal y permanente de los espacios aéreos distales a los bronquiolos terminales con destrucción de las paredes alveolares.0 Enfisema primario es muy raro en animales pero muy importante en humanos. La clasificación de enfisema en medicina humana (centriacinar, paracinar, paraseptal) no se utiliza en medicina veterinaria. Los tipos de enfisema pulmonar más comunes en los animales domésticos son: • Enfisema Alveolar. Este tipo de enfisema es difícil de evaluar en casos leves pues requiere de técnicas especiales como lo el de sellar la tráquea e inyectar los pulmones intravenosamente con fijador. Ejemplo de enfisema alveolar se ve en caballos con Enfermedad Crónica Obstructiva Pulmonar (Heaves COPD). Este padecimiento es raro en cerdos. • Enfisema Intersticial. Este tipo de enfisema es muy común en bovinos y en menor grado en cerdos. Se presenta un ensanchamiento por gas de los septos interlobulillares y espacios sub-pleurales. Este tipo de enfisema es causado posiblemente por movimientos respiratorios violentos (asfixia) en especies con muy poca ventilación colateral (comunicación entre lobulillos pulmonares) como son los cerdos y lo bovinos. • Bulla enfisematosa: Acumulaciones grandes y focales de gas (aire) en los pulmones (bullas). PATOGÉNESIS DE ENFISEMA PULMONAR: Durante mucho tiempo se pensó que el enfisema pulmonar se originaba principalmente cuando había obstrucción de las vías aéreas. Estudios recientes han revelado que el enfisema alveolar en humanos se debe a los efectos de enzimas proteolíticas (elastasas) liberadas por células fagocíticas en la región terminal de los bronquiolos y en los alvéolos pulmonares. Todavía se desconoce si lo mismo ocurre en animales como por ejemplo en caballos con Enfermedad Crónica Obstructiva Pulmonar (Heaves COPD), daño tóxico pulmonar, inflamación (bronquiolitis), etc. Al igual que edema pulmonar, enfisema pulmonar puede desarrollarse durante la agonía cuando los animales inspiran violentamente tratando de corregir estado hipoxémicos que preceden a la muerte. NEUMONIAS No existe una clasificación universal de neumonías en medicina veterinaria. Los méritos de una razonable clasificación de neumonías equivalen a su utilidad en la práctica rutinaria de la medicina veterinaria. Una clasificación basada en el tipo y localización del exudado permite predecir con cierto grado de confiabilidad (pocas excepciones) la ruta de entrada de los patógenos, su posible patogénesis y la etiología más probable. En base al tipo y localización del exudado las neumonías de los animales domésticos se clasifican en las siguientes cinco categorías: 1.- Bronconeumonías supurativas 2.- Bronconeumonías Fibrinosas 3.- Neumonías Intersticiales 4.- Neumonías Embólicas 5.- Neumonías Granulomatosas. Tomar nota que dos o más tipos de neumonías pueden coexistir en el mismo animal. Bronconeumonía Supurativa La bronconeumonía supurativa también se conoce con los nombres de bronconeumonía y neumonía lobulillar. Tiene siempre una distribución cranioventral y la textura del pulmón afectado (consolidado) es firme. La puerta de entrada de patógenos causantes de este tipo de neumonía es aerógena y es generalmente causada por bacterias o micoplasmas que producen un daZo moderado a los pulmones. Como ejemplo de estos microorganismos figuran la Pasteurella multocida, Actinomyces pyogenes, Bordetella bronchiseptica, Mycoplasma hyopneumoniae). Se considera que para que un animal muera por bronconeumonía supurativa es necesario que por lo menos el 60% de los pulmones estén afectados. LESIONES MACROSCÓPICAS: El pulmón afectado esta consolidado, tiene una apariencia lobulillar acentuada y el color varía de rojo intenso en casos agudos (hiperemia) a gris en casos crónicos (inflamación, atelectasia, fibrosis). Típicamente, los bronquios contienen exudado purulento el cual es fácilmente visible al comprimir el parénquima pulmonar. En los casos mas crónicos, el exudado se vuelve mas mucoide debido a la hiperplasia de células caliciformes. HISTOPATOLOGÍA: Gran número de neutrófilos en los espacios broncoalveolares (forma aguda) 6 mezcla de neutrófilos, macrófagos alveolares y moco (forma crónica). Ejemplos de enfermedades que se manifiestan típicamente como una bronconeumonía supurativa figuran las neumonías enzoóticas de los cerdos, becerros y corderos. Secuelas comunes de bronconeumonía supurativa incluyen abscesos pulmonares y bronquiectasia. Bronquiectasia es la dilatación permanente de un bronquio debido a la destrucción de sus paredes por el proceso inflamatorio. Bronconeumonía Fibrinosa La Bronconeumonía fibrinosa también se conoce con los nombres de pleuroneumonía o neumonía lobar. La distribución en este tipo de neumonía es generalmente Cranioventral aunque existen algunas raras excepciones.1 La textura del pulmón afectado varía es de firme a dura. La puerta de entrada es aerógena y es causada por agentes que producen un daZo severo al pulmón. Como ejemplo de este tipo de microorganismos figuran la P. hFmolytica en bovinos y el Actinobacillus pleuropneumoniae en cerdos. Algunos autores consideran a la bronconeumonía fibrinosa como una forma peraguda, severa y generalmente fatal de bronconeumonía supurativa. La muerte puede ocurrir cuando hay 50% o menos de pulmón afectado. Las bronconeumonías fibrinosas van generalmente acompañadas de una toxemia severa debido a toxinas bacterianas y a la severidad de la necrosis del tejido pulmonar. LESIONES MACROSCÓPICAS: Siempre existe una efusión pleural, presencia de fibrina sobre las superficies pleurales (apariencia de vidrio molido en casos agudos), en superficie de corte el pulmón afectado muestra frecuentemente áreas irregulares de necrosis. Los animales que sobreviven la fase aguda de la bronconeumonía fibrinosa desarrollan secuestros pulmonares los cuales consisten en grandes áreas de tejido necrótico rodeado de tejido conectivo y de granulación. HISTOPATOLOGÍA: Ensanchamiento notable de los septos interlobulillares debido a dilatación y trombosis de los vasos linfáticos; perdida total de los espacios aéreos debido a una exudación exuberante de fibrina, neutrófilos hacia el lumen de los bronquios, bronquiolos y alvéolos. Frecuentes se presentan áreas de necrosis coagulativa rodeadas de un anillo de leucocitos. La pleura esta marcadamente engrosada debido a la infiltración de células inflamatorias. Ejemplos de enfermedades que se manifiestan con una bronconeumonía fibrinosa figuran: Fiebre de Embarque, pleuroneumonía porcina, pleuroneumonía contagiosa bovina. Secuelas comunes de bronconeumonía fibrinosa incluyen secuestros pulmonares, gangrena o adhesiones pleurales. Secuestros pulmonares son grandes porciones necróticas del parénquima pulmonar que están aisladas del resto del pulmón viable por tejido de granulación. Neumonía Intersticial Las neumonías intersticiales también se conocen con el nombre de neumonitis:2 La distribución las neumonías intersticiales es difusa y su textura es típicamente elástica. Los cambios de color y textura son muchas veces poco marcados y difíciles de diagnosticar a la necropsia requiriendo de histopatología para su confirmación. Las neumonías intersticiales van frecuentemente acompañadas de edema, enfisema o bronconeumonía, estas últimas se conocen como neumonías broncointersticiales . La puerta de entrada puede ser hematógena (septicemias, viremias, toxinas en sangre) o aerógena ("air-borne virus" > alergenos, > inhalación de tóxicos). LESIONES MACROSCÓPICAS: Los pulmones no colapsan cuando se abre la cavidad toráxica, en ocasiones se pueden ver impresiones costales en la pleura visceral. El color de los pulmones con neumonía intersticial varía de acuerdo al índice sangre:tejido y al tipos de respuesta inflamatoria, proliferación de las células pulmonares i grado de fibrosis. HISTOPATOLOGÍA: La lesión primaria está centrada en la pared alveolar, la cual siempre está engrosada debido a presencia de exudados (fibrina o leucocitos) en el intersticio alveolar y/o proliferación de los neumocitos tipo 2. Los casos crónicos de neumonía intersticial generalmente van seguidos de fibrosis alveolar. Ejemplos de enfermedades que se manifiestan con una neumonía intersticial figuran: Influenza porcina, PRRS y Circovirus porcino-2. Daño alveolar causa necrosis de neumocitos tipo 1 6 necrosis de neumocitos tipo 1 causa 6 proliferación de neumocitos tipo 2 ("fetalización/epitelización" pulmonar) 6 los neumocitos tipo 2 eventualmente se transforman en neumocitos tipo 1 6 REPARACIÓN o INFLAMACION y FIBROSIS. Neumonía Broncointersticial: Virus respiratorios 6 necrosis del epitelio bronquial y bronquiolar 6 bronconeumonía + daZo a neumocitos tipo I 6 necrosis y proliferación de neumocitos tipo II 6 REPARACIÓN. Este término se ha popularizado mucho entre los patólogos de Norteamérica. Neumonía Embólica Las distribución de la neumonía embólica es multifocal al azar y afectando todos lo lóbulos pulmonares. La puerta de entrada es obviamente hematógena. La patogénesis básica es la de émbolos circulantes 6 adhesión a la pared de los capilares pulmonares 6 evasión de la fagocitosis intravascular. En términos generales, los infartos pulmonares y la neumonía embólica son similares, excepto que esta última, los émbolos son generalmente sépticos. Ejemplos de enfermedades que se manifiestan con una neumonía embólica figuran: Endocarditis vegetativa (lado derecho), ruptura de abscesos hepáticos hacia la vena cava en ganado bovino, onfaloflebitis. LESIONES MACROSCÓPICAS: Número variable de focos pequeños de inflamación los cuales se ven en los casos agudos como un centro blanquecino rodeado de un halo hiperémico. Secuelas comunes de neumonía embólica incluyen abscesos pulmonares distribuidos al azar en todos los lóbulos pulmonares. HISTOPATOLOGÍA: Focos de necrosis en las paredes alveolares rodeadas de una intensa reacción inflamatoria con edema y neutrófilos en los estadios iniciales y posteriormente con macrófagos y tejido conectivo en estadios mas crónicos. Es frecuente ver en los focos de necrosis e inflamación colonias de bacterias en HE o en tinciones de Gram. Neumonía Granulomatosa Las neumonías granulomatosas pueden tener una puerta de entrada aerógena o hematógena. Las lesiones son multifocales caracterizadas por la presencia de nódulos (granulomas) pulmonares. Muy frecuentemente, las lesiones pulmonares van acompañadas por nódulos similares en otros órganos. Ejemplos de enfermedades que se manifiestan con una neumonía granulomatosa figuran: la tuberculosis, micosis sistémicas (profundas), algunos parásitos como Muellerius capillaris, Fasciola hepatica y larvas migratorias. LESIONES MACROSCÓPICAS: Nódulos firmes distribuidos en el parénquima pulmonar. Las neumonías granulomatosas pueden ser fácilmente confundidas con neoplasias requiriéndose del uso de la histopatología. HISTOPATOLOGÍA: Nódulos formados por un centro generalmente necrótico infiltrado en su periferia por macrófagos, células gigantes y finalmente rodeadas de tejido conectivo mezclado con linfocitos y células plasmáticas. Las neumonías granulomatosas son especialmente causadas por agentes que no pueden ser fácilmente eliminados a través de la fagocitosis. Ejemplos de este tipo de agentes están las micobacterias, hongos (sistémicos), huevecillos de parásitos, larvas,, etc. Aspiración de partículas vegétales es causa común de neumonía granolomatosa en cerdos conocida vulgarmente como neumonía por almidón. Es interesante notar que en el caso de las neumonías granulomatosas casi siempre es posible observar microscópicamente el agente causal. EJEMPLOS DE ENFERMEDADES ESPECÍFICAS CUASANTES DE NEUMONIAS EN CERDOS Influenza Porcina: Enfermedad altamente contagiosas, transitoria pero que puede causar bajas de defensa en el pulmón lo que resulta en neumonías secundarias causadas principalmente por Pasteurella multocida y Haemophilus parasuis. LESIONES MACROSCÓPICAS: Las lesiones a la necropsia son mínimas (traqueitis y neumonía broncointersticial) a menos que haya complicaciones bacterianas. Los pulmones pueden estar hiperémicos, edematosos, no se colapsan bien al abrir el tórax y presentan una textura algo elástica. Síndrome Disgenésico y Respiratorio Porcino (SDRP); "Aborto y falla reproductiva epidémica de los cerdos"; Debido a que este arterivirus causa infección persistente, sobre expresión de IL-10, e inmunodeficiencia adquirida en lechones y cerdos jóvenes, muchos brotes de la enfermedad se caracterizan clínicamente por un aumento inexplicable en la incidencia de diarreas, neumonías bacterianas, artritis, etc. La infección viral favorece frecuentemente la colonización por Streptococcus suis tipo II en granjas infectadas con esta bacteria. LESIONES MACROSCÓPICAS: En casos no complicados con neumonías secundarias las lesiones a la necropsia consisten en una neumonía intersticial. El pulmón muestra hiperemia, tiene textura elástica y no colapsa al abrirse el tórax. Esta lesión no es específica y no puede diferenciarse fácilmente de otras infecciones respiratorias virales como la causada por CVP-2. HISTOPATOLOGÍA: Neumonía intersticial sin cuerpos de inclusión caracterizada por un engrosamiento simple de los septos alveolares con o sin proliferación de neumocitos tipo II. Muy frecuentemente se ven lesiones de Pneumocystis carinii caracterizadas por la presencia de un material espumoso y puntiforme en los alvéolos. El diagnóstico concluyente requiere de aislamientos o histoquímica. Los tejidos no deben dejarse en formol por mucho tiempo pues disminuye la detección del virus por histoquímica. En ocasiones frecuentes el virus de SDRP se encuentra en combinación con otros virus como CVP-2 o el de pseudo rabia. Síndrome de emaciación postdestete (Circovirus porcino-2). Este síndrome fue descrito por primera vez en Canadá y EU y posteriormente un otros países. . El PCV-2 se considera como el agente viral responsable de este síndrome y causante de una depresión del sistema inmune de los cerdos. Recientemente se ha asociado este agente a un nuevo problema en granjas porcinas conocido como Síndrome de dermatitis y nefropatía porcina. LESIONES MACROSCÓPICAS: Los cerdos afectados muestran una pobre ganancia en peso y en los casos más severos una franca emaciación con atrofia nutricional de la grasa y del músculo. Algunos cerdos muestran ictericia. Las lesiones consisten y neumonía intersticial caracterizada por falta de colapso, impresiones costales, textura elástica y en algunos casos edema. Característico también es la presencia de una linfadenomegalia generalizada. HISTOPATOLOGÍA. Neumonía intersticial o broncointersitical caracterizada por engrosamiento de los septos, necrosis y exfoliación del epitelio bronquiolar, y proliferación de células mononucleares en la BALT, submucosa y manojos bronco-vasculares. El tejido linfoide se caracteriza por una depleción marcada de linfocitos y proliferación de macrófagos (histiocitos). Afortunadamente para los patólogos, cerdos afectados por CP-2 muestran con frecuencia típicas inclusiones en el citoplasma de las células mononucleares de los ganglios linfáticos, placas de Peyer en intestino y con menos frecuencia en el tejido linfoide del pulmón. Estos cuerpos de inclusión son parecidos a racimos anfofílicos de uvas. Confirmación puede hacerse por detección in situ del CP-2. El Síndrome de dermatitis y nefropatía porcina se caracteriza por una vasculitis linofo-histiocitica en piel, ganglios linfáticos, bazo, hígado, al igual que una glomerulopatia fibrinoide necrosante muy marcada. Los túbulos renales están repletos de cilindros hialinos. Neumonía Enzoótica Porcina. Esta es una enfermedad multifactorial de cerdos jóvenes de alta morbilidad pero baja mortalidad. Aunque es causada por el Mycoplasma hyopneumoniae 1, otros factores predisponentes como la temperatura, humedad, hacinamiento, concentraciones de amoníaco y estrés juegan un papel muy importante en su epidemiología y patogénesis. Muy comunmente va acompaZada por infecciones secundarias de P. multocida, Haemophilus spp, A. pyogenes, Mycoplasma hyorhinis, etc). LESIONES MACROSCÓPICAS: Bronconuemonía supurativa crónica con hiperplasia marcada del tejido linfoide peribronquial. Al comprimir el pulmón consolidad sale exudado mucopurulento por los bronquios. En los casos más crónicos, el pulmón afectado tiene la apariencia de carne de pescado (gris-pálido). HISTOPATOLOGÍA: Engrosamiento moderado de los septos con abundantes neutrófilos y macrófagos en los espacios broncoelveolares. Confirmación del diagnostico requiere aislamiento o detección in situ del M. hyopneumonae. Pleuroneumonía Porcina. Esta enfermedad contagiosa es causada por Actinobacillus (Haemophilus) pleuropneumoniae. Este es un patógeno primario que entra la pulmón por vía aerógena y causa un neumonía fibrinosa. LESIONES MACROSCÓPICAS: esta bronconeumonía fibrinosa puede tener una distribución cranioventral (unilateral o bilateral). Con mucha frecuencia esta neumonía tiene con una distribución dorsocaudal en la cual aparecen las áreas afectadas como grandes "chipotes" de color rojizo. A la superficie de corte se pueden ver áreas de necrosis rodeadas por un anillos blanquecino. HISTOPATOLOGÍA: idéntica a la pasteurelosis neumónica de los bovinos incluyendo las llamadas "células de avena." Los cerdos que sobreviven a la fase aguda desarrollan grandes secuestros pulmonares y adhesiones pleurales. Estos cerdos también tienden a tener muy poco rendimiento en cuanto a ganancias de peso. Aunque muchos porcicultores utilizan las vacunas contra A. pleuropneumoniae, su eficacia está por ser evaluada en "condiciones de campo." Pasteurelosis Neumónica en Cerdos: Infección secundaria causada por P. multocida.2 LESIONES: En algunos casos produce un bronconeumonía fibrinosa peraguda y mortal, en otros, produce solo una bronconeumonía crónica supurativa. Streptococcus suis tipo II: Esta es una enfermedad zoonótica de mucha importancia en la porcicultura de E.U. y Canadá (Chile?). Tiene varias presentaciones: neonatal septicemia, meningitis, artritis, poliserositis, necrosis del miocardio,3 endocarditis, aborto y neumonía. LESIONES: No-específicas frecuentemente combinadas con las de otros patógenos. En los pulmones se puede presentar una bronconeumonía fibrinosa o supurativa o neumonía embólica en casos de endocarditis vegetativa. CAVIDAD TORACICA Neumotórax: Aire en la cavidad torácica; trauma, iatrogénico (p.e. biopsia), ruptura de bullas enfisematosas o ruptura de esófago (gas en el mediastino). LESIONES MACROSCÓPICAS: Falta de retracción del diafragma, atelectasia, neumomediastino. Hidrotórax: Trasudado (líquido seroso) en cavidad torácica. Causas comunes de hidrotórax incluyen la falla cardiaca congestiva, hipoproteinemia (enfermedades del hígado, riñón, intestino, inanición) y obstrucción linfática. LESIONES: Líquido en la cavidad abdominal (los trasudados deben diferenciarse de exudados). La presencia de trasudados no inflamatorios en la cavidad abdominal causa irritación de las serosas y eventualmente cierto grado de inflamación y fibrosis. Hemotórax: Sangre en la cavidad torácica. Causas comunes incluyen trauma, heridas penetrantes, ruptura de vasos sanguíneos (aneurismas), coagulopatias, etc. Quilotórax: Linfa en la cavidad torácica; ruptura de vasos linfáticos (ductos linfático); trauma, iatrogénico (cirugía), neoplasias, idiopático (perros y gatos). LESIONES: Líquido lechosos en cavidad. Análisis de este líquido revela gran cantidad de triglicéridos. Pleuritis (pleuresía): Inflamación de la pleura. Las pleuritis pueden existir sola en combinación con neumonía (p.e. neumonía fibrinosa/pleuroneumonía). Dependiendo del exudado las pleuritis se clasifican en: purulentas (empiema , piotórax), fibrinosas, granulomatosas. Pleuritis aguda 6 adhesiones de tejido conectivo. Microbiología es usualmente necesaria para determinar la etiología precisa. En cerdos pleuritis (sin neumonía) ha sido asociada a P. multocida. Otra forma específica de pleuritis piogranulomatosa con gránulos de azufre ocurre en infecciones por Nocardia asteroides. ENFERMEDADES NEOPLASTICAS DE LOS PULMONES Aspectos Generales: (Solo se mencionan generalidades. Para mayores detalles consultar libros especializados (Meuten,. Tumors in Domestic Animals, 2002) Tumores primarios en los animales domésticos son raros (comunes en humanos > perros, gatos, > otras especies); pueden originarse a partir de cualquier línea celular del pulmón (carcinomas > sarcomas); generalmente aparecen como un nódulo o masa solitaria, con o sin metástasis a otros tejidos o al mismo pulmón. Mesotelioma:1 Raro tumor de las membranas serosas (mesotelio) el cual se disemina rápidamente por medio de implantación tumoral. LESIONES: arborescencias múltiples involucrando las superficies serosas. Histopatología y citología se requieren para su confirmación. Tumores Secundarios Metastáticos en el Pulmón: Osteo/condro/fibro/hemangio/linfo-sarcomas; melanomas, varios carcinomas ( uterinos, renales, etc). FIN 0 Sobre inflado sin destrucción de los alvéolos se conoce como hiperinflación en lugar de enfisema. 1 2 La infección por Actinobacillus pleuropneumoniae en cerdos puede producir una bronconeumonía fibrinosa sin distribución cranioventral. Para mas detalles leer: Pathology of Domestic Animals, Jubb, Kennedy, Palmer eds. Third edition, Volume 2, 1993, páginas 460-470. 1 Muy pocos laboratorios pueden cultivar esta bacteria ("fastidiosa"). 2 Mannheimia haemolytica no produce neumonías en cerdos pero está asociada a abortos. 3 Las lesiones son similares al Corazón de Mora. 1 En humanos está asociada con asbestosis.