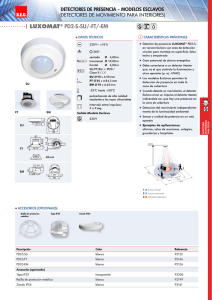
Pituophis deppei deppei
Anuncio

UNIVERSIDAD VERACRUZANA FACULTAD DE MEDICINA VETERINARIA Y ZOOTECNIA Identificación morfológica de células sanguíneas del Cincuate (Pituophis deppei deppei) mantenido en cautiverio en el Estado de Puebla TRABAJO RECEPCIONAL EN LA MODALIDAD DE: TESINA COMO REQUISITO PARCIAL PARA OBTENER EL TÍTULO DE MÉDICO VETERINARIO ZOOTECNISTA PRESENTA: JOSÉ FERNANDO AGUILERA GONZÁLEZ ASESOR: MVZ Edgar Reina Ponce VERACRUZ, VER. AGOSTO 2011 ÍNDICE GENERAL RESUMEN…………………………………………………………………………………... ix I. INTRODUCCIÓN………………………………………………………………………….... 10 1.1. Ubicación Taxonómica…………………………………………………...…………….. 11 1.2. Descripción de la Especie……………………………………………...………………. 11 1.3. Distribución………………………………………………………………………………. 13 1.4. Estado Actual…………………………………………………………………………….. 14 II. ANTECEDENTES…………………………………………………………………....…… 15 III. JUSTIFICACIÓN………………………………………………………………………….. 16 IV. OBJETIVOS……………………………………………………………………………...... 17 4.1. Objetivo General…………………………………………………………………………. 17 4.2. Objetivo Específico……………………………………………………………………… 17 V. MATERIALES Y MÉTODOS…………………………………………………………..... 18 5.1. Alojamiento y parámetros ambientales……………………………………………….. 18 5.2. Manejo e inmovilización……………………………………………………………….... 19 5.3. Obtención de parámetros: morfometría, peso y sexo……………………………….. 19 5.4. Toma de muestra………………………………………………………………………... 21 5.5. Manejo de la muestra…………………………………………………………………… 21 5.6. Características de tinción……………………………………………………………… 22 5.7. Tinción Wright…………………………………………….…………………………….. 22 5.8. Análisis del Frotis Sanguíneo………………………………………………………….. 23 ii VI. RESULTADOS Y DISCUSIÒN………………………………………………………….. 24 6.1. Evaluación Citológica……….…………………………………………………………... 24 6.1.1. Características Celulares en Formato de Registro……...……………………. 25 6.2. Eritrocitos maduros, inmaduros y policromáticos…………………………….……… 27 6.3. Leucocitos……………………………………………………………………….……….. 28 6.4. Granulocitos…………………………………………………………………….……….. 28 6.4.1 .Heterófilos…………………………………………………………...…………….. 28 6.4.2. Eosinófilos……………………………………...………………………….………. 29 6.4.3. Basófilos………………………………………………………………...….……… 30 6.5. Mononucleares…………………………………………………………….………….… 30 6.5.1. Linfocitos……………………………………………………………...….……….. 30 6.5.2. Monocitos…………………………………………………………………............. 31 6.6. Trombocitos……………………………………………….………………………….… 32 VIII. LITERATURA CITADA…………………………………….…………………………..... 37 iii ÍNDICE DE CUADROS Cuadro 1. Datos morfométricos de Pituophis deppei deppei…………………………… 20 iv ÍNDICE DE FIGURAS Figura 1. Distribución potencial de Pituophis deppei deppei, P. d. jani, Pituophis lineaticollis lineaticollis……………………………………………………………………… 13 Figura 2. Áreas Potenciales de Distribución de la Herpetofauna de México. Especie: Pituophis deppei. CONABIO, 2010. Portal de Geoinformación. Sistema Nacional de Información Sobre Biodiversidad.. ………………………………………………….…….. 14 Figura 3. Terrario de exhibición…………………………………………………………... 18 Figura 4. División para iluminación y ventilación……………………………………….. 18 MONOCROMÁTICAS………………………………………………………………………. 20 Figura 5. PD1-101-2626 ♂…………………………………………………………………. 20 Figura 6. PD2-101-2632 ♀………………………………………………………………… 20 Figura 7. PD3-101-2662 ♂……………………………………………………………….... 20 Figura 8. PD4-101-2648 ♂…………………………………………………………............ 20 Figura 9. Lectura de Frotis ........................................................................................... 23 Figura 10. Distribución celular: Monocapas……………………………………………... 25 Figura 11. Distribución celular: Sábanas……………………………………………….... 25 Figura 12. Distribución celular: Aglutinadas……………………………………………... 25 Figura 13. Eritrocitos maduros…………………………………………………………….. 33 Figura 14. Eritrocito inmaduro (Rubricito basofílico) y trombocitos……………………. 33 Figura 15. Eritrocito policromático…………………………………………………….…... 33 Figura 16. Ligera anisocitosis y poikilositosis…………………………………………… 33 Figura 17. Heterófilo (PD3♂)…………………………………………………………...….. 33 Figura 18. Heterófilo (PD1♂)……………………………………………………………..... 33 Figura 19a. Eosinófilo (PD1♂)…………………………………………………………...... 33 Figura 19b. Eosinófilo (PD3♂)………………………………………………………...…... 33 Figura 20. Basófilo (PD2♂)…………………………………………………………...…..... 34 Figura 21. Linfocito (PD1♂)………………………………………………………............... 34 Figura 22. Linfocito (PD2♀.)…………………………………………………………...…... 34 Figura 23. Linfocito (PD3♂)……………………………………………………………....... 34 Figura 24. Monocito (PD1♂)……………………………………………………………….. 34 Figura 25. Azurófilo monocitoide (PD1♂)………………………………………………... 34 v Figura 26. Trombocitos (PD2♀) y eritrocito inmaduro (Rubricito)……………………. 34 Figura 27. Trombocito (PD2♀)…………………………………………………………….. 34 COLOR……………………………………………………………………………………...... 35 Figura 28. Eritrocitos maduros……………..……………………………………………… 35 Figura 29. Eritrocito inmaduro (Rubricito basofílico) y trombocitos………………...….. 35 Figura 30. Eritrocito policromático………………………………………………………… 35 Figura 31. Ligera anisocitosis y poikilositosis…………………………………………… 35 Figura 32. Heterófilo (PD3♂)……………………………………………………………..... 35 Figura 33. Heterófilo (PD1♂)………………………………………………………………. 36 Figura 34a. Eosinófilo (PD1♂)…………………………………………………………….. 36 Figura 34b. Eosinófilo (PD3♂)…………………………………………………………….. 36 Figura 35. Basófilo (PD2♂)………………………………………………………………… 36 Figura 36. Linfocito (PD1♂)………………………………………………………………... 36 Figura 37. Linfocito (PD2♀.)……………………………………………………………….. 36 Figura 38. Linfocito (PD3♂)………………………………………………………………... 36 Figura 39. Monocito (PD1♂)………………………………………………………….......... 36 Figura 40. Azurófilo monocitoide (PD1♂)……………………………………………...… 36 Figura 41. Trombocitos (PD2♀) y eritrocito inmaduro (Rubricito)……………………. 36 Figura 42. Trombocito (PD2♀)…………………………………………………………...... 36 ANEXOS Anexo 1. Medidas morfométricas de Pituophis deppei deppei consideradas en este estudio. Anexo 2. Formato: “Evaluación Citológica”. vi AGRADECIMIENTOS Sin orden de importancia, agradezco a las siguientes instituciones y personas. A la Universidad Veracruzana. Facultad de Medicina Veterinaria y Zootecnia, por brindarme una formación profesional de calidad. Especial agradecimiento a la Dra. Dora Romero Salas, por su amistad, experiencia, ejemplo de dedicación y motivación durante el proceso de formación académica. Mil gracias Doctora. A la Asociación Veterinaria de Reptiles y Anfibios A. C., por el apoyo otorgado, pero sobre todo por dejarme participar en sus actividades cotidianas. En especial al Presidente de la Asociación, MVZ Edgar Reina Ponce, así como también LAFS Orlando Reina Ponce, LAFS Juan Carlos Gómez, por su amistad y compartir sus conocimientos en el cuidado y conservación de los reptiles. A mis amigos, Anabel, Chris, Ger, Mariel, Mila, Tomy, todos ellos Médicos Veterinarios y Zootecnistas, ejemplos de esfuerzo, dedicación, profesionalismo, superación y sobre todo por compartir sus conocimientos y experiencia. A mis amigos y compañeros de generación, Alexander, Alex, Aglae, Arely, Gladys, Luis por tantas experiencias y momentos inolvidables. A mis amigos de toda la vida, Rodrigo y Esteban, gracias por sus consejos y acompañarme en las buenas y en las malas. vii DEDICATORIAS A mi Madre y Padre Graciela y Gilberto Por su amor y apoyo incondicional toda mi vida, los AMO, son motivación, ímpetu, alegría, valor, razón por la cual he convertido mis sueños realidad, este es un triunfo de Nosotros. A mis Hermanos Gabriela y Gilberto Lo hicimos hermanos, Ustedes son mi ejemplo a seguir gracias por acompañarme en esta trayectoria tan importante en mi vida, por compartir sus anhelos, logros, sueños, sonrisas y la confianza puesta en mis hombros. A mis Tíos Esperanza y Rafael Por su amor, paciencia y comprensión en mi vida estudiantil, siempre compartieron alegría, esperanza e infinidad de momentos tan felices en Veracruz. Gracias por siempre tíos. A mis Primos Berenice y Alfonso Por sus consejos, apoyo absoluto, atención enseñanzas ,risas y ganas de ser alguien en la vida. viii “La alegría de ver y entender, es el más perfecto don de la naturaleza” Albert Einstein. ix RESUMEN Aguilera González José Fernando. 2011. Identificación morfológica de células sanguíneas del Cincuate (Pituophis deppei deppei) mantenido en cautiverio en el Estado de Puebla. Tesina. Facultad de Medicina Veterinaria y Zootecnia. Universidad Veracruzana, Veracruz, Ver. México. Se llevó a cabo un estudio hematológico por medio de citología, en el mes de mayo, con número de muestra de cuatro ejemplares (N=4) clínicamente sanos de la especie Pituophis deppei deppei mantenidos en cautiverio en un encierro de 80x60x60cm, con temperatura de 24-28ºC y humedad relativa de 40-60%, pertenecientes a la colección herpetológica de la Asociación Veterinaria de Reptiles y Anfibios A. C., la contención física fue manual, la cantidad a colectar dependió del peso de cada serpiente, estimando un volumen total de sangre del 5 a 8% de peso corporal, considerando que un reptil clínicamente sano puede perder hasta un 10% sin consecuencias detrimentales (Jacobson, 2005). Inmediatamente después de la toma, se realizaron 2 o 3 frotis sanguíneos, empleando la tinción tipo Romanowsky-Wright, identificando los componentes formes y describiendo las características celulares más representativas, como son: tipo de célula a identificar, celularidad, distribución celular, tamaño, forma, citoplasma y núcleo, gránulos, radio N:C, lobulado y patrón de cromatina nuclear. Los tipos celulares descritos son: eritrocito maduro, inmaduro, policromáticos, heterófilos, basófilos, eosinófilos, linfocitos, monocitos, azurófilo y trombocitos, a cada tipo se realizó un registro fotográfico digital, generando catálogo de imágenes digitales, con propósito de futura revisión para determinar los cambios más representativos en base a las observaciones realizadas por medio de citodiagnóstico. Palabras Clave: Hematología, Pituophis deppei deppei, identificación celular, citodiagnóstico 9 I. INTRODUCCIÓN La Clase Reptilia comprende miles de especies clasificadas en cuatro Ordenes: Chelonia, Crocodylia, Lepidosauria y Rincocéfalia. En la actualidad se estima que en México existen 1627 especies de reptiles, de los cuales 581 pertenecen al orden Serpentes, con 12 Familias y 90 Géneros (Liner, 2007), debido a esto la herpetofauna mexicana está incluida en los primeros lugares a nivel mundial (CONABIO, 2009), el futuro de estos vertebrados depende en gran medida de la planificación, manejo del patrimonio natural, así como del esfuerzo que hagamos por mantenerlos en vida libre y cautiverio. Los factores más importantes a considerar para tener éxito en la conservación de estos organismos en colecciones herpetológicas, son las condiciones ambientales, medidas de bioseguridad y los cuidados Médicos Veterinarios orientados al entendimiento de indicadores fisiológicos mediante la observación sistemática en busca de signos o síndromes que revelen alguna patología, así como la toma de muestras biológicas que permiten contar con una herramienta diagnóstica proporcionando información referida al estado de salud de los animales. Uno de los primeros sistemas que deben ser examinados es el sanguíneo, tejido conjuntivo cuya matriz es líquida y sumamente especializado, cumpliendo funciones tan importantes como la respuesta inmunitaria, transporte de gases, nutrientes y eliminación de los desechos metabólicos (Jacobson, 2005). En reptiles, resulta de vital importancia la correcta evaluación del hemograma, incluyendo el frotis de sangre, ya que la morfología de los eritrocitos y leucocitos, pueden variar por estados fisiológicos (edad, sexo, estado reproductivo), nutrición, parasitosis, enfermedades inflamatorias y otros procesos patológicos o por factores ambientales (hábitat, estación del año, altitud) (Frye, 1991). En México, la hematología aplicada a reptiles, es practicada por muy pocos profesionales dedicados a la medicina herpetológica, por la escasa información referida a la morfología normal de los componentes celulares, puesto que este grupo de vertebrados, es extremadamente diverso en términos de especies, anatomía y fisiología. 10 1.1 .Ubicación Taxonómica Reino: Animalia Phylum: Cordata Clase: Reptilia Orden: Serpentes Familia: Colubridae Género: Pituophis Epíteto específico: deppei Nombre científico: Pituophis deppei Nombre del Autor: (Duméril, 1853) (Instituto de Biología. "Pituophis deppei - IBUNAM:CNAR:AR3160". UNIBIO) 2.1. Descripción de la especie Los nombres comunes con los que se conoce al Pituophis deppei deppei son, Cincuate o Alicante. Su nombre proviene del náhuatl “Cin” que significa maíz y “Coatl” que significa serpiente. El Género Pituophis, esta compuesto por cinco especies: Pituophis catenifer, once subespecies, Pituophis deppei, dos subespecies (P. d. deppei y P. d. jani), Pituophis lineaticollis, dos subespecies, Pituophis melanolecus, tres subespecies, y Pituophis ruthveni (Uetz, 2007). La especie Pituophis deppei deppei, es un ofidio endémico a México, de talla mediana, presenta una longitud promedio de 160 cm de cabeza a cola, considerándose más delgado que otras variedades pertenecientes al Género Pituophis. De hábitos diurnos y terrestres, habita en una amplia variedad de climas, desde áridos hasta templados, con una distribución en tipos de vegetación encino y pino-encino, así como en ambientes con matorral xerófilo y chaparral, en altitudes que van de 1524 a 2438 msnm. Se alimenta de vertebrados tales como roedores, crías de conejos, aves y lagartijas. Serpiente ovípara cuya reproducción es durante primavera, con una puesta a principios de verano de 4 a 24 huevos, incubando las crías en otoño (Ramírez y Arizmendi, 2004) 11 Físicamente se observa, cabeza de forma triangular ligeramente distinguida del cuerpo, pupila circular y escamado cefálico con las siguientes características: en región supracefálica, escama rostral visible desde encima, presenta dos internasales ligeramente más largas que anchas; dos prefrontales rectangulares, característica que difiere de otros miembros pertenecientes al Género Pituophis, los cuales presentan cuatro; frontal cuadrangular; supraoculares grandes y parietales de forma triangular, preocular presente, dos a cuatro postoculares, loreal constante y ligeramente alargada; ocho (a veces nueve) supralabiales, cuarta o quinta y sexta en contacto con el ojo, las suturas de las escamas labiales están marcadas de negro. Hileras de escamas dorsales (medio cuerpo) 27 con un número máximo de 31. Escamado ventral de 211 a 233 (promedio 221), caudales 52 a 79 (promedio 62), escama anal única y sin divisiones (Stull, 1940). La región dorsal del cuerpo presenta una coloración amarilla-mostaza con parches cuadrangulares negros (43 a 59) a lo largo del cuerpo, lateralmente tiene manchas intercaladas negras, pequeñas y alargadas que contrasta con las manchas dorsales del cuerpo. La región ventral es lisa de color blanco a crema (Duellman, 1960). 12 1.3. Distribución El Cincuate (Pituophis deppei), se distribuye por los Estados de Aguascalientes, Chihuahua, Coahuila, Distrito Federal, Durango, Guanajuato, Hidalgo, Jalisco, México, Michoacán, Nuevo León, Oaxaca, Puebla, San Luis Potosí, Querétaro, Veracruz y Zacatecas (Ramírez y Arizmendi, 2004) (Figura 1 y 2). Las condiciones de menor humedad producen un ambiente xerofítico, favoreciendo la distribución geográfica de un mayor número de reptiles adaptados a estas condiciones (Méndez-de la Cruz et al., 1992). Figura 1. Distribución potencial de Pituophis deppei deppei, P. d. jani, Pituophis lineaticollis lineaticollis. (Duellman, 1960). 13 Figura 2. Áreas Potenciales de Distribución de la Herpetofauna de México. Especie: Pituophis deppei. CONABIO, 2010. Portal de Geoinformación. Sistema Nacional de Información Sobre Biodiversidad. 1.4. Estado actual De acuerdo a la Norma Oficial “NOM-059-ECOL-2010” declara como “AMENAZADA” a la especie Pituophis deppei deppei, la cual coincide parcialmente con la categoría “VULNERABLE” de la clasificación de la Unión Internacional para la Conservación de la Naturaleza (IUCN). 14 II. ANTECEDENTES En México, la hematología aplicada a reptiles ha sido poco estudiada, a pesar de que se cuenta con la metodología necesaria y sólo unos cuantos reportes describen la identificación de células sanguíneas; para este estudio el trabajo más actualizado en México es el de Mendoza et al. (2011) titulado “Morfología de las células sanguíneas y perfil leucocitario de Crotalus polystictus (Cope1865)”, otros como Rossini (2010) con “Descripción morfológica de células sanguíneas para la baba (Caiman crocodilus crocodilus)” en Venezuela, Roberto et al. (2007) “Blood cell morphology of the Moorish gecko, Tarentola mauritanica” en Italia, y Carvahlo et al. (2006) “Morphological, cytochemical, and ultrastructural observations on the blood cells of the reptile Tupinambis merianae” en Argentina . La mayoría de los estudios en el País, enfatizan la importancia de perfiles hematológicos, como los realizados por Padilla (2008) cocodrilos de pantano (Crocodylus moreletii), y Mora (2003) en pero con muy poca información relacionada a la identificación de células sanguíneas. En Latinoamérica destacan los trabajos realizados por Rojas (2005) sobre “Caracterización morfológica de células sanguíneas de Caimán Frente Lisa (Paleosuchus trigonatus)”, Troiano et al. (1998; 1997) en Tortuga terrestre argentina (Chelonoidis chilensis chilensis) Cascabel tropical (Crotalus durissus terrificus) estableciendo los valores hematológicos de referencia. Sin embargo, en países como Estados Unidos, Reino Unido y Australia, han llevado a cabo grandes avances en la toma y manejo de muestra, hemoparásitos, perfiles hematológicos, identificación de células sanguíneas; los autores más destacados en la literatura encontrada son Campbell (2010); Campbell and Ellis (2007a); Strik et al. (2007); Hernandez-Divers (2006); Jacobson (2005), Canfield (1998) y Frye (1991) Para el presente estudio, no se encontró reporte describiendo o identificando las células sanguíneas para la especie Pituophis deppei deppei. 15 III. JUSTIFICACIÓN Clínica de reptiles, es sin duda, un área que pocos Médicos Veterinarios llevan a cabo, dado la complejidad del diagnóstico y características biológicas propias del gran número de especies pertenecientes a la Clase Reptilia. Los estudios que se han realizado en el País son pocos, enfocándose a la determinación de perfiles hematológicos. La identificación de la conformación celular es de gran utilidad al comparar e interpretar el hemograma desde el punto vista patológico, proporcionando marcadores que favorecen diagnósticos específicos para determinar el estado físico. Considerando la importancia de los componentes celulares de la sangre, el presente trabajo pretende dar a conocer la morfología normal de células sanguíneas de la especie Pituophis deppei deppei, por medio de tinción tipo Romanowsky (Wright), elaborando a su vez una técnica descriptiva en base a la observación y vaciado de datos en formato de registro “Evaluación Citológica” (Ver Anexo 2) con las características celulares más relevantes y catálogo de imágenes digitales, con propósito de una futura revisión para determinar los cambios más representativos por citodiagnóstico, aportando una herramienta paraclínica que apoye al Médico Veterinario o cualquier profesional interesado en el área de hematología aplicada a reptiles. 16 IV. OBJETIVOS 4.1. Objetivo General Obtener información del estado físico general de la especie Pituophis deppei deppei mantenida en cautiverio en el herpetario de la Asociación Veterinaria de Reptiles y Anfibios A. C., en base a identificación celular por medio de citología. 4.2. Objetivos Específicos A) Identificar células sanguíneas del Cincuate (Pituophis deppei deppei) en cautiverio, por medio de frotis de sangre. B) Aportar formato de registro (Ver Anexo 2) con las características celulares a identificar. C) Generar catálogo de imágenes digitales, monocromáticas y color, de las células observadas. 17 V. MATERIALES Y MÉTODOS 5.1. Alojamiento y parámetros ambientales El encierro de las especies en estudio, es un terrario para exhibición (Figura 3) con las siguientes medidas: 80x60x60 centímetros, estructurado con madera terciada (triplay), base impermeabilizada y división superior protegida por malla para iluminación, proporcionada con focos de bajo consumo (General Electric®) y ventilación por ventilador/extractor 50/60 Hz (Steren®)(Figura 4). Tipo de substrato empleado, turba Sphagnum canadiense (Premier®). Temperatura mantenida en cautiverio, entre 24-28º Celsius y humedad relativa de 40-60%, éstos parámetros se registraron con termómetro/higrómetro digital (Steren®). Figura 4. División superior para iluminación y ventilación Figura 3. Terrario de exhibición 18 5.2. Manejo e inmovilización El método de contención física, refleja el tamaño del ejemplar, mecanismo de defensa de la especie y experiencia del manejador. Se utilizó una toalla, saco y gancho herpetológico, para asegurar inicialmente al organismo. Con serpientes no venenosas, el manejo de inmovilización se lleva acabo sujetando el cuello inmediatamente caudal a la cabeza (evitando ejercer demasiada presión, debido a que los ofidios presentan sólo un cóndilo occipital) mientras se sujeta el cuerpo con la otra mano. En general es requerido un segundo manejador por cada metro de longitud de la serpiente (Bertelsen, 2007). En todo manejo, siempre hay que considerar la seguridad del personal y bienestar animal. 5.3. Obtención de parámetros: morfometría, peso, sexo Para la obtención de datos morfométricos se empleó un cordel de 130cm y cinta métrica, el vaciado de datos se llevó a cabo en una hoja de registro ex professo con las siguientes medidas corporales: Longitud Total (LT), Longitud Hocico Cloaca (LHC), Longitud Cloaca Cola (LCC), Longitud Cabeza (LCb), Ancho Cabeza (ACb), Peso (P) y Sexo (S) (Ver Anexo 1). Para el pesaje se utilizó una balanza gramera de 3000gr (Cramry®). Además, registro fotográfico, vista dorsal región cefálica de cada ejemplar (Figura 5 a 8) (Cuadro 1). El sexado, se realizó empleando un estilete de punta roma y lubricante. La técnica consiste en insertar gentilmente el estilete en dirección craneocaudal, paramedial a la cloaca. En hembras, la profundidad aproximada varía de 2 a 6 escamas ventrales, y en machos de 7 a 12 escamas (Raiti, 2002). El sexo se clasificó en hembras y machos, con la simbología correspondiente (♂, ♀) en base a la profundidad descrita anteriormente. 19 Cuadro 1. Datos morfométricos de Pituophis deppei deppei Identificación PD1-101-2626 PD2-101-2632 PD3-101-2662 PD4-101-2648 LT (cm) 159 113 101.5 129 LHC (cm) 142 109 88 114.5 Figura 5. PD1-101-2626 ♂ Figura 7. PD3-101-2662 ♂ LCC (cm) 17 4 13.5 15 LCb (cm) 3 2.3 2.1 2.8 Acb (cm) 2.7 2.2 2 2.5 Peso (gr) 640 300 240 410 Sexo ♂ ♀ ♂ ♂ Figura 6. PD2-101-2632 ♀ Figura 8. PD4-101-2648 ♂ 20 5.4. Toma de muestra La toma de muestras se llevó a cabo en base a las recomendaciones descritas por Campbell and Ellis (2007a); Strik et al. (2007), Hernandez-Divers (2006); Jacobson (2005) y Frye (1991). La sangre se extrajo de la vena caudal (vena coccígea), localizándose ventral al cuerpo de las vértebras caudales, siendo el sitio común para recolección de sangre en reptiles, especialmente en lagartos, grandes serpientes y cocodrilos (Campbell and Ellis 2007a), La cantidad total de una muestra sanguínea a colectar depende del peso corporal. El volumen total de sangre varía entre especies, éste puede ser del 5-8% del peso corporal, tomando en consideración que un reptil clínicamente sano puede perder hasta un 10% del volumen sanguíneo (Jacobson, 2005) sin consecuencias detrimentales. Se utilizaron jeringas estériles de 3 mililitros (ml) y 1ml (dependiendo de la cantidad a extraer) con aguja calibre 22 o 23. En cuanto a la técnica antiséptica, el producto empleado, fué iodopovidona al 10%, debido a la capacidad microbicida tópica de amplio espectro (Strik et al., 2007). El sitio de punción debe ser caudal a la cloaca, en un espacio que varia del 2550% LCC, para evitar lesionar los hemipenes, en caso de machos y/o las glándulas de almizcle, en ambos sexos (Hernandez-Divers, 2006). 5.5. Manejo de la muestra Para la realización del frotis sanguíneo, es necesario contar con el siguiente material: sangre periférica sin coagular, porta objetos de vidrio nuevos, colorante tipo Romanowsky (Wright), puente de tinción, agua destilada, pipeta pasteur, aceite de inmersión y microscopio con objetivo de inmersión (x100), éstos últimos para la evaluación citológica. Inmediatamente después de la toma de muestra, se procedió a realizar dos o tres frotis (dependiendo de la cantidad muestreada) siguiendo la técnica recomendad por Campbell and Ellis (2007a), éste método usualmente provee buena distribución celular y campos adecuados en 21 monocapas, es decir, los eritrocitos están relativamente cerca el uno del otro, sin aglutinaciones, para una evaluación propiamente dicha. 5.6. Características de tinción Las tinciones hematológicas son un conjunto de procesos cuya finalidad es la coloración de las estructuras celulares dependiendo de la polaridad, facilitando el contraste entre los elementos formes suspendidos en la matriz extracelular (plasma) permitiendo que las células sanguíneas sean visualizadas microscópicamente con mayor facilidad. (Baines and Lewis, 2006). En el presente trabajo la tinción empleada es de tipo Romanowsky la cual está compuesta de una mezcla de eosina, azul de metileno y sus productos de oxidación (Azures). Los colorantes azures tiñen estructuras ácidas, resultando en una coloración azul o púrpura y la eosina tiñe bases, resultando en una coloración rosácea. Éstas características de tinción dependen del potencial de hidrógeno (pH) de la tinción y del agua de enjuague y/o destilada, así como de la naturaleza de las células presentes (Harvey, 2001). 5.7. Tinción Wright La tinción de Wright es un tipo de tinción usada en histología para facilitar la diferenciación de los tipos celulares sanguíneos, consiste en azul de metileno (C16H18ClN3S, cloruro de tetrametiltionina) colorante básico, y sus productos derivados por desmetilación oxidativa (azures) compuesto básico que tiene afinidad por estructuras ácidas de la célula, así como de eosina Y (C20H8Br4O5, tetrabromofluoresceína) o eosina B (C20H8Br2N2O9, dibromodinitrofluoresceína) (Bain and Lewis, 2006) La eosina es un compuesto ácido cuya propiedad está basada en su polaridad negativa, lo que le permite enlazarse con constituyentes celulares de carga positiva (Samour and Howlett, 2007). La combinación de éstos compuestos da una coloración púrpura-azulada a los núcleos de los leucocitos y un color rosa-anaranjado a los eritrocitos 22 PROTOCOLO: A) Preparar un frotis con sangre fresca, sin anticoagulante y secado al aire. B) Fijar con metanol durante 1 minuto. C) Cubrir la película de sangre con colorante tipo Romanowsky, (1.5ml) por 2 minutos, homogenizar cuidadosamente. D) Añadir agua destilada (1.5ml) al portaobjeto, observándose color verde metálico en la superficie del portaobjeto (dos minutos). E) Lavar con agua destilada dos o tres veces. E) Examinar el portaobjeto bajo el microscopio. (Atlas de histología vegetal y animal, 2008) 5.8. Análisis del Frotis Sanguíneo Los frotis sanguíneos fueron examinados inicialmente con objetivo de baja potencia (x40), determinando la presencia de eritrocitos aglutinados, agregados de leucocitos, plaquetas y/o microfilarias. Es importante examinar los bordes del portaobjetos (Figura 9), dado que en esta área se puede observar leucocitos y plaquetas. Al examinar el centro de la extensión se aprecia una concentración elevada de células sanguíneas, imposibilitando la lectura del portaobjetos. El sitio ideal para su análisis, deberá estar compuesto por: células en monocapas bien teñidas, es decir, los eritrocitos están relativamente cerca uno del otro, sin presentar aglutinaciones y por lo general, el área de estudio está situada en los bordes del portaobjeto (Harvey, 2001). Otras características al momento de realizar la evaluación de la muestra citológica, incluye: celularidad, distribución celular, tamaño, forma, citoplasma y núcleo, indicando el patrón de cromatina nuclear (Campbell and Ellis, 2007a). Para el vaciado de dichas características, se realizó un formato de registro “Evaluación Citológica” (Ver Anexo 2) con las características celulares observadas para su posterior análisis. Figura 9. Lectura de Frotis. Tomado de: Atlas of Veterinary Hematology. p 17. 23 VI. RESULTADOS Y DISCUSIÓN 6.1. Evaluación Citológica Para la identificación celular se utilizó un microscopio óptico convencional marca Nikon® de 2 obturadores con micrómetro integrado en un lente, perteneciente a la Asociación Veterinaria de Reptiles y Anfibios A. C., el registro fotográfico se realizó con cámara de 10.1 megapixeles, marca Sony® Cybershot Tx9. La información recopilada mediante observación del frotis sanguíneo, fué vaciada en el formato de registro, identificando especies muestreadas en el frotis como PD1♂, PD2♀, PD3♂ y PD4♂ para su análisis. El organismo PD3♂, al momento de la toma de muestra, iniciaba el proceso de ecdysis (muda de piel); el cambio celular observado fué, aumento en el número de eritrocitos inmaduros, los cuales son reportados por Campbell and Ellis (2007a) en reptiles juveniles y proceso de ecdysis. La técnica, se basa en observaciones preliminares, identificando primero la célula a estudiar. Para reptiles se reportan los siguientes tipos celulares de la serie roja: eritrocito, eritrocito inmaduro, eritrocitos policromáticos; para la serie blanca se reportan: heterófilos, basófilos, eosinófilos, monocitos, linfocito y azurófilo (Campbell and Ellis, 2007a; Strik et al., 2007; Frye, 1991). Los reticulocitos son detectados con tinciones vitales, como el Azul de Metileno. Estas células, como el de las aves, presentan un halo distintivo de reticulum agregado alrededor del núcleo celular, y corresponden a los eritrocitos policromáticos encontrados con tinciones tipo Romanowsky (Campbell and Ellis, 2007a). La celularidad, se clasificó en: Escasa, Moderada y Marcada, identificada con objetivo de bajo aumento (x40), la distribución celular se clasificó en: Monocapas, Sábanas y Aglutinadas (Figura 10 a 12). 24 Distribución Celular: Monocapas (Figura 10), Sábanas (Figura 11) y Aglutinadas (Figura 12), dependiendo del espacio observado entre células. Figura 10. Distribución celular: Monocapas Figura 11. Distribución celular: Sábanas Figura 12. Distribución celular: Aglutinadas 6.1.1. Características celulares en formato de registro Tamaño: para los eritrocitos nucleados de la mayoría de las especies de reptiles se reporta entre 14x8µm – 23x14µm (Campbell, 2006). Campbell and Ellis (2007a) reportan para los leucocitos las siguientes medidas en micra (µm): heterófilos 10-23µm, eosinófilos 11-17µm, basófilos 8-15µm y linfocitos 5-10µm. Strik et al. (2007) reporta para los heterófilos 10-23µm, generalmente variando entre especies e incluso individualmente en la muestra, eosinófilos 9-20µm, basófilos 7-20µm, linfocitos con un diámetro de 5-10µm pequeños y 15µm en los grandes y monocitos de 8-25µm (Strik et al., 2007). 25 Forma: dependiendo de la célula, se clasifica en Elíptica, Redondeada o Poligonal (Campbell, 2007b). Citoplasma: atendiendo a las características de coloración dada la afinidad de los componentes celulares, se clasifica en basofílico, para las estructuras alcalinas de la célula y eosinofílico para aquellas que fijan el colorante de naturaleza ácida (Baines and Lewis, 2006). Además se especifica, de manera muy general, la intensidad con la que se fijaron los colorantes en: denso, pálido u homogéneo, proporcionando a la vez un espacio para designar otro tipo de coloración Gránulos: para realizar la identificación y diferenciación entre las células de la serie granulocítica y mononuclear, es importante establecer el tipo de gránulos observables en el citoplasma y la coloración. Para su descripción se decidió clasificarlos en Fusiformes, Esféricos, Angular o Pleomórficos (Campbell, 2007b). Núcleo: para comparar los hallazgos encontrados en el frotis, es necesario incluir la forma, clasificándolo en redondo, irregular-redondeado u oval y la posición, centrado o excéntrico (Campbell, 2007b). Este tipo descriptivo permite emplear más de una característica seleccionada, por ejemplo: núcleo redondo a oval excéntrico; núcleo irregularmente redondeado central. Radio (N:C): facilita la evaluación del tamaño, relacionando la cantidad de citoplasma y núcleo (Campbell, 2007b). Se clasificó en alto o bajo. Lobulado: si aplica, es importante para diferenciar entre células pertenecientes a otras especies y Ordenes de reptiles: Los heterófilos de los saurios presentan uno o dos lóbulos (Strik et al., 2007). Patrón de cromatina nuclear: este patrón indica el grado de madurez celular (Campbell, 2007b). 26 6.2. Eritrocitos maduros, inmaduros y policromáticos A diferencia de los eritrocitos encontrados en mamíferos, los de reptiles presentan núcleo. Los eritrocitos encontrados en extensiones de sangre periférica, se agrupan en eritrocitos maduros, inmaduros y policromáticos (Strik et al., 2007). Los eritrocitos maduros son típicamente más grandes que los de aves, peces y mamíferos, pero más pequeños que los de anfibios (Campbell, 2006) Los eritrocitos maduros identificados en este estudio (Figura 13), presentan las siguientes características celulares; tamaño de 12.5µm a 19.5µm de forma elíptica con citoplasma de color rosa-anaranjado (eosinofílico), núcleo redondeado (ligeramente elongado) centrado con márgenes irregulares, bajo radio (N:C) y un patrón de cromatina uniforme granular denso. Los eritrocitos maduros de Pituophis deppei deppei son morfológicamente similares a los reportados para otros reptiles (Canfield, 1998). Otro tipo de eritrocito encontrado, es el denominado eritrocito inmaduro, observándose en el frotis del organismo identificado como PD3♂ en proceso de ecdysis, con la siguiente descripción: tamaño de 11.5µm, forma redondeada ligeramente irregular con citoplasma de color púrpura-azulado (basofílico), núcleo redondo ligeramente irregular, centrado, alto radio (N:C) y patrón de cromatina granular fina con distribución irregular, indicando inmadurez celular, de acuerdo con las características mencionadas por Campbell and Ellis (2007a), se concluye que es un rubricito basofílico (Figura 14). El último tipo de eritrocito identificado en el frotis del organismo PD3♂, es el perteneciente a los policromáticos (Figura 15) con un tamaño de 10µm, forma similar a los eritrocitos pero ligeramente mas redondeada, citoplasma basofílico pálido, núcleo oval centrado, alto radio (N:C) y patrón de cromatina granular densa con distribución irregular (Mendoza et al., 2011). Se considera normal una ligera anisocitosis (Figura 16) y poikilositosis en las tinciones de la serie roja de reptiles, esto puede estar asociado con tasa metabólica lenta y el tiempo de vida esperado (600 a 800 días en algunas especies) en eritrocitos de reptiles sanos (Frye, 1991). 27 6.3. Leucocitos La clasificación de los leucocitos de reptiles puede ser problemática debido, en parte, a la presencia de variaciones morfológicas dentro de Ordenes y especies. Algunos autores clasifican a los granulocitos en tres tipos celulares – eosinófilos, azurófilos y neutrófilos – y otras fuentes únicamente diferencian dos – eosinófilos y heterófilos, o eosinófilos y neutrófilos (Strik et al., 2004; Frye, 1991; Canfield, 1998). En general, y para el presente estudio, se dividen en dos grupos: granulocitos y mononucleares. 6.4. Granulocitos La serie granulocitos, puede ser dividida en acidófilos y basófilos, en base a la apariencia en tinciones con colorantes tipo Romanowsky. Los acidófilos comprenden los heterófilos y eosinófilos. Los heterófilos y los eosinófilos pueden ser distinguidos, el uno del otro por la apariencia y color de sus gránulos (Campbell and Ellis, 2007a). Los basófilos, linfocitos y monocitos se asemejan a los encontrados en aves y mamíferos y se clasifican acorde a ellos. 6.4.1. Heterófilos Los heterófilos reportados en la literatura, los describen generalmente como células grandes de 10-23µm, redondas con citoplasma claro-transparente que contiene numerosos gránulos rojo-rosados en forma de coma o esféricos, que parcialmente obscurecen el núcleo, la forma del mismo, depende de la especie en estudio y puede variar de redondo a oval, excéntrico (ofidio, chelonios y crocodílidos) con dos o mas lóbulos (saurios), generalmente varia entre especies e incluso en frotis individuales (Mendoza et al., 2011; Rossini y García, 2010; Strik et al., 2007; Roberto et al., 2007; Campbell, 2006; Carvalho et al., 2006) El heterófilo encontrado en laminilla del organismo PD3♂ (Figura 17), presenta un tamaño de 19µm, forma redondeada con citoplasma ligeramente basofílico pálido, con gránulos pleomórficos, basófilos y ligeramente eosinofílicos, núcleo redondo a oval excéntrico, bajo radio (N:C) y patrón de cromatina granular densa con distribución irregular. En laminilla de PD1♂ (Figura 18), el heterófilo tiene un 28 tamaño de 12µm, forma redondeada con citoplasma basofílico pálido, con gránulos esféricos ligeramente visibles, núcleo oval excéntrico, bajo radio (N:C) y patrón de cromatina granular densa. Probablemente debido a un menor tiempo de exposición a la tinción. 6.4.2 . Eosinófilos Campbell and Ellis (2007a) describen al eosinófilo como una célula grande de 11µm a 17µm, redonda con citoplasma ligeramente azul y núcleo redondo a oval (lobulado en algunas especies de saurios), excéntrico y con un gran número de gránulos eosinofílicos circulares. El tamaño varía entre especies, por ejemplo los ofidios presentan los más grandes y los saurios los más pequeños. Strik et al. (2007) considera un tamaño de 9µm a 20µm, casi del mismo tamaño que los heterófilos, citoplasma claro con gránulos eosinofílicos, esféricos y núcleo redondo elongado, lenticular o bilobulado que puede ser excéntrico o centrado. Mendoza et al. (2011) en Crotalus polystictus, los describe como células esféricas que poseen gránulos citoplasmáticos y núcleo esférico, con medidas de 10.2µmx8.24µm. El eosinófilo se describe del organismo PD1♂ (Figura 19a) y PD3♂ (Figura 19b) con un tamaño de 15µm a 18µm de forma redondeada, citoplasma eosinofílico denso con gránulos esféricos de color rojos-rosáceos, núcleo excéntrico redondo con márgenes irregulares, bajo radio (N:C) y patrón de cromatina granular densa con distribución irregular. Al momento de realizar la primera evaluación de este tipo celular, se clasificó, como heterófilo, por presentar la característica de núcleo excéntrico, al observar detenidamente la coloración del citoplasma y compararla, se decidió clasificarlo como eosinófilo; Strik et al. (2007) sugiere que representa un granulocito coincidente con un segundo tipo de heterófilo. 29 6.4.3. Basófilos Generalmente, los describen como células pequeñas de 7µm a 20µm, con gránulos pequeños, metacromáticos que obscurecen el núcleo, localizado centralmente (Strik et al., 2007); Campbell and Ellis (2007a), los describen de un tamaño de 8µm a 15µm, redondos (típicamente mas pequeños que los heterófilos y eosinófilos en el frotis) con número variable de gránulos esféricos basofílicos, obscureciendo el núcleo. Mendoza et al. (2011) los considera células esféricas con gránulos color violeta que cubren el citoplasma, distinguiéndose el núcleo por su gran tamaño. Se describe un basófilo en laminilla PD2♂ (Figura 20) con tamaño de 9µmx11µm, forma redondeada-esférica con márgenes irregulares, citoplasma basofílico denso, gránulos no visibles o muy condensados, núcleo oval excéntrico con márgenes irregulares, bajo radio (N:C) y patrón de cromatina nuclear densa con distribución irregular. 6.5. Mononucleares Debido a que este tipo de células son congruentes con los observados en mamíferos y aves, las consideraciones para clasificación permanecen a las descritas en animales domésticos. 6.5.1. Linfocitos Al igual que en los mamíferos, los linfocitos son variables en tamaño y forma, se reportan con tamaño de 5µm a 10µm y hasta 15µm. El aspecto más importante en el diferencial leucocitario en reptiles, es diferenciarlos de los trombocitos (Strik et al., 2007). Los linfocitos presentan una núcleo de forma redonda, central o ligeramente excéntrico, la cromatina nuclear está densamente condensada en los maduros y típicamente exhiben un alto radio (N:C). El citoplasma de linfocitos normales es homogéneo, generalmente carece de vacuolas y gránulos, moderadamente basofílico (azul-pálido). Los linfocitos inmaduros son de mayor tamaño, con mayor cantidad de citoplasma basofílico de moderado a intenso y en 30 algunos, cromatina con gránulos azurofílicos (Strik et al., 2007; Campbell and Ellis, 2007a). Estos tipos celulares, se describen en laminilla PD1♂, PD2♀ y PD3♂ (Figura 21, 22 y 23) con una forma redonda irregular, citoplasma basofílico-denso, alto radio (N:C) y cromatina uniforme granular densa. En PD1 y PD2, se observan linfocitos de tamaño 5µm a 8µm, uno presenta abundante citoplasma, en PD3 el núcleo excéntrico con gran cantidad de citoplasma basofílico, indica un linfocito de talla grande. 6.5.2. Monocitos Los monocitos, son descritos como células de mayor tamaño en sangre de reptiles, con tamaño de 8µm a 25µm, variando en forma de ameboide a redonda y núcleo redondo a oval; puede presentar lobulado (forma de frijol), cromatina menos condensada comparada con linfocitos. Abundante citoplasma ligeramente pálido a moderado-basofílico, dependiendo del estado reactivo. Puede estar presente material fagocitado, vacuolas o gránulos eosinófilos o azurófilos. Los monocitos de reptiles, suelen ser referidos como monocito, azurófilo monocitoide, monocito azurofílico o azurófilo (Campbell and Ellis, 2007a; Strik et al., 2007; Frye, 1991) El tipo de monocito (Figura 24) observado en PD1♂, presenta forma ameboide, citoplasma basofílico-pálido, con gránulos pleomórfos ligeramente observables de color eosinófilo, núcleo redondo a oval con márgenes irregulares, ligeramente centrado, alto radio (N:C) y patrón de cromatina granular densa con distribución irregular. Se identifica otro tipo celular, compatible con las características del denominado azurófilo monocitoide (Figura 25) presentando una forma redondeada con citoplasma ligeramente basófilo y gránulos dispersos de color eosinófilo, núcleo lobulado (forma de frijol) excéntrico, alto radio (N:C) y patrón de cromatina granular denso con distribución irregular. 31 6.6. Trombocitos Se describen de tamaño pequeño (generalmente más pequeños que los eritrocitos), elípticos a fusiformes con núcleo oval central y cromatina densa, poco citoplasma, sin color ó ligeramente azul-pálido y pueden contener gránulos azurófilos. Cuando se activan, se observan agregados con citoplasma decrecido, casi inexistente, algunos con márgenes irregulares (Strik et al., 2007). En PD2♀ (Figura 26) se observan trombocitos agregados, con menor cantidad de citoplasma y cromatina densa y un eritrocito inmaduro, probablemente un rubricito. El trombocito observado en laminilla PD2♀ (Figura 27) presenta forma elíptica, con citoplasma azul-pálido y márgenes regulares delimitados, núcleo oval centrado en forma de riñón, alto radio (N:C) y cromatina uniforme granular densa. 32 MONOCROMÁTICAS Figura 13. Eritrocitos maduros Figura 15. Eritrocito policromático Figura 14. Eritrocito inmaduro (Rubricito basofílico) y trombocitos Figura 16. Ligera anisocitosis y poikilositosis (cabeza de flecha) Figura 17. Heterófilo (PD3♂) Figura 18. Heterófilo (PD1♂) Figura 19a. Eosinófilo (PD1♂) Figura 19b. Eosinófilo (PD3♂) 33 Figura 20. Basófilo (PD2♂) Figura 22. Linfocito (PD2♀) Figura 21. Linfocito (PD1♂) Figura 23. Linfocito (PD3♂) Figura 24. Monocito (PD1♂) Figura 25. Azurófilo monocitoide (PD1♂) Figura 26. Trombocitos (PD2♀) y eritrocito inmaduro (rubricito) Figura 27. Trombocito (PD2♀) 34 COLOR Figura 28. Eritrocitos maduros Figura 29. Eritrocito inmaduro (Rubricito basofílico) y trombocitos Figura 30. Eritrocito policromático Figura 31. Ligera anisocitosis y poikilositosis (cabeza de flecha) Figura 32. Heterófilo (PD3♂) Figura 33. Heterófilo (PD1♂) Figura 34a. Eosinófilo (PD1♂) Figura 34b. Eosinófilo (PD3♂) 35 Figura 35. Basófilo (PD2♂) Figura 37. Linfocito (PD2♀) Figura 36. Linfocito (PD1♂) Figura 38. Linfocito (PD3♂) Figura 36. Monocito (PD1♂) Figura 37. Azurófilo monocitoide (PD1♂) Figura 39. Trombocitos (PD2♀) y eritrocito inmaduro (rubricito) Figura 40. Trombocito (PD2♀) 36 VII. LITERATURA CITADA Atlas de Histología Vegetal y Animal. 2008. Universidad de Vigo. Facultad de Biología. Departamento de Biología Funcional y Ciencias de la Salud. [consultado el 14 de febrero de 2011]. Disponible en: http://webs.uvigo.es/mmegias/inicio.html Baines, B. J, and S. M. Lewis. 2006. Staining blood and bone marrow films. In: Dacie and Lewis. Practical Haematology (10ed). Elsvier Churchill Livingstone. p 53-55 Bertelsen, M. F. 2007. Squamates (Snakes and Lizards). In: zoo animal and wildlife immobilization and anesthesia, edited by West, G., Heard, D., Caulkett, N. Wiley-Blackwell Publishing. p 234. Carvalho, R. L., M. M. Antoniazzi, C. Jared, A. M. J. Silva, A. A. Santos and M. I. Egami. 2006. Morphological, cytochemical, and ultrastructural observations on the blood cells of the reptile Tupinambis merianae (Squamata). Comp Clin Pathol 15:169-174. Campbell, T. W. 2006. Clinical pathology. In: Reptile Medicine and Surgery, edited by D. Mader. 2ed St. Louis: Saunders Elsevier. p. 248-257. Campbell, T. W., and C. K. Ellis (ed). 2007a. Hematology of reptiles. In: Avian and Exotic Animal Hematology and Cytology. 3ed. Iowa: Blackwell Publishing Co. p 51-81. Campbell, T. W. 2007b. Basics of Cytology and Fluid Cytology. Vet Clin Exot Anim 10:1-24. Campbell, T. W., and K. R. Grant. 2010. Herptile Hematology Case Studies. In: Clinical Cases in Avian and Exotic Animal Hematology and Cytology. Blackwell Publishing Co. p 95-121. Canfield, P. J. 1998. Comparative cell morphology in the peripheral blood film from exotic and native animals. Aust Vet J 76(12):793-800. 37 CONABIO, 2009. Comisión Nacional para el Conocimiento y Uso de la Biodiversidad. México. [consultado el Biodiversidad Mexicana, La gran Familia, Reptiles. 16 de marzo de 2011]. Disponible en: http://www.biodiversidad.gob.mx/especies/gran_familia/animales/reptiles/reptiles .html CONABIO, 2010. Comisión Nacional para el Conocimiento y Uso de la Biodiversidad. Portal de Geoinformación.. Sistema Nacional de Información Sobre Biodiversidad. [consultado el 09 de mayo de 2011]. Disponible en: http://www.conabio.gob.mx/informacion/gis/?vns=gis_root/biodiv/distpot/reptilia/ serpent/mastc_mentgw Duellman, W. E. 1960. A Taxonomic Study of the Middle American Snake, Pituophis deppei. University of Kansas Publication, Museum of Natural History, edited by E. Raymond Hall, Chairman, Henry S. Fitch, Robert W. Wilson. Vol 10, No. 10. pp. 599-610 Frye, F. L. (ed). 1991. Hematology as applied to clinical reptile medicine. In: Vol. 1, Biomedical and Surgical Aspects of Captive Reptile Husbandry. 2ed. Melbourne, FL: Krieger Publishing Co. p 209-277. Harvey, J. W. (ed). 2001. Examination of Blood Samples. In: Atlas of Veterinary Hematology. Blood and bone marrow of domestic animals. Philadelphia: WB Saunders Co. p 3-20. Hernandez-Divers, S. J. 2006. Diagnostic techniques. In: Reptile Medicine and Surgery, edited by D. Mader. 2ed. St. Louis: Saunders Elsevier. Hidalgo-Silva, J., C. D. Paniagua, N. P. Santigosa, A. Plaza, I. Camacho and F. Recio. 2007. Hematological and Biochemical Reference Intervals of Free-Living Mediterranean Pond Tutles (Mauremys leprosa). J Wild Dis 43(3):798-801. Instituto de Biología. "Pituophis deppei - IBUNAM:CNAR:AR3160". UNIBIO: Colecciones Biológicas. 2005-09-27. Universidad Nacional Autónoma de México. [consultado el 13 de febrero de 2011]. Disponible en: http://unibio.unam.mx/collections/specimens/urn/IBUNAM:CNAR:AR3160. 38 Jacobson, E. R. 2005. Collecting Biological Simples for Clinical Evaluation. [consultado el 16 de febrero de 2011]. On line: http//iacuc.ufl.edu/AnimalUseGuides/BiolSampColl.doc Liner, E. A. 2007. A checklist of the amphibians and reptiles of México. Museum of Natural Science, Lousiana State University. 80:1-30. Mendoza, A. F. J., E. M. Cantú, D. Lazcano, K. W. Sester y E. M. Deloya. 2011. Morfología de las células sanguíneas y perfil leucocitario de Crotalus polystictus (Cope 1865). Ciencia UANL/Vol XIV, No. 1, ENERO-MARZO 2011. Mora, R. N. C. 2003. Perfil hematológico del Cocodrilo de Pantano (Crocodylus moreletii) en cautiverio en Veracruz, México. Tesis de Licenciatura. Universidad Veracruzana. Veracruz, Ver., México. 49 p. Padilla, S. E. 2008. Hematología, Índice Corporal y Lesiones Externas del Cocodrilo de Pantano Crocodylus Moreletii en los Humedales del Norte del Estado de Campeche, México. Tesis de Maestría. El Colegio de la Frontera Sur. Unidad Campeche, San Francisco de Campeche., México. 79 p. Uetz, Peter. 2010. The Reptile Database. [consultado el 08 de mayo de 2011]. Disponible en: http://www.reptile- database.reptarium.cz/species.php?genus=Pituophis&search_param=%28%28 gen%3D%27Pituophis%27%2Cexact%29%29 Raiti, P. 2002. Snakes. In: BSAVA Manual of Exotic Pets. 4ed, edited by Meredith A., and S. Redrobe. England: British Small Animal Veterinary Association. p 241. Ramírez, B. A., y M. C. Arizmendi. 2004. Pituophis deppei. Sistemática e historia natural de algunos anfibios y reptiles de México. Facultad de Estudios Superiores Iztacala, Unidad de Biología, Tecnología y Prototipos (UBIPRO), Universidad Nacional Autónoma de Mexico. Bases de datos SNIB-CONABIO. Proyecto W013. México. D. F. [consultado el 08 de mayo de 2011]. Disponible en:http://www.conabio.gob.mx/conocimiento/ise/fichasnom/Pituophisdeppei00.p df 39 Roberto, S., F. Pupin, M. A. L. Zuffi, S. Scali, E. Boncompagni, A. Binda, P. Galeotti y M. Fasola 2007. Blood cell morphology of the Moorish gecko, Tarentola mauritanica. Amphibia-Reptilia 28:503-508. Rojas, M. G. 2005. Caracterización morfológica de células sanguíneas de Caimán Frente Lisa (Paleosuchus trigonatus) (SCHNEIDER, 1801) mantenidos en cautiverio en Perú. Revista de la Asociación de Veterinarios de Vida Silvestre, Vol 1, Num 4. Rossini, M. V., y G. C. García. 2010. Descripción morfológica de las células sanguíneas de la baba (Caiman crocodilus crocodilus) en vida silvestre. Rev. Fac. Cs. Vets. 51(2):63-70 Samour, J. and J. C. Howlett. 2007. Blood samples. In : Avian Medicine. Second Edit. Elsvier Mosby. p 47-48. SEMARNAT. 2010. Norma Oficial Mexicana NOM-059-ECOL-2010, Protección ambiental-Especies nativas de México de flora y fauna silvestres-Categorías de riesgo y especificaciones para su inclusión, exclusión o cambio-Listado de especies en riesgo. Secretaria de Medio Ambiente y Recursos Naturales. Publicada en el Diario Oficial de la Federación el 26 de noviembre de 2010. Strik, N. I., A. R. Alleman y K. E. Harr. 2007. Circulating Inflamatory Cells. In: Jacobson, E. R. (Ed). Infectious Diseases and Pathology of Reptiles: Color Atlas and Text. CRC Press. Florida. p. 167 – 218. Stull, O. G. 1940. Variations and Relationship in the Snake of the Genus Pituophis, United States.. National Museum. Washington, D.C., Smithsonian Institution. Bulletin 175, p. 25. April 23. Troiano, J. C., J. C. Vidal, J. Gould et al. 1997. Hematological reference intervals of the south American rattlesnake (Crotalus durissus terrificus, Launrenti, 1768) in captivity. Comp Hemat Inter 1:109-112. Troiano, J. C., M. C. Silva. 1998. Valores hematológicos de referencia en tortuga terrestre argentina (Chelonoidis chilensis chilensis). Analecta Veterinaria 18,1/2:47-51. 40 ANEXOS Anexo 1 Medidas morfométricas de Pituophis deppei deppei consideradas en este estudio. IDENTIFICACIÓN LT (cm) LHC (cm) LCC (cm) LCb (cm) ACb (cm) Peso (gr) PD1-101-2626 159 142 17 3 2.7 640 ♂ ♀ PD2-101-2632 113 109 4 2.3 2.2 300 ♂ ♀ PD3-101-2662 101.5 88 13.5 2.1 2 240 ♂ ♀ PD4-101-2648 129.5 114.5 15 2.8 2.5 410 ♂ ♀ Sexo MEDIDAS: LT: Longitud Total; medida en centímetros, desde la escama rostral hasta la punta de la cola. LHC: Longitud Hocico Cloaca; medida en centímetros, desde la escama rostral hasta el inicio de la escama cloacal. LCC: Longitud Cloaca Cola; medida en centímetros, desde la escama cloacal hasta la punta de la cola. LCb: Longitud Cabeza; medida en centímetros, desde la escama rostral hasta la cresta occipital. ACb: Ancho Cabeza; medida en centímetros, desde la escama supralabial de maxilar izquierdo a derecho en línea perpendicular a la cresta occipital. Peso: medida en gramos. 41 Anexo 2 Formato: “Evaluación Citológica” ESPECIE: ________________________________________________________ SEXO: ♀ ( ) ♂ ( ) PESO: __________ Kg Longitud Total: ___________ cm Identificación: ____________________ Tinción: _________________________ TIPO DE CÉLULA: Eritrocito maduro ( ) Eritrocito inmaduro ( ) Eritrocito Policromático ( ) Heterófilo ( ) Basófilo ( ) Eosinófilo () Monocito ( ) Linfocito ( ) CELULARIDAD ESCASA ( ) MODERADA ( ) MARCADA ( ) DISTRIBUCIÓN CELULAR: MONOCAPAS ( ) SABANAS ( ) AGLUTINADAS ( ) TAMAÑO: CARACTERÍSTICAS CELULARES de _________ µ a _________ µ FORMA: Elíptica ( ) Redondeada ( ) Poligonal ( ) CITOPLASMA: Basofílico “púrpura-azulado” Eosinofílico “rosa-anaranjado” ( ) ( ) GRÁNULOS: Fusiformes ( ) Esféricos Angular ( ) Pleomérficos No aplica () () () Denso Pálido ( ) Homogéneo ( ) ( ) COLOR GRÁNULOS: Púrpura-Azulado ( ) Rojo-Rosáceos ( ) Otro color_______________________ NÚCLEO: Redondo ( ) Irregular-Redondeado ( ) Oval ( ) Púrpura-azulado ( ) Rosa-anaranjado () RADIO (N:C): N:C ( ) N:C ( ) POSICIÓN: Centrado ( ) Excéntrico ( ) LOBULADO: No aplica ( ) Bilobulado ( ) Multilobulado ( ) PATRON DE CROMATINA NUCLEAR Cromatina Uniforme Granular Fino Cromatina Granular Fina con Distribución Irregular Cromatina Uniforme Granular Densa Cromatina Granular Densa con Distribución Irregular ( ( ( ( ) ) ) ) 42