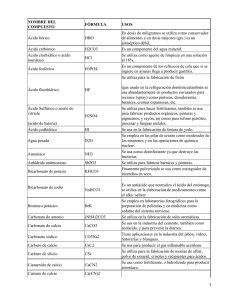
Completar La tabla periódica se organiza en filas horizontales, que
Anuncio

1. Completar Elemento a. La tabla periódica se organiza en filas horizontales, que se llaman _____________, y columnas verticales que reciben el nombre de _______________ b. ________________Se transforman fácilmente en iones positivos. Quedan situados a la izquierda y el centro de la tabla c. __________________No forman iones. En condiciones normales, no se combinan con ningún otro elemento químico d. Los elementos están colocados por orden creciente de su ___________________ c. Grupo VI A d. e. f. g. Grupo 15 Grupo IV A Grupo 13 Grupo 3 al 12 h. Grupo II A i. Grupo 1 ( )Metales alcalinos ( )Metales alcalinotérreos ( )Metales de transición ( )Terreos ( )Carbonoideos ( )Nitrogenoideos ( )Calcogenos o familia del oxigeno ( )Halógenos ( )Gases nobles Z Ne Sc Fe Br Sr Cd Po 6. Completar la siguiente tabla Elemento Z Conf. Electrónica Periodo Grupo Si 2. Relacionar la columna de la izquierda con la derecha colocando dentro del paréntesis la letra correspondiente a. Grupo VIII A b. Grupo VII A Electronegatividad S Fe Ag Y 7. Indica según la tabla periódica, en las siguientes parejas cuál átomo tiene 3. Defina a. El mayor tamaño atómico a. b. c. d. Enlace químico Enlace iónico y covalente Ley del octeto Orbitales y núcleo Atómico 4. Utilizando la configuración electrónica, determinar los tipos de enlace que se forman con las siguientes parejas de elementos. a. SF6 b. CCl4 c. H2O d. CaS 5. Elabora utilizando la tabla periódica una gráfica (Ne) (Ge) y (As) (Ca) y (Ga) (B) y (Tl) b. La mayor energía de ionización (O) y (S) (Cl) (Cu) y (Au) (Co) (I) y (Ag) (Mn) y (Se) y (O) 8. En la siguiente representación de un periodo de la tabla periódica, los elementos se nombran con letras de manera arbitraria Grupo IA IIA IIIA IVA VA VIA VIIA VIIIA Periodo A B C D E F G H 4 electronegatividad en función del número siguiente tabla (Al) y (Cs) y (Ba) c. La menor afinidad electrónica (K) y (Rb) que muestre la variación de la atómico teniendo en cuenta la información de la (He) y ( ) Es un gas noble ( ) Tiene dos electrones de Valencia ( ) Es menos electronegativo ( ) Pertenece a la familia del carbono ( ) Es un halógeno ( ) Pertenece al sexto grupo ( ) Se caracteriza por presentar 5 electrones de valencia 9. a. b. c. d. Las sales provienen de una reacción entre Óxido y ácido Hidruro y Ácido Base y Ácido Hidróxido y Peróxido 10. a. b. c. d. El perclorato de Sodio proviene de del Ácido Percloroso Hipocloroso Perclórico Clórico 11. a. b. c. d. Una de las sustancias es un Hidrácido Ácido Fosfórico Ácido Hipoyodoso Acido Carbonico Ácido Sulfhidrico 12. Escriba el frente de cada sal el tipo según corresponde a. Cloruro de Sodio. _____________ b. Bicarbonato de Sodio. __________________ c. Sulfato de Potasio. ______________ d. Bicarbonato de Sodio. ________________ e. Nitrato Básico de Aluminio. _____________ 13. Indica si los siguientes nombres son correctos de acuerdo con la nomenclatura sugerida por la IUPAC. En caso de que no lo sean, escríbalos. a. Sulfato (IV) de Litio (I).___________________ b. Fosfito de Calcio. _______________________ c. Acido Yodhídrico. ________________________ d. Clorato (III) Ferroso. ______________________ e. Acido de Cloro (VII) ______________________ 14. El óxido de carbono (IV), o Dióxido de Carbono es el óxido que se encuentra en mayor proporción en la atmósfera. Además, como resultado de las actividades humanas hay péquelas cantidades de oxido de carbono (II), oxido de nitrógeno (II), oxido de nitrógeno (IV). Escriba las formulas de todos los compuestos y las estructuras de Lewis para los óxidos de azufre, además de los nombres faltantes teniendo en cuenta los diferentes tipos de nomenclatura. 15. Las sales se originan de la reacción entre un ácido y una base, como producto secundario se forman también moléculas de agua. Emplea este concepto para completar las siguientes ecuaciones químicas. E indica el nombre de la sal resultante. 16. El nitrógeno reacciona con el oxígeno para formar un óxido ácido, este se combina con agua para producir ácido nítrico el cual al reaccionar con un hidróxido forma el nitrato de calcio. Establece las reacciones que se llevan a cabo y los nombres de las sustancias involucradas en el proceso. 17. El azufre al reaccionar con el oxigeno forma un óxido de azufre, el cual al tener contacto con el agua produce el ácido sulfúrico. Cuando este ácido se combina con un hidróxido se forma sulfato de hierro (III) y agua. Plantea todas las reacciones llevadas a cabo y los nombres de cada sustancia involucrada en este proceso. Conteste las preguntas 18 a y 22 teniendo en cuenta la siguiente información 18. El compuesto A es una sustancia inorgánica que recibe el nombre de a. Óxido de Sulfato b. Ácido Sulfúrico c. Hidróxido de sulfato d. Sulfato de Hidrógeno 19. El nombre del compuesto E aplicando la nomenclatura tradicional es Óxido Carbónico y trabaja con numero de oxidación A. +4 B. -4 C. +2 D. -2 20. Cuál de los siguientes compuestos corresponde a un ácido oxácido a. A b. B c. C d. D 21. El compuesto D , representa un oxido acido, el nombre correcto de este compuesto es a. Oxido sulfuroso b. Oxido sulfúrico c. Oxido hiposulfuroso d. Oxido sulfhídrico 22. Entre los compuestos presentes en la reacción cual es el que absorben las plantas y liberan los demás organismos, además es el que ataca la atmosfera y contamina el medio ambiente a. A b. B c. C d. E 23. El perclorato de Sodio proviene de del Ácido a. Percloroso b. Hipocloroso c. Perclórico d. Clórico 24. Una de las sustancias es un Hidrácido a. Ácido Fosfórico b. Ácido Hipoyodoso c. Ácido Carbónico d. Ácido Sulfhídrico Conteste las preguntas 25 a 31 teniendo en cuenta la siguiente información 25. El Ag2SO4 se caracteriza por ser una sal, y las sales tienen diferentes tipos de clasificación (hidracidas, Oxácida, acidas, básicas), por lo tanto este compuesto se clasifica como A. Hidracidas B. Oxácidos C. Acidas D. Básicas 26. Teniendo en cuenta la formulación de la pregunta anterior, el NaCl recibe el nombre de a. Cloruro de sodio b. Sodio de Cloro c. Sodio Clorhídrico d. Clorato de Sodio 27. El nombre adecuado para el compuesto cuya fórmula Na2SO4 es a. Sulfito de sodio b. Sulfato de sodio c. Sodio sulfuroso d. Sodio sulfhídrico 28. Cuáles de las siguientes parejas de elementos representan sales hidracidas a. NaCl y AgCl b. Na2SO4 y AgCl c. Na2SO4 y NaCl d. Ag2SO4 y AgCl 29. Cuáles de las siguientes parejas de compuestos representan sales oxacidas a. NaCl y AgCl b. Na2SO4 y Ag2SO4 c. Na2SO4 y NaCl d. Ag2SO4 y AgCl 30. Si tomamos al Na2SO4 y cambiamos el sodio por el hidrogeno, el compuesto que se forma es a. Acido b. Sal c. Oxido d. Hidróxido 31. El nombre del compuesto al cambiar el sodio por el hidrogeno es a. Ácido sulfúrico b. Oxido de Sodio c. Hidróxido sulfuroso d. Hidrogeno de sulfato 24. Completar la siguiente tabla teniendo en cuenta las funciones químicas correspondientes N. stock REACCIÓN FUNCIÓN TIPO FORMULA N. tradicional N. Sistemática Acido Crómico Permanganato Aúrico Ca3(PO4)2 Fe+3 + O-2 Hidróxido Carbónico H2CO3 Cloruro de cobalto (III) Fosfato Calcio Ácido sulfhídrico Fe(OH)3