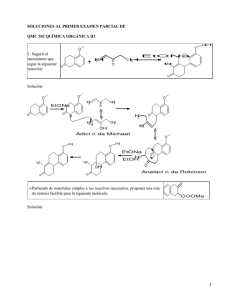
Síntesis y retrosíntesis
Anuncio

¿QUÉ ES ANÁLISIS RETROSINTÉTICO? Se describe la aproximación a la síntesis de la prefeldina en base a una reacción hetero diels−alder intramolecular de un sistema dienal. Esta estrategia se modificó a la alquilación interna de un hidroxi−epoxido promovida por la acción de ácidos de Lewis sobre un sistema silano alilico. La saudina es un diterpeno con reagrupamiento bis−acetalico único. El análisis retrosintético permite contemplar la molécula como dos mitades que pueden unirse mediante una adición de Michael. Una de estas mitades se sintetizó mediante el tandem adición de Michael−condensación aldolica. Se describe la síntesis formal enantiomerica del ácido trisporico, sustancia de interés para el estudio de los aspectos reproductivos de los hongos mucorales. COREY Y EL ANÁLISIS RETROSINTÉTICO Se podría definir la síntesis orgánica como la preparación de compuestos orgánicos de estructura compleja usando materiales de partida sencillos y baratos. A la hora de sintetizar una molécula orgánica compleja aparecen elementos de auténtica creación artística, como sucede por ejemplo, con la arquitectura. Un plan de síntesis se ha comparado con un juego de ajedrez en tres dimensiones usando 40 piezas en cada lado, lo que da una idea de su complejidad. Pues bien, a pesar de ello, en cada nueva síntesis se desarrollan metodologías desconocidas que pueden modificar la estrategia inicial. A comienzos de los años 60 Corey acuña el término y desarrolla el concepto de análisis retrosintético. Considerando la molécula objetivo, él estableció las reglas que permiten dividirla en fragmentos más pequeños indicando qué enlaces han de ser rotos: de esta forma pueden obtenerse componentes más pequeños y manejables, que luego al unirlos dan lugar a la síntesis planificada. Fue importante en esta época, los 60, la visión de futuro de Corey demostrando que este análisis de lógica retrosintética podía ser incluido en un programa de ordenador: hoy en día todos los laboratorios de química orgánica pueden acceder a alguno de los múltiples programas comerciales que ayudan enormemente a la planificación de una síntesis orgánica. En los laboratorios de Corey se ha realizado en las últimas cuatro décadas la síntesis total de más de un centenar de moléculas muy complejas, muchas de ellas con importante actividad biológica, en todos los casos atendiendo a principios lógicos simples. La mayor parte de estas síntesis se recogen el su libro The Logic of Chemical Synthesis publicado en 1989 y considerado hoy en día como la Biblia de la síntesis orgánica. Para el desarrollo de las diferentes síntesis, Corey ha puesto a punto todo un arsenal de más de medio centenar de métodos, incluyendo tanto reactivos como reacciones enteramente nuevos, que reflejan frecuentemente la sencillez del genio, y que son de uso habitual en cualquier laboratorio de química orgánica del mundo: esto convierte a Corey, probablemente, en el químico que más metodología ha desarrollado a lo largo de la historia. Su dominio de la estrategia de síntesis le ha llevado a moverse con comodidad en campos frontera dentro de la química, como es el uso de los compuestos organometálicos en química orgánica o el estudio de rutas biogenéticas. Recientemente ha venido desarrollando el empleo de catalizadores de una actividad similar a la de las enzimas, capaces de producir un único enantiómero usando cantidades muy pequeñas (y a pesar de ello recuperables) del catalizador, por otra parte fácilmente accesible y de estructura sencilla: es lo que él denomina robots moleculares. *Lo más importante del trabajo de Corey ha sido la puesta a punto de una teoría general de síntesis en química orgánica conocida con el nombre de análisis retrosintético, que consiste en someter a la molécula orgánica final que se quiere sintetizar a una serie de disecciones por etapas, de acuerdo con un conjunto de reglas simples, teniendo en cuenta el carácter y el contexto estructural de los enlaces que se rompen. El análisis general, de este modo es un árbol de posibles rutas de síntesis. Corey también fue capaz de comprender el poder potencial de los ordenadores como ayuda en el análisis de los cientos de productos intermedios que 1 pueden resultar de una retrosíntesis, comprensión de la que son producto programas que, bajo supervisión, son capaces de estimar la ruta más simple hacia una nueva molécula. ESTRATEGIAS DE SINTESIS En el planeamiento de la síntesis de un producto debemos tener en cuenta: −La formación de las uniones C−C y C−heteroátomo que llevan al esqueleto de la molécula. −La introducción, interconversión y/o eliminación de grupos funcionales. −Los problemas estereoquímicos. Si bien tomamos inicialmente estos aspectos como independientes en las etapas iniciales del planeamiento, en algún punto más avanzado del análisis deberemos considerar su interacción. Podemos formular una regla de máxima simplicidad que dice que debe existir la máxima correlación entre las diferentes operaciones sintéticas individuales de manera que cada una permita, facilite o simplifique a las demás. Antes de comenzar a elaborar un plan, debemos: −Conocer los detalles estructurales de la molécula a sintetizar (modelado molecular). −Conocer los antecedentes químicos de la molécula (si es conocida) o de compuestos relacionados, especialmente su reactividad, estabilidad y comportamiento en distintas condiciones de reacción. Durante la preparación de un plan de síntesis debemos tener en cuenta: −La posibilidad de realizar un paso de síntesis debe ser alta (minimizar reacciones competitivas). −Existencia de caminos/procedimientos alternativos para cada paso. −Cumplir la regla de máxima simplicidad. Una forma de aproximación al diseño de una síntesis es elegir un material de partida que tenga alguna relación estructural con nuestro objetivo (o con una parte de él) y usando la experiencia y el conocimiento de reacciones orgánicas armar una secuencia de pasos que permita la conversión. Esta aproximación hacia delante solo es aplicable a casos sencillos y aún así puede dar lugar a secuencias poco eficientes. Por ejemplo si queremos sintetizar ácido 3−fenilpropanoico, podemos pensar en salir de un derivado del benceno con una cadena lateral funcionalizada como benzaldehido, y hacerla crecer en 2 C: 2 Sin embargo cuando la molécula es más compleja, encontrar el material de partida apropiado puede no ser tan obvio. En ese caso la estrategia que se sigue es una de análisis hacia atrás, es decir de productos a reactivos que se denomina análisis retrosintético. La metodología consiste en desarmar gradualmente el producto rompiendo uniones (uniones estratégicas) para dar fragmentos más simples que llamamos bloques de construcción o sintones. La operación de romper uniones se denomina desconexión y se efectúa siguiendo ciertas reglas lo que permite una aproximación más racional y sistematizada a resolver el problema. APLICACIONES DE LA RETROSÍNTESIS Si se intenta aplicar la estrategia de hidratación de alquinos en la preparación de la a−hidroxi etilcetona que se da a continuación, se obtendrá no sólo el producto deseado sino también otra hidroxicetona regioisomérica y por tanto la síntesis no tendrá ninguna utilidad. Retrosintesis Mezcla de hidroxicetonas Al contrario que en el ejemplo anterior, la 1,4−dimetoxibutan−2−ona se puede analizar recurriendo a los alquinos como equivalentes sintéticos del anión acilo. La retrosíntesis se basaría en la hidratación de un alquino simétrico, como se indica a continuación: El bencilidenacetal que se indica a continuación presenta un total de tres estereocentros y aparentemente no es un compuesto 1,2−difuncionalizado. Sin embargo, la desconexión del grupo metilo conduce a un alcohol y este compuesto, por desconexión del acetal origina un triol que se podría obtener por dihidroxilación de un alqueno. 3 Funcionalización de compuestos carbonílicos La reacción de halogenación de cetonas permite la obtención de compuestos 1,2−difuncionalizados. Como el átomo de halógeno es un buen grupo saliente se puede aprovechar para su sustitución mediante la reacción con especies nucleofílicas. El aminoalcohol que se indica a continuación se puede analizar aplicando esta estrategia. Su retrosíntesis sería: A continuación se indica la retrosíntesis de una diolefina que se basa en la reacción condensación aciloínica: La retrosíntesis se inicia con la desconexión de los enlaces dobles mediante la reacción de Wittig. Esto lleva a una 1,2−dicetona que se podría obtener mediante la oxidación de una ð−hidroxicetona, que es el producto resultante de la condensación aciloínica del fenilacetato de etilo. Adición de grupo funcional (AGF) La adición de un grupo funcional (AGF) es una operación retrosintética que en algunos sustratos facilita su desconexión. Los hidrocarburos saturados, puesto que carecen de funciones, son los candidatos más obvios a ser analizados mediante la adición de un grupo funcional, por ejemplo un doble enlace. Como ejemplo supongamos que se desea sintetizar el 4−propiloctano. La retrosíntesis de este compuesto se podría iniciar con la adición de un doble enlace en la zona de ramificación. La olefina resultante de la operación AGF se podría obtener en la deshidratación de un alcohol y este compuesto se podría desconectar a un reactivo organometálico, por ejemplo butil−litio y a una cetona, la 4−heptanona. Otro ejemplo de aplicación de la estrategia AGF se encuentra en la síntesis del 5−fenilpentanoato de etilo. Una forma de conectar la función de éster etílico con el anillo aromático consiste en la introducción de dos enlaces dobles entre las dos funciones, tal y como se indica en el análisis retrosintético. 4 5