Boletín Medicina Molecular
Anuncio

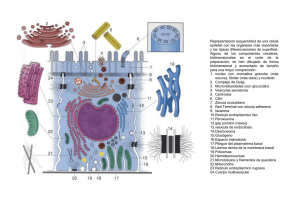
Boletín 6 Medicina Molecular 3 de septiembre de 2008 Boletín 6 3 de septiembre de 2008 1 Índice Novedades 3 3D interactivo en MedMol 3 Revisiones 3 Traduciendo descubrimientos moleculares a nuevas terapias para la arterioesclerosis 3 Temas 9 Integrinas 9 Moléculas 11 LEDGF/p75 11 Glosario 13 Poro nuclear 13 Endosoma 14 Lisosoma 15 Retículo endoplásmico 16 Técnicas 17 Sistema de dos híbridos 17 Noticias 19 Un anillo de cohesina une las cromátidas hermanas en la mitosis 19 Construcción de tejidos en 3D 19 Eventos 20 Términos de Uso Boletín 6 3 de septiembre de 2008 2 Del 29 de Septiembre al 4 de Octubre se celebra en Singapur el congreso sobre células madre, cáncer y envejecimiento “Stem cells, Cancer and Aging” 20 La segunda conferencia anual sobre RNAi y terapia tendrá lugar el próximo 22 de Octubre en Boston (USA) 21 Durante el 2 y 3 de Octubre se celebra en Dublín el congreso “Biormarker Discovery Europe” 21 Términos de Uso Boletín 6 3 de septiembre de 2008 3 Novedades 3D interactivo en MedMol A partir de ahora se encuentra disponible contenido 3D interactivo en la sección de Moléculas de MedMol. Junto con el texto explicativo se ofrece también modelos 3D interactivos que facilita la comprensión del texto. Para más información sobre cómo usar el modelo pinche aquí. Ver Instrucciones Ver Modelos 3D de la molécula LEDGF/p75 Revisiones Traduciendo descubrimientos moleculares a nuevas terapias para la arterioesclerosis Resumen La arterioesclerosis se caracteriza por un engrosamiento de la pared arterial. La arterioesclerosis es la principal causa de la enfermedad coronaria y cerebrovascular, dos de las causas más comunes de enfermedad y muerte en el mundo. Mediante ensayos clínicos se ha confirmado que ciertas lipoproteínas y el sistema renina-angiotensina-aldosterona son importantes en la patogénesis de la enfermedad cardiovascular ateroesclerótica y que actuaciones sobre estos factores producen beneficios demostrados. Nuevas iniciativas orientadas a entender cómo factores de riesgo como la hipertensión, la disregulación de lípidos en sangre y la diabetes contribuyen en la patología ateroesclerótica y también a entender la patogénesis de las placas ateroescleróticas a nivel molecular, están permitiendo descubrir nuevas dianas terapéuticas. Introducción Durante el establecimiento de la ateroesclerosis la pared arterial sufre un engrosamiento gradual que acaba con la formación de la placa ateroesclerótica que produce el estrechamiento del lumen de la arteria. Consecuentemente se reduce el aporte sanguíneo a los órganos. Esta reducción es especialmente dramática por su repercusión en el caso del corazón y del cerebro. Las placas pueden romperse bruscamente causando la formación de un coágulo que muchas veces es la causa subyacente del infarto de miocardio y del accidente cerebrovascular. La iniciación y la progresión de la lesión son procesos muy complejos existiendo aún muchos aspectos desconocidos de la aterogénesis. Además, los nuevos hallazgos deben traducirse a nuevas aproximaciones terapéuticas y muchas veces este paso es complicado. En esta revisión se discuten los avances de investigación más interesantes dentro del tema de la arterioesclerosis, resaltando especialmente aquellos con implicaciones terapéuticas. Actualmente existen 2 aproximaciones conceptuales a la terapia de la arterioesclerosis: por un lado la manipulación del metabolismo de las lipoproteínas plasmáticas y del metabolismo celular del colesterol y por otro la manipulación de los procesos inflamatorios. Aquí se discuten ambas aproximaciones y también otros nuevos tipos de terapia. También se analiza cómo los estudios de asociación a escala de genoma están influyendo en este tema. Términos de Uso Boletín 6 3 de septiembre de 2008 4 Estado actual La evidencia más convincente para elegir un gen como diana terapéutica es encontrar una asociación basada en pura genética mendeliana entre ese gen y un mayor riesgo de padecer la enfermedad. Ese es el caso de la hipercolesterolemia familiar homocigota que está causada por una mutación en el gen que codifica el receptor de la LDL. Esta observación lleva directamente a pensar que la elevada concentración de colesterol LDL en plasma puede causar ateroesclerosis. Esta observación también condujo a la idea de que incrementar la expresión de receptores para LDL reducirá la concentración de LDL en sangre y reducirá por tanto el riesgo de padecer arterioesclerosis. Recientemente se ha identificado una mutación en el gen de la LRP6 (proteína 6 relacionada con el receptor de la LDL) como responsable de la enfermedad coronaria prematura que es autosómica dominante y se acompaña de características del síndrome metabólico caracterizado por hiperlipemia, hipertensión y resistencia a la insulina. Genes candidatos a dianas terapéuticas suelen testarse genotipando grandes cohortes de pacientes y examinando si existen SNPs específicamente asociados con la arterioesclerosis. Recientemente los estudios de asociación a escala de genoma están permitiendo descubrir nuevos genes asociados a la arterioesclerosis y a sus factores de riesgo. También se están realizando estudios en ratones transgénicos para identificar y validar nuevas dianas terapéuticas y para investigar en profundidad en los mecanismos de establecimiento de la enfermedad arterioesclerótica. Sin embargo están surgiendo dudas sobre el modo en que se realizan los estudios en ratón y en la validez de su extrapolación al hombre. Metabolismo de las lipoproteínas. Es un punto clave en la intervención contra la arterioesclerosis. Un conjunto de iniciativas se centran en la LDL y otro en la HDL. Estudios tanto en animales como en humanos han demostrado que es necesario que se acumulen lipoproteínas que Términos de Uso Boletín 6 3 de septiembre de 2008 5 contienen apoB, como la LDL, para el establecimiento de la arteriosesclerosis. Las estatinas reducen la biosíntesis de colesterol y aceleran el aclaramiento por el hígado de la LDL del plasma. Las estatinas han sido uno de los grandes éxitos de la medicina traslacional que ha impulsado posteriores iniciativas orientadas a descubrir los mecanismos moleculares que rigen la concentración de LDL en plasma. El número de receptores de LDL presentes en los hepatocitos es un factor clave pero la regulación de la concentración de LDL es un proceso muy complejo. Así, por ejemplo, la enfermedad de la hipercolesterolemia autosómica recesiva está causada por una alteración en los mecanismos de reciclaje del receptor de LDL. Estudios genéticos de asociación han descubierto que mutaciones en el gen que codifica la PCSK9 (Proprotein Convertase Subtilisisn/kesin 9) se asocian a una forma de hipercolesterolemia autosómica dominante. Un estudio independiente también encontró que ratones con una dieta elevada en colesterol tenían una expresión reducida de Pcsk9 en hígado y que por el contrario la sobreexpresión hepática de este gen causaba una marcada hipercolesterolemia. Estudios posteriores mostraron que la PCSK9 se une a los receptores de LDL llevándolos a una ruta de degradación impidiendo su reciclaje. Las estatinas aumentan la PCSK9 con lo que esto podría ser la explicación de que en algunos casos los tratamientos con estatinas no tengan el efecto deseado. Por todo esto PCSK9 es una diana terapéutica muy atractiva para reducir las concentraciones de colesterol LDL. Las VLDL ( Very Low Density Lipoproteins) son las proteínas precursoras de las LDL y están muy elevadas a nivel hepático en individuos con resistencia a la insulina, con diabetes tipo 2 y con hiperlipemia familiar combinada. Mutaciones en la apoB, proteína estructural clave en la VLDL y LDL, causan disminución en la concentración de LDL y mutaciones en la MTP (triglyceride transfer protein), que es necesaria para cargar triglicéridos en la apoB, causan ausencia de LDL en plasma. Están en desarrollo estrategias terapéuticas basadas tanto en la inhibición de la producción de apoB con oligonucleótidos antisentido como en la inhibición de la MTP con moléculas pequeñas. Estudios de asociación a escala de genoma probablemente descubrirán nuevas dianas para reducir la concentración de LDL. Existe otro conjunto de iniciativas centradas en la HDL ya que su concentración es inversamente proporcional al riesgo de padecer arterioesclerosis. En animales la infusión de apoA-I, el mayor componente de la HDL, reduce la extensión de la ateroesclerosis. Existen 2 ensayos clínicos en humanos basados en este hecho que parecen estar teniendo resultados positivos. Se detectó que la causa de la elevada concentración de HDL en algunos japoneses se debía a la deficiencia de CETP (Cholesteryl Ester Transfer Protein). Esto inició la persecución de tratamientos basados en la inhibición de esta enzima. El primer producto ensayado, el torcetrapib, fracasó porque, además de inhibir la enzima CETP, aumentaba la presión arterial y la concentración de aldosterona. Se están iniciando estudios basados en la inhibición de la lipasa endotelial que rompe la HDL. Estudios a escala de genoma pueden descubrir nuevas dianas terapéuticas. El mecanismo mejor establecido por el que la HDL protege de la ateroesclerosis es favorecer el proceso denominado trasporte reverso del colesterol, que lo lleva desde los macrófagos hasta el hígado para ser excretado por la bilis. Las proteínas ABCA1 y ABCG1 intervienen en este proceso. El LXR (Liver X receptor), que es un receptor nuclear que se estimula por derivados oxidados del colesterol, estimula la transcripción de ABCA1 y ABCG1. LXR es una diana terapéutica de varias iniciativas centradas en el aumento del transporte reverso de colesterol. La HDL tiene otras propiedades que podrían intervenir en su capacidad anti-aterogénica. Entre ellas su capacidad de activar la NOS3 (Nitric oxide Synthase 3), su efecto antiinflamatorio in vitro e in vivo y su capacidad de unirse a los lipopolisacáridos de la pared bacteriana. Los componentes proteicos de la HDL también han sido utilizados como dianas terapéuticas. Procesos inflamatorios La inflamación es crucial en el desarrollo de las placas ateroescleróticas. Los tres puntos relacionados con la inflamación en los que se centran las posibles terapias contra la arterioesclerosis son: Lípidos activos Sistema renina-angiotensina-aldosterona Términos de Uso Boletín 6 3 de septiembre de 2008 6 Procesos celulares Las prostaglandinas son lípidos activos que son clave en el proceso de la inflamación. El efecto cardioprotector de la aspirina parece deberse a la inhibición de COX1 en las plaquetas. COX1 es una isoenzima de la ciclo-oxigenasa que lleva a cabo el primer paso de la síntesis de las prostaglandinas a partir del ácido araquidónico. Sin embargo, inhibidores selectivos de COX2, la otra isoenzima de la ciclo-oxigenasa, producen un efecto contrario, aumentando el riesgo de accidentes aterotrombóticos. Este efecto parece deberse a la inhibición de la síntesis de la prostaciclina PGI2 que es ateroprotectora en ratones. La prostaglandina E2 parece tener un efecto promotor de aterosclerosis. El conocimiento exhaustivo y completo de este complejo network de la inflamación en el que las prostaglandinas parecen jugar un complicado papel probablemente abra nuevas vías de intervención en el proceso arteriosclerótico. Los leucotrienosson otra familia de lípidos activos importantes en la inflamación. Se ha demostrado por estudios de asociación que el gen ALOX5AP se asocia con el riesgo de infarto de miocardio. Este gen codifica la enzima FLAP importante en la ruta 5-LO-LTB4. Inhibición de esta ruta es otro punto de intervención en la terapéutica de la ateroesclerosis. Los fosfolípidos oxidados son otros lípidos activos proinflamatorios que se han involucrado en la aterogénesis. Enzimas como mieloperoxidasas y fosfolipasas son, por tanto, también punto de atención en el desarrollo de nuevas terapias de la ateroesclerosis. También se ha encontrado que la inmunización con formas oxidadas de LDL produce una respuesta beneficiosa mediada por el anticuerpo natural T15. Esta es otra posible vía terapéutica a investigar. Sistema renina angiotensina Este sistema es crucial en la determinación de la tensión arterial y su importante papel en la arterioesclerosis ha sido demostrado en animales y en humanos. Recientes líneas de evidencia parecen indicar que su efecto pro-aterogénico no es únicamente debido al aumento de la tensión arterial. Aunque ya existen tratamientos basados en la inhibición de enzimas Términos de Uso Boletín 6 3 de septiembre de 2008 7 de este sistema, entender nuevas vías de acción no directamente relacionadas con la tensión arterial puede abrir nuevas líneas de investigación que permitan nuevas estrategias terapéuticas. Procesos celulares en la lesión Las moléculas de adhesión de las células endoteliales de la lesión son fundamentales en la evolución del proceso aterogénico, ya que reclutan leucocitos y células fundamentales en el proceso. Bloquear estas moléculas de adhesión es otra estrategia terapéutica posible. La células endoteliales son capaces de detectar el flujo turbulento y parece que el factor de Kruppel-like factor 2 es fundamental en la transducción de esta señal. Este factor es otra posible diana terapéutica. El reclutamiento de monocitos al lugar de la lesión, que luego se diferenciarán a macrófagos, es otro proceso clave en el establecimiento de la lesión arterioesclerótica. Ser capaces de bloquear de forma selectiva el tipo de monocitos que acuden a la lesión es muy importante para poder evitar la formación de la placa aterosclerótica. Ly6C, CCR2 y CX3CR1 parecen ser los marcadores de superficie de esta subpoblación de monocitos. Estudios de asociación basados en SNPs han proporcionado evidencias de que los TLRs (Toll-like Receptors) son importantes en la arteriosclerosis humana. Si es viable la intervención a este nivel es otra línea de investigación en la que incidir. Las células dendríticas y la señalización vía CCR7 parecen ser otro punto de intervención my prometedor para conseguir la regresión de las lesiones. La posibilidad de la terapia celular es otra vía terapéutica que está suscitando interés. Trombosis asociada a la ateroesclerosis La aparición de procesos agudos como el infarto de miocardio o el accidente cerebrovascular dependen de la formación de trombos oclusivos. El proceso de formación de un trombo puede desencadenarse por ruptura de la lesión ateroesclerótica y exposición del material trombogénico o por erosión de la capa fibrosa que delimita la lesión. En la ruptura de la placa parecen intervenir las enzimas denominadas metaloproteinasas de la matriz (MMP : Matrix MetaloProteinases). En concreto la MM9 producida por macrófagos es la más frecuentemente detectada. Su importancia en la ruptura de la placa se ha comprobado en ratón. También han sido involucradas las catepsinas, proteasas lisosomales capaces de degradar elastina y colágeno aún al pH neutral de la matriz extracelular. También parece que los procesos de necrosis y apoptosis que tienen lugar en la lesión ateroesclerótica, tanto en macrófagos como en células de músculo liso, aumentan el riesgo de ruptura de la placa. El papel de la muerte celular en los distintos estadíos de la lesión no se conoce con exactitud y es un área importante para futuras investigaciones. Genética de la ateroesclerosis en humanos La enfermedad cardiovascular por arterioesclerosis se agrupa en familias y tienen un fuerte componente genético pero determinar los genes involucrados no es tarea fácil. Estudios en familias con enfermedad coronaria prematura sólo descubrieron al gen LRP6 como posiblemente involucrado. Recientemente los estudios de asociación a escala de genoma están permitiendo detectar nuevos genes involucrados en estas complejas patologías. Así se han identificado los genes CDKN2A que codifica la enzima INK4A y el gen CDKN2B que codifica a INK4B. Ambas proteínas son miembros de la familia INK4 que son supresores del ciclo celular donde regulan el paso de G1 a S. Además tienen un papel en la inhibición de crecimiento mediada por el TGFbeta que parece ser un proceso implicado en la ateroesclerosis. Similares estudios han mostrado que los genes PSRC1, MIA3 y SMAD3 que codifican reguladores del crecimiento celular están significativa- Términos de Uso Boletín 6 3 de septiembre de 2008 8 mente asociados con el riesgo de padecer infarto de miocardio. Otro gen detectado como asociado al riesgo de infarto ha sido la chemoquina CXCL12 que juega un papel en la movilización, ŞhomingŤ y diferenciación de los progenitores vasculares en respuesta al daño vascular. Otro gen relacionado parece ser el que codifica la proteína metilen-tetrahidrofolato-deshidrogenasa 1-like, aunque aún su posible conexión con el riesgo a infarto no se conoce. Los genes que codifican las proteínas apoE, ABCA1, aopA-V, CETP, lipoprotein-lipasa y lipasa hepática se han detectado como asociados a síndromes con afectación de las concentraciones de lípidos. Un SNP que afecta al gen de la GCKR que codifica un regulador de la glucoquinasa tiene una asociación altamente significativa con la concentración de triglicéridos. La glucoquinasa es la primera enzima de la vía glicolítica y podría afectar a la síntesis de triglicéridos. Tres estudios de asociación a escala de genoma posteriores en torno a la diabetes encontraron que tanto el gen ANGPTL3, que codifica la angiopoyetina-like 3 que afecta al metabolismo de los triglicéridos en ratón, como el gen MLXIPL que codifica un factor de transcripción que conecta el flujo hepático de carbohidratos con la síntesis de ácidos grasos están relacionados con la concentración de triglicéridos. Los genes CELSR2, PSRC1, SORT1, CILP2, PBX4, TRIB1 parecen asociarse con la concentración de colesterol-LDL. El gen SORT1 paralelamente fue detectado en estudios de asociación con infarto de miocardio como posible gen involucrado. Este gen codifica la sortilisina 1 que es un receptor multiligando de superficie. El gen GALNT2 que codifica la N-acetil-galactosaminil-transferasa 2, que es una enzima involucrada en la O-glicosilación se encontró como asociado a la concentración del colesterol- HDL. Todos estos genes detectados como asociados a la arterioesclerosis y a sus factores de riesgo son posibles nuevas dianas terapéuticas sobre las que iniciar nuevas líneas de investigación en el tratamiento y prevención de la arterioesclerosis. Conclusiones La arterioesclerosis ha sido objeto de una intensa investigación tanto básica como aplicada que ha resultado en un avance sustancial en el conocimiento de la patogénesis de la enfermedad a nivel molecular. Esto ha conducido al desarrollo de terapias eficaces como por ejemplo la reducción en plasma de lipoproteínas aterogénicas utilizando estatinas, o el bloqueo de la actividad del sistema renina-angiotensina con los inhibidores ACE o los bloqueantes de receptores de angiotensina. La integración de resultados de estudios de biología celular, fisiología animal, genética humana y de terapéutica basada en mecanismos permitirá seleccionar la nueva generación de dianas terapéuticas. El colesterol LDL y la presión arterial seguirán siendo indicadores aceptables para medir la eficacia de algunos nuevos fármacos pero es probable que algunas nuevas terapias necesiten nuevos indicadores de eficacia. Nuevos biomarcadores y nuevas técnicas no invasivas de visualización (imaging) serán necesarias para mejorar los ensayos clínicos de nuevas terapias. La gran inversión de la comunidad biomédica en la investigación multidisciplinar sobre la arteriosclerosis permite aventurar la aparición de nuevas terapias tanto para la prevención como para el tratamiento de la arterioesclerosis. Bibliografía Translating molecular discoveries into new therapies for atherosclerosis (Ver página Web) Términos de Uso Boletín 6 3 de septiembre de 2008 9 Temas Integrinas Resumen Las integrinas forman parte de las moléculas de adhesión celular (CAMs: Cell Adhesion Molecules). Son proteínas de membrana formadas por dos cadenas, la alfa y la beta. Participan en interacciones con proteínas CAMs de otras superfamilias en las que se requiere, en muchos casos, la participación de cationes divalentes como el calcio o el magnesio. Las integrinas pueden interaccionar con componentes de la matriz extracelular y, a nivel intracelular, interaccionan con proteínas que las conectan funcionalmente con el citoesqueleto y con enzimas que desencadenan cascadas de señalización. Estas rutas de señalización son integradas en la célula junto con otras señales, a veces procedentes de otros tipos de CAMs, pudiendo respuestas tan diversas como la proliferación, la migración, la diferenciación, la muerte o la activación, según el caso. Su participación en procesos celulares básicos hace que las CAMs sean fundamentales en procesos como la embriogénesis o la regeneración de tejidos. Las integrinas juegan un papel importante en la patogenia de múltiples enfermedades autoinmunes y en el desarrollo de metástasis en los procesos tumorales. Concepto La familia de las integrinas incluye un amplio grupo de proteínas heterodiméricas constituidas por dos subunidades transmembrana denominadas cadena alfa y cadena beta. Las diferentes subfamilias de integrinas se clasifican según el tipo de cadena beta que poseen. Hasta ahora se conocen unas 16 cadenas alfa y unas 8 cadenas beta diferentes que combinándose de forma específica generan 20 integrinas diferentes. En el extremo amino terminal de las cadenas alfa hay 7 u 8 regiones homólogas tipo integrina, la región tercera y cuarta en algunos casos se unen a cationes divalentes (Ca++, Mg++). Los cationes ejercen un papel clave en la función adherente de las integrinas. Las cadenas beta son glicoproteínas transmembrana que poseen regiones muy conservadas en la porción extracelular. Ambas cadenas poseen regiones ricas en cisteínas que participan en la formación de puentes disulfuro intracatenarios. La cadena alfa suele ser la principal responsable de la interacción con el ligando. Las integrinas tienen un dominio citoplasmático pequeño que no genera señales intracelulares directamente. Pueden interaccionar con proteínas adaptadoras originando señales intracelulares al unirse a sus ligandos. Generalmente las integrinas se agrupan en los complejos de adhesión focal en la membrana donde se asocian a proteínas citoplasmáticas como la talina y la actina alfa, que a su vez interaccionan con proteínas unidas al citoesqueleto como la vinculina, la tensina y la actina. En estos complejos se asocian también proteínas intracelulares involucradas en la generación de señales de activación como la quinasa de adhesión focal (FAK: Focal Adhesion Kinase), serin/treonin quinasas como la proteín quinasa C (PKC: Protein Kinase C). Estas enzimas generan cascadas de señalización celular que dirigen fenómenos como la reorganización del citoesqueleto o la inducción de genes. Estas señales pueden tener efecto sinérgico o antagónico con rutas activadas por otros receptores celulares produciéndose complejos procesos de integración de señales que convergen en puntos comunes y finalmente resultan en respuestas de activación, proliferación, diferenciación o muerte celular. Las diferentes subfamilias de integrinas, clasificadas según su cadena beta, tienen varias nomenclaturas. Tres importantes subfamilias son la subfamilia beta-1, la beta-2 y la beta-7. Las proteínas de la subfamilia beta-1 se caracterizan por presentar la cadena beta-1 de tipo CD29. Su cadena alfa puede ser de varios tipos. En este grupo se incluyen las proteínas VLA (Very Late Activation) con 6 tipos diferentes de cadena alfa (CD49a-f) que generan las proteínas VLA1, VLA2, VLA3, VLA4, VLA5 y VLA6. Las proteínas VLA se expresan Términos de Uso Boletín 6 3 de septiembre de 2008 10 en la mayor parte de las células del organismo, excepto en los granulocitos. En basófilos y neutrófilos no existen este tipo de integrinas y sólo en eosinófilos se expresa la integrina VLA4 (alfa-4/beta-1). Los linfocitos expresan diversas integrinas beta-1 especialmente si están activados ya que se ha comprobado un incremento significativo días después de la activación. Las integrinas que comparten la cadena beta-2, conocida como CD18, se denominan integrinas linfoides y se asocian a tres isoformas de cadena alfa que recibe el nombre de CD11 formando las integrinas: LFA-1 (Lymphocyte Function-associated Antigen-1) o CD11a/CD18 MAC-1, CR3 o CD11b/CD18 p150,95 o CD11c/CD18 Estas integrinas se localizan en los leucocitos y participan en la adhesión a las células endoteliales activadas, necesaria para la extravasación de los linfocitos a través del endotelio hacia el foco inflamatorio y en la quimiotaxis de los leucocitos hacia los sitios de inflamación. Los miembros de la subfamilia de las integrinas beta-7 se expresan principalmente en linfocitos localizados en placas de Peyer, en la lámina propia y en el epitelio intestinal. La afinidad de las integrinas por sus ligandos varía y depende principalmente del estado conformacional del heterodímero y de la densidad y localización de las integrinas en la membrana. Los factores que producen la activación celular de linfocitos, como antígenos o citocinas, inducen indirectamente el cambio en la conformación de las integrinas aumentando su afinidad por el ligando. Los cambios en la distribución de integrinas en la membrana celular parecen estar causados por modificaciones del citoesqueleto que ocurren como consecuencia de las señales intracelulares generadas durante la activación celular. La presencia de cationes divalentes también puede influir en la conformación de las integrinas afectando las interacciones con sus ligandos. Las integrinas median interacciones célula-célula y célula-matriz extracelular. Se unen a proteínas de la matriz extracelular como la fibronectina y la laminina, a otras moléculas de adhesión como las ICAM-1 de la superfamilia de las inmunoglobulinas o a moléculas solubles como el fibrinógeno y el Factor de von Willebrand relacionadas con la coagulación. La unión entre las integrinas y componentes de la matriz extracelular como la laminina se lleva a cabo gracias a las regiones MIDAS (Metal Ion-Dependent Adhesion Site) formadas por dos subunidades de la cadena alfa junto con el átomo de calcio. La región MIDAS reconoce la secuencia de aminoácidos RGDS presente en la fibronectina. Esta secuencia se introduce en el hueco formado por las dos subunidades y el residuo de aspartato (D) se une por coordinación al ión de calcio. Las integrinas median interacciones en una gran variedad de células. Así, por ejemplo, las plaquetas activadas usan la proteína VLA-2 para su adhesión al colágeno, y la VLA-6 para interaccionar con la laminina. Las células endoteliales también se pueden unir al colágeno y a la laminina mediante VLA-2. La VLA-4, ligando para las moléculas de adhesión vascular de tipo I (VCAM-I: Vascular Cell Adhesion Molecules-I), se expresa de forma diferencial de modo que está presente en monocitos, linfocitos T y B y eosinófilos, pero no en neutrófilos y basófilos. Este patrón de expresión puede que sea un mecanismo de reclutamiento selectivo de leucocitos ante diferentes condiciones. Las integrinas son moléculas clave en un gran número de procesos. Defectos en su síntesis pueden originar graves trastornos como la deficiencia de adhesión leucocitaria tipo I. Esta enfermedad se debe a una deficiencia autosómica recesiva que provoca un defecto en las integrinas de tipo beta-2. Esta deficiencia afecta a procesos dependientes de adhesión Términos de Uso Boletín 6 3 de septiembre de 2008 11 leucocitaria como la fagocitosis de organismos opsonizados (ver el sistema del complemento) ya que el receptor de iC3b es una integrina <br/><br/> Actualmente se han aprobado dos fármacos que actúan sobre las interacciones de las integrinas. Se trata de dos anticuerpos monoclonales humanizados que actúan reconociendo e interaccionando con dos integrinas. El efalizumab que interacciona con la integrina LFA-1 y se aplica en el tratamiento de las placas cronificadas de enfermos con psoriasis, y el natalizumab que interacciona con VLA-4 y se emplea en el tratamiento de la esclerosis múltiple. Bibliografía Anti-adhesion therapies 3. Adhesion molecules and receptors Adhesion molecules and atherosclerosis (Ver página Web) Moléculas LEDGF/p75 Resumen P75 es una isoforma de la proteína LEDGF (“Lens Epithelium-Derived Growth Factor”) que suele nombrarse LEDGF/p75 o simplemente p75. LEDGF es una proteína recientemente descubierta capaz de interaccionar con el coactivador general PC4 (Positive Cofactor 4). LEDGF se relaciona con la respuesta frente al estrés y tiene funciones antiapoptóticas. Recientemente ha surgido gran interés la isoforma p75 ya que se ha comprobado que interacciona estrechamente con la integrasa del virus HIV-1. p75 forma parte del complejo de preintegración (PIC: Pre-Integration Complex) y, aunque no es imprescindible, ayuda a la integración del cDNA vírico en regiones transcripcionalmente activas del genoma. Para ver un modelo 3D de la integrasa del virus unida a LEDGF/p75 pinche aquí Función de esta molécula LEDGF es una proteína relacionada con la supervivencia celular ya que actúa como coactivador transcripcional de proteínas antiapoptóticas relacionadas con el estrés. Se encuentra asociada a la cromatina condensada en el núcleo. Está codificada en el gen PSIS1 del que derivan dos isoformas p75 y p52. La isoforma p52 también tiene actividad de activador transcripcional, está presente en más tejidos y no interactúa con la integrasa del virus HIV-1. Las dos isoformas, p75 y p52, comparten la región N terminal pero la p75 cuenta con un dominio adicional C-terminal que es el que participa en la interacción con la integrasa. Mediante esta región N terminal ambas isoformas establecen múltiples interacciones con la maquinaria transcripcional y con secuencias específicas del genoma. Tan sólo la isoforma p75 tiene el dominio de unión a la integrasa del HIV-1 llamado IBD (“Integrase Binding Domain”) en la zoma C terminal. Para ver el modelo con el detalle de la interacción pinche aquí A pesar del gran interés que han suscitado recientemente, aún no se conocen con exactitud las redes de transcripción reguladas por ambas proteínas. Términos de Uso Boletín 6 3 de septiembre de 2008 12 Patologías relacionadas con esta molécula Una aberración cromosómica que afecta al gen que codifica la proteína LEDGF se asocia a un tipo de leucemia mieloide crónica pediátrica. Algunas patologías de tipo autoinmune parecen asociarse a alteraciones de la p75. La participación de la isoforma p75 en el ciclo de vida del virus del SIDA es el punto más candente en medicina ya que ofrece un nueva posible diana terapéutica para el SIDA. La p75 juega un importante papel en la fase temprana de la infección vírica al interaccionar con la integrasa. Actualmente se investiga en nuevas estrategias contra el virus basadas en la interacción integrasa- p75. La interacción entre integrasa y p75 se produce entre el dominio IBD de la p75, situado en su dominio C-terminal, y el dominio catalítico de la integrasa del virus del SIDA. Estudios cristalográficos y de resonancia magnética nuclear han confirmado las regiones de interacción entre ambas proteínas. En la imagen se representan únicamente los dominios IBD de dos moléculas p75 interactuando con los dominios catalíticos de un dímero de integrasa. La interacción se lleva a cabo en dos regiones cuya interfaz describiremos a continuación: En la primera interfaz de interacción los aminoácidos interactuantes son F406 de p75 y W131 de la integrasa del virus HIV-1. En la segunda interfaz de interacción participan por parte de la integrasa vírica el residuo W132 de un monómero y la región comprendida entre I161 y E170 del otro monómero y por parte de la p75 los residuos I365 y D366 (para ver modelo 3D pinche aquí). Aunque aún se desconoce la conformación que adquiere la integrasa durante el proceso de integración del genoma vírico en el genoma del hospedador, se ha comprobado que la p75 aparece asociada a la integrasa tanto en el citosol como en el núcleo. La unión de p75 a la integrasa proporciona una mayor estabilidad y actividad a la integrasa. Por un lado parece que p75 protege a la integrasa de su ubiquitinación y degradación en el proteasoma en el citosol. p75 posee también secuencias NLS, que permiten que el cDNA vírico atraviese el complejo del poro nuclear. Por último, aunque no es imprescindible en el proceso de integración, se ha comprobado que p75 aumenta la capacidad de integración del cDNA vírico y aumenta su integración en regiones transcripcionalmente activas y ricas en AT. El conocimiento de los elementos clave de esta interacción entre LEDGF/p75 y la integrasa del virus del SIDA ha permitido diseñar péptidos capaces de bloquear esta interacción que parece fundamental en el ciclo de vida del virus. Así se ha conseguido diseñar y sintetizar péptidos similares a la región entre los residuos 355 a 377 de la p75 que experimentalmente han mostrado cierta actividad inhibitoria de la catálisis de la integrasa. También existen datos acerca de un derivado del ácido benzoico llamado D77 que parece ser capaz de bloquear la interacción entre p75 y la integrasa viral. Esta molécula es una nueva diana terapéutica para el SIDA que abre nuevas vías de actuación. Bibliografía D77, one benzoic acid derivative, functions as a novel anti-HIV-1 inhibitor targeting the interaction between integrase and cellular LEDGF/p75 Inhibitory profile of a LEDGF/p75 peptide against HIV-1 integrase: insight into integrase-DNA complex formation and catalysis Identification of the LEDGF/p75 binding site in HIV-1 integrase Blocking interactions between HIV-1 integrase and cellular cofactors: an emerging anti-retroviral strategy Retroviral DNA integration: HIV and the role of LEDGF/p75 Isolation of cDNAs encoding novel transcription coactivators p52 and p75 reveals an alternate regulatory mechanism of transcriptional activation Identification and characterization of a functional nuclear localization signal in the HIV-1 integrase interactor LEDGF/p75 (Ver página Web) Términos de Uso Boletín 6 3 de septiembre de 2008 13 Glosario Poro nuclear Definición El complejo del poro nuclear es una estructura que permite el intercambio de moléculas entre el citosol y el núcleo de la célula. Se trata de un complejo molecular muy grande (de unos 125 millones de Da), tiene forma de cesta de baloncesto y atraviesa la envoltura nuclear. Está formado por unas 100 proteínas ordenadas en simetría ortogonal. El complejo del poro presenta unos canales acuosos que están permanentemente abiertos y por ellos difunden libremente sustancias de hasta 5000 Da. Proteínas de hasta 60000 Da pueden pasar por transporte activo con una velocidad que depende del tamaño de la proteína. El número de poros del núcleo es variable y se adapta a los requerimientos del tráfico de sustancias. Normalmente hay unos 3000 poros por núcleo. La envoltura nuclear es la estructura que delimita el núcleo separando del citoplasma el material genético que contiene. Está formada por dos membranas continuas. La membrana interna está en contacto con proteínas clave para la estabilidad del núcleo que constituyen la lámina nuclear y la membrana externa es muy parecida a la del retículo endoplásmico. De hecho ambas estructuras están unidas formando un continuo. El poro nuclear permite la comunicación entre el citoplasma y el núcleo ya que permite el paso de sustancias a través de la envoltura nuclear. Así, posibilita la necesaria entrada de proteínas y bases nitrogenadas al interior del núcleo y la salida Términos de Uso Boletín 6 3 de septiembre de 2008 14 de ARNm, ARNt y ribosomas al citoplasma. Durante la mitosis el poro se desorganiza al igual que la envoltura nuclear y se vuelve a reorganizar en interfase a la vez el núcleo. Para que una proteína sea reconocida para introducirse en el núcleo debe presentar en su secuencia de aminoácidos una señal de localización nuclear. Esta señal es una secuencia de unos pocos aminoácidos que aunque es variable siempre es rica en aminoácidos cargados positivamente. La señal de localización celular no se elimina de las proteínas ya que el proceso de importación o exportación puede repetirse para una misma proteína. Esta señal de localización nuclear se ha encontrado en proteínas de algunos virus, como el SV40. En el proceso de transporte a través del poro participan varios elementos. La señal de localización nuclear es reconocida en el citosol por una proteína llamada importina. La importina es capaz de interaccionar con elementos móviles del complejo del poro permitiendo el paso de la proteína al interior del núcleo. Ya en el núcleo la proteína se separa y la importina vuelve al citosol saliendo por el poro. El proceso implica un gasto de energía en forma de GTP que va unido a la importina. Existe además un sistema análogo de exportación muy parecido en el que participa una proteína llamada exportina. Mediante este sistema de la exportina salen los ARN mensajeros ya procesados en el núcleo. Hay procesos, como el ensamblaje de las subunidades del ribosoma, que requieren varios pasos de sus elementos a través del poro. En estos casos primero se sintetizan las subunidades proteicas en el citosol que son internalizadas por la importina al núcleo donde se unen a ARN ribosómico y una vez ensamblados salen por el poro vía exportina. (Ver página Web) Endosoma Definición El endosoma es una vesícula con membrana encargada de transportar el material procedente del exterior que ha sido captado mediante endocitosis. Este material endocitado podrá ser degradado, si el endosoma se fusiona con lisosomas, reciclado o transportado a través de la célula vía transcitosis. Actualmente no se considera que los endosomas sean orgánulos celulares sino compartimentos dentro del citoplasma que funcionan como transportadores de material procedente del exterior que entra a la célula por endocitosis. El destino de este material puede ser reciclaje, degradación y transcitosis. El proceso de formación del endosoma comienza en primer lugar con la formación del endosoma temprano por fusión de varias vesículas endocíticas procedentes de la membrana plasmática que pueden están recubiertas por la proteína clatrina. El reciclado de estos materiales permite que algunas moléculas sean recuperadas y llevadas de nuevo a membrana plasmática como ocurre en la endocitosis mediada por receptor, donde el receptor es reciclado. Para llevar a cabo el proceso de degradación del material endocitado, los endosomas tempranos se convierten en endosomas tardíos que se fusionan con los lisosomas iniciándose así la degradación del material. En el transporte vía transcitosis el material endocitado se transporta en endosomas de un extremo de la célula a otro liberándose mediante exocitosis. Términos de Uso Boletín 6 3 de septiembre de 2008 15 Este tipo de transporte es característico de la transferencia de anticuerpos maternos de la leche materna desde el intestino hasta a la sangre del recién nacido. Los anticuerpos maternos, presentes en la leche, son captados por las células intestinales del recién nacido y se transportan vía transcitosis a los vasos sanguíneos que irrigan el intestino. El proceso de endocitosis puede ser empleado por algunos virus como mecanismo de entrada en la célula. Uno de los casos más estudiados es el del virus de la gripe. El virus de la gripe tiene en su envuelta la proteína hemaglutinina que cambia de conformación según el pH. Cuando el virus ha sido endocitado y se ha producido el descenso de pH en la vesícula tras la fusión con el lisosoma la hemaglutinina cambia de conformación permitiendo que el virus salga de la vesícula al citosol donde puede llevar a cabo su replicación. Se han descrito alteraciones en endosomas en muchas enfermedades. En neuronas de enfermos de Alzheimer se han encontrado endosomas de gran tamaño probablemente debido a la expresión de formas mutadas de la proteína APP o a la expresión de la APP-BP1 (APP Binding Protein 1). (Ver página Web) Lisosoma Definición El lisosoma es un orgánulo pequeño característico de células eucariotas. Su función es la digestión tanto de material endocitado (nutrientes, microorganismos, orgánulos, restos de otras células, etc.) como de material de desecho intracelular (orgánulos inservibles). La alteración de la función de las enzimas lisosomales causa enfermedades crónico-progresivas graves. El lisosoma es una vesícula delimitada por membrana. Contiene multitud de enzimas digestivas que sólo son activas a pH ácido (en torno a 5) por lo que no suponen peligro para la propia célula al no ser activas al pH característico del citosol (mucho más básico que el del interior del lisosoma). Para mantener el pH ácido en el interior el lisosoma cuenta con bombas de protones. Las enzimas lisosómicas son principalmente hidrolasas ácidas. Entre ellas se encuentran proteasas, lipasas, fosfatasas y nucleasas. Las hidrolasas lisosómicas se sintetizan en el retículo endoplásmico y acaban su maduración en el aparato de Golgi donde son marcadas con manosa-6-fosfato. Del aparato de Golgi surgen por gemación los lisosomas, conteniendo aquellas proteínas que fueron marcadas con manosa-6-fosfato. Las proteínas que se encuentran en la membrana de la vesícula están altamente glicosiladas para evitar su degradación por las hidrolasas del lisosoma. Los lisosomas que surgen del aparato de Golgi se conocen como lisosomas primarios. Para digerir orgánulos o microorganismos, estos lisosomas se fusionan con vesículas autofágicas o fagocíticas respectivamente, y forman lisosomas secundarios. Hay unos orgánulos conocidos como orgánulos relacionados con los lisosomas que son específicos de ciertas células y se caracterizan por poseer enzimas propias de los lisosomas. Algunos Términos de Uso Boletín 6 3 de septiembre de 2008 16 ejemplos son los melanosomas de melanocitos y los gránulos densos de plaquetas. Fallos en el funcionamiento de estos orgánulos causan enfermedades como la enfermedad de Hermansky-Pudlak. Defectos en la función lisosomal producen las enfermedades conocidas como enfermedades lisosomales. En ellas las macromoléculas no se degradan y se van almacenando dentro de los lisosomas lo que hace que aparezcan como grandes vesículas en el citoplasma. Ocurren por deficiencia de las hidrolasas ácidas o de algunas de sus subunidades, de sus activadores, de sus transportadores o del marcaje para dirigirlas a los lisosomas. Las enfermedades lisosomales se clasifican según la macromolécula que queda almacenada: Enfermedades lisosomales con acúmulo de glicolípidos, como la enfermedad de Gaucher, la de Tay-Sachs o la de Fabry Enfermedades lisosomales con acúmulo de esfingomielina, como la enfermedad de Niemann Pick (tipos A y B) Enfermedades lisosomales con acúmulo de triglicéridos, como la enfermedad de Wolman Enfermedades lisosomales con acúmulo de glucosaminoglicanos, como la enfermedad de Hunter (ó mucopolisacaridosis tipo II) Enfermedades lisosomales con acúmulo de glucógeno, como la enfermedad de Pompe Enfermedades lisosomales con acúmulo de glicoproteínas, como la sialidosis También hay enfermedades lisosomales producidas por defectos en los transportadores localizados en la membrana del lisosoma como la cistinosis y la enfermedad de Salla, en las que se acumula cistina y ácido siálico respectivamente. También hay enfermedades que se deben a fallos en el marcaje de las proteínas en el Golgi, como la mucolipidosis II y la mucolipidosis III que es menos grave. (Ver página Web) Retículo endoplásmico Definición El retículo endoplásmico es un orgánulo distribuido por todo el citoplasma de la célula eucariota. Forma parte del sistema endomembranoso. Existen dos tipos de retículo endoplásmico que llevan a cabo funciones diferentes, el rugoso y el liso. El rugoso se encarga de la síntesis y el plegamiento correcto de las proteínas mientras que el liso lleva a cabo la síntesis de lípidos, almacenamiento de calcio y detoxificación de drogas. El retículo endoplásmico es un orgánulo formado por una serie de túbulos, sacos y vesículas rodeados de membrana e interconectados entre sí. Se pueden distinguir dos tipos: el rugoso y el liso. En las células musculares se encuentra un tercer tipo derivado del retículo endoplásmico liso conocido como retículo sarcoplásmico. El retículo endoplásmico rugoso presenta en su superficie ribosomas que se encuentran sintetizando proteínas cuyo destino puede ser la membrana plasmática, el exterior de la célula o los lisosomas y endosomas. En el retículo rugoso las proteínas que están siendo sintetizadas por los ribosomas se pliegan y sufren también algunas modificaciones posttraduccionales como la N-glicosilación sobre residuos de asparragina. El plegamiento de las proteínas recién sintetizadas es dirigido por las chaperonas. Las proteínas que se pliegan de forma inadecuada son degradadas en un proceso conocido como UPR (Unfolded Protein Response) o respuesta a proteínas mal plegadas. Fallos en esta respuesta pueden causar el acúmulo de proteínas anómalas en el interior del retículo que puede producir el llamado “estrés del retículo endoplásmico”. Este Términos de Uso Boletín 6 3 de septiembre de 2008 17 tipo de estrés se relaciona con la patogenia de importantes enfermedades como la diabetes o la ateroesclerosis. La respuesta a proteínas mal plegadas está también relacionada con los procesos de autofagia en la que se produce la degradación de los propios componentes de la célula por formación de autofagosomas a partir de membranas del retículo endoplásmico. Tras su paso por el retículo endoplásmico las proteínas pasan mediante vesículas a la cara cis del aparato de Golgi de donde seguirán hacia su localización definitiva. Las proteínas residentes en el retículo endoplásmico son recuperadas del aparato de Golgi mediante vesículas que proceden de la cara cis del mismo y regresan al retículo. Debido a su implicación en la producción de proteínas que posteriormente serán secretadas el retículo endoplásmico rugoso es muy abundante en células secretoras, como las células principales del estómago o las células plasmáticas productoras de anticuerpos. El retículo endoplásmico liso no presenta ribosomas. Sus funciones principales son la síntesis de lípidos de membrana, el almacenamiento de calcio y la detoxificación de drogas. Debido a esta última función, el retículo endoplásmico liso es muy abundante en hepatocitos y aumenta con la ingesta de sustancias tóxicas como el alcohol. En células musculares lisas y estriadas encontramos una forma especializada de retículo endoplásmico liso conocida como retículo sarcoplásmico. El retículo sarcoplásmico es un importante almacén del calcio que se utiliza en el proceso de contracción muscular. (Ver página Web) Técnicas Sistema de dos híbridos Resumen La técnica denominada sistema de dos híbridos o sistema del doble híbrido o Y2H (Yeast two hybrid) se utiliza para detectar interacciones entre proteínas y ha sido especialmente útil para estudios a gran escala ya que permite analizar grandes conjuntos de proteínas en un único experimento global. Concepto Muchos factores de transcripción constan de 2 dominios, ambos imprescindibles para que se produzca la expresión del gen que regulan. La técnica Y2H se basa en esta característica de algunos factores de transcripción. Un conjunto de proteínas se fusiona a uno de los dominios (dominio A) del factor de transcripción y el otro conjunto al otro dominio (dominio B). Esto se consigue utilizando técnicas de ingeniería genética con las que se generan 2 genotecas, una con genes fusionados al dominio A (conjunto A) y la otra con genes fusionados al dominio B (conjunto B). Los plásmidos con los genes fusionados se integran en levaduras y sólo cuando interactúan proteínas de ambos conjuntos los dos dominios del factor de transcripción se unen y son capaces de inducir la expresión del gen regulado por ese factor de transcripción. Este Términos de Uso Boletín 6 3 de septiembre de 2008 18 gen es un gen llamado “reportero” que permite detectar su expresión porque suele ser el gen de una enzima cuya expresión produce la síntesis de un producto fácilmente detectable. Muchas veces se ha utilizado como gen reportero el gen lacZ que codifica la enzima beta-galactosidasa que metaboliza la galactosa y en el ensayo habitual produce un color azul en las colonias positivas en las que se ha producido una interacción entre una proteína del conjunto A y otra del conjunto B. Durante los últimos años este tipo de ensayo ha sido muy útil para detectar a gran escala interacciones entre proteínas. Así por ejemplo se han analizado proteomas completos detectando nuevas interacciones entre proteínas y colaborando de forma significativa a aumentar el conocimiento de las complejas redes de interacción entre proteínas de un organismo completo. La debilidad de esta técnica es que puede dar muchos falsos positivos sobre todo en los ensayos a gran escala ya que se expresan juntas y a la vez proteínas que en condiciones fiosiologicas no tienen por qué coincidir nunca en el espacio (pueden expresarse en compartimentos o tipos celulares distintos) ni en el tiempo (su regulación puede hacer que nunca se expresen a la vez). Las distintas modificaciones postraduccionales (fosforilación, glicosilación) son otra de las causas de algunos falsos positivos ya que este tipo de modificaciones puede impedir que ocurran en estado fisiológico interacciones detectadas por el sistema Y2H. Aún así es un filtro de selección realmente útil que ha permitido descubrir importantes interacciones que han podido ser confirmadas posteriormente por técnicas más específicas como la coinmunoprecipitación. (Ver página Web) Términos de Uso Boletín 6 3 de septiembre de 2008 19 Noticias Un anillo de cohesina une las cromátidas hermanas en la mitosis Fuente:The cohesin ring concatenates sister DNA molecules Durante la fase S del ciclo celular cada cromosoma se replica generando 2 copias idénticas que se denominan cromátidas hermanas ya que deben mantenerse juntas hasta que al final de la mitosis se separan para ir una a cada célula hija. La cohesión entre cromátidas es esencial en la mitosis y está mediada por un complejo proteico llamado cohesina. Este complejo está constituido por las subunidades Smc1, Smc3, Scc1 y Scc3 que forman una especie de anillo. Las proteínas Smc1 y Smc3 son proteínas con estructura de tipo coiled-coil con un dominio ATPasa en un extremo. Ambas forman un heterodímero en forma de V que se cierra mediante la Scc1 a la que se une la Scc3. Se había propuesto un modelo en el que la cohesina mantenía juntas a la cromátidas metiéndolas dentro de su anillo. En este trabajo se ha testado este modelo transformando en uniones covalentes las interacciones fundamentales que formarían el anillo de cohesina, creando anillos de cohesina químicamente estables. Trabajando con minicromosomas de levadura y con estos anillos de cohesina reforzados por uniones covalentes entre sus subunidades a través de puentes disulfuro de cisteínas ingenierizadas se ha podido comprobar el modelo propuesto ya que se han obtenido estructuras resistentes a la desnaturalización constituidas por 2 cromátidas hermanas unidas a cohesina. (Ver página Web) Construcción de tejidos en 3D Fuente:Directed assembly of cell-laden microgels for fabrication of 3D tissue constructs Este trabajo supone un gran avance en la ingeniería de tejidos. Los tejidos vivos están compuestos de bloques repetidos que se ensamblan en una microarquitectura tridimensional específica que en gran medida determina su función. Hasta ahora la mayoría de los tejidos artificiales se crean ensamblando células sobre un soporte biodegradable que determina la forma pero muchas veces no consigue simular la función. Uno de los mayores retos en este área es conseguir tejidos ingenierizados en los que las interacciones célula-célula, célula-matriz extracelular y célula factores solubles mimeticen realmente las interacciones de las células de los tejidos vivos y a un nivel superior también la arquitectura multicelular simule la de los tejidos vivos. Términos de Uso Boletín 6 3 de septiembre de 2008 20 Los microgeles son materiales muy atractivos para las aplicaciones de ingeniería de tejidos por sus propiedades físicas (capacidad para crear formas definidas, resistencia mecánica, biodegradabilidad) y biológicas (biocompatibilidad y parecido a la matriz extracelular, capacidad de atrapar células a una densidad similar a los tejidos vivos). Existen 2 aproximaciones diferentes en el uso de microgeles para construir tejidos: una con un enfoque descendente (top-down) que trata de controlar la forma y tamaño de porciones relativamente grandes de hidrogel y otra con un enfoque ascendente (botom-up) en la que se tratan de ensamblar unidades o bloques más pequeños tratando de imitar la estructura del tejido vivo organizado a base de la repetición de pequeñas unidades funcionales. En este trabajo los autores han conseguido construir tejidos sintéticos con una estructura tridimensional determinada a base de pequeñas unidades de microgel. Su sistema es muy escalable y se basa en la tendencia de los sistemas líquidos multifase de minimizar sus superficies de contacto. La fase hidrofóbica en presencia de agua sufre el efecto hidrofóbico en el que tiende a minimizar la superficie expuesta al agua. Los autores agitando microgeles hidofílicos en un medio hidrofóbico consiguen ensamblar de forma organizada las unidades de microgel debido a que las unidades de microgel tienden a minimizar la superficie expuesta al aceite. (Ver página Web) Eventos Del 29 de Septiembre al 4 de Octubre se celebra en Singapur el congreso sobre células madre, cáncer y envejecimiento “Stem cells, Cancer and Aging” (Más Información) Entre otros, en el congreso se tratarán temas como modelos del envejecimiento, rutas de señalización presentes en el cáncer y en el desarrollo y células madre cancerosas. (Ver página Web) Términos de Uso Boletín 6 3 de septiembre de 2008 21 La segunda conferencia anual sobre RNAi y terapia tendrá lugar el próximo 22 de Octubre en Boston (USA) (Más Información) Nuevas aproximaciones para optimizar la llegada del RNAi a su diana y el análisis de las distintas indicaciones terapéuticas son algunos de los temas que se tratarán durante la conferencia. (Ver página Web) . Durante el 2 y 3 de Octubre se celebra en Dublín el congreso “Biormarker Discovery Europe” (Más Información) Durante el evento se tratarán temas como la aplicación de las nuevas tecnologías al descubrimiento y detección de biomarcadores, la aplicación de los biomarcadores en el diseño de ensayos clínicos y su aplicación en la medicina personalizada. (Ver página Web) Términos de Uso Volver Volver Volver