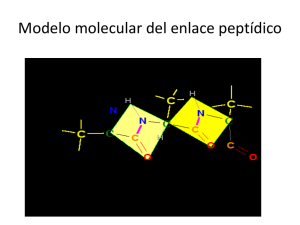
FUERZAS INTERMOLECULARES Archivo
Anuncio

06/05/2016 Fuerzas intermoleculares nucleares fuertes fuerzas naturales fundamentales nucleares débiles gravitacionales electromagnéticas 1 Fuerzas intermoleculares fuerzas electromagnéticas fuerzas entre átomos/moléculas determinan las propiedades de: sólidos líquidos gases partículas en solución partículas reaccionantes organización de estructuras biológicas 2 1 06/05/2016 Fuerzas intermoleculares fuerzas electromagnéticas fuerzas entre átomos/moléculas propiedades sólidos líquidos momentos dipolares eléctricos polarizabilidad reflejan el grado de control que los núcleos atómicos ejercen sobre los electrones en una molécula produciendo acumulación o permitiendo que los electrones respondan a campos externos 3 Fuerzas intermoleculares determinan las propiedades: punto de fusión punto de ebullición presión de vapor solubilidad densidad viscosidad 4 2 06/05/2016 Fuerzas intermoleculares factores moleculares: distribución de densidades electrónicas electronegatividad momento dipolar forma tamaño 5 Fuerzas intermoleculares fuerzas intermoleculares (atractivas) coulombicas o eléctricamente puras ión-ión Q2 = - z2 e Q1 = + z1 e r W* = − Q=+ze iónr dipolo permanente ,- ,. = /01* - 2- 2. 3. /01* W* ∝ 1 r +q θ W = − z e μ cosθ *5 ; 4πDr W*.5 ∝ -q dipolo permanentedipolo permanente W*5-5.∅ = − θ1 dipolo fijo -q µ1 μ? μ; (2cosθ? cosθ; − senθ? senθ; cos∅) 4 π D r> +q +q θ2 r -q ∅ µ2 1 r; W*5-5.∅ = − μ? μ; 4 π D r> W* ∝ 1 r> 6 3 06/05/2016 Fuerzas intermoleculares E E E E efecto de orientación efecto de distorsión 7 Fuerzas intermoleculares m =∝ E m =∝A ∝B E m: momento dipolar inducido E: campo eléctrico α: polarizabilidad (momento dipolar por unidad de campo) αo : polarizabilidad de distorsión αµ : polarizabilidad de orientación (polares) 8 4 06/05/2016 Fuerzas intermoleculares fuerzas intermoleculares (atractivas) van der Waals (polarización) efecto de orientación producido por acción mutua de los momentos dipolares de las moléculas efecto de distorsión producido por la interacción de un momento dipolar inducido de una molécula con el momento dipolar permanente de otra efecto de dispersión producido por la sincronización del movimiento electrónico en 2 moléculas que origina momentos dipolares momentáneos orientados que causan atracción entre ellas 9 Fuerzas intermoleculares fuerzas intermoleculares (atractivas) van der Waals (polarización) efecto de orientación dipolo permanente-dipolo permanente ( Keeson) W*5 = − 2 μ? ; μ; ; 3 (4πD); k T r L W*,5 ∝ 1 rL ión-dipolo inducido W*5 efecto de distorsión 2 Q; αA =− 2 (4πD); r / W*,5 ∝ 1 r/ dipolo permanente-dipolo inducido (Debye) W*5 = − 2 μ; α 2 (4πD); r L W*,5 ∝ 1 rL dipolo instantaneo-dipolo instantaneo (London) efecto de dispersión W* = − 3 h ν α? α; 4 (4πD); r L 23 ∝A ; h c W* = − 8 π; (4πD); r I W* ∝ 1 rL fuerzas retardadas W* ∝ 1 rI 10 5 06/05/2016 Fuerzas intermoleculares potencial de interacción total = potencial atractivo + potencial repulsivo W(*) = − A B + rL rR expresión empírica m, entero grande W (r ) + B rR repulsión r Si m = 12 A − L r atracción W(*) = − A B + ?; L r r potencial de Lennard- Jones 11 Fuerzas intermoleculares AU ⇌ AW ∆EWXY = EpW + EcW − EpU + EcU EcW ≅ EcU EpW ≅ 0 ∆EWXY ≅ −EpU ]^X_ − V ]U`a ) Q WXY = ∆HWXY = ∆EWXY + p(V ]^X_ = RT/p ≅V ] WXY = ∆E ]WXY + R T ∆H ]WXY = ∆H ] WXY − R T ∆E 12 6 06/05/2016 Fuerzas intermoleculares ]WXY = ∆H ] WXY − R TWXY ∆E ]WXY = TWXY ∆SeWXY − R TWXY ∆E ]WXY = TWXY (∆SeWXY − R ) ∆E ∆svap liq ≈ 90 J/K mol (Regla de Trouton) ]WXY ≅ TWXY cte ∆E TWXY ≅ ] ijk ∆h lm3 13 Fuerzas intermoleculares moléculas con µ =0 solo efecto de dispersión W* = − 3 h ν α? α; 4 (4πD); r L molécula He Ne Ar Kr Xe n° electrones 2 10 18 36 54 αο /(10-40 C m2/V) 0,226 0,436 1,81 2,74 4,46 Tb /K 4,216 27,3 87,3 119,9 165,1 14 7 06/05/2016 Fuerzas intermoleculares H2 N2 O2 n° electrones 2 14 16 10 18 26 αο /(10-40 C m2/V) 0,90 1,91 1,72 2,9 5,0 7,1 Tb /K 20,4 77,3 90,2 111,7 184,5 231 molécula CH4 C2H6 C3H8 crece el volumen, la polarizabilidad y la temperatura de ebullición 15 Fuerzas intermoleculares moléculas con µ ≠0 efecto de dispersión, distorsión y orientación molécula (CH3)3CH (CH3)2C=CH2 (CH3)3N isobutano isobutileno trimetilamina αο /(10-40 C m2/V) 9,30 9,30 8,99 µ /10-30 C m 0,440 1,63 2,23 Tb /K 263 267 278 molécula (CH3)2CH2 propano (CH3)2O C2H4O dimetil eter óxido de etileno αο /(10-40 C m2/V) 7,1 6,7 5,8 µ /10-30 C m 0,28 4,34 6,34 Tb /K 231 248 284 16 8 06/05/2016 Fuerzas intermoleculares molécula para diclorobenceno meta αο /(10-40 C m2/V) orto ≌ 17 µ /10-30 C m 0 5,74 8,34 Tb /K 446 445 453 molécula para dinitrobenceno meta αο /(10-40 C m2/V) orto ≌ 21 µ /10-30 C m 0 13 20 Tb /K 572 576 592 m. grandes, predomina int. dispersión, α cte., crece µ, teb. cte 17 Fuerzas intermoleculares moléculas que pueden formar puente hidrógeno fluoruro de hidrógeno, agua, alcoholes, aminas molécula (CH3)2O C2H5OH C2H4O dimetil eter alcohol etílico óxido de etileno αο /(10-40 C m2/V) 7,1 5.8 5,8 µ /10-30 C m 0,28 5.67 6,34 Tb /K 231 352 284 molécula NH3 H2O HF C2H4O óxido de etileno αο /(10-40 C m2/V) 2,60 1,77 0,89 5,8 µ /10-30 C m 4,87 6,17 6,37 6,34 Tb /K 240 373 293 284 18 9 06/05/2016 Fuerzas intermoleculares la energía de interacción adicional es de 20-40 kJ/mol X H 0,17 nm X F, O o N X 0,26 nm F F H cierta direccionalidad H H F cierto grado de estructuración tridimensional O H3C H O C C O H CH3 O compuesto H2O NH3 CH3OH CH3NH2 HF CH3COOH ∆Svap/(J/K mol) 109 97 105 97 26 62 19 Fuerzas intermoleculares H2O H H O PF, PE y ∆Hvap anormalmente elevados volumen molar del sólido > que volumen molar del líquido elevada tensión superficial elevada constante dieléctrica 20 10 06/05/2016 Fuerzas intermoleculares se rompen aniones H H O se rompen 21 Fuerzas intermoleculares cationes se rompe se rompe H H O 22 11 06/05/2016 Fuerzas intermoleculares I II III Capa I: interacción ión – dipolo, moléculas del agua fuertemente orientadas alrededor del ión (inmovilización de las moléculas de agua, depende de la densidad de carga del ión) Capa II: interacción puente hidrógeno, orientación parcial de los dipolos del agua, el ión destruye la estructura normal del agua Capa III: estructura normal del agua 23 Fuerzas intermoleculares evidencia, medidas de viscosidad η =1+A c+Bc η} η , viscosidad de la solución ηo , viscosidad del agua B, coeficiente de Jones-Dole si B > 0 ⇒ η > ηo ⇒ menor tendencia a fluir ⇒ capacidad estructuradora si B < 0 ⇒ η < ηo ⇒ mayor tendencia a fluir ⇒ capacidad desordenadora coeficiente B 0,4 Mg++ Ca++ citrato, sulfato, fosfato Ba++ 0,2 Li+ Na+ 0 Cl - F- K+ Rb+ 0.06 0.10 0.14 0.18 0.14 radio iónico (nm) I Br - Cs+ 0.18 0.22 - perclorato, tetrametil amonio 24 12 06/05/2016 Fuerzas intermoleculares solutos apolares hidrocarburo !" ⇌ hidrocarburo!" ΔG° y 0 ΔG° & ΔH° + T ΔS° 0 0 se forma una especie de jaula !clatrato, iceberg" alrededor de la superficie hidrofóbica ⇒ estructuración del agua ⇒ ∆S° 0 ⇒ formación puentes hidrógeno ⇒ ∆H° 0 efecto hidrofóbico 25 Fuerzas intermoleculares Hidrocarburo ∆G° ∆H° ∆S° ∆Cp !kcal/mol" !kcal/mol" !cal/K mol" !cal/grado mol" -3,2 -37 65 etano 6,3 6,1 -4,0 -33 propano 6,2 -5,1 -37 69 80 butano 6,3 -5,7 -40 69 benceno 3,4 -7,6 -36,6 84 naftaleno 1,8 -10,2 -40 82 fenantreno 0,4 -13,0 -42 263 pireno -0,8 -15,0 -50 130 metano 26 13 06/05/2016 Fuerzas intermoleculares solutos apolares + agente caotrópico hidrocarburo (Xa) ⇌ hidrocarburo(*3X I) ΔG° < 0 ∆G° (kcal/mol) ∆H° (kcal/mol) ∆S° (cal/K mol) metano 0,03 1,3 4,1 etano -0,05 1,9 propano -0,19 -0,26 1,7 1,9 6,5 6,3 7,2 Hidrocarburo butano forma complejos urea-agua estables, compite por el agua estructurada de alrededor del HC ruptura de desestructuración puentes H de la jaula proceso entrópicamente conducido 27 interacción hidrofóbica Fuerzas intermoleculares ΔG° < 0 interacciones de van der Waals ruptura de puentes H ΔH° > 0 desestructuración de la jaula ΔS° > 0 proceso entrópicamente conducido 28 14