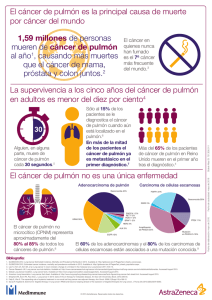
Cribado de cáncer de pulmón - Avalia-t
Anuncio

Cribado de cáncer de pulmón Lung cancer screening Informes de Evaluación de Tecnologías Sanitarias avalia-t Núm. 2007 / 06 INFORMES, ESTUDIOS E INVESTIGACIÓN MINISTERIO DE CIENCIA E INNOVACIÓN MINISTERIO DE SANIDAD Y POLÍTICA SOCIAL Cribado de cáncer de pulmón Lung cancer screening avalia-t Núm. 2007 / 06 MINISTERIO DE CIENCIA E INNOVACIÓN Cribado de cáncer de pulmón / Aida Fernández Rubio ; Alberto Ruano Raviña . – Madrid : Ministerio de Ciencia e Innovación ; 2009. 140 p. ; 24 cm + 1 CD-ROM. – (Informes, Estudios e Investigación ; avalia-t num. 2007/06) NIPO: 477-09-028-5 ISBN: 978-84-95463-64-7 Depósito Legal: C 2451-2009 1. Evaluación de Tecnología Biomédica – España 2. Estudios Observacionales 3. Toma de Decisiones 4. Estudios de Seguimiento I. España. Axencia de Avaliación de Tecnoloxías Sanitarias de Galicia (avalia-t) Este documento se ha realizado en el marco de colaboración previsto en el Plan de Calidad para el Sistema Nacional de Salud elaborado por el Ministerio de Sanidad y Política Social, al amparo del convenio de colaboración suscrito por el Instituto de Salud Carlos III, organismo autónomo del Ministerio de Ciencia e Innovación, y Fundación Escola Galega de Administración Sanitaria (FEGAS) Para citar este informe: Fernández Rubio A, Ruano Raviña A. Cribado de cáncer de pulmón. Plan de Calidad para el Sistema Nacional de Salud del Ministerio de Sanidad y Política Social. Axencia de Avaliación de Tecnoloxías Sanitarias de Galicia; 2007. Informes de Evaluación de Tecnologías Sanitarias: avalia-t Nº. 2007 / 06 Este informe ha sido sometido a un proceso de revisión externa. La Axencia de Avaliación de Tecnoloxías Sanitarias de Galicia agradece al Dr. Miguel Souto Bayarri, del Servicio de Radiología del Complejo Hospitalario Universitario de Santiago, al Dr. Alberto Fernández Villar, del Servicio de Neumología del Complejo Hospitalario Universitario de Vigo y al Dr. Esteve Fernández i Muñoz, del Servicio de Prevención y Control del Cáncer del Hospital Durán i Reynals (Instituto Catalá de Oncología) su colaboración desinteresada y los comentarios aportados. Los revisores externos del documento no suscriben necesariamente todas y cada una de las conclusiones y recomendaciones finales, que son responsabilidad exclusiva de los autores. Este documento puede ser reproducido parcial o totalmente para uso no comercial, siempre que se cite explícitamente su procedencia. Conflicto de intereses: Los autores declaran la ausencia de conflictos de interés en la elaboración del presente documento. Edita: Ministerio de Ciencia e Innovación NIPO: 477-09-028-5 ISBN: 978-84-95463-64-7 Depósito Legal: C 2451-2009 Impresión: Tórculo Artes Gráficas, S.A http://publicaciones.060.es Cribado de cáncer de pulmón Lung cancer screening MINISTERIO DE CIENCIA E INNOVACIÓN MINISTERIO DE SANIDAD Y POLÍTICA SOCIAL Índice Lista de abreviaturas. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 9 Lista de tablas. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 11 Lista de figuras . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 13 Resumen . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 15 Summary . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 19 1. Introducción. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 23 1.1. Epidemiología del cáncer de pulmón. . . . . . . . . . . . . . . . . . . . . . . . . 23 1.1.1. Epidemiología del cáncer de pulmón en España. . . . . . . . . . . .24 1.1.2. Supervivencia del cáncer de pulmón . . . . . . . . . . . . . . . . . . . . 24 1.2. Factores de riesgo del cáncer de pulmón. . . . . . . . . . . . . . . . . . . . . 25 1.2.1. El tabaco y el cáncer de pulmón . . . . . . . . . . . . . . . . . . . . . . . 25 1.2.2. Otros factores de riesgo del cáncer de pulmón . . . . . . . . . . . . 27 1.3. Historia natural, tipos histológicos y estadiaje del cáncer de pulmón. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 29 1.4. Diagnóstico del cáncer de pulmón. . . . . . . . . . . . . . . . . . . . . . . . . . .31 1.4.1. Pruebas clínicas de diagnóstico y confirmación diagnóstica. . . 32 1.5. Características de un programa de cribado. . . . . . . . . . . . . . . . . . . . 33 1.5.1. Cribado de cáncer de pulmón . . . . . . . . . . . . . . . . . . . . . . . . . 36 1.5.2. Pruebas de cribado para el cáncer de pulmón. . . . . . . . . . . . . 37 1.5.3. Otras pruebas potenciales para el cribado del cáncer de pulmón. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 39 2. Objetivos. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 41 2.1. Objetivos principales . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 41 2.2. Objetivos secundarios. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 41 3. Métodos. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 43 3.1. Búsqueda de literatura. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 43 3.2. Selección de los estudios . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 44 3.3. Contextualización. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 46 3.3.1. Fuentes de información . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 46 3.3.2. Cálculo del número de personas susceptibles de ser cribadas . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 46 4. Resultados. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 49 4.1. Resultados de la búsqueda. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 49 4.2. Evaluación de la calidad de los estudios. . . . . . . . . . . . . . . . . . . . . . 51 4.3. Resultados de revisiones sistemáticas . . . . . . . . . . . . . . . . . . . . . . . 51 4.4. Resultados de estudios individuales. . . . . . . . . . . . . . . . . . . . . . . . . 57 4.4.1. Resultados para pruebas de imagen combinadas o no con pruebas biológicas . . . . . . . . . . . . . . . . . . . . . . . . . . 57 4.4.2. Resultados para otras pruebas. . . . . . . . . . . . . . . . . . . . . . . . .60 4.5. Resultados de coste-efectividad. . . . . . . . . . . . . . . . . . . . . . . . . . . . 63 4.6. Estudios en marcha. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 67 4.7. Resultados de contextualización de la situación española. . . . . . . . 68 4.7.1. Tabaquismo en España . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 68 4.7.2. Modalidad de cribado . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 69 4.7.3. Población susceptible de ser cribada a nivel nacional y por Comunidades Autónomas. . . . . . . . . . . . . . . . . . . . . . . . 70 5. Discusión . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 79 5.1. Discusión del método. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 79 5.1.1. Discusión de la búsqueda . . . . . . . . . . . . . . . . . . . . . . . . . . . . 79 5.1.2. Discusión de los criterios de inclusión y exclusión . . . . . . . . . . 79 5.1.3. Discusión de la contextualización. . . . . . . . . . . . . . . . . . . . . . . 81 5.2. Discusión de los resultados de efectividad. . . . . . . . . . . . . . . . . . . . 83 5.2.1. Cribado universal frente a cribado selectivo. . . . . . . . . . . . . . . 83 5.2.2. Cribado con pruebas de imagen combinadas o no con pruebas biológicas . . . . . . . . . . . . . . . . . . . . . . . . . . 83 5.2.3. Cribado con otras pruebas. . . . . . . . . . . . . . . . . . . . . . . . . . . . 88 5.2.4. Limitaciones de los estudios existentes . . . . . . . . . . . . . . . . . . 89 5.3. Discusión de los resultados de seguridad. . . . . . . . . . . . . . . . . . . . . 92 5.4. Discusión de los costes. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 93 5.5. Discusión de los resultados de contextualización. . . . . . . . . . . . . . . 94 5.5.1. Aspectos organizativos . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 95 5.6. Discusión de la periodicidad del cribado. . . . . . . . . . . . . . . . . . . . . . 96 6. Conclusiones. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 97 7. Recomendaciones. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 99 Bibliografía. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 101 Anexos. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 113 ANEXO A. Estrategia de búsqueda. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 115 ANEXO B. Estudios incluidos. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 119 ANEXO C. Estudios excluidos. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 121 ANEXO D. Revisiones sistemáticas incluidas. . . . . . . . . . . . . . . . . . . . . . . 131 ANEXO E. Estudios primarios incluidos sobre cribado de cáncer de pulmón. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 137 ANEXO F. Niveles de evidencia (SIGN). . . . . . . . . . . . . . . . . . . . . . . . . . . . 140 Lista de abreviaturas ACCP: American College of Chest Physicians. ADN: ácido desoxirribonucléico. AHRQ: Agency for Health Research and Quality. AJCC: American Joint Committee on Cancer. ALCA: Anti-Lung Cancer Association. AVG: años de vida ganados. CPCP: cáncer de pulmón de célula pequeña. CPCNP: Cáncer de pulmón de célula no pequeña. DARE: Database of Abstracts of Reviews of Effectiveness. EBUS: ultrasonografía endobronquial. Gadolinio-DTPA: gadolinio ácido dietilenotriamina pentaacético. HRCT: high resolution computed tomography. HTA: health technology assessment. IARC: International Agency for Research on Cancer. I-ELCAP: International Early Lung Cancer Action Project. IME: Índice médico español. JHLP: Johns Hopkins Lung Project. LDCT: low dose computed tomography. MSKLP: Memorial-Sloan Kettering Lung Project. NCI: National Cancer Institute. NHS CRD: National Health Service Centre for Reviews and Dissemination. Cribado de cáncer de pulmón 9 NHSEED: National Health Service Economic Evaluation Database. NLST: National Lung Screening Trial. NY-ELCAP: New York Early Lung Cancer Action Project. OMS: Organización Mundial de la Salud. PAAF: punción aspirativa con aguja fina. PET: positron emission tomography. QALY: quality-adjusted life year. RMN: resonancia magnética nuclear. SEER: Surveillance, Epidemiology and End Results. SEPAR: Sociedad Española de Neumología y Cirugía Torácica. SIGN: Scottish Intercollegiate Guidelines Network TC: tomografía computarizada. TCEFS o SPECT: tomografía de emisión fotónica simple. TCMC: tomografía computarizada multicorte o multidetector. VOC: volatile organic compounds. 10 INFORMES, ESTUDIOS E INVESTIGACIÓN Lista de tablas Tabla 1. Criterios de una enfermedad para ser objeto de un programa de cribado.. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 34 Tabla 2. Criterios de la prueba y el programa de cribado.. . . . . . . . . . . . . . . . 34 Tabla 3. Diferencias entre las pruebas diagnósticas de un programa de cribado y las de la práctica asistencial.. . . . . . . . . . . . . . . . . . . . . . . 35 Tabla 4. Pruebas potenciales de cribado del cáncer de pulmón.. . . . . . . . . . 40 Tabla 5. Resumen de las revisiones sistemáticas y los ensayos clínicos incluidos. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 50 Tabla 6. Valoración de la calidad de los estudios incluidos.. . . . . . . . . . . . . . 51 Tabla 7. Resultados de estudios comparativos de las revisiones sistemáticas. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 56 Tabla 8. Resultados de los estudios primarios incluídos.. . . . . . . . . . . . . . . . 61 Tabla 9. Coste-efectividad por año de vida ganado en un programa de cribado de cáncer de pulmón.. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 64 Tabla 10. Costes totales del cribado. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 65 Tabla 11. Fumadores diarios por sexo y Comunidad Autónoma.. . . . . . . . . . . 71 Tabla 12. Fumadores diarios de ≥ 20 cigarrillos/día por sexo y Comunidad Autónoma. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 72 Tabla 13. Fumadores diarios por sexo y edad en España.. . . . . . . . . . . . . . . . 73 Tabla 14. Fumadores diarios de ≥ 20 cigarrillos/día por sexo y edad en España.. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 73 Tabla 15. Estimación de la población a cribar en mujeres.. . . . . . . . . . . . . . . . 75 Tabla 16. Estimación de la población a cribar en hombres. . . . . . . . . . . . . . . . 76 Tabla 17. Estimación de la población a cribar en ambos sexos.. . . . . . . . . . . . 77 Tabla 18. Resumen de recomendaciones de diferentes instituciones sobre el cribado de cáncer de pulmón con distintas pruebas.. . . . . 87 Cribado de cáncer de pulmón 11 Lista de figuras Fig. 1. Historia natural y niveles de prevención del cáncer. . . . . . . . . . . . . . 36 Fig. 2. Resultados de la búsqueda bibliográfica. . . . . . . . . . . . . . . . . . . . . . 50 Fig. 3. Esquema estudio NLST.. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 67 Fig. 4. Modelo de cáncer.. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 86 Fig. 5. Lead-time bias.. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 90 Fig. 6. Length bias.. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 90 Fig. 7. Sobrediagnóstico. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 91 Cribado de cáncer de pulmón 13 Resumen 1. Introducción: el cáncer de pulmón es una de las principales causas de muerte en los países industrializados, ocupando el segundo lugar solamente por detrás de las enfermedades cardiovasculares. A pesar de su alta incidencia y mortalidad, presenta una baja prevalencia debido a que la mayoría de los casos son detectados en estadíos tardíos, por lo que sería muy importante disponer de pruebas de cribado capaces de detectar la enfermedad lo antes posible. El tabaco es el principal factor de riesgo, siendo el causante del 85-90% de todos los casos. 2. Objetivos: el objetivo principal de este informe es analizar la efectividad de diferentes pruebas propuestas para el cribado del cáncer de pulmón: tomografía computarizada helicoidal de baja resolución, radiografía de tórax y citología de esputo en el diagnóstico precoz del cáncer de pulmón. Además, se pretende conocer el potencial de otras pruebas de cribado y estimar la población susceptible de ser cribada para el cáncer de pulmón en España y por comunidades autónomas. 3. Métodos: se ha realizado una revisión sistemática de la literatura científica hasta enero de 2009 en diferentes bases de datos: a) bases de datos especializadas en revisiones sistemáticas, b) bases de datos específicas para Guías de Practica Clínica, c) bases de datos generales como Medline (PubMed), EMBASE, ISI Web of Knowledge, Índice medico español, y d) páginas especializadas. Se elaboraron estrategias de búsqueda específicas para cada base de datos utilizando los correspondientes descriptores y diferentes palabras clave. Dos revisores independientes revisaron y seleccionaron los artículos obtenidos siguiendo unos criterios de selección previamente establecidos, entre los que se fijaron: idioma, diseño y tipo de publicación, tamaño muestral y objetivo del estudio entre otros. Para conocer el número de personas susceptibles de ser cribadas en España, desglosadas por sexo y por comunidades autónomas, se obtuvo información sobre la población entre 50 y 74 años, prevalencia de fumadores y prevalencia de fumadores de más de 20 cigarrillos/día. De este modo se calculó el número de fumadores que deberían ser cribados en un hipotético programa de cribado de cáncer de pulmón. 4. Resultados: la bibliografía acerca del cribado de cáncer de pulmón es muy abundante y de diversa procedencia. Se localizaron 1.939 artículos de los que finalmente se seleccionaron 11 que cumplían los criterios de selección previamente establecidos (6 revisiones sistemáticas y 5 Cribado de cáncer de pulmón 15 estudios individuales). La mayoría de los estudios tratan del cribado de cáncer de pulmón con pruebas de imagen, principalmente tomografía computarizada de baja dosis y todos incluyen población de riesgo. El resto de las pruebas (biológicas o moleculares) sirven para complementar a las de imagen ya que por sí solas no son capaces de detectar con precisión el cáncer de pulmón. Ninguno de los estudios refleja reducción de la mortalidad aunque en algunos se observa mejora de la supervivencia del grupo cribado frente al no cribado. Todos ellos concluyen que el cribado de cáncer de pulmón no reduce la mortalidad y que no es eficaz en el momento actual. En cuanto al número de personas que se deberían cribar en un hipotético programa de cribado de cáncer de pulmón en España serían un total de 1.298.469, 889.000 varones y unas 408.000 mujeres aproximadamente. Las diferencias son grandes en función de la población de cada comunidad autónoma. Estos datos dan idea de la dificultad organizativa y de los costes que entrañaría un programa de cribado de cáncer de pulmón en el caso de que se demostrase un beneficio para la población. 5. Discusión: los estudios incluidos presentan limitaciones metodológicas. Muchos de ellos no tienen un período de seguimiento adecuado que permita conocer la verdadera efectividad del cribado de cáncer de pulmón, también se utilizan criterios variables para seleccionar a la población de riesgo (rango de edad, hábito tabáquico, etc). Sin embargo, existe coincidencia en indicar que actualmente el cribado de cáncer de pulmón no es efectivo para esta enfermedad. Muchos estudios tampoco tienen protocolos establecidos acerca de cómo manejar los nódulos sospechosos y tampoco valoran las repercusiones sobre la seguridad de los pacientes de los sucesivos cribados con TAC helicoidal (sometiéndolos quizás a un exceso de radiación innecesaria). Por otra parte, en caso de realizar un cribado de cáncer de pulmón, existirían graves repercusiones organizativas y económicas dado el elevado número de personas susceptibles de ser cribadas en España. 6. Conclusiones: a) No existe una prueba de cribado de cáncer de pulmón que disminuya la mortalidad ni aumente la proporción de curaciones, por lo que no se recomienda, en la actualidad, realizar un programa de cribado para el cáncer de pulmón. b) La modalidad de cribado más adecuada para el cáncer de pulmón es el cribado selectivo en fumadores. c) De todas las pruebas disponibles, las de imagen son las más adecuadas en el momento actual para un hipotético cribado. La tomografía computarizada es la que ofrece mayor sensibilidad y especificidad. d) Las pruebas de imagen suponen la exposición a radiación. Se debe ser cuidadoso cuando se 16 INFORMES, ESTUDIOS E INVESTIGACIÓN realizan pruebas de imagen repetitivas y valorar adecuadamente si son realmente necesarias. e) Los estudios publicados sobre cribado de cáncer de pulmón presentan deficiencias metodológicas y no puede descartarse la presencia de sesgos que afecten a los resultados. 7. Recomendaciones: la mejor manera de evitar el cáncer de pulmón es no fumar. Es más útil invertir los recursos de un programa de cribado de cáncer de pulmón en programas de prevención y abandono del tabaquismo bien diseñados. Para conocer la verdadera eficacia de las pruebas disponibles para el cribado de cáncer de pulmón son necesarios ensayos aleatorizados, bien diseñados, con un seguimiento amplio y homogéneo y con puntos finales bien definidos. Los estudios NELSON y National Lung Screening Trial (NLST) ofrecerán una buena información para conocer la eficacia del cribado con tomografía computarizada de baja dosis (LDCT). Es necesario conocer con más detalle qué características de los fumadores serían las más adecuadas para incluirlos en un programa de cribado de cáncer de pulmón. Para conocer la efectividad de un hipotético programa de cribado en España es necesaria la existencia de buenos datos sobre el consumo de tabaco de la población a nivel nacional, desglosados por comunidades autónomas, por intensidad de hábito tabáquico, por sexo y edad. También sería muy útil disponer de información unificada de base poblacional sobre mortalidad e incidencia del cáncer de pulmón a nivel nacional y autonómico. Sería conveniente revisar este informe en 2011, cuando se disponga de nuevos datos sobre estudios publicados y también sobre la efectividad de las nuevas pruebas biológicas disponibles o de nuevas pruebas de imagen. Cribado de cáncer de pulmón 17 Summary 1. Introduction: Lung cancer is one of the leading causes of death in industrialised countries, ranking second only after cardiovascular diseases. Despite its high incidence and mortality, lung cancer has a low prevalence due to the fact that most cases are detected in the late stages, so that it would be of the utmost importance to have screening tests which were capable of detecting the disease as early as possible. Smoking is by far the principal risk factor, though only about 15% of heavy smokers get to develop lung cancer. 2. Objectives: The principal aim of this report was to analyse the effectiveness of the different lung-cancer screening tests proposed, i.e., low-resolution computerised helical tomography, chest radiography and sputum cytology, for early diagnosis of lung cancer. Furthermore, we sought to ascertain the potential of other screening tests and to estimate the population eligible for lung cancer screening in Spain, both as a whole and by autonomous region (comunidad autónoma). 3. Methods: We conducted a systematic review of the scientific literature published until January 2009, targeting different databases, namely: a) specialised systematic-review databases; b) specific databases for Clinical Practice Guidelines; c) general databases, such as Medline (PubMed), EMBASE, ISI Web of Knowledge and Spanish medical index; and d) specialised web pages. Specific search strategies were drawn up for each database using the relevant descriptors and different key words. Two independent reviewers examined and selected papers retrieved in accordance with pre-established selection criteria that specified language, design and type of publication, sample size and study objective, among other criteria. To ascertain the number of persons eligible for screening in Spain, broken down by sex and autonomous region, data were obtained on the population aged 50 to 74 years, prevalence of smokers, and prevalence of smokers of over 20 cigarettes/day. This information was then used to calculate the number of smokers who ought properly to be screened under a hypothetical lung cancer screening programme. 4. Results: The bibliography on lung cancer screening is very abundant and of diverse origin. Of the total of 1,939 papers located, 11 (6 systematic reviews and 5 individual studies) that met the pre-established selection criteria were selected. Most studies addressed lung cancer screening based on imaging tests (mainly low-resolution computerised helical Cribado de cáncer de pulmón 19 tomography), and all included the risk population. The remaining tests (whether biological or molecular) served to complement the imaging tests, since in themselves the former cannot accurately detect lung cancer. None of the studies reported a reduction in mortality, though in some an improvement in survival in the screened versus the unscreened group was observed. All concluded that lung cancer screening did not reduce mortality and was not as yet effective. With regard to the number of persons who should be screened under a hypothetical lung cancer screening programme in Spain, the target population would total 1,298,469, made up of approximately 889,000 men and 408,000 women. There were great differences in terms of the populations of the respective autonomous regions. These data give an idea of the organisational difficulty and costs which a lung cancer screening programme would entail, if it were shown to be of benefit to the population. 5. Discussion: The studies reviewed display methodological limitations. In addition to their failure to have an adequate follow-up period that would enable the true effectiveness of lung cancer screening to be known, many use variable criteria to select the risk population (age range, tobacco habit, etc.). Nevertheless, they all coincide in indicating that, at the present time, lung cancer screening is not effective for this disease. Moreover, many studies have neither established protocols governing how suspicious nodules are to be managed, nor assessed the repercussions on patient safety of successive screening with helical CT (thereby possibly subjecting such patients to unnecessary excess radiation). Furthermore, in the event that lung cancer screening were to be implemented, there would be severe organisational and economic repercussions in view of the high number of persons eligible for screening in Spain. 6. Conclusions: a) There is no lung cancer screening test that reduces mortality or increases the proportion of cures, so that currently the implementation of a lung cancer screening programme is not to be recommended. b) The most appropriate method of lung cancer screening is selective screening of smokers. c) Of all the tests available, imaging tests are currently the most appropriate for hypothetical screening. Computerised tomography is the test that affords greatest sensitivity and specificity. d) Imaging tests involve exposure to radiation. Care is called for when conducting repeated imaging tests and proper assessment should be made as to whether these are really necessary. e) Studies published on lung cancer screening display methodological deficiencies, and the presence of biases that may affect the results cannot be ruled out. 20 INFORMES, ESTUDIOS E INVESTIGACIÓN 7. Recommendations: The best way of preventing lung cancer is to refrain from smoking. It is more useful to invest the hypothetical lung cancer screening programme resources in well-designed smoking-prevention and cessation programmes. To ascertain the true efficacy of available lung cancer screening tests, well-designed randomised trials are needed, with uniform, sufficiently long follow-up periods and well-defined final points. The NELSON study and National Lung Screening Trial (NLST) will furnish sound data for measuring the efficacy of screening with low-dose computerised tomography. More detailed information is required on the characteristics of those smokers who would be best suited for inclusion in a lung cancer screening programme. To ascertain the effectiveness of a hypothetical screening programme in Spain, good data are required on population tobacco use at a national level, broken down by autonomous region, intensity of tobacco habit, sex and age. It would likewise be very useful to have unified, population-based data on national and regional lung cancer mortality and incidence. This report should be reviewed and revised in 2011, when there are new data on published studies and the effectiveness of any new biological or imaging tests available. Cribado de cáncer de pulmón 21 1. INTRODUCCIÓN El cáncer representa la segunda causa de muerte en los países industrializados, solo por detrás de las enfermedades cardiovasculares. En estos países el cáncer de pulmón es la primera causa de muerte de origen tumoral entre los hombres y la tercera, después del cáncer de mama y colon, entre las mujeres. El principal factor de riesgo del cáncer de pulmón es el tabaco. La incidencia en Europa es elevada, sobre todo en Europa Central y del Este, y no solo en hombres, ya que el número de nuevos casos es cada vez mayor entre las mujeres debido al aumento del tabaquismo entre ellas, especialmente en el Norte de Europa. En el año 2006 se diagnosticaron 386.300 casos de cáncer de pulmón en Europa, significando un 12,1 % de todos los tipos de cáncer (1). En EUA, según el registro SEER (Surveillance, Epidemiology and End Results), que agrupa datos epidemiológicos de 17 estados norteamericanos, para el año 2008 se habían diagnosticado en torno a 215.020 nuevos casos de cáncer de pulmón (114.690 hombres y 100.330 mujeres) y se producirían un total de 161.840 muertes (2). Considerando cada sexo se puede observar que el cáncer de pulmón es el segundo más frecuente tanto en hombres como en mujeres. Respecto a la mortalidad es el tipo de cáncer que ocasiona más muertes (3). 1.1. Epidemiología del cáncer de pulmón La incidencia anual del cáncer de pulmón a nivel mundial es de 1,4 millones de casos (3), y casi la mitad de estos tumores (49,9 %) se localizan en los países industrializados (4). En determinados países, como EUA, Canadá, Dinamarca, Reino Unido o Australia, se ha llegado a una fase meseta y su incidencia ha disminuido entre los hombres, mientras que en otros como España, China o Japón, estas cifras están aumentando (4). En 2006 se estimaron para Europa unas 335.000 muertes (19,7 % del total de muertes) relacionadas con el cáncer de pulmón. El cáncer de pulmón resulta ser, por tanto, la primera causa de muerte por cáncer, seguida del cáncer colorrectal, del de mama (en mujeres) y del de estómago. En la Unión Europea, en ese mismo año, se produjeron 236.000 muertes por cáncer de pulmón (172.000 muertes por esta patología entre los hombres, representando el 26,3 % del total de muertes por cáncer y 64.000 muertes entre las mujeres que se corresponde con el 12,5 % del total de muertes por cáncer) (1). Cribado de cáncer de pulmón 23 1.1.1. Epidemiología del cáncer de pulmón en España La situación en España es similar a la del resto de los países industrializados. El cáncer de pulmón es el tipo de cáncer más frecuente en hombres (sin contar el cáncer de piel no-melanoma) y el que tiene mayor tasa de mortalidad, con una frecuencia siempre mayor en hombres que en mujeres (5). Respecto a la incidencia, hubo 18.820 nuevos casos (16.690 en hombres y 2.130 en mujeres) en el año 2006. Se observa que hay una gran heterogeneidad en la incidencia dependiendo de la Comunidad Autónoma. Así, se observa que entre 1983-86 y 1993-97 las tasas de cáncer de pulmón aumentan entre los hombres en ambos períodos en torno a un 18 %, mientras que entre las mujeres estas tasas aumentan más debido a los diferentes patrones del consumo de tabaco entre ellas (5). La incidencia del cáncer de pulmón entre las mujeres españolas es menor que en otros países. La razón hombre/ mujer, en España, es de 8,5 hombres frente a 1 mujer. La mayor incidencia del cáncer de pulmón (> 50 %) se encuentra en mayores de 70 años (6). En términos de mortalidad general, el cáncer de pulmón representa aproximadamente un 26 % del total las defunciones (por cualquier causa) y es, como para el resto de los países, la primera causa de muerte (de origen tumoral) en hombres y la tercera en las mujeres (1, 7). Con las tasas de mortalidad ajustadas para cada provincia se puede tener información de dónde hay realmente más incidencia de cáncer de pulmón. Según esta información, la tasa de mortalidad en España, en 2006, es muy heterogénea y presenta grandes diferencias entre el valor máximo y mínimo tanto para hombres como para mujeres. Para los hombres, la tasa media es de 65,3 muertes por 100.000 habitantes. En el caso de las mujeres, la tasa es mucho menor (8). 1.1.2. Supervivencia del cáncer de pulmón La supervivencia del cáncer de pulmón es muy baja: está en torno al 10-15 % a los 5 años y no ha cambiado en las últimas décadas a pesar de los grandes esfuerzos realizados durante los últimos años en el diagnóstico precoz y en su tratamiento. Esto se debe a que la mayoría de los tumores se detectan en estadíos avanzados (9) los cuales presentan una supervivencia a los 5 años menor del 5 %, mientras que, si son diagnosticados en estadíos tempranos y tratados a tiempo, la supervivencia puede llegar al 50 % (3). La detección temprana de la enfermedad es el factor que más incide en el aumento de la supervivencia. Según datos del registro SEER, la supervivencia a los 5 años es del 49,5 % para tumores en estadíos tempranos, del 20,6 % para tumores localizados, del 2,8 % para tumores distales y del 8,3 % para tumores en estadíos no identificados (2). Según datos de un estudio realizado en 2009 en 24 INFORMES, ESTUDIOS E INVESTIGACIÓN Europa, la supervivencia a los 5 años (en menores de 60 años) presenta un rango del 11-20,5 % (10). En España se ha estimado, para el período 2000-2002, una supervivencia total a los 5 años del 12,2 %. Este valor es ligeramente mayor en hombres (12,5 %). Considerando la edad se observó que esta supervivencia es menor en edades más avanzadas (del 15,4 % en personas de 15-59 años, del 12,4 % entre 60 y 74 años y del 8,4 % entre 75-99 años) (10). 1.2. Factores de riesgo del cáncer de pulmón El cáncer de pulmón es una enfermedad multifactorial. Sus factores de riesgo se pueden agrupar en dos grandes grupos: intrínsecos y extrínsecos. A diferencia de otros tipos de cáncer, donde los factores genéticos son los principales factores de riesgo de la enfermedad, en el cáncer de pulmón tienen mucha más influencia los factores extrínsecos. De entre todos los factores extrínsecos el tabaco es el principal factor de riesgo (11) por lo que una de las soluciones para poder evitar la mayoría de los casos de cáncer de pulmón es con buenos programas de prevención primaria para eliminar o reducir el tabaquismo. 1.2.1. El tabaco y el cáncer de pulmón Numerosos estudios han confirmado que el tabaco es el principal factor de riesgo del cáncer de pulmón. El tabaco es el responsable del 80-90 % de los casos de cáncer de pulmón en hombres y del 55-80 % en mujeres, respectivamente (7). Sin embargo, solamente un 10‑15 % de los grandes fumadores llegan a desarrollar cáncer de pulmón a lo largo de su vida (12), lo que sugiere que además del tabaco existen otros factores que hacen variar el riesgo de desarrollar la enfermedad. El tabaco contiene aproximadamente cuatro mil compuestos químicos, de los cuales unos cincuenta son carcinogénicos, algunos muy potentes. El riesgo de cáncer de pulmón es unas 15 veces mayor en fumadores que en no fumadores; se puede observar además que en este riesgo influyen varios aspectos relacionados con el hábito tabáquico (13). Un factor muy importante, incluso más que el número de cigarrillos fumados, es la duración del hábito, lo que nos da idea de la clara relación dosis-respuesta entre el tabaco y el desarrollo de cáncer de pulmón (14). Numerosos estudios han confirmado que el riesgo de cáncer de pulmón es notablemente mayor al aumentar el número de cigarrillos fumados por día o el número de paquetes fumados al año. También parecen tener influencia la intensidad de la inhalación, el uso o no de filtro o el tipo de tabaco (14, 15). El uso de filtros permite reducir la cantidad de alquitrán inhalada. Además, Cribado de cáncer de pulmón 25 la incorporación de poros de ventilación alrededor del filtro permite diluir el humo y con ello el contenido de alquitrán y nicotina (16). Se ha observado que tanto el tabaco fumado como cigarrillos o como pipas está altamente relacionados con el cáncer de pulmón (13). Además, el humo del tabaco contiene alquitrán, en el que se encuentran muchos compuestos químicos carcinogénicos (17) como hidrocarburos aromáticos policíclicos y nitrosaminas. Por último, aunque no hay muchos estudios que lo evalúen, se ha observado que el tipo de tabaco (rubio o negro) también influye en el desarrollo de cáncer de pulmón, habiéndose observado que las personas que fuman únicamente tabaco negro tienen mayor riesgo de desarrollar la enfermedad. Otro dato importante referente al tabaquismo es que los exfumadores, en función del número de años transcurridos desde que han dejado de fumar, parecen tener menor riesgo de desarrollar la enfermedad que los fumadores; sin embargo, este riesgo sigue siendo mayor que en personas que no han fumado nunca (18). Se ha podido comprobar que el tabaco aumenta el riesgo de todos los tipos histológicos de cáncer de pulmón (13). También es muy importante la exposición al humo del tabaco en los llamados “fumadores pasivos”. Esto se debe a que el humo presente en el ambiente tiene los mismos componentes que el que se inhala al fumar, aunque en menores proporciones (1-10 %). Se han encontrado gran cantidad de biomarcadores relacionados con el humo del tabaco en estas personas (19-22), por lo que el humo ambiental del tabaco también ha sido declarado como un carcinógeno humano (13). A pesar de la gran cantidad de estudios realizados, no hay datos que confirmen que el riesgo de desarrollar cáncer de pulmón entre las mujeres sea superior al de los hombres si ambos están expuestos a una misma cantidad de tabaco (23). Mientras que la prevalencia de fumadores en España parece que ha llegado a un valor máximo en los hombres, en las mujeres sigue aumentando cada vez más. En los últimos años la prevalencia ha pasado de un 6,1 % a un 44 % en determinadas regiones de España (9). Según datos la Encuesta Nacional de Salud, en 2006 en torno al 26,4 % de la población mayor de 16 años es fumadora habitual; el 3,1 % es fumadora ocasional; el 20,5 % se considera ex fumadora y, finalmente, el 50,0 % nunca ha fumado (24). La distribución del tabaquismo en 2006 (entre fumadores diarios y mayores de 16 años) en España es bastante heterogénea, tanto si se considera en relación al sexo como a las diferentes Comunidades Autónomas. Respecto al sexo, el porcen- 26 INFORMES, ESTUDIOS E INVESTIGACIÓN taje de fumadores diarios es mayor entre los hombres que entre las mujeres (31,6 % frente a 21,5 %, respectivamente). Teniendo en cuenta la edad se observa que la mayor proporción (34,7 %) de fumadores tiene entre 25 y 44 años. Esta proporción también es elevada (26,9 %) entre los 16 y 24 años, mientras que en mayores de 45 años apenas supera el 20 %. Finalmente, considerando las diferencias geográficas, se puede observar que Cantabria es la región con mayor porcentaje de fumadores diarios (31,3 %) mientras que el País Vasco es la región con menor porcentaje (21,5 %). La prevalencia de fumadores ocasionales oscila entre el 2-4 % en todas las Comunidades Autónomas (24). Globalmente, el 42,3 % de los fumadores fuma más de 20 cigarrillos/ día y aunque el 44,4 % de la población continua fumando con la misma intensidad, se observa que el 32,9 % han reducido el consumo de cigarrillos mientras que en torno al 26,7 % han dejado de fumar en los últimos cuatro años (24). 1.2.2. Otros factores de riesgo del cáncer de pulmón A pesar de que el tabaco es el principal factor de riesgo del cáncer de pulmón, hay otros factores que influyen en el riesgo de desarrollar esta enfermedad, como los genéticos o las radiaciones ionizantes, y en concreto la presencia de radón, que es considerado como el segundo factor de riesgo más importante tras el tabaco (25). En el cáncer de pulmón, los factores genéticos no tienen tanta importancia en su desarrollo como en otros tipos de cáncer. Además, determinadas enfermedades pulmonares previas, como la tuberculosis o el asma pueden también incrementar el riesgo de padecer la enfermedad (11). Las exposiciones ocupacionales y determinadas enfermedades ocasionadas por éstas como berilosis o silicosis también están relacionadas con el riesgo de cáncer de pulmón. En este caso, los compuestos más importantes son el asbesto, la sílice cristalina, el arsénico y sus derivados, el níquel o el cromo. Se calcula que, aproximadamente, un 13-18 % de los casos de cáncer de pulmón se deben a exposiciones ocupacionales (26). Otro factor que influye es la contaminación atmosférica, por lo que los casos de cáncer de pulmón son ligeramente más frecuentes en las zonas urbanas que en las rurales (27). Sin embargo, es muy difícil determinar esta Cribado de cáncer de pulmón 27 influencia, debido a la complejidad y posibles factores de confusión a la hora de evaluar la exposición a estos factores. Diversos estudios epidemiológicos han comprobado que una dieta pobre en verduras podría aumentar el riesgo de cáncer de pulmón (28) mientras que otros afirman que el vino tinto podría proteger frente a la aparición de la enfermedad (29). Otros aspectos que también influyen en la aparición del cáncer de pulmón son: • Raza: se ha observado que tanto la incidencia como la mortalidad es mayor en afroamericanos que en caucásicos, americanos blancos o asiáticos. La supervivencia a los 5 años en afroamericanos está en torno al 14 % (3). Esto también está relacionado con el nivel socioeconómico debido al menor acceso a los recursos sanitarios y a la mayor exposición a factores de riesgo. • Nivel socioeconómico: se ha visto que a nivel mundial el cáncer de pulmón es más frecuente en grupos de bajo nivel socioeconómico. Una posible explicación sería que un nivel socioeconómico bajo está asociado con una mayor exposición a factores de riesgo (mayor tabaquismo, mala dieta…) (15, 30-32). • Edad: tanto la incidencia como la mortalidad van aumentando con la edad, siendo muy raros los casos en edades tempranas. La mayor incidencia se encuentra en torno a los 65-70 años, y la edad de diagnóstico es siempre mayor en hombres que en mujeres. Esto se debe a que en los hombres la enfermedad también se desarrolla en edades más tardías. Además, cuantos más años se haya fumado mayor será el riesgo ya que la cantidad de alteraciones generadas por los carcinógenos será mayor. No obstante, ninguno de los factores citados influye tanto en el desarrollo de cáncer de pulmón como el tabaco, teniendo algunos de ellos un fuerte efecto sinérgico (33). 1.3.Historia natural, tipos histológicos y estadificación del cáncer de pulmón Se define como historia natural de las neoplasias a la evolución previsible de un tumor desde su origen hasta que, una vez que éste se hace detectable, 28 INFORMES, ESTUDIOS E INVESTIGACIÓN se manifiesta clínicamente y se puede extender a los ganglios y a otros órganos. En el cáncer de pulmón se cumple el mismo esquema que para el resto de los cánceres. En él, la fase de exposición puede ser más o menos larga dependiendo de la duración e intensidad del consumo de tabaco así como del tipo histológico y la etapa en la que se detecte el cáncer. Esta fase puede incluso llegar a ser de hasta 20 años. Sin embargo, las fases posteriores (lesiones presintomáticas y enfermedad) son muy cortas por lo que es muy difícil tratar la enfermedad a tiempo. Así, la enfermedad evoluciona muy rápidamente por lo que la supervivencia del cáncer de pulmón es muy baja. Teniendo en cuenta el tipo celular que genera el tumor, el cáncer de pulmón se clasifica en distintos tipos histológicos. Desde el punto de vista clínico se diferencian dos tipos principales: • Cáncer de pulmón de célula no pequeña (CPCNP): representa entre el 80-85 % de los casos de cáncer de pulmón. Dentro de este tipo se diferencian tres subtipos: carcinoma de células escamosas o epidermoide (directamente relacionado con el tabaco), el adenocarcinoma, que es más habitual en mujeres y carcinoma indiferenciado de células grandes. La mayoría de los pacientes (80%) presentan enfermedad metastásica siendo muy escasos los pacientes que presentan el tumor en estadíos localizados (34). • Cáncer de pulmón de células pequeñas (CPCP) o microcítico: representa el 15-20 % de los cánceres de pulmón. Sin embargo, a pesar de representar un porcentaje muy bajo es el de peor pronóstico debido a que suele estar diseminado en el momento del diagnóstico. Para la estadificación del cáncer se emplea el sistema TNM que aporta información detallada del tamaño del tumor (T), estado de los ganglios linfáticos (N) y metástasis (M). Según esta clasificación, el tamaño del tumor tiene un pronóstico bueno y se recomienda hacer una subclasificación en varios grupos dependiendo del tamaño (T1 a su vez dividido en T1a (≤ 2 mm) y T1b (> 2 mm - ≤ 3 mm), T2 también con T2a (> 3 mm - ≤ 5 mm) y T2b (> 5 mm - ≤ 7 mm) y T3 (> 7 mm) (35). Para la componente N (estado de los ganglios linfáticos) se diferencian 5 subgrupos (N0, Nx, N1, N2 y N3) dependiendo de que haya o no metábasis en los ganglios o no. Finalmente, para la componente M (metástasis) se diferencian 3 subgrupos (M0, Mx y M1) según haya o no metástasis a distancia (36). Cribado de cáncer de pulmón 29 Respecto a la agrupación por estadíos se distinguen 8 tipos diferentes dependiendo de las posibles combinaciones de los tres componentes anteriormente descritos. Estos estadíos son: • • • • • • • 0: carcinoma in situ. IA: T1 N0 M0 IB: T2 N0 M0 IIA: T1 N1 M0 IIB: T2 N1 M0 ó T3 N0 M0 IIIA: T3 N1 M0, T1 N2 M0, T2 N2 M0 ó T3 N2 M0. IIIB: T4 N0 M0, T4 N01M0, T4 N2 M0, T1 N3 M0, T2 N3 M0, T3 N3 M0 ó T4 N3 M0. • IV: cualquier T, cualquier N M1. Esta clasificación comenzará a utilizarse en febrero de 2010. En el caso del CPCP se suele emplear, de forma práctica y con finalidad terapeútica, los términos de enfermedad limitada y extendida. Entendiendo que la enfermedad está limitada si todo el tumor conocido está localizado en el tórax y es susceptible de ser irradiado con intención radical mientras que la enfermedad extendida se considera cuando están afectados los ganglios linfáticos mediastínicos de ambos lados, los supraclaviculares ipsilaterales y hay obstrucción de la vena cava superior (36). 1.4. Diagnóstico del cáncer de pulmón El gran problema en el diagnóstico del cáncer de pulmón es que los síntomas no suelen aparecer hasta que hay metástasis en tejidos cercanos después de la primera transformación de células malignas, de aquí que sea una enfermedad asociada a una supervivencia tan baja. Los síntomas iniciales de la enfermedad tienen un cuadro muy inespecífico y compartido con otras enfermedades respiratorias. Algunos de estos síntomas están relacionados con la metástasis (37). Para un buen diagnóstico es necesario maximizar la rentabilidad de la prueba seleccionada, tanto para el diagnóstico como para la estadificación, y, por otra parte, hay que evitar la realización de pruebas invasivas innecesarias para el paciente (38). Ante la sospecha clínica de un cáncer de pulmón se deriva el paciente a neumología donde se le realizarán una serie de pruebas (39). Inicialmente se recomienda realizar a todos los pacientes una anamnesis y exploración física, radiografía de tórax, hemograma, bioquímica y pruebas de coagulación, electrocardiograma y tomografía de tórax y abdominal superior. A conti- 30 INFORMES, ESTUDIOS E INVESTIGACIÓN nuación para confirmar el diagnóstico se realizan diferentes pruebas como broncoscopia, PAAF guiada con radiografía o tomografía computarizada, citología de esputo, PAAF o biopsia, toracocentesis combinada o no con biopsia pleural y biopsia quirúrgica empleando diferentes pruebas (mediastinoscopia, mediastinotomía, toracoscopia o toracotomía) (34). Hay que tener en cuenta que el diagnóstico del cáncer de pulmón depende del tamaño y localización del tumor primitivo, de la existencia o no de metástasis y de las posibilidades de tratamiento. De este modo, a aquellos pacientes con sospecha de carcinoma de células no pequeñas, en estadío aparentemente inicial y sin contraindicación quirúrgica, se les realiza toracotomía diagnóstica y terapéutica; mientras que a los pacientes con posibles carcinomas, tanto de células pequeñas (microcíticos) como no microcíticos con posible metástasis, se les realizan pruebas lo menos invasivas posible, como son la toracocentesis en un derrame pleural, biopsia excisional de un ganglio periférico, broncoscopia o punción transtorácica con aguja (40). Debe existir un buen protocolo de seguimiento para poder determinar cómo tratar los nódulos no calcificados (NCN) detectados con tomografía computarizada de baja dosis (LDCT) (41). Este protocolo puede variar en función de que se trate de un protocolo ante la detección de nódulos después de que el presente debute con sintomatología, detección incidental de nódulos (42) o de que sea un protocolo específicamente desarrollado para un programa de cribado. Para programas de cribado se han propuesto algunos, uno de ellos es el siguiente: • Nódulos ≤ 5 mm deben ser examinados con LDCT un año después de ser diagnosticados. • Nódulos de 5-10 mm deben ser examinados con LDCT 3 meses después. Si no se observan cambios se vuelven a examinar con LDCT a los 6, 12 y 24 meses del test basal. En caso de observar aumento de tamaño se recomienda un diagnóstico histológico. • Nódulos > 10 mm deben ser sometidos a tomografía computarizada con contraste, PET combinado o no con diagnóstico histológico (depende del oncólogo, del radiólogo y del personal de cirugía torácica del centro hospitalario) Se recomienda realizar LDCT con el fin de confirmar aquellos nódulos no calcificados que han resultado sospechosos en la radiografía de tórax (43). Cribado de cáncer de pulmón 31 Según datos del registro SEER (Estados Unidos), para la raza blanca, en el momento del diagnóstico un 52% de todos los casos presentan metástasis a distancia y otro 22% enfermedad regional, lo que da una idea del alcance de la enfermedad en el momento del diagnóstico para la mayoría de los casos. 1.4.1. Pruebas clínicas de diagnóstico y confirmación diagnóstica Tras la exploración física lo primero que se hace es una radiografía de tórax a aquellos pacientes con sospecha de cáncer de pulmón. En ella, se puede observar el tamaño, extensión y localización de las lesiones, aspecto, bordes, presencia de lesiones en la pared torácica y evaluar la densidad de la radiografía para estimar si hay o no calcificación. Puede incluso dar una aproximación del estadificación del tumor. Además, se recomienda realizar radiografías para determinar lesiones que pueda haber en el pulmón como alteraciones en el mediastino, líquido en la pleura o lesiones de la pared torácica (44). A partir de los resultados de la radiografía se realiza un tomograma, para ver el rango de amplitud corporal que debe cubrir la posterior tomografía computarizada. Existen otras pruebas de imagen que confirman los resultados de la radiografía como por ejemplo el escáner o tomografía computarizada (TC), la tomografía de emisión de positrones (PET) o la resonancia magnética nuclear (RMN) con o sin contraste. Esta última tiene baja sensibilidad y especificidad para la estadificación ganglionar por lo que se debe hacer con contraste. Es muy útil para detectar metástasis en el cerebro o en la médula espinal. Recientemente, se ha desarrollado una prueba, denominada ultrasonografía endobronquial (EBUS), que permite la estadificación de ganglios linfáticos mediastínicos en pacientes con sospecha o diagnosticados de cáncer primario o metastático (45). Una vez obtenidos los resultados de las pruebas de imagen, se debe verificar la presencia de células tumorales tomando muestras biológicas. Las muestras histológicas o citológicas pueden obtenerse mediante broncoscopias, citología de esputo, mediastinoscopia, toracocentesis o toracoscopia. Para el cáncer de pulmón en particular se usa la biopsia quirúrgica o la punción aspirativa con aguja fina (PAAF) guiada por tomografía computarizada o fluorescencia. El diagnóstico definitivo lo dará la presencia de células neoplásicas en la muestra obtenida. 32 INFORMES, ESTUDIOS E INVESTIGACIÓN Además, se realizarán estudios de extensión tumoral para investigar si hay o no metástasis. Un punto importante a tener en cuenta es que cada paciente debe recibir un tratamiento personalizado determinado por un grupo multidisciplinar de especialistas (neumólogos, oncólogos y cirujanos torácicos). 1.5. Características de un programa de cribado Se define cribado a la aplicación de procedimientos de selección (cuestionario, examen físico, test) a poblaciones de individuos aparentemente «sanos» con objeto de identificar, en la fase de latencia, a aquellos que pueden estar enfermos o que presentan un riesgo incrementado de padecer una determinada enfermedad porque presentan un determinado factor de riesgo. Es decir, se trata de diferenciar a las personas aparentemente sanas que probablemente padecen una enfermedad o presentan un factor de riesgo de las aparentemente sanas que probablemente no padecen la enfermedad o no presentan el factor de riesgo (46). Es muy importante destacar que el cribado no es una prueba diagnostica definitiva (47). La finalidad del cribado es disminuir tanto la morbilidad como la mortalidad mediante una detección y tratamiento precoz y adecuado en la etapa presintomática, aumentar la supervivencia y mejorar la calidad de vida de las personas que padecen la enfermedad frente a los resultados de un diagnóstico clínico habitual. Hay diferentes tipos de cribado pero los dos tipos principales son el cribado universal y el cribado selectivo. Antes de poner en marcha un programa de cribado, se deben tener en cuenta una serie de principios o criterios establecidos ya en 1968 por Wilson y Jungner y que siguen vigentes en la actualidad (48). La enfermedad a tratar debe ser un importante problema de salud, aunque esto no signifique que deba tener una alta prevalencia. Además, también serían de interés para realizar un cribado aquellas enfermedades que, si no se descubren o tratan a tiempo, tienen graves consecuencias para el individuo y sus familiares, así como las que sean moderadas para un individuo, pero que repercutan gravemente en la colectividad. A todo esto debemos añadir una serie de criterios que deben cumplir tanto las enfermedades como los programas de cribado (tablas 1 y 2): Cribado de cáncer de pulmón 33 Tabla 1. Criterios de una enfermedad para ser objeto de un programa de cribado. La enfermedad debe ser un problema de salud importante. Se debe conocer correctamente la historia natural de la enfermedad. La enfermedad debe tener una fase de latencia identificable o de síntomas incipientes, ya que para localizar y tratar eficazmente las enfermedades en una fase temprana debe existir, evidentemente, un período razonable en la evolución natural de la enfermedad durante el cual no estén presentes los síntomas. Deben existir unos criterios de diagnóstico bien establecidos con una norma sobre qué personas deben tratarse como enfermos y debe seguirse una política claramente definida respecto a los sujetos “dudosos”. El tratamiento efectuado en la fase de subclínica debe ser más efectivo que el efectuado después del diagnóstico clínico habitual. Fuente: Cerdá Mota, 2006 (49). Tabla 2. Criterios de la prueba y el programa de cribado. La prueba debe ser aceptada por los usuarios, es decir, debe ser segura, rápida, sencilla, fácil de aplicar, poco molesta y eficaz. Los resultados de las pruebas de cribado deben ser válidos y fiables. El programa de cribado debe ser eficaz (considerando los sesgos propios del programa de cribado: lead time bias, length bias, sobrediagnóstico), efectivo y factible considerando la aceptabilidad, los costes, la capacidad y el rendimiento del programa. Evaluar la relación entre el beneficio y el daño. Fuente: Cerdá Mota, 2006 (49). De los criterios anteriores es importante resaltar la relevancia de la validez y la fiabilidad de las pruebas de cribado (46, 47): • Validez: es el grado con que los resultados de la prueba son confirmados por exámenes diagnósticos posteriores, es decir, el grado de concordancia entre los resultados del examen de cribado y los de la prueba de referencia que da el resultado definitivo. Mide la sensibilidad y especificad de la prueba. Así, se debe escoger una prueba sensible cuando existe un grave perjuicio para el sujeto si no se detecta la enfermedad, y una prueba muy específica cuando los resultados falsos positivos puedan causar un daño físico, emocional o económico al paciente sometido al cribado. • Fiabilidad (reproducibilidad): el resultado de una prueba de cribado es fiable cuando es reproducible, es decir, cuando su repetición bajo las mismas condiciones ofrece los mismos resultados. Existen cuatro 34 INFORMES, ESTUDIOS E INVESTIGACIÓN fuentes de variabilidad de cribado: variabilidad biológica (inherente a la condición que se mide), fiabilidad del instrumento de medida, variabilidad interobservador y variabilidad intraobservador. También es muy importante determinar el rendimiento de los casos detectados por el programa de cribado empleando indicadores como la prevalencia detectada de la enfermedad preclínica y los valores predictivos de la prueba, sobre todo el valor predictivo positivo. Sin embargo, aunque una enfermedad cumpla todos estos requisitos que permiten incluirla en un programa de cribado y se disponga de las pruebas apropiadas, no siempre se recomienda realizar el cribado. Hay que considerar que el programa de cribado incluye desde la identificación de la población en situación de riesgo hasta el diagnóstico de la enfermedad o de sus signos precoces en algunas personas y su tratamiento. Por ello es necesario tener un protocolo perfectamente diseñado, tanto en el seguimiento como en el diagnóstico y en el tratamiento de aquellas enfermedades que tengan una prueba positiva (50). Hay que tener en cuenta que todos los programas de cribado presentan una serie de sesgos que, en la mayoría de los casos son muy difíciles de eliminar. Estos sesgos son: lead-time bias, length bias y sobrediagnóstico que se explicarán más adelante. En la tabla 3 se pueden ver las diferencias entre las pruebas diagnósticas de un programa de cribado y las de la práctica asistencial (49). Tabla 3. Diferencias entre las pruebas diagnósticas de un programa de cribado y las de la práctica asistencial. Prueba diagnóstica de cribado Prueba diagnóstica asistencial Aplicada a personas con buen estado de salud aparente Aplicada a personas con problemas definidos Para un colectivo Individualizada Menos precisa Más precisa Más barata Más cara No constituye base para un tratamiento Sí constituye base para un tratamiento Fuente: Cerdá Mota, 2006 (49). Puede deducirse por tanto que la aplicación de pruebas de cribado es sustancialmente diferente a las pruebas clínicas de diagnóstico, algo que se debe tener en cuenta cuando se diseñe un programa de cribado. Cribado de cáncer de pulmón 35 1.5.1. Cribado de cáncer de pulmón Para que un programa de cribado sea efectivo y beneficioso, no solo debe ser capaz de detectar casos de cáncer de pulmón en estadíos tempranos sino que también debería ser capaz de poder modificar la evolución natural de la enfermedad que, en el caso particular del cáncer de pulmón, es muy rápida. Lo ideal sería que estos programas de cribado fueran capaces de reducir la mortalidad en la población cribada. En la fig. 1 se puede observar la historia natural y los niveles de prevención del cáncer. Considerando este esquema, el programa de cribado actuaría a nivel de una prevención secundaria, es decir, una detección precoz de la enfermedad. Fig. 1. Historia natural y niveles de prevención del cáncer. F. riesgo Exposición Comienzo biológico Lesiones presintomáticas Síntomas Curación/muerte Enfermedad Punto de detección DETECCIÓN PRECOZ Prevención primaria Prevención secundaria Diagnóstico/Tto Prevención terciaria Fuente: Díaz-Rubio, 2006 (51). Para el cáncer de pulmón podemos partir de las siguientes cuestiones: 1. ¿Hay razones para cribar?: Sí, ya que hoy día se sabe que el cáncer de pulmón es la primera causa de muerte de origen tumoral en los países occidentales, por lo que es un gran problema de salud. Además, presenta altas tasas de incidencia y mortalidad, aunque baja prevalencia, ya que la mayoría de los casos son detectados en estadíos avanzados y, por tanto, la tasa de supervivencia es muy baja. Sería muy útil disponer de una prueba capaz de detectar el cáncer de pulmón en estadíos tempranos y que permita alargar la supervivencia e incluso aumentar el porcentaje de curaciones. 36 INFORMES, ESTUDIOS E INVESTIGACIÓN 2. ¿Hay pruebas que permiten detectar la enfermedad precozmente?: Existen pruebas para la detección precoz del cáncer de pulmón. En los últimos años se están desarrollando nuevas pruebas que podrían complementar las ya existentes en la detección y así evitar la realización de pruebas invasivas innecesarias. 3. Falsos positivos y negativos: Es muy importante que las pruebas sean capaces de minimizar la detección de falsos positivos y negativos, por lo que estas deberían ser válidas y lo más específicas y sensibles posible. Para el cáncer de pulmón las consecuencias tanto de un falso positivo como de un falso negativo son muy importantes, ya que llevan a la realización de pruebas invasivas innecesarias o bien a la pérdida de casos de enfermedad con sus consecuencias. 4. Costes: Sería muy útil disponer de pruebas asequibles económicamente pero que al mismo tiempo sean lo bastante efectivas para poder detectar casos de cáncer de pulmón con la mayor exactitud posible y con los menores costes económicos y organizativos para el sistema sanitario. 5. ¿Qué tipo de población cribar?: El cáncer de pulmón está directamente relacionado con el tabaco, pero además, hay un pequeño porcentaje de casos ocasionados por otros factores, como pueden ser las exposiciones ocupacionales o el radón. Lo ideal sería cribar a aquellos individuos fumadores, que tienen un mayor riesgo a priori, ya que el mayor número de casos de cáncer de pulmón se concentra en ellos. 1.5.2. Pruebas de cribado para el cáncer de pulmón Se han propuesto diversas pruebas para el cribado de cáncer de pulmón. Lo más común es clasificar este tipo de pruebas en dos grupos: de imagen y biológicas. En función de su frecuencia de uso las pruebas más usadas en el cribado de cáncer de pulmón son la radiografía de tórax, la tomografía computarizada y la citología de esputo. La radiografía de tórax (Rx) es una prueba no invasiva que permite, en el caso del cáncer de pulmón, determinar la presencia de manchas, masas o nódulos. Supone la exposición de una parte del cuerpo a una pequeña dosis de radiación ionizante. La tomografía computarizada, también conocida con el nombre de CT por sus siglas en inglés (computed tomography), se denominó en un prin- Cribado de cáncer de pulmón 37 cipio tomografía axial computarizada (TAC) porque solo permitía realizar cortes axiales del cuerpo. En artículos científicos se emplea el término de tomografía computarizada helicoidal de baja resolución (LDCT, por sus siglas en inglés) o de baja dosis. Es un procedimiento que produce imágenes en distintos planos que, al ser combinadas en un ordenador, aportan una visión más detallada del cuerpo (a diferencia de la radiografía normal, que da una única imagen). Esta prueba proporciona información precisa sobre el tamaño, forma y posición de un tumor e incluso es capaz de ayudar a localizar ganglios linfáticos afectados. Es más sensible que la radiografía de tórax a la hora de detectar cánceres de pulmón en estadíos iniciales. Se han realizado una serie de modificaciones con el objetivo de aumentar la resolución temporal (el tubo de radiación gira en torno al paciente al mismo tiempo que el paciente es movido a través del escáner) y espacial, mejorar la calidad de la imagen y reducir la dosis de radiación (52). Se pueden distinguir varios tipos de tomografías: • Tomografía computarizada helicoidal de baja resolución (LDCT, por sus siglas en inglés): permite obtener una imagen o sección del cuerpo por medio de radiografías realizadas a lo largo del eje axial del cuerpo. • Tomografía computarizada helicoidal de alta resolución (HRCT, por sus siglas en inglés): permite obtener cortes más finos (de entre 1 y 2 mm) que la tomografía convencional, por lo que permite estudiar estructuras mucho más pequeñas y con mayor precisión (53). • Tomografía computarizada de emisión fotónica simple (TCEFS o SPECT): muy útil para detectar metástasis a ganglios linfáticos mediastínicos. • Tomografía computarizada multicorte o multidetector (TCMC): permite obtener una máxima resolución en tres planos cubriendo el máximo volumen en el mínimo tiempo posible. Actualmente es el estándar para las exploraciones torácicas. Presenta una serie de ventajas frente a la tomografía convencional como son la cobertura de regiones anatómicas más extensas, la optimización del uso de contraste intravenoso, una mejor adecuación de los tiempos de adquisición a la utilización de los contrastes yodados, una mayor capacidad de procesado y posprocesado de las imágenes, y reconstrucciones retrospectivas sin adquisición adicional de datos (53). 38 INFORMES, ESTUDIOS E INVESTIGACIÓN La citología de esputo es un método de diagnóstico sencillo y no invasivo, pero de rentabilidad muy variable. Consiste en un examen, al microscopio, de las células del pulmón que se encuentran en el esputo (moco y otras materias expulsadas desde los pulmones al expectorar). La recogida de las muestras debe ser en ayunas, después de una inspiración profunda y previo enjuague bucal. Para inducir el esputo se administra una solución salina al paciente (en caso de no conseguir esputo, se aumenta la concentración de sales hasta obtener la muestra necesaria). 1.5.3.Otras pruebas potenciales para el cribado del cáncer de pulmón A pesar de que las anteriores son las tres pruebas más usadas, según la literatura existen otras muchas que podrían servir como pruebas de cribado en un futuro próximo (tabla 4). Algunas de ellas se usan habitualmente en el diagnóstico clínico de la enfermedad y otras están comenzando a utilizarse en clínica, como la broncoscopia de autofluorescencia (54). La tomografía de emisión de positrones, más conocida como PET por sus siglas en inglés, es una prueba que consiste en administrar un contraste con glucosa radiactiva que es absorbida por las células cancerosas haciendo que éstas produzcan una radiactividad que es detectada por una cámara especial. Esta prueba puede ser muy útil en etapas tempranas para detectar si el cáncer se ha propagado a los ganglios linfáticos o para comprobar si una mancha observada en una radiografía es cáncer. Para un mejor diagnóstico se puede combinar con tomografía computarizada. El análisis de compuestos orgánicos volátiles (VOC) es una prueba no invasiva que consiste en analizar los cambios en la producción y metabolización de los compuestos orgánicos volátiles de muestras del aire exhalado. Las muestras son recogidas en una habitación cerrada en la que el paciente inhala por la nariz y exhala por la boca durante 12 minutos, se guardan en un incubador que las mantiene a la temperatura corporal y se analizan en un colorímetro donde se representan diferentes colores dependiendo de la composición de compuestos orgánicos del aire. Esta prueba podría ser útil para el diagnóstico precoz del cáncer de pulmón ya que la composición del aire exhalado es diferente dependiendo de si hay o no cáncer de pulmón, aunque al haberse desarrollado recientemente no se conocen todavía sus índices de validez (55). El análisis de condensación del aire exhalado en la respiración es otra prueba no invasiva en la que el aire exhalado entra en un sistema de re- Cribado de cáncer de pulmón 39 frigeración para condensarse (56). Este aire condensado contiene macromoléculas, como por ejemplo proteínas, que pueden ser empleadas como herramienta para el diagnóstico de problemas pulmonares e incluso usadas como potenciales pruebas de cribado para el cáncer de pulmón (57-60). Sin embargo, el análisis de las proteínas analizadas con esta prueba puede verse afectado por determinados factores, como el tipo y cantidad de comida ingerida antes de la recogida de la muestra, el humo del tabaco, medicamentos o la presencia de enfermedades sistémicas (61). Para poder solucionar algunos de estos problemas se suele realizar la recogida de las muestras tras un período de ayuno. Es muy específica (91,9 %) y sensible (71,4 %) en muestras seleccionadas (62). El análisis de alteraciones en el ADN permite determinar alteraciones específicas en microsatélites de ADN, al poder observar diferencias entre el ADN de tejido normal y el tumoral. La proteómica consiste en analizar cambios genéticos producidos en la sangre o tejidos del tumor respecto al tejido normal, como puede ser la presencia de determinados anticuerpos específicos (63). Presenta un gran potencial para el diagnóstico de tumores tanto invasivos como preinvasivos (64). Estas dos últimas pruebas se encuentran en fases muy iniciales para aplicarse tanto en la clínica como en cribado. En la tabla 4 pueden observarse las diferencias entre las pruebas anteriormente mencionadas. Tabla 4. Pruebas potenciales de cribado del cáncer de pulmón.* Coste estimado Disponibilidad en clínica Estado de desarrollo Potencial para su aplicación en el cribado Invasivo PET +++ + ++ ++ NO (exceptuando radiofármacos) VOC ++ + + ¿? NO +++ + + + NO Alteraciones en ADN ++ + + +++ SÍ (muestra de tejido) Proteómica ++ + + +++ (tumores preinvasivos e invasivos) SÍ (muestra de tejido o sangre) Prueba Condensación aire exhalado *Elaboración propia +: Bajo ++: Medio 40 +++: Alto ¿?: No se conoce INFORMES, ESTUDIOS E INVESTIGACIÓN 2. OBJETIVOS 2.1. Objetivos principales • Evaluar la eficacia y efectividad del cribado de cáncer de pulmón. 2.2. Objetivos secundarios • Analizar la efectividad de la tomografía helicoidal de baja resolución en el cribado de cáncer de pulmón. • Analizar el papel la radiografía de tórax y de la citología de esputo en el cribado de cáncer de pulmón. • Conocer la potencial utilidad de otras pruebas de cribado de cáncer de pulmón. • Estimar la población potencial a cribar en un programa de cribado en las Comunidades Autónomas de España. Cribado de cáncer de pulmón 41 3. MÉTODOS Se han considerado tres secciones en este apartado: la búsqueda de la literatura, la selección de los estudios para elaborar el documento y, por último, el cálculo del número potencial de personas a cribar en un hipotético programa de cribado de cáncer de pulmón en España. 3.1. Búsqueda de literatura Se realizó una búsqueda bibliográfica en las siguientes bases de datos automatizadas: • Bases de datos especializadas en revisiones sistemáticas: Biblioteca Cochrane y base de datos del NHS CRD (National Health Service Centre for Reviews and Dissemination), que incluye HTA (Health Technology Assessment) con informes de evaluación, DARE (Database of Abstracts of Reviews of Effects) con revisiones de efectividad y NHS EED (National Health Service Economic Evaluation Database) con documentos de evaluación económica. • Bases de datos específicas para guías de práctica clínica (GPC): Tripdatabase. • Bases de datos generales: Medline (PubMed), EMBASE, ISI WEB of Knowledge e Índice médico español. • Páginas especializadas: National Cancer Institute (NCI) de Estados Unidos, National Cancer Institute (NCI) de Canadá, Agency for Health Research and Quality (AHRQ) de Estados Unidos. Todo este proceso se completó con una búsqueda general en Google (con el fin de buscar otra información de interés) y con una revisión manual de las referencias bibliográficas de los artículos seleccionados para recuperar aquellos estudios no identificados con la anterior estrategia de búsqueda. Se elaboraron estrategias de búsqueda concretas para cada base de datos utilizando los correspondientes descriptores y diferentes palabras clave (ver anexo A). El marco temporal de la búsqueda ha sido diferente dependiendo del tipo de información buscada. Así, para las revisiones sistemáticas se han incluido aquellas publicadas desde el 1 enero de 2005 hasta la actualidad. Para el análisis de las diferentes pruebas de imagen se ha buscado información en Cribado de cáncer de pulmón 43 las bases generales desde el 1 de enero del 2004, y para el análisis de pruebas biológicas y pruebas de imagen diferentes a TC (PET, Rx,…) se incluyen estudios publicados desde el 1 de enero del 2000. Además, aunque no sea objetivo de nuestro estudio, también se han seleccionado estudios de coste-efectividad publicados desde el 1 de enero del 2000 y se han incluido en la discusión determinadas revisiones sistemáticas que no son consideradas de buena calidad por no especificar las bases de datos de las cuales se recoge la información, pero que sí pueden aportar información interesante. Se han hecho actualizaciones de la búsqueda periódicamente desde el momento de la búsqueda inicial realizándose la última actualización en enero de 2009. 3.2. Selección de los estudios Tras la lectura de los resúmenes de los artículos obtenidos en la búsqueda se procedió a la selección de los estudios, en la que participaron dos investigadores. Cada investigador leyó los estudios de forma independiente y los seleccionó basándose en una serie de criterios previamente establecidos para lograr así homogeneidad en la información obtenida, paso previo a toda revisión sistemática. Cualquier discrepancia sobre la inclusión o la exclusión de los estudios se resolvió por consenso. Dichos criterios aparecen a continuación. Según el idioma Se incluyeron todos aquellos estudios publicados en español, inglés, francés, portugués e italiano. Se excluyeron investigaciones publicadas en otros idiomas. Según el diseño del estudio Respecto al diseño del estudio, se incluyeron informes de evaluación de tecnologías sanitarias, revisiones sistemáticas, metanálisis, ensayos clínicos y estudios de cohortes. Se excluyeron el resto de diseños epidemiológicos. Según el tipo de publicación Se incluyeron artículos originales de investigación y revisiones sistemáticas. Se excluyeron aquellos estudios observacionales incluidos en las revisiones sistemáticas, editoriales, notas clínicas, cartas al director, comunicaciones a congresos y estudios de un solo caso. 44 INFORMES, ESTUDIOS E INVESTIGACIÓN Según el tamaño de la muestra En este caso se han tenido en cuenta una serie de restricciones para estudios originales, considerando para pruebas de imagen y biológicas un tamaño muestral ≥ a 300 pacientes en cada brazo para un cribado universal y ≥ a 100 pacientes en cada brazo para un cribado selectivo (población de riesgo). Se excluyen estudios con tamaños muestrales menores. Según el objetivo del estudio Se seleccionaron los estudios sobre cribado de cáncer de pulmón que tuviesen como objetivo evaluar la eficacia y efectividad de las diferentes pruebas de cribado. Se excluyeron aquellos estudios con finalidad diferente a la realización de un cribado de cáncer de pulmón (estadificación, diagnóstico clínico, etc.). Según la prueba diagnóstica Se incluyeron estudios de cribado de cáncer de pulmón que empleasen pruebas de imagen (TC, PET, Rx…) o pruebas biológicas (citología de esputo, compuestos orgánicos volátiles (VOC), análisis del aire exhalado, esputo inducido…). Según el tipo de cribado Se incluyeron todos los estudios en los que se realizó un programa de cribado, tanto universal como selectivo (exclusivamente en fumadores). Se excluyeron estudios que incluyeran cribados en otras poblaciones de alto riesgo diferentes a fumadores, como por ejemplo exposiciones ocupacionales o elevada exposición a radón. Según el tipo de participantes Se incluyeron estudios realizados en adultos (≥ 18 años). Según la variable resultado Se incluyeron estudios cuyo objetivo era evaluar la validez de la prueba de cribado, mortalidad o supervivencia del cáncer de pulmón. Cribado de cáncer de pulmón 45 3.3. Contextualización En este apartado se plantea cual puede ser el número de personas susceptibles de ser cribadas en España para el cáncer de pulmón, desglosado por sexo y Comunidades Autónomas. Para ello es necesario disponer de fuentes de información a partir de las que obtener estos datos. 3.3.1. Fuentes de información Con el objetivo de obtener datos referentes a la situación del cáncer de pulmón y del tabaquismo en España, se ha recurrido al Instituto Nacional de Estadística (24) y a la Encuesta Nacional de Salud. Los datos corresponden al año 2006. Estos datos permiten conocer la diferente prevalencia del tabaco en las Comunidades Autónomas, desglosarlo por sexos y estimar en cuáles de ellas puede ser más elevada la potencial aparición de cáncer de pulmón y, por tanto, dónde podría haber mayor beneficio con una hipotética detección precoz del cáncer de pulmón. 3.3.2. Cálculo del número de personas susceptibles de ser cribadas Es muy importante considerar una serie de factores antes de decidir la puesta en marcha de un programa de cribado en población general como son la frecuencia y los intervalos de aplicación de las pruebas de cribado o las particularidades epidemiológicas de cada zona geográfica (65). En este informe se determina únicamente el número de personas susceptibles de ser cribadas empleando la información obtenida a partir de las fuentes anteriormente citadas. Para ello se ha calculado el número de personas que podrían ser candidatas a ser sometidas a un programa de cribado de cáncer de pulmón por sexo y Comunidad Autónoma. Como no se dispone de esta información de forma directa, es necesario realizar una serie de cálculos a partir de los datos disponibles y obtener de este modo la carga potencial de cáncer de pulmón en cada comunidad y ver qué población puede ser subsidiaria de una hipotética prueba de cribado efectiva. Para realizar los cálculos se ha empleado la siguiente fórmula: Población a cribar = Población total (50-74 años) x % fumadores diarios x % fumadores de ≥ 20 cigarrillos/día 46 INFORMES, ESTUDIOS E INVESTIGACIÓN Además, con el objetivo de poder saber con mayor precisión la carga potencial de cáncer de pulmón en las diferentes comunidades, se ha estimado el porcentaje de población en riesgo de desarrollar cáncer de pulmón mediante la siguiente fórmula: Fumadores diarios de ≥ 20 cigarrillos/día de 50-74 años (población a cribar) Población en riesgo (%) = ­­­—————————————————————— Población de 50-74 años Los datos se han desglosado por Comunidades Autónomas, hombres, mujeres y población total. Cribado de cáncer de pulmón 47 4. RESULTADOS 4.1. Resultados de la búsqueda La búsqueda en las bases de datos seleccionadas proporcionó un total de 1.939 referencias bibliográficas. Después de la eliminación de los duplicados, se obtuvieron 954 referencias. La revisión manual de la bibliografía citada en los artículos originales no aportó referencias adicionales. La lectura a texto completo y la evaluación de todos los artículos seleccionados por los dos revisores concluyó con la inclusión consensuada de 11 publicaciones (ver anexo B). Las actualizaciones periódicas aportaron 2 artículos adicionales (Fig. 2). A pesar de que el número de artículos recuperados ha sido elevado, muchos de ellos han sido excluidos. Las causas más frecuentes de exclusión de los artículos seleccionados fueron: inexistencia de un grupo control, tamaño insuficiente de la muestra, haber sido incluidos en revisiones sistemáticas posteriores o incluir población de riesgo diferente a fumadores. Los motivos de exclusión de los artículos seleccionados para la lectura a texto completo se exponen en el anexo C. Se localizaron un total de 8 revisiones sistemáticas, de las cuales se excluyeron 2 por no cumplir alguno de los requisitos de inclusión (66, 67). Finalmente, se incluyeron 6 revisiones sistemáticas (68-73) (ver anexo D). Respecto a los 5 estudios primarios incluidos, 4 evalúan la factibilidad del cribado de cáncer de pulmón con pruebas de imagen y 1 con pruebas biológicas (74-78) (ver anexo E). La mayoría de los estudios proceden de Europa y EUA. En la figura 2 se resumen los resultados de la búsqueda y en la tabla 5 se muestra un resumen de las revisiones sistemáticas y ensayos clínicos incluidos, clasificados según la prueba de cribado empleada o evaluada en cada uno de ellos. Cribado de cáncer de pulmón 49 Fig. 2. Resultados de la búsqueda bibliográfica. Tabla 5. Resumen de las revisiones sistemáticas y los ensayos clínicos incluidos Prueba Revisiones sistemáticas Ensayos clínicos LDCT vs. Rx / no cribado 4 3 LDCT 1 - Rx con o sin citología de esputo vs. Rx únicamente 1 Citología de esputo - 1 Total 6 5 50 1 INFORMES, ESTUDIOS E INVESTIGACIÓN 4.2. Evaluación de la calidad de los estudios Para evaluar el nivel de calidad de los estudios se ha empleado la escala utilizada por el Scottish Intercollegiate Guidelines Network (SIGN), que ha sido revisada recientemente (79). Según esta escala (Anexo F), el nivel de las revisiones y los estudios primarios incluidos en este informe queda reflejado en la tabla 6. Tabla 6. Valoración de la calidad de los estudios incluidos. Estudio Nivel de calidad Bach y cols., 2007 2++ Yau y cols., 2007 2++ Black y cols.,2007 2++ Vidal Serrano y cols.,2007 2++ Hunt y cols., 2006 2++ Hunt y cols., 2006 2++ Toyoda y cols., 2008 1- Fujikawa y cols., 2008 1- Blanchon y cols., 2007 1- Marcus y cols., 2006 1- Melamed y cols., 2000 1- 4.3. Resultados de revisiones sistemáticas Se incluyeron finalmente seis revisiones sistemáticas que analizan la eficacia y efectividad de diferentes pruebas de cribado de cáncer de pulmón en población de riesgo (ver anexo D). Todas ellas emplean LDCT o radiografía de tórax combinada o no con citología de esputo. La primera revisión incluida la publicó en 2007 el American College of Chest Physicians (ACCP) con el objetivo de analizar la efectividad del cribado mediante la utilización de LDCT frente a la radiografía de tórax en pacientes de alto riesgo (asintomáticos, sin historia previa de cáncer de pulmón, edad ≥ 40 años, consumo de tabaco ≥ 10-20 paquetes/año, fumadores y Cribado de cáncer de pulmón 51 exfumadores). Se entiende por paquetes/año al consumo de tabaco durante toda la vida del individuo. Se calcula multiplicando el número de paquetes fumados al día por el número de años fumando esa cantidad. Además, se incluyen resultados de otras pruebas como citología de esputo, análisis de compuestos orgánicos volátiles o alteraciones en el ADN y proteómica. Según los estudios incluidos en la revisión, la prevalencia detectada con la LDCT para el cáncer de pulmón es del 2,7 % en las poblaciones de alto riesgo y del 0,7-1 % en las de bajo riesgo. La efectividad (para la detección de estadíos tempranos) fue superior al 50 % en todos los estudios evaluados en la revisión para el brazo cribado con LDCT mientras que en el brazo control no superó el 21 % en ninguno de los estudios. Ninguna de las pruebas de cribado consigue reducir las tasas de mortalidad. Tanto la radiografía de tórax como la LDCT son eficaces para la detección de tumores en estadíos tempranos, pero no reducen la detección de tumores en estadíos tardíos. Respecto a otras pruebas, se afirmó que la proteómica mejora la calidad del cribado y puede usarse tanto en tumores invasivos como preinvasivos. No se especifican valores de sensibilidad, especificidad, valor predictivo positivo ni valor predictivo negativo. De todas maneras, debido al corto período de seguimiento hay poca evidencia sobre la reducción de la mortalidad y, por tanto, no se recomienda la realización de un programa de cribado con LDCT (a excepción de personas con alto riesgo de desarrollar cáncer de pulmón donde se discutirá esta posibilidad de modo individualizado con el paciente) ni tampoco el uso de la radiografía de tórax o la citología de esputo (ni aislada ni combinada con otras pruebas). Esta revisión también analizó la supervivencia en tres estudios, pero en ninguno de ellos se observó reducción de la mortalidad (68). En 2007, el London Health Sciences Centre publicó otra revisión en la que se incluyeron 22 estudios recogidos desde 1966 hasta 2006 y que comparan entre sí dos pruebas de cribado. La cuestión que se planteó en esta revisión fue si sería factible realizar un cribado con LDCT en población de riesgo (edad ≥ 40 años, fumadores de > 1 paquete/año y exfumadores) y mayoritariamente hombres. Se parte de tres hipótesis clave para el cribado de cáncer de pulmón con la LDCT: 1) características del programa de cribado con LDCT; 2) porcentaje de casos de cáncer de pulmón detectados en estadíos tempranos, y 3) reducción potencial de la tasa de mortalidad por cáncer de pulmón. Los programas de cribado consistieron en realizar LDCT frente a no LDCT o radiografía de tórax combinada o no con citología de esputo. Los valores medios para especificidad, sensibilidad, valor predictivo positivo y valor predictivo negativo de los estudios incluidos fueron 81 %, 81 %, 8% y 99 %, respectivamente. Los autores del estudio consideran que la exactitud de la tomografía computarizada de baja resolución depende en gran 52 INFORMES, ESTUDIOS E INVESTIGACIÓN medida del radiólogo y del umbral que marca la diferencia entre lesiones sospechosas y no sospechosas. Se concluyó que la tomografía computarizada de baja resolución detecta más nódulos no calcificados (nódulos sospechosos de malignidad que deben ser evaluados en pruebas posteriores) y en estadío I que la radiografía de tórax y otras pruebas. Sin embargo, también se observó que no hay una relación entre el estadío temprano y el hecho de que el nódulo sea pequeño. Hasta el momento no hay evidencia de que el cribado reduzca la mortalidad. Según los autores de esta revisión el protocolo ideal para un programa de cribado debería incluir una clara definición de población de alto riesgo (69). También en 2007, el Health Technology Assessment Group de Aberdeen publicó otra revisión cuyo principal objetivo era examinar la evidencia de la efectividad clínica del cribado de cáncer de pulmón con tomografía computarizada (LDCT) en pacientes con alto riesgo (edad ≥ 40 años, fumadores de ≥ 10 paquetes/año; algunos estudios también incluían población expuesta a asbestos). Determinados estudios incluyeron no fumadores como grupo control. La revisión evaluó 12 estudios (dos ensayos clínicos aleatorizados y diez estudios de cribado sin grupo control) publicados desde 1994 hasta enero de 2005. Solo uno de los estudios empleó un grupo control cribado con radiografía de tórax, el resto eran estudios de un único brazo cribado con tomografía computarizada. La sensibilidad para la LDCT (de los estudios en los que se pudo calcular este valor) osciló entre el 80-90 % y la sensibilidad osciló entre el 1,8-32 %. Se observó que, en los estudios incluidos, el valor predictivo positivo fue bajo (< 20 %) mientras que el valor predictivo negativo fue superior al 95 %. La prevalencia fue del 0,4-3,2 % mientras que la incidencia fue algo más baja (0,07-1 %) (para los casos de cáncer de pulmón detectados al inicio del estudio). Ninguno de los estudios mostró reducción de la mortalidad en el grupo cribado. Se concluyó que, a pesar de que la tomografía computarizada es capaz de detectar muchos tumores en estadíos tempranos, debido a la ausencia de ensayos clínicos aleatorizados con una duración adecuada no se puede obtener evidencia clara de que un programa de cribado con tomografía computarizada sea efectivo, ya que no se apreció reducción de la mortalidad. Este tipo de estudios con tomografía computarizada solo puede aportar un mejor entendimiento de la historia natural de los nódulos y de los casos de cáncer de pulmón detectados (70). En 2007, la Agencia de Evaluación de Tecnologías Sanitarias de Andalucía publicó una revisión en la que se recogieron los resultados de 12 estudios originales (1 ensayo clínico aleatorizado, 1 estudio que empleó como control una serie histórica y 10 series de casos) de los que 11 evaluaron la efectividad y 1 el coste-efectividad de la tomografía computarizada Cribado de cáncer de pulmón 53 (LDCT) como prueba de cribado para cáncer de pulmón en población de riesgo (asintomáticos, edad ≥ 40 años, exfumadores o fumadores de ≥ 10 paquetes/año). Todos los estudios, a excepción de uno, tuvieron un período de seguimiento inferior a 5 años; además, también hubo diferencias respecto a la periodicidad de los tests, el grosor de los cortes de la LDCT o a la definición y seguimiento de los casos detectados. Se observaron valores altos de falsos positivos (87,9-99 %). El valor predictivo positivo fue bajo (4-12,1 %). Debido a la falta de información sobre los falsos negativos, no se han podido reflejar los datos sensibilidad ni del valor predictivo negativo. A pesar de que la LDCT es capaz de detectar tumores en estadíos tempranos —y, por tanto, con mejor pronóstico—, no hay evidencia de un cambio en el pronóstico de la enfermedad. Tampoco se considera coste-efectivo, ya que no hay reducción de la mortalidad (corto tiempo de duración de los estudios), de la tasa de falsos positivos, del coste económico de las pruebas realizadas ni tampoco aumento de la adherencia. Para poder obtener mejores resultados sería necesario tener en cuenta aspectos como el número de intervenciones en individuos sanos, la exposición a la radiación o la ansiedad generada por la espera de los resultados de las pruebas, factores que no han sido considerados en ninguno de los estudios publicados (73). En junio de 2006, se publicó una revisión con el objetivo de evaluar si la tomografía computarizada de baja dosis (LDCT) mejora la supervivencia en pacientes asintomáticos de bajo y alto riesgo de cáncer de pulmón (fumadores, exfumadores, expuestos a asbestos, hombres y mujeres, edad ≥ 40 años) respecto a la radiografía de tórax. La revisión incluyó 9 estudios (3 revisiones sistemáticas, 4 estudios de cohortes, 1 revisión no sistemática y 1 estudio retrospectivo) que analizaban el grado de sobrediagnóstico en este tipo de programas de cribado con tomografía computarizada. Por lo general, se observó que la prevalencia de cáncer de pulmón en los estudios incluidos, empleando la LDCT, se encuentra entre el 0,40 % y el 2,70 %. No se indican datos de especificidad, sensibilidad, valor predictivo positivo ni de valor predictivo negativo. A pesar de que la LDCT detecta tres veces más nódulos y tumores en estadíos más tempranos que la radiografía de tórax, ninguna de las revisiones realizadas con LDCT considera que haya suficiente evidencia para considerarla como una buena prueba de cribado para el cáncer de pulmón ya que no se observó reducción de la mortalidad aunque sí se observa mejor supervivencia en el grupo cribado. Estos resultados se deben al escaso tiempo de seguimiento ya que a excepción del estudio ELCAP, en ninguno de los estudios incluidos el seguimiento es superior a 5 años, a que la población de estudio solo representa un caso particular de pacientes (población de riesgo) y a la ausencia de ensayos clínicos que analicen el impacto de la LDCT en la mortalidad (71). 54 INFORMES, ESTUDIOS E INVESTIGACIÓN En abril de 2006, se realizó otra revisión similar a la anterior pero con el objetivo de evaluar si la radiografía de tórax mejora la supervivencia en hombres asintomáticos con riesgo de cáncer de pulmón (fumadores habituales, con edades comprendidas entre 40-45 años). Todos los estudios incluidos realizaron un programa de cribado consistente en una radiografía de tórax con o sin citología de esputo frente a un grupo control con únicamente radiografía de tórax. La revisión incluyó 10 estudios (7 ensayos clínicos aleatorizados, 1 revisión sistemática con metanálisis de ensayos clínicos aleatorizados, 1 revisión no sistemática y 1 revisión sistemática). Todos los estudios incluidos mostraron una tendencia a aumentar la incidencia de cáncer de pulmón, la tasa de cirugías y una mayor supervivencia en el grupo cribado con ambas pruebas. No se especifican datos de especificidad, sensibilidad, valor predictivo positivo ni valor predictivo negativo. No se observó reducción de la mortalidad, e incluso el metanálisis realizado demostró aumentó de ésta en un 11 % en el grupo cribado únicamente con radiografía de tórax. Se comprobó que se diagnostican más casos de cáncer de pulmón en estadíos tempranos en el grupo de cribado con ambas pruebas pero no hay reducción de la mortalidad debido a la corta duración de los estudios evaluados. Tampoco se reduce la detección de tumores en estadíos avanzados. No hay evidencia para realizar un cribado de cáncer de pulmón con radiografía de tórax con o sin citología de esputo como prueba de cribado (72). A pesar de que es muy importante la seguridad en este tipo de programas de cribado ninguna de las revisiones sistemáticas la evalúa. En la tabla 7 se recoge la información de los estudios primarios comparativos incluidos en tres de las revisiones evaluadas en este informe (69, 70, 73). No se ha podido obtener dicha información de las otras tres revisiones sistemáticas incluídas por la ausencia de esa información (68, 71, 72). Cribado de cáncer de pulmón 55 Tabla 7. Resultados de estudios comparativos de las revisiones sistemáticas. Revisión sistemática Nº estudios comparativos Población Yau y cols., 2007 Black y cols., 2007 4 ≥ 40 años, fum (> 50%) y exfum 2 2 ≥ 50 años, fum 30 PY, exfum (< 10 años), citología esputo anormal+EPOC Programa de cribado Vidal Serrano y cols., 2007 Pacientes asintomáticos voluntarios, 50-74 años, fum ≥ 20 PY, exfum (<10 años) LDCT vs. radiografía de tórax o citología de esputo Cribado único con LDCT vs. radiografía de tórax/no cribado LDCT vs. radiografía de tórax/ Duración programa de cribado 6-18 meses No se especifica < 5 años % pacientes con nódulos LDCT: 11-56 % No se especifica No se especifica No se especifica No se especifica (test basal) % pacientes con nódulos (test post.) control histórico Control: No se especifica LDCT: 2-16 % Control: No se especifica % pacientes con cáncer (test basal) LDCT: 0,19-2,7 % LDCT: 1,89-3,26 % LDCT: 1,9-2 % Control: No se especifica Control: No se especifica Control: No se especifica % pacientes con malignidad (test post.) LDCT: 0,20-2 % No se especifica LDCT: 0,6-2 % % estadio I LDCT: 53-88 % LDCT: 1 % LDCT: 42-62 % Control: No se especifica Control: 0,38 % (Solo datos Control: No se especifica FP/FN 206-761/3-18 No se especifica 89,3-95,2 %/ No se especifica VPP/VPN (%) 3–12/99-100 % No se especifica No se especifica Sensibilidad / Especificidad 55-88/49-95 % No se especifica No se especifica Control: No se especifica Control: No se especifica de uno de los estudios) Fum: fumadores Exfum: exfumadores PY: paquetes/añoDatos aportados por rangos, reflejando el valor más pequeño y el mayor de los estudios comparativos incluidos en cada revisión sistemática. 56 INFORMES, ESTUDIOS E INVESTIGACIÓN 4.4. Resultados de estudios individuales A continuación se describen los resultados de los distintos estudios individuales incluidos en la revisión (ver anexo E). 4.4.1. Resultados para pruebas de imagen combinadas o no con pruebas biológicas En 2008, Toyoda y cols. publicaron un estudio con el objetivo de evaluar la sensibilidad y especificidad de la tomografía computarizada de baja resolución (LDCT) y de la radiografía de tórax en un estudio con 4.689 y 13.381 en cada brazo, respectivamente. La población fue reclutada entre 1998 y 2002 e incluyó tanto hombres como mujeres, fumadores actuales, exfumadores, no fumadores y con edades comprendidas entre 40 y 80 años. Se realizaron un total de 7.190 LDCT y 36.085 radiografías de tórax y, además, citología de esputo adicional en ambos grupos. Se observó que para la LDCT los valores de sensibilidad y especificidad son del 88,9 % y 92,6 % y para la radiografía de tórax, del 78,3 % y 97,0 %. En ambos casos, la especificidad fue más elevada en los test sucesivos que en el basal. Según los autores, esto puede ser debido a que la sensibilidad basal está afectada por el length bias y el sobrediagnóstico. Además, en ambos casos, la sensibilidad era mayor para la detección de adenocarcinoma que para no adenocarcinoma (100 % frente a 61,5 % para la LDCT y 95,8 % frente a 50,0 %, para la radiografía de tórax). Respecto al consumo de tabaco, el estudio reflejó que ambas pruebas presentan mejor rendimiento para no fumadores. Se observó también que hay más sobrediagnóstico con LDCT que con la radiografía de tórax. Se concluyó que la LDCT tiene mayor sensibilidad y menor especificidad que la radiografía de tórax (74). En 2008, Fujikawa y cols. publicaron otro estudio para evaluar el cribado de cáncer de pulmón con radiografía de tórax. El estudio fue realizado en Japón en población ≥ 40 años y sin signos de cáncer de pulmón en radiografía de tórax durante al menos un año antes de iniciarse el programa de cribado. Esta población fue sometida a un programa de cribado anual con radiografía de tórax y LDCT durante 4 años. Todos aquellos pacientes con resultado negativo en la radiografía fueron sometidos a tomografía computarizada. Hubo incorporación de nuevos pacientes cada año en ambos grupos del cribado. Finalmente, se incluyeron un total de 22.720 pacientes para el brazo cribado con radiografía de tórax y 3.305 para el de tomografía computarizada. El porcentaje de casos de cáncer de pulmón detectados, en todo el estudio, en estadíos III y IV fue mayor con la tomografía computarizada que con la radiografía de tórax (10,2 % para el estadío III y 1,4 % para Cribado de cáncer de pulmón 57 el estadío IV). Además, con la LDCT todos los casos son detectados en el test basal. Se observó mejor supervivencia en el grupo cribado con LDCT, tanto si eran tratados con cirugía como si no. Según los autores, este estudio tiene una serie de limitaciones (las poblaciones incluidas en cada brazo tienen características diferentes, no hay igualdad en la periodicidad del cribado y además no se realizan pruebas de seguimiento para determinar la mortalidad y la aparición de nuevos casos de cáncer de pulmón), por lo que este tipo de análisis no son adecuados para comparar la eficacia del cribado de cáncer de pulmón con tomografía computarizada frente a radiografía de tórax. Se concluyó que la tomografía computarizada detecta más casos de cáncer de pulmón en estadíos tempranos. Éstos podrían ser menos propensos a la malignidad que los casos detectados con radiografía de tórax o por presentar síntomas de la enfermedad. Sin embargo, se consideró que serían necesarios estudios de mayor duración para poder evaluar la reducción de la mortalidad (78). En 2007, Blanchon y cols. publicaron un ensayo clínico aleatorizado, “Depiscan”, con el objetivo de evaluar el cribado de cáncer de pulmón con tomografía computarizada de baja dosis (LDCT) frente a la radiografía de tórax. Los investigadores seleccionaron y reclutaron 1.000 sujetos durante un año, de los que se incluyeron en el estudio 765 (29 % mujeres y 71 % hombres), todos ellos con alto riesgo (asintomáticos, con edades comprendidas entre 50 y 75 años, fumadores habituales o exfumadores desde hace menos de 15 años y con un consumo medio ≥ 15 cigarrillos/día al menos durante 20 años). El programa de cribado consistió en realizar a los participantes un cribado anual durante el período de octubre de 2002 a diciembre de 2004. Las pruebas de LDCT y radiografía de tórax fueron realizadas en 14 centros de Francia. Se observó que en el brazo cribado con LDCT se detectan más casos de cáncer de pulmón que en el de radiografía de tórax (2,4 % y 0,3 %, respectivamente). Además, también se detectan tumores en estadíos más tempranos con LDCT (3 casos de cáncer de pulmón para la LDCT frente a 1 para la radiografía de tórax). Sin embargo, solo se detectan tumores en estadíos tardíos en el brazo cribado con LDCT. Además, también es mayor el número de otras lesiones en el brazo cribado con LDCT. Se concluyó que la LDCT detecta hasta 10 veces más nódulos no calcificados que la radiografía de tórax y se observó una prevalencia de nódulos no calcificados de cualquier tamaño del 45,2 % en el brazo cribado con la LDCT. Un dato importante de este estudio es que la proporción de tumores en estadíos tardíos es mayor en el cribado basal, a diferencia de lo que se había observado en otros estudios anteriores. La razón de esto no está del todo clara, aunque se propuso que podría ser debido a que los criterios de selección de los pacientes no hayan sido lo suficientemente cuidadosos y a que se hayan 58 INFORMES, ESTUDIOS E INVESTIGACIÓN incluido grandes fumadores o pacientes con síntomas. Se considera que sería necesario realizar más ensayos clínicos aleatorizados que comparen la LDCT frente a la radiografía de tórax o frente a un grupo sin ningún tipo de cribado para poder evaluar así los beneficios y riesgos del cribado con LDCT y la mortalidad del cáncer de pulmón (75). En 2006 Marcus y cols. publicaron un estudio sobre el “Mayo Lung Project” para evaluar el sobrediagnóstico y la reducción de la mortalidad en un programa de cribado de cáncer de pulmón con radiografía de tórax y citología de esputo en hombres fumadores, ≥ 40 años y sin síntomas de cáncer de pulmón en radiografía de tórax y citología de esputo anteriores al programa de cribado. El estudio incluye 9.211 pacientes divididos en dos brazos: uno (brazo cribado) con 4.618 sujetos a los que se realizó radiografía de tórax y citología de esputo cada 4 meses durante 6 años y posterior seguimiento de un año y medio, y otro, control con 4.593 participantes a los que se recomendó realizar radiografía de tórax y citología de esputo anual. Este estudio constó de dos etapas ya que se realizó una evaluación de los resultados en dos ocasiones, en 1983 y en 1999, por lo que hubo un incremento del tiempo de seguimiento de 16 años. Tanto en el primer período del estudio como al aumentar el tiempo de seguimiento, no se observó reducción de la mortalidad y además, ésta fue similar en ambos brazos, aunque se observó mayor supervivencia en el brazo cribado. En ambos períodos hubo mayor número de casos diagnosticados en el brazo cribado y se apreció que el sobrediagnóstico permanecía en este brazo frente al del control. Según los autores de este estudio el sobrediagnóstico pudo ser consecuencia del escaso tiempo de seguimiento o porque los pacientes compartían perfiles o factores de riesgo. Al aumentar el tiempo de seguimiento, se realizaron más pruebas de radiografía de tórax y como consecuencia (a pesar de que esto solo incrementó el riesgo de cáncer de pulmón en un 5 %) se observó un aumento del número de casos de cáncer de pulmón. Otra posible explicación pudo ser el hecho de que los pacientes sometidos al programa de cribado eran más proclives a ser sometidos luego a una radiografía de tórax. A pesar de todo, en el caso del cáncer de pulmón es muy difícil eliminar el sobrediagnóstico debido a la corta supervivencia de los pacientes (76). En el año 2000, Melamed publicó un estudio con el objetivo de evaluar si la citología de esputo era una buena prueba de cribado de cáncer de pulmón. En este estudio se reclutaron 10.040 pacientes del área metropolitana de Nueva York durante 3 años y medio (hombres ≥ 45 años y fumadores de, al menos, 1 paquete/día). El programa de cribado consistió en realizar una radiografía de tórax anual en un brazo con 5.072 pacientes y, por otro lado, un cribado doble que podía consistir en una radiografía de tórax, citología Cribado de cáncer de pulmón 59 de esputo o una radiografía de tórax anual más citología de esputo cada 4 meses en 4.968 pacientes distribuidos de forma aleatoria en cada una de las opciones anteriores. El programa duró entre 5 y 8 años, dependiendo de la inclusión del paciente, y después se hizo un seguimiento durante 2 años más tras la finalización del programa de cribado. La participación se mantuvo elevada (99 %) durante todo el programa. Se detectaron prácticamente el mismo número de casos en el grupo cribado únicamente con radiografía de tórax que en el de cribado doble, sin embargo, en el grupo cribado únicamente con citología de esputo se detectaron muy pocos casos de cáncer de pulmón. También hubo detección de nuevos casos de cáncer de pulmón durante el período de seguimiento pero en menor proporción que durante el cribado. Se comprobó que la radiografía de tórax es más efectiva para adenocarcinomas periféricos, mientras que la citología de esputo detecta más carcinomas epidermoides en estadío temprano; por tanto ambas pruebas usadas de forma individual se complementan a la hora de detectar cáncer de pulmón. Se comparó la supervivencia a los 5 años de los pacientes del programa de cribado con la población no cribada, y se observó que era mayor en el grupo del cribado (35 % y 13 %, respectivamente). Finalmente, se observó que en una población de riesgo sometida a radiografía de tórax anualmente la citología de esputo no aumenta la supervivencia, pero sí el número de casos detectados en estadíos tempranos, aunque en ninguno de los grupos se redujo la mortalidad (77). A pesar de que es muy importante la seguridad en este tipo de programas de cribado ninguno de los estudios incluidos la ha evaluado. En la tabla 8 se puede ver un resumen de los estudios primarios analizados anteriormente. 4.4.2. Resultados para otras pruebas Uno de los objetivos de nuestro estudio era evaluar la posibilidad de realizar un cribado de cáncer de pulmón con pruebas diferentes a las de imagen o biológicas, como podría ser el uso de compuestos orgánicos volátiles (VOC), broncoscopia de autofluorescencia, proteómica, análisis de ADN o condensación del aire exhalado; sin embargo, no se han encontrado estudios que cumplan nuestros criterios de inclusión para estas pruebas. 60 INFORMES, ESTUDIOS E INVESTIGACIÓN Tabla 8. Resultados de los estudios primarios incluídos. Estudio Toyoda y cols., 2008 (74) Fujikawa y cols., 2008 (78) Blanchon y cols., 2007 (75) Marcus y cols., 2006 (76) Melamed y cols., 2000 (77) Población 18.070 pacientes (hombres y mujeres, fum actuales, exfum, no fum, edad: 40-80 años 26.025 pacientes 765 pacientes 9.211 pacientes (población (71 % (hombres, general, ≥40 años) hombres y fumadores) 29 % mujeres, asintomáticos, edad media: 56 años, fum habituales o ex fum desde hace menos de 15 años, consumo medio de ≥ 15 cigarrillos/día al menos durante 20 años) 10.040 hombres, ≥ 45 años, fum (≥ 1 paquete/día) Pruebas de cribado -LDCT: 4.689 pacientes (Test basal: 4.689, test post: 2.494) -LDCT: 3.305 con resultado negativo en la radiografía (Test basal: 2.550, test post: 755) -Radiografía de tórax: 5.072 pacientes -Radiografía de tórax: 13.381 pacientes (Test basal: 13.381, test post: 22.704) -Radiografía de tórax: 22.720 pacientes (Test basal: 2.670, test post: 20.050) Periodicidad de cribado Anual (19982002) Anual (durante 4 años) Anual (durante 2 años) Durante 6 años (no se especifica periodicidad) Durante 5-8 años (no se especifica periodicidad) Seguimiento No se especifica No se especifica No se especifica 1,5 años (participación del 99%) 2 años Casosb/ Nódulos detectados (%) LDCT : 0,85 % LDCT : 0,59 % Radiografía: 0,15 % LDCT: 87 % NCNa/ 2 % casos No se especifica Radiografía: 0,22 % Radiografía: 0,23 % casos (Test basal) No se especifica información de los nódulos Radiografía: 75 No se especifica información de los % NCN/ 0,26 % casos nódulos LDCT: 385 pacientes Radiografía: 380 pacientes -Brazo cribado: radiografía de tórax + citología de esputo cada 4 meses (3.725 pacientes) -Brazo control: recomendación de radiografía de tórax + citología de esputo anual (3.636 pacientes) -Radiografía de tórax + citología de esputo: 4.968 pacientes -Citología de esputo Radiografía+ citología: 0,30 % casos No se especifica información de los nódulos NOTA: % determinado del total de pacientes incluidos en el estudio cont. Cribado de cáncer de pulmón 61 Estudio Toyoda y cols., 2008 (74) Fujikawa y cols., 2008 (78) Casos/ Nódulos detectados (%) LDCT: 0,20 % LDCT : 0 % Radiografía: 0,04 % Radiografía: 0,03 % (Test post.) No se especifica información de los nódulos No se especifica información de los nódulos Estadío de los casos detectados No se especifica LDCT: Todos en estadíos iniciales Radiografía: 5/10 (50%) en estadío IA Blanchon y cols., 2007 (75) No se especifica LDCT: 3/8 (38 %) en estadíos iniciales y 5 (62 %) en estadíos tardíos Marcus y cols., 2006 (76) Radiografía + citología: 15 % casos Melamed y cols., 2000 (77) Radiografía: 0,60 % casos Radiografía: 14 % casos Radiografía+ citología: 0,14 % casos No se especifica información de los nódulos No se especifica información de los nódulos NOTA: datos totales del estudio tras el aumento del seguimiento NOTA: % determinado del total de pacientes incluidos en el estudio No se especifica 15 de 44 (33 %) casos en estadíos iniciales y 29 de 44 (67 %) en estadíos avanzados Radiografía: 1/1 (100%) en estadío inicial Prueba opcional Citología de esputo (en 3.539 de los sometidos a LDCT y en 5.417 de los sometidos a radiografía) No hay derivación a otras pruebas Toracotomía en No hay derivación 3 sospechas a otras pruebas de cáncer de pulmón (se confirman: 2 hamartomas y granuloma tuberculoide) No hay derivación a otras pruebas Supervivencia (a 5 años) No se evalúa Mayor en el brazo con LDCT (estadísticamente significativo) No se evalúa No se evalúa 35 % población cribada vs. al 13 % en población no cribada Mortalidad No se evalúa No se evalúa No se evalúa No hay diferencias en la mortalidad entre ambos brazos del estudio No se evalúa FP/FN 2 FN (1 con LDCT y 1 con radiografía) No se especifica No se especifica No se especifica No se especifica Sensibilidad / especificidad LDCT: 88,9 %/92,6 % No se especifica No se especifica No se especifica No se especifica Radiografía: 78,3 %/97,0 % NCN: nódulos no calcificados. Casos: casos de cáncer de pulmón. Resultados proporcionados en rango reflejándose el valor menor y el mayor en cada caso. a b 62 INFORMES, ESTUDIOS E INVESTIGACIÓN 4.5. Resultados de coste-efectividad A pesar de que no era nuestro objetivo analizar el coste-efectividad del cribado de cáncer de pulmón, se han analizado 4 estudios de coste-efectividad (uno de ellos es una revisión sistemática incluida en el apartado de resultados de revisiones sistemáticas que, además, incluye una evaluación de costeefectividad) (68, 80-82). En 2007 el American College of Chest Physicians publicó una revisión que incluye un análisis de coste-efectividad. En ella se incluyen 5 estudios que analizaron el coste‑efectividad del cribado con tomografía computarizada de baja resolución (LDCT). En la tabla 9 se muestran los resultados obtenidos. Dos de los estudios incluidos en esta revisión (80, 83) indicaron que el cribado es más coste-efectivo en poblaciones con alta incidencia de cáncer de pulmón (68). Cribado de cáncer de pulmón 63 Tabla 9. Coste-efectividad por año de vida ganado en un programa de cribado de cáncer de pulmón. Fuente de origen Población de estudio Mahadevia y cols., 2003 100.000 fum habituales, exfum. recientes y exfum, 60 años, > 20 PYa, 55% hombres Marshall y cols., 2001* 100.000 fum, 6074 años, media de PY=45, 45% hombres Chirikos y cols., 2002* Coste-efectividad por QALY b Coste del cribado con LDCTd, $ (diagnóstico con TC) 116.300 $ fum habituales Régimen de cribado 300 $ (429) Anual (durante 20 años) 50.473 $ 150 $ (280) Anual (durante 5 años) Características según prototipo en el tto de costes y esperanza de vida 46.513 $ 291 $ (340416) Anual (durante 5 años) Marshall y cols., 2001* 100.000 fum, 6074 años, media de PY=45, 45% hombres 15.274 $ 150 $ (no se especifica) Un único cribado Wisnivesky y cols., 2003* 1.000 participantes, ≥60 años, ≥10 PY 2.500 $ 165 $ (300) Un único cribado 558.600 $ exfum recientes 2.322.700 $ exfumc PY: paquetes/año Todas las estimaciones incluyen lead time bias de 1-1,5 años a excepción de los resultados de Chirikos. Costes estimados por QALY (años de vida ganados ajustados por calidad de vida). c Se considera que dejaron de fumar hace ≥ 5 años. d LDCT: tomografía computarizada de baja dosis. * No diferencian coste según el hábito tabáquico. Todos los estudios incluyen población de riesgo. $: $ americanos. Fuente: Bach y cols., 2007 (68). a b 64 INFORMES, ESTUDIOS E INVESTIGACIÓN Otra de las revisiones recuperadas fue publicada en 2005 con el fin de determinar si el cribado con tomografía computarizada (LDCT) para población de riesgo en Australia era o no coste-efectivo. Es un hipotético estudio de cohortes con pacientes (hombres) de riesgo (fumadores habituales) a los que se les realiza a un doble cribado: por un lado, tomografía computarizada durante 5 años a partir de los 60 años y tratamiento de los casos detectados, y, por otro lado, no cribado y tratamiento de los pacientes que presenten síntomas. Para los datos de sensibilidad y especificad se recogió la información procedente de seis estudios diferentes que también incluían población de alto riesgo y la mortalidad se analizó con base en otros estudios ya realizados. Los costes del cribado, empleando tomografía computarizada, se basaron en datos del Medicare Benefits Schedule del 2002. Para el tratamiento no se consideraron los costes de la primera visita médica y se realizó un descuento de un 3 % anual. Los costes están reflejados en la tabla 10 (81). Tabla 10. Costes totales del cribado. Grupo cribadoa (sin descuento del 3%) Costes de cribado Seguimiento de cribado anormal y costes de diagnóstico Costes de tratamiento Total AVGc Grupo controlb (sin descuento del 3%) 11.939.834 $ 0$ (12.607.292 $) (0 $) 4.031.230 $ 215.968 $ (4.121.128 $) (234.205 $) 4.159.595 $ 3.428.451 $ (4.405.535 $) (3.768.623 $) 20.130.658 $ 3.644.419 $ (21.133.955 $) (4.002.828 $) 104,121 103,834 Costes estimados en $ australianos para una cohorte de 10.000 hombres de 60-64 años y con una probabilidad de cáncer de pulmón de 0,0052. Se estimó un promedio de 1.649 $ por paciente. c AVG: años de vida ganados en un seguimiento a los 15 años tras el inicio del programa de cribado. Fuente: Manser y cols., 2005 (81). a,b Cribado de cáncer de pulmón 65 A continuación se resumen los resultados del coste-efectividad para hombres y mujeres (con la misma probabilidad anual de cáncer de pulmón) por años de vida ganados (AVG) y por QALY. Para hombres de 65-69 años el coste-efectividad fue de 68. 079 $ por AVG y de 137.798 $ por QALY. Para mujeres de 60-64 años el coste-efectividad fue de 51.001 $ por AVG y de 88.583 $ por QALY. En este estudio también se reflejaron los datos para hombres de 60-64 años con diferentes consumos de tabaco. Se observó que a mayor riesgo respecto al hábito tabáquico mayor coste-efectividad (81). En 2001 se publicó un estudio con el fin de evaluar el efecto potencial en la salud y el coste-efectividad de un programa de cribado de cáncer de pulmón con LDCT. Se hizo una comparación entre dos grupos (cribado con LDCT y no cribado) en una cohorte hipotética con 100.000 pacientes de 60-74 años con un 45 % de representación masculina. En el estudio se estimó un aumento de costes de 25 millones de dólares americanos (del grupo cribado frente al grupo de referencia) y de 150 $ para cada LDCT realizada. Finalmente, se estimó que en una cohorte de alto riesgo (incidencia 2,7 %) los costes por año de vida ganado (AVG) eran de 5.940 $ mientras que para una cohorte de bajo riesgo (incidencia 0,7 %) los costes eran de 23.100 $ por AVG. Con estos resultados se consideró que el cribado con LDCT en población de riesgo y ≥ 60 años es coste-efectivo. Se estimó que a mayor incidencia de cáncer de pulmón mayor coste-efectividad. Además, si se considera un lead-time bias de un año, el coste es aún mayor (15.274 $ para una cohorte de alto riesgo y 58.183 $ para una de bajo riesgo y 11.500 $ para la población cribada y 20.400 $ para el control) aunque éste se ve afectado por la especificidad calculada en un estudio observacional con un seguimiento de un año (80). En el año 2000, Caro y cols. realizaron un estudio para evaluar el costeefectividad de un programa de cribado con radiografía de tórax. En el estudio se incluyó información de 4 ensayos clínicos aleatorizados, de los cuales dos analizaban radiografía de tórax frente a radiografía de tórax combinada con citología de esputo; uno evaluó radiografía de tórax combinada con citología de esputo cada 4 meses frente al mismo cribado anual, y un último estudio evaluó radiografía de tórax con citología de esputo bianual frente a no cribado durante 3 años. La población hipotética de estudio incluyó 100.000 hombres fumadores de 45-80 años. El método empleado para el análisis de coste-efectividad fue el de Markov y se evaluó el beneficio del cribado en términos de años de vida ganados (AVG) y número de muertes evitadas. La mortalidad anual se analizó teniendo en cuenta la distribución de los estadíos. Se concluyó que había una reducción del 18 % de mortalidad en el grupo cribado, lo cual supone 2.700 (2,7 %) muertes menos, 38.290 AVG con un coste de 3.000 $ americanos por persona. Incluso si la reducción de la mor- 66 INFORMES, ESTUDIOS E INVESTIGACIÓN talidad era del 6 % se sigue manteniendo que el cribado es coste-efectivo. Según los autores de este estudio el programa de cribado será coste‑efectivo siempre que los costes sean inferiores a 1.800 $ (82). 4.6. Estudios en marcha Actualmente hay en marcha dos ensayos clínicos aleatorizados que intentan conocer en detalle los resultados del cribado de cáncer de pulmón con LDCT (84). El primero de ellos es el National Lung Screening Trial (NLST), llevado a cabo por el National Cancer Institute (EUA). Este estudio compara la efectividad de la LDCT frente a la radiografía de tórax en población de riesgo (50.000 pacientes, fumadores habituales o exfumadores, 55-74 años y sin historia previa de cáncer) para evaluar si el cribado de cáncer de pulmón con LDCT reduce al menos en un 20 % la mortalidad en el grupo cribado. Los pacientes fueron reclutados desde septiembre de 2002 hasta febrero de 2004 e incluidos en el brazo cribado con LDCT o en el brazo de comparación con radiografía de tórax. El programa de cribado consiste en realizar un test basal seguido de otros test anuales durante 2 años. Una vez acabado el programa de cribado, los pacientes son sometidos a un período de seguimiento de 8 años mediante la realización de cuestionarios u otras pruebas dependiendo del centro. Se espera que los resultados estén disponibles entre 2009-2010 (84). En la fig. 3 queda reflejado el esquema del estudio. Fig. 3. Esquema estudio NLST. Adaptado de Aberle y cols., 2008 (54). Cribado de cáncer de pulmón 67 El segundo estudio es el NELSON Trial, que se ha iniciado en 2003 en Holanda y Bélgica. En este caso el objetivo es comparar la tasa de mortalidad en población de riesgo al ser sometida a un programa de cribado en el que hay un brazo al que se le realiza LDCT y un brazo control que no recibe ningún tipo de cribado. Los participantes fueron reclutados hasta 2005 por medio de un cuestionario médico. Se incluyen un total de 19.000 pacientes (15.000 voluntarios de alto riesgo: fumadores habituales o exfumadores, 5075 años y 4.000 participantes reclutados de un estudio danés), aunque se siguen reclutando pacientes y se espera poder alcanzar entre 17.300 y 27.900 pacientes para poder observar reducción de la mortalidad (10 años después del reclutamiento). Este estudio es el único que incluye un brazo control sin ningún tipo de cribado (84). 4.7. Resultados de contextualización de la situación española A partir de los datos obtenidos de las diferentes fuentes de información consultadas, se pretende conocer la distribución del tabaquismo en las diferentes Comunidades Autónomas españolas y poder así estimar la población a cribar en cada una de ellas en el caso de que se hubiese demostrado beneficio con cualquier modalidad de cribado. 4.7.1. Tabaquismo en España En 2006, la proporción de fumadores diarios mayores de 16 años en España era de un 26,4 %, de los cuales el 42,3 % fumaba más de 20 cigarrillos/día; además, esta intensidad era más frecuente entre los 25 y 44 años (24). El 31,56 % de los hombres fumaban diariamente frente al 21,51 % de las mujeres. Respecto a los fumadores ocasionales la diferencia no era tan grande observándose un 3,77 % entre los hombres y un 2,37 % entre las mujeres. Los datos para los exfumadores también eran mayores para los hombres (28,14 %) que para las mujeres (13,20 %). Sin embargo, la proporción de mujeres que nunca ha fumado era superior a la de los hombres (62,92 % frente al 36,52 %, respectivamente) (24). Se puede observar cierta variabilidad en el tabaquismo en las diferentes Comunidades Autónomas. Así, por ejemplo, Cantabria es la comunidad con mayor número de fumadores habituales (31,3 %) y País Vasco la de menor (21,5 %). Respecto al número de cigarrillos fumados al día, Ceuta y Melilla son las comunidades que mayor porcentaje de fumadores de ≥ 20 cigarrillos/ día tienen (59,2 %), mientras que Navarra es la comunidad con menor por- 68 INFORMES, ESTUDIOS E INVESTIGACIÓN centaje (34,5 %). Si se considera el consumo actual, en Andalucía, el 26,9 % de la población fuma más que en años anteriores, mientras que este mismo dato para La Rioja es aproximadamente un 10 % menor (15,1 %). Para los dos primeros factores (hábito tabáquico y número de cigarrillos fumados al día), los valores son siempre mayores en hombres que en mujeres, mientras que para el consumo actual y el abandono del tabaco (respecto a un período anterior) los porcentajes son mayores entre las mujeres (24). 4.7.2. Modalidad de cribado Debemos partir del hecho de que en la actualidad no se recomienda ninguna prueba de cribado para el cáncer de pulmón, ni para población general ni para población de riesgo. Pero, en caso de que existiese una prueba eficaz, sería necesario considerar el ámbito geográfico del cribado, tipo de población a cribar y edad en la que habría que cribar para poder estimar un impacto cuando menos organizativo y de costes. • Cribado a población general o universal: No sería efectivo, ya que está suficientemente demostrado que el cáncer de pulmón está directamente relacionado con el tabaco, y éste es la principal causa de la enfermedad, ya que en torno al 85-90 % de todos los casos de cáncer de pulmón los produce el tabaquismo (responsable del 90 % de los casos entre los hombres y del 78 % entre las mujeres) (7). Sin embargo, solo entre un 10-15 % de los grandes fumadores llegan a desarrollar la enfermedad (12). No sería razonable un cribado de cáncer de pulmón en población general. • Cribado en población de riesgo: Debido a que el tabaco es el principal factor de riesgo de la enfermedad, lo más lógico sería realizar un cribado en fumadores, puesto que tienen alto riesgo de padecer cáncer de pulmón. En este apartado habría que hacer ciertas consideraciones: —— ¿Qué tipo de fumadores?: Según datos de la Encuesta Nacional de Salud, en el año 2006, el 26,4 % de la población ≥ 16 años fuma diariamente, el 3,1 % es fumador ocasional, el 20,5 % se declara como exfumador y el 50,0 % nunca ha fumado. Teniendo en cuenta el consumo diario en España, se observa que gran parte de los fumadores consumen más de 20 cigarrillos/día (dato algo menor en mujeres, que fuman 10‑19 cigarrillos/día) (24). Estudios recientes consideran que lo ideal, en caso de existir una prueba lo suficientemente efectiva, sería realizar un cribado a población Cribado de cáncer de pulmón 69 de alto riesgo (fumadores de, al menos, 20 paquetes/año) (8587). Estos fumadores son los que se incluyen en otros estudios publicados ya que es la considerada como población de alto riesgo para el cáncer de pulmón (fumadores actuales o exfumadores de 10‑20 paquetes/año) (68-77) por lo que sería la población objetivo para la realización de un programa de cribado. —— ¿A qué edad cribar?: en España, la edad media de muerte por cáncer de pulmón está en torno a los 67 años (8) además, más del 50 % de los casos de cáncer de pulmón son mayores de 70 años (6). Los casos detectados en ≤ 50 años son escasos, por lo que lo ideal sería realizar el programa de cribado a personas de entre 50 y 74 años. Además, es necesario tener un período de inducción para que aparezca la enfermedad, lo que refuerza un cribado en mayores de 50 años. En resumen, en caso de existir una buena prueba de cribado, habría que realizarla en fumadores de un paquete al día durante más de 20 años (20 paquetes/año) y tanto en hombres como en mujeres de entre 50 y 74 años. Este rango de edad es el que utilizan algunos de los estudios revisados. 4.7.3. Población susceptible de ser cribada a nivel nacional y por Comunidades Autónomas Para poder determinar cuánta población sería susceptible a ser cribada en España, es necesario evaluar la situación del tabaquismo en las diferentes comunidades, tanto para el total de la población como para hombres y mujeres por separado de 50 a 74 años. Según datos de la Encuesta Nacional de Salud para el año 2006, el 42,3 % del total de los fumadores fumaban más de 20 cigarrillos/día y este dato era, además, mayor en hombres que en mujeres (50,2 % y 31,6 %, respectivamente). En las tablas 11-14 se puede observar la situación del consumo de tabaco y de los fumadores de más de 20 cigarrillos/día por sexo y comunidad y por sexo y edad en España. Con la información reflejada en las tablas se podría conocer la carga potencial de cáncer de pulmón por Comunidades Autónomas (24). 70 INFORMES, ESTUDIOS E INVESTIGACIÓN Tabla 11. Fumadores diarios por sexo y Comunidad Autónoma. COMUNIDAD AMBOS SEXOS* HOMBRES* MUJERES* Andalucía 28,8 35,1 22,7 Aragón 26,3 29,8 22,9 Asturias 26,3 2 26,5 26,1 Baleares 27,0 33,7 20,3 Canarias 29,8 37,51 22,1 Cantabria 31,31 34,3 28,61 Castilla y León 23,5 29,5 17,7 Castilla La Mancha 27,0 34,1 19,8 Cataluña 23,7 29,0 18,6 Valencia 30,0 34,5 25,5 Extremadura 25,0 29,5 20,5 Galicia 22,4 29,6 15,82 Madrid 26,5 28,3 24,9 Murcia 30,0 36,3 23,3 Navarra 25,6 30,6 20,6 País Vasco 21,5 2 26,7 16,6 La Rioja 27,0 32,2 21,6 Ceuta y Melilla 26,7 35,8 17,9 Total 26,4 31,6 21,5 Porcentajes. Valor mayor. 2 Valor menor. * 1 Cribado de cáncer de pulmón 71 Tabla 12. Fumadores diarios de ≥ 20 cigarrillos/día por sexo y Comunidad Autónoma. COMUNIDAD AMBOS SEXOS* HOMBRES* MUJERES* Andalucía 39,5 46,5 29,2 Aragón 46,3 55,6 34,9 Asturias 43,5 57,3 31,2 Baleares 45,8 54,1 32,5 Canarias 48,3 56,0 35,4 Cantabria 43,2 52,9 32,9 Castilla y León 41,6 52,9 24,4 Castilla La Mancha 46,7 55,0 33,1 Cataluña 41,2 47,6 31,9 Valencia 43,5 50,6 34,5 Extremadura 39,0 44,9 31,1 Galicia 41,8 48,5 30,7 Madrid 43,2 52,6 33,5 Murcia 42,3 48,3 33,1 Navarra 34,52 44,22 21,52 País Vasco 40,7 49,6 28,2 La Rioja 37,2 45,6 25,8 Ceuta y Melilla 59,2 1 1 69,1 40,41 Total 42,3 50,2 31,6 Porcentajes. Valor mayor. 2 Valor menor. * 1 72 INFORMES, ESTUDIOS E INVESTIGACIÓN Tabla 13. Fumadores diarios por sexo y edad en España. EDAD AMBOS SEXOS* HOMBRES* MUJERES* 16-24 años 26,9 25,0 28,9 25-34 años 35,3 1 40,2 1 30,2 35-44 años 34,1 37,4 30,71 45-54 años 33,6 38,8 28,5 55-64 años 19,9 28,4 11,8 65-74 años 10,3 18,6 3,9 ≥ 75 años 4,5 2 8,9 1,42 Total 26,4 31,6 21,5 2 Porcentajes. Valor mayor. 2 Valor menor. * 1 Tabla 14. Fumadores diarios de ≥ 20 cigarrillos/día por sexo y edad en España. EDAD AMBOS SEXOS* HOMBRES* MUJERES* 16-24 años 25,7 2 36,0 16,32 25-34 años 37,3 41,9 30,9 35-44 años 46,8 55,1 36,4 45-54 años 51,61 63,81 35,9 55-64 años 51,6 1 58,5 37,61 65-74 años 39,7 41,1 35,0 ≥ 75 años 29,0 28,82 - Total 42,3 50,2 31,6 Porcentajes. Valor mayor. 2 Valor menor. * 1 Cribado de cáncer de pulmón 73 Se ha hecho una estimación del número de personas, en cada comunidad, que podrían ser candidatas a ser cribadas. Además, se ha hecho una estimación de la proporción de población en riesgo de cáncer de pulmón para poder ver la carga potencial de esta enfermedad en cada una de las Comunidades Autónomas (tablas 15-17). A continuación podemos ver un ejemplo de los cálculos realizados para obtener estos datos. En este caso, se hacen los cálculos para mujeres fumadoras de ≥ 20 cigarrillos/día de 50-74 años en Andalucía. Para el resto de comunidades y para hombres y ambos sexos se realizaron las mismas operaciones. Para calcular el % de población en riesgo: % fumadoras diarias (tabla 11) x % fumadoras de ≥ 20 cigarrillos/día (tabla 12) 0,227 x 0,292 = 0,0663, que corresponde a un 6,63 % Para calcular la población a cribar: % de población en riesgo x población total de 50-74 años 0,0663 x 999.617 = 66.275 personas Los resultados de estos cálculos se recogen en las siguientes tablas: 74 INFORMES, ESTUDIOS E INVESTIGACIÓN Tabla 15. Estimación de la población a cribar en mujeres. COMUNIDAD AUTÓNOMA POBLACIÓN DE 50-74 AÑOSa % POBLACIÓN EN RIESGOb POSIBLE POBLACIÓN A CRIBARc Andalucía 999.617 6,63 66.275 Aragón 178.487 7,99 14.261 Asturias 172.823 8,14 13.860 Baleares 128.892 6,60 8.507 Canarias 246.167 7,82 19.250 Cantabria 81.497 9,411 7.669 Castilla y León 360.609 4,322 15.578 Castilla La Mancha 239.375 6,55 15.679 Cataluña 956.242 5,93 56.705 Comunidad Valenciana 666.252 8,80 58.630 Extremadura 140.205 6,38 8.945 Galicia 426.557 4,85 20.688 Madrid 804.041 8,34 67.057 Murcia 159.181 7,71 12.269 Navarra 67.813 4,43 3.560 País Vasco 320.652 4,68 15.167 La Rioja 40.132 5,57 2.235 Ceuta y Melilla 15.023 7,23 1.086 6.015.709 6,79 408.467 Total * b 1 2 Personas. Porcentaje. Valor mayor. Valor menor. *Los datos totales pueden verse afectados debido al efecto del redondeo de las cifras. a,c Cribado de cáncer de pulmón 75 Tabla 16. Estimación de la población a cribar en hombres. COMUNIDAD AUTÓNOMA POBLACIÓN DE 50-74 AÑOSa % POBLACIÓN EN RIESGOb POSIBLE POBLACIÓN A CRIBARc Andalucía 934.152 16,32 152.454 Aragón 171.567 16,66 28.429 Asturias 156.176 15,18 23.708 Baleares 126.595 18,23 23.060 Canarias 240.420 21,00 50.584 Cantabria 76.687 18,14 13.911 Castilla y León 356.523 15,61 55.653 Castilla La Mancha 232.101 18,76 43.542 Cataluña 888.819 13,38 122.343 Comunidad Valencina 623.918 17,46 108.937 Extremadura 136.806 13,25 18.140 Galicia 390.073 14,36 56.014 Madrid 693.460 14,89 103.256 Murcia 149.508 17,53 26.209 Navarra 78.445 13,53 10.614 País Vasco 298.870 13,242 39.570 La Rioja 40.198 14,68 5.901 Ceuta y Melilla 15.385 24,74 3.806 5.608.903 15,86 889.572 Total 1 b 1 2 Personas. Porcentaje. Valor mayor. Valor menor. *Los datos totales pueden verse afectados debido al efecto del redondeo de las cifras. a,c 76 INFORMES, ESTUDIOS E INVESTIGACIÓN Tabla 17. Estimación de la población a cribar en ambos sexos. COMUNIDAD AUTÓNOMA POBLACIÓN DE 50-74 AÑOSa % POBLACIÓN EN RIESGOb POSIBLE POBLACIÓN A CRIBARc 1.933.769 11,38 220.063 Aragón 350.054 12,18 42.637 Asturias 32.899 11,44 3.764 Baleares 255.387 12,37 31.591 Canarias 486.587 14,39 70.020 Cantabria 97.164 13,52 13.137 Castilla y León 717.132 9,78 70.136 Castilla La Mancha 471.476 12,61 59.410 Cataluña 1.845.363 9,76 180.107 Comunidad Valenciana 1.290.173 13,05 168.3368 Extremadura 277.011 9,75 27.009 Galicia 816.630 9,36 76.4437 Madrid 1.497.498 11,45 171.464 Murcia 308.635 12,65 39.042 Navarra 158.454 9,14 14.483 País Vasco 618.522 8,752 54.121 La Rioja 80.332 10,04 8.065 Ceuta y Melilla 30.408 15,581 4.738 11.624.612 11,17 1.298.469 Andalucía Total b 1 2 Personas. Porcentaje. Valor mayor. Valor menor. *Los datos totales pueden verse afectados debido al efecto del redondeo de las cifras. a,c Cribado de cáncer de pulmón 77 Como se puede ver en los datos reflejados en las tablas 15-16, el porcentaje de población total en riesgo es más de dos veces mayor en los hombres (15,86 % para los hombres y 6,79 % para las mujeres) y en cifras absolutas representa 889.572 hombres y 408.467 mujeres. Al analizar los datos por Comunidades Autónomas se puede ver que entre las mujeres, Castilla y León es la comunidad que tiene menor proporción de población en riesgo (4,32 %), mientras que Cantabria es la que tiene mayor proporción (9,41 %). Para los hombres, la mayor proporción se localiza en Ceuta y Melilla (24,74 %) mientras que el País Vasco presenta la menor proporción (13,24 %) con un valor próximo al del total de la población (15,86 %). Si se consideran ambos sexos juntos, el País Vasco se mantiene con la menor proporción (8,75 %) mientras que Ceuta y Melilla tienen la mayor proporción (15,81 %). Los datos aquí presentados tienen múltiples limitaciones que se comentarán posteriormente. Sin embargo, cabe destacar que solo hay un 5 % de diferencia en las comunidades con mayor o menor porcentaje de mujeres en riesgo de cáncer de pulmón y un 10 % en los hombres. 78 INFORMES, ESTUDIOS E INVESTIGACIÓN 5. DISCUSIÓN 5.1. Discusión del método La discusión del método se ha estructurado en tres apartados: discusión de la búsqueda, discusión de los criterios de inclusión y exclusión y discusión de la contextualización. 5.1.1. Discusión de la búsqueda Se decidió realizar una búsqueda exhaustiva en lugar de una búsqueda específica porque se prefirió revisar información no válida (ruido) para evitar la omisión de artículos relevantes. La búsqueda se realizó en numerosas bases de datos empleando operadores booleanos que permitiesen obtener el mayor número de registros posible. Los términos utilizados fueron la combinación de “lung cancer” y “screening” fundamentalmente, con lo que es difícil que se haya perdido información relevante. 5.1.2. Discusión de los criterios de inclusión y exclusión Se establecieron una serie de requisitos que deberían cumplir los estudios para ser incluidos. Los límites temporales han variado en función de la prueba de cribado considerada. Así, para revisiones sistemáticas, se han incluido aquellas publicadas desde el 1 de enero de 2005 hasta la actualidad; para las diferentes pruebas de imagen, se han incluido estudios publicados desde el 1 de enero de 2004 y, por último, para otras pruebas (biológicas y de imagen diferentes a la tomografía computarizada), se han incluido estudios publicados desde el 1 de enero del 2000. Se ha realizado este tipo de selección porque muchos de los estudios publicados antes de 2004 están incluidos en revisiones posteriores y, por tanto, no aportaban ninguna información adicional. Para otras pruebas se ha marcado como fecha más antigua el 1 de enero de 2000, porque este tipo de estudios podrían no haber sido incluidos en revisiones sistemáticas posteriores en las que, sin embargo, sí se hubiesen considerado las pruebas de imagen. Estos criterios han conllevado la exclusión de algunos estudios de referencia, como el Memorial-Sloan Kettering Lung Project (MSKLP) (88), Johns Hopkins Lung Project (JHLP) (89), Anti-Lung Cancer Association (ALCA) (90) e Hitachi: Hitachi Employee’s Health Insurance Group (91) entre otros. Sin embargo, la evidencia que aportan se recoge en las revisiones posteriormente publicadas. Cribado de cáncer de pulmón 79 De acuerdo con el idioma, se incluyeron estudios en español, inglés, francés, portugués e italiano, debido a que son los idiomas de los que los autores pueden extraer datos. Únicamente se ha localizado un estudio en japonés, que no se ha incluido. Para el diseño del estudio y el tipo de publicación, se han incluido informes de evaluación de tecnologías sanitarias, revisiones sistemáticas, metanálisis, ensayos clínicos y estudios de cohortes. Se han excluido el resto de los estudios epidemiológicos, estudios primarios incluidos en las revisiones sistemáticas y publicaciones que ofrecen información subjetiva, como son editoriales, notas clínicas y cartas al editor. Se excluyeron, además, comunicaciones a congresos y estudios de un solo caso, ya que la información presente en estos dos últimos tipos de publicación no permite realizar una valoración adecuada de la metodología del estudio. Un criterio de exclusión que merece ser comentado es el hecho de excluir estudios sin grupo de comparación, lo que ha llevado a la exclusión de estudios como el International Early Lung Cancer Action Program (I-ELCAP), New York Early Lung Cancer Action Program (NY‑ELCAP) y Mayo Clinic (92). Este tipo de estudios no han sido considerados de nuestro interés, ya que, al no tener grupo de comparación, no nos aportarían buena información sobre la efectividad de la prueba de cribado empleada. Todos estos estudios, y sobre todo el ELCAP, han sido muy criticados precisamente por no disponer de grupo control (93). Respecto al tamaño de la muestra, se incluyeron estudios con más de 300 pacientes en cada brazo para programas de cribado universal o 100 pacientes en cada brazo para programas de cribado selectivo respectivamente. Se consideró que tamaños menores no aportarían la información adecuada para estudios de este tipo, debido al escaso número de casos de cáncer de pulmón esperados y a potenciales sesgos de selección al escoger a los participantes. De acuerdo con el objetivo del estudio, solamente se incluyeron estudios que evaluasen la eficacia y efectividad de las diferentes pruebas de cribado de cáncer de pulmón, y se excluyeron todos aquellos estudios con una finalidad diferente al cribado poblacional, como son los estudios de estadificación, de diagnóstico clínico o estudios piloto sobre nuevas pruebas diagnósticas. De acuerdo con el tipo de cribado, se excluyeron todos los estudios que realizasen un cribado universal o selectivo a poblaciones de riesgo diferentes a fumadores, como pueden ser exposiciones ocupacionales. 80 INFORMES, ESTUDIOS E INVESTIGACIÓN 5.1.3. Discusión de la contextualización Para el presente informe se ha considerado de interés realizar una contextualización a la situación española de un hipotético programa de cribado en el que se contemplase la existencia de una prueba efectiva para el cribado de cáncer de pulmón. Para ello se han hecho una serie de estimaciones para conocer la potencial carga de cáncer de pulmón en cada una de las Comunidades Autónomas de España. La primera asunción, como se ha mencionado, es hipotética, ya que no existe hoy por hoy ninguna prueba lo suficientemente efectiva para el cribado del cáncer de pulmón y, por tanto, partimos de una hipótesis falsa. Sin embargo, es relativamente previsible que en los próximos años surjan pruebas lo suficientemente sensibles y específicas para diagnosticar precozmente esta enfermedad, lo que daría lugar a la posibilidad de comenzar programas de cribado en población de riesgo. Está más que confirmado que el tabaquismo es el principal factor de riesgo del cáncer de pulmón. En los fumadores, también influye mucho el tiempo que dura este hábito o el número de cigarrillos/día. Se ha visto que a mayor tiempo desde el cese del hábito tabáquico menor será el riesgo aunque éste siempre será mayor que el de nunca fumadores (94). Si el cese se produce antes de los 35 años el riesgo puede llegar a ser casi igual que el de no fumadores. De aquí surge la segunda asunción que se corresponde al tipo de fumadores que se han considerado para ser incluidos en un programa de cribado. Se han considerado fumadores de ≥ 20 cigarrillos/día de entre 50 y 74 años. La literatura es clara en cuanto a que el cribado de cáncer de pulmón debe hacerse en fumadores; sin embargo, existen discrepancias en cuanto a la carga de consumo de tabaco necesaria para incluir a los sujetos en un programa de cribado. El dato más utilizado son los paquetes/año, una unidad que engloba tanto la intensidad como la duración del hábito, de modo que 20 paquetes/año son equivalentes a 20 años fumando un paquete al día. En España no se dispone de esta información a nivel estatal, por lo que se han considerado fumadores de ≥ 20 cigarrillos/día, pues se entiende que puede ser una buena aproximación a esa cifra de 20 paquetes/año. En general, los fumadores (sobre todo los hombres) tienden a fumar uno o más paquetes diarios (las mujeres algo menos) (24) y, si se incluyen aquellos ≥ 50 años, seguramente llevarán fumando más de 20 años (la edad de consolidación del tabaquismo se sitúa antes de los 20 años). Para las mujeres puede asumirse algo similar. Aquellas fumadoras de ≥ 50 años probablemente tendrán una cantidad acumulada de tabaco ≥ 20 paquetes/año. A pesar de estos datos, Cribado de cáncer de pulmón 81 este cribado hipotético (y muchos otros estudios sobre cribado de cáncer de pulmón (75)) deja fuera del cribado a los que fuman menor cantidad, que indudablemente tienen mucho mayor riesgo de cáncer pulmonar que los nunca fumadores, y también deja fuera a exfumadores. Respecto a los exfumadores, algunas investigaciones incluyen a exfumadores recientes en los sujetos a cribar, pero otras los excluyen (76). Puede concluirse a este respecto que el número total de sujetos considerados en riesgo respecto al tabaco y al cáncer de pulmón está infraestimado en nuestro hipotético cribado. Respecto a las edades consideradas para el cribado, es poco frecuente encontrar casos de cáncer pulmonar en menores de 50 años (aunque los hay) y también en mayores de 74 años (donde sí hay más casos que entre los menores de 50). En este último caso, sí que hay fenómenos de mortalidad o enfermedad competitiva (otros cánceres, enfermedades cardiovasculares), y también se especula con que aquellos fumadores mayores de cierta edad presenten cierto sesgo de supervivencia debido a su dotación genética, que les hace más “resistentes” al efecto del tabaco. Además, el beneficio ocasionado por el cribado no será igual a los 50 que a los 74 años. Todas estas razones han inducido a excluir sujetos mayores de 74 años (11). Una limitación importante de las estimaciones realizadas es que se ha asumido que todos los fumadores de ≥ 20 cigarrillos/día fuman esa cantidad independientemente de su edad. La única diferenciación es por Comunidad Autónoma de residencia y sexo. No hemos podido conseguir datos para cada Comunidad Autónoma que diferencien el consumo de tabaco por tramos de edad. Según la Encuesta Nacional de Salud, a medida que aumenta la edad disminuye el consumo de tabaco (8). Casi un 40 % de los hombres fumadores fuman ≥ 20 cigarrillos/día a los 50 años, porcentaje que se convierte en casi un 20 % para el tramo de edad de 65 a 74 años. Sin embargo, en las mujeres, el porcentaje de fumadoras diarias de ≥ 20 cigarrillos/día es el mismo a los 50 años que entre 65 y 74 años. Como la mayoría (por ahora) de los fumadores de esas edades son hombres, esto podría tener implicaciones en el número de personas a cribar, ya que previsiblemente se reducirían los hombres en los tramos de edad más elevados. En este sentido, el número de hombres a cribar podría estar sobreestimado en total en torno a un 5-10 %, aunque pensamos que este dato no afectaría de modo importante ni a las diferencias entre Comunidades Autónomas ni a las dificultades logísticas de un hipotético programa de cribado como se verá más adelante (sección de implicaciones organizativas). 82 INFORMES, ESTUDIOS E INVESTIGACIÓN 5.2. Discusión de los resultados de efectividad En primer lugar se comentan los hallazgos correspondientes al tipo de cribado (universal frente a selectivo); a continuación, aspectos referentes a las diferentes pruebas de cribado y, finalmente, las limitaciones de los estudios existentes. 5.2.1. Cribado universal frente a cribado selectivo Como se ha observado, en todos los estudios incluidos, a excepción del publicado por Fujikawa y cols. en 2008 (78), se realiza un cribado en población de riesgo, ya que esta enfermedad está directamente relacionada con el tabaco, por lo que un cribado en población general no sería efectivo ni deseable porque incrementaría aún más el número de falsos positivos y la exposición innecesaria de la población a radiaciones. 5.2.2. Cribado con pruebas de imagen combinadas o no con pruebas biológicas En este apartado se comentarán todos los estudios relacionados con el cribado de cáncer de pulmón con pruebas de imagen, tanto las revisiones sistemáticas como los estudios individuales. Los resultados comentados en este apartado puede verse en las tablas 7 y 8 (ver sección resultados) y en los anexos D y E. En cuanto a las revisiones sistemáticas, se puede observar que independientemente del tipo de prueba de cribado empleada, con ninguna hay reducción de la mortalidad, aunque sí mayor supervivencia y mayor detección de tumores en estadíos tempranos en el grupo cribado frente al grupo control. Ninguna de estas revisiones recomienda realizar un cribado de cáncer de pulmón, puesto que no hay evidencia suficiente para asegurar que este tipo de programas sean efectivos para esta enfermedad al no observarse en ningún caso menor mortalidad. Para poder valorar la mortalidad se necesitarían realizar ensayos clínicos aleatorizados y de mayor duración que los existentes, ya que el tiempo de seguimiento puede ser una de las causas por las que no se aprecia descenso de la mortalidad. En la actualidad hay dos estudios en marcha de los que se espera obtener resultados sobre si el programa de cribado reduce o no la mortalidad frente al grupo no cribado. Solo una de las revisiones considera que únicamente sería factible realizar un programa de cribado con tomografía computarizada en población de riesgo (69). Cribado de cáncer de pulmón 83 Excepto una revisión que evalúa radiografía de tórax combinada con citología de esputo frente a radiografía de tórax (72), el resto evalúan tomografía computarizada convencional o de baja dosis (LDCT) frente a radiografía de tórax. En todas ellas se detectan más casos de cáncer de pulmón y en estadíos más tempranos en el grupo cribado que en el control. Algún estudio ha indicado también que la exposición a la radiación puede aumentar la mortalidad en un 11 % (72, 95). En relación a los estudios primarios incluidos, se observó que todos ellos evalúan la efectividad de las diferentes pruebas de imagen y todos se centran en población de riesgo (fumadores y ≥ 40 años), por lo que en todos ellos, excepto en el estudio de Fujikawa, se hace un cribado selectivo. Todos incluyen un número de pacientes lo suficientemente grande como para poder obtener resultados sólidos y aunque en ninguno de ellos se puede observar reducción de la mortalidad debido al corto tiempo de seguimiento de los estudios, sí se apreció un aumento de la supervivencia (podría ser un lead-time bias). Sin embargo, el tipo de análisis en cada uno de los estudios es diferente, por lo que se discutirán de forma independiente. A pesar de que el número de estudios primarios publicados con pruebas biológicas es también abundante solo hemos podido incluir un estudio que evalúa citología de esputo ya que el resto de los estudios encontrados para esta prueba no cumplían nuestros criterios de inclusión. En este estudio, publicado en el 2000 por Melamed y cols., se concluyó que pruebas como citología de esputo adicionales a las pruebas de imagen (en este caso, radiografía de tórax) no aumentan la supervivencia ni reducen la mortalidad pero sí aumentan el número de casos de cáncer detectados en estadíos tempranos (77). Esto indica que son pruebas que por sí solas no serían capaces de detectar casos de cáncer de pulmón pero sí complementarían las pruebas de imagen. Por ello, hasta el momento, no se pueden considerar como pruebas de cribado individuales aunque sí como pruebas de apoyo en el diagnóstico de cáncer de pulmón. En el estudio publicado por Marcus y cols. se puede ver el efecto del tiempo de seguimiento del programa de cribado en el sobrediagnóstico, ya que al alargar este tiempo se realizan más pruebas y esto puede aumentar el riesgo de cáncer de pulmón. En esta enfermedad en particular es muy difícil eliminar el sobrediagnóstico, y además las propias pruebas de cribado pueden influir en el riesgo de su desarrollo. De todas formas, se observa que, independientemente del tiempo de seguimiento, la mortalidad es similar en ambos grupos (cribado y control), pero hay mayor supervivencia en el grupo cribado (76). En el estudio de Blanchon y cols. se observa mayor número de 84 INFORMES, ESTUDIOS E INVESTIGACIÓN tumores en estadíos tardíos en el cribado basal, a diferencia de lo que se ha obtenido en otros estudios publicados, y, además, se considera que, aunque la LDCT y la radiografía de tórax son buenas pruebas para el diagnóstico de cáncer de pulmón, sería buena la incorporación de nuevas pruebas alternativas y así evitar la realización de pruebas invasivas innecesarias (75). Esto se debe a que la historia natural del cáncer podría no ser como se creía en un principio (un cáncer agresivo y avanzado tiene un precursor indolente y tratable), sino que, según un estudio publicado recientemente por Bach, se consideraría que en realidad hay dos tipos de cánceres. Este modelo indica que hay unos cánceres de crecimiento lento y poco agresivos y otros de crecimiento rápido y agresivos, por lo que no se puede asegurar que el número de tumores en estadíos tempranos será equivalente al de tumores en estadíos tardíos en los tests sucesivos (Fig. 4) (96). Una de las revisiones incluidas hace referencia al tamaño del tumor y considera que no hay relación entre el estadío temprano y que el nódulo sea pequeño (68), lo que significa que podrían detectarse tumores avanzados pero de pequeño tamaño, un aspecto con importantes implicaciones en el cribado. Solo una de las revisiones incluidas (73) hace referencia a la necesidad de evaluar también las intervenciones en individuos sanos (falsos positivos), la exposición a la radiación o a la ansiedad que genera la espera de los resultados. Es muy importante considerar tanto la preocupación y la ansiedad debidas a los falsos positivos como el exceso de seguridad que puede haber en los falsos negativos (97). Hay discordancia respecto al tipo de seguimiento que se debe realizar en los nódulos sospechosos. Aquellos nódulos que no muestran cambio de tamaño o que desaparecen a los dos años son considerados como nódulos benignos, mientras que aquellos que muestran variaciones de tamaño son sospechosos de malignidad, por lo que deben ser sometidos a un seguimiento (42, 98). Unos autores consideran que éste debe ser a los 3, 6 y 12 meses de su detección mientras que otros consideran que nódulos de 5-10 mm deben ser sometidos a tomografía computarizada a los 3 meses. Si estos nódulos han cambiado de tamaño se deben realizar las pruebas diagnósticas adecuadas mientras que si no hay crecimiento se realizará una tomografía computarizada de nuevo al año. Además, cuando los nódulos son de más de 7 mm debe realizarse FDG-PET y en caso de cambio de tamaño se realiza PAAF o biopsia intraoperatoria mientras que en nódulos de ≥ 10 mm y sin crecimiento aparente se realiza una tomografía a los 3 meses de la detección (98, 99). Los datos de la literatura indican que un porcentaje importante de todos los casos de cáncer de pulmón se diagnostican ya en una fase avanzada Cribado de cáncer de pulmón 85 (más de un 50% tienen enfermedad regional o metastásica). El cribado debería de reducir este porcentaje en el momento del diagnóstico precoz, pues influye de modo decisivo en la supervivencia. Los estudios revisados no indican de modo evidente esa reducción en el porcentaje de casos detectados con enfermedad avanzada. A pesar de que con los resultados obtenidos parece ser más favorable un cribado con LDCT, hay que tener en cuenta que la resolución de esta prueba varía mucho dependiendo del radiólogo, es decir, existe una gran influencia de la variabilidad intra e interobservador y del umbral entre lesiones sospechosas y no sospechosas. Un estudio publicado recientemente evalúa la variabilidad interobservador y concluye que no es muy elevada, pero que podría mejorarse (100). Además, como se ha podido observar en los resultados, con la LDCT se obtienen más falsos positivos, que pueden causar también variabilidad dependiendo del observador, lo que no ocurriría con pruebas biológicas, ya que en éstas los resultados son aportados por la máquina y no hay posibilidad de variabilidad debido a la interpretación del observador. Se sabe que la sensibilidad de la LDCT es 4 veces mayor que la radiografía de tórax, pero genera más falsos positivos, emplea mayor radiación y es más cara (97). Fig. 4. Modelo de cáncer. Adaptado de Aberle y cols., 2008 (67). 86 INFORMES, ESTUDIOS E INVESTIGACIÓN El cáncer de pulmón cumple algunos de los requisitos para poder ser sometido a un programa de cribado pero, sin embargo, no hay evidencia suficiente para recomendar un cribado para esta enfermedad, al menos con las pruebas de imagen existentes hasta el momento. Un documento publicado por la American Cancer Society (ACS) en febrero de 2009 suscribe esta afirmación e indica que el cribado debería ser realizado exclusivamente en aquellos casos en los que personas con riesgo elevado deseasen someterse a CT con esta finalidad, pero siempre en una base individual y dialogada con su médico (101). Tampoco está clara la periodicidad del cribado. Los estudios realizados emplean diferentes periodicidades cuando se realiza LDCT (74-78). Hay que tener en cuenta también que cuanto más elevada sea la periodicidad mayor es la radiación que va a recibir un paciente cribado. En la tabla 18 se muestra un resumen de las recomendaciones de diferentes instituciones sobre el cribado de cáncer de pulmón. Puede observarse que hay un amplio consenso en que hoy por hoy no se recomienda el cribado selectivo del cáncer de plumón. Tabla 18. Resumen de recomendaciones de diferentes instituciones sobre el cribado de cáncer de pulmón con distintas pruebas. Institución Prueba National Cancer Institute1 Rayos X y citología National Cancer Institute1 de esputo LDCT Recomendación El cribado de cáncer de pulmón no reduce la mortalidad. Hay gran evidencia de que el cribado genera falsos positivos y aumenta la realización de pruebas de diagnóstico invasivas y tratamientos innecesarios No hay suficiente evidencia para asegurar que el cribado reduce la mortalidad por cáncer de pulmón. Hay gran evidencia de que el cribado genera falsos positivos y aumenta la realización de pruebas de diagnóstico invasivas y tratamientos innecesarios El cribado de cáncer de pulmón no es una práctica rutinaria ni en población ni en población de riesgo como es el caso de los fumadores American Cancer Society Rayos X y citología US Preventive Services Task Force2 Rayos X, citología de esputo y LDCT No hay suficiente evidencia ni a favor ni en contra del cribado de cáncer de pulmón en individuos asintomáticos con LDCT, rayos X, citología de esputo o con cualquier combinación de las mismas LDCT Actualmente, no hay suficiente evidencia para sugerir que el diagnóstico de cáncer de pulmón en estadios tempranos reduce la mortalidad por esta enfermedad. Hoy día no se puede recomendar un cribado de cáncer de pulmón con tomografía computarizada Canadian Coordination Office for Health Technology Assessment3 de esputo Cribado de cáncer de pulmón 87 Society of Thoracic Radiology LDCT Actualmente no se recomienda un cribado universal para cáncer de pulmón. Los pacientes que deseen participar deben ser motivados a participar en ensayos clínicos aleatorizados para que el valor del cribado con tomografía computarizada sea analizado con la mayor brevedad posible (http://www.cancer.gov/cancertopics/pdq/screening/lung/healthprofessional) (http://www.ahrq.gov/clinic/uspstf/uspslung.htm) 3 (http://www.cadth.ca/media/pdf/213_ct_cetap_e.pdf) Fuente: Bach y cols., 2007 (68). 1 2 5.2.3. Cribado con otras pruebas Como ya se ha comentado en el apartado de resultados, no se ha encontrado ningún estudio que cumpla nuestros criterios de inclusión y que evalúe pruebas diferentes a las citadas en apartados anteriores. Aberle y cols. publican en 2008 una revisión sistemática donde se evalúan otras pruebas de diagnóstico basadas en biomarcadores moleculares. En esta revisión se considera que estas pruebas no son muy sensibles si se emplean aisladamente pero combinadas con otras pruebas de imagen su sensibilidad es mayor y así evitar en determinadas ocasiones la realización de pruebas invasivas innecesarias (67). Se considera que las nuevas tecnologías como el análisis inmunocitoquímico del esputo con anticuerpos monoclonales (102), la identificación de mutaciones genéticas (103), la metilación anormal del ADN (104-106), las muestras anormales de inmunotinción u otros cambios moleculares (107109) pueden contribuir a la detección temprana del cáncer de pulmón y al cribado de la enfermedad. Hoy día se continúa investigando sobre posibles blancos en el esputo, fluidos bronquiales o aire exhalado que podrían también ayudar a detectar el cáncer de pulmón en estadíos tempranos (110, 111). Por el momento, cualquiera de esas pruebas está lejos de poder utilizarse en el cribado de cáncer de pulmón. 88 INFORMES, ESTUDIOS E INVESTIGACIÓN 5.2.4. Limitaciones de los estudios existentes En todo programa de cribado existen limitaciones y riesgos. Como se ha podido observar en este informe, en ninguno de los estudios incluidos se observa reducción de la mortalidad aunque sí un aumento de la supervivencia. Estos resultados podrían deberse al escaso tiempo de seguimiento de los estudios, ya que en la mayoría de ellos éste tiempo no es superior a 5 años. En todo caso, dado el escaso tiempo de supervivencia del cáncer de pulmón, en caso de que el cribado fuese efectivo debería observarse un descenso de la mortalidad en los casos detectados precozmente. Además, las características de los fumadores que se incluyen en los estudios individuales varían dependiendo del estudio. Todos los estudios, excepto uno, reclutan fumadores aunque hay diferencias en la cantidad de paquetes/año por lo que los resultados obtenidos pueden variar, encontrándose así mayor número de casos de cáncer de pulmón en estudios que incluyen pacientes que fuman mayores cantidades al año o tienen más consumo de tabaco acumulado a lo largo de la vida. También hay que considerar que ninguno de los estudios especifica cómo se manejan o siguen los pacientes con nódulos pulmonares detectados por el cribado. Esto es una limitación ya que los resultados de los distintos estudios no son comparables ni reproducibles. En un programa de cribado deben existir criterios claros de actuación y derivación ante la detección de un nódulo sospechoso de cáncer. Hay tres tipos de sesgos que pueden afectar a los estudios sobre cribado de cáncer de pulmón: • Lead-time bias (sesgo de adelanto de diagnóstico): la detección precoz con un programa de cribado es lo que hace que la supervivencia sea mayor (112). Debido a este sesgo aumenta la duración media de la enfermedad (mayor supervivencia). Los programas de cribado pretenden adelantar el momento de diagnóstico y retrasar el momento de la muerte (o conseguir la curación) alargando la supervivencia causada por este sesgo. Si la supervivencia no se alarga, lo que se espera entonces es que las condiciones de calidad de vida sean mejores (Fig. 5). Cribado de cáncer de pulmón 89 Fig. 5. Lead-time bias. Fuente: NCI (www.cancer.gov/NLST) (113). • Length bias (sesgo por duración de la enfermedad): consiste en la mayor detección de una enfermedad en etapas menos agresivas y con mejor supervivencia mientras que las etapas más agresivas son menos detectadas (112). En este caso el programa de cribado debería ser capaz de diagnosticar por igual todos los tipos de cánceres para así tratarlos adecuadamente y prolongar la supervivencia y la calidad de vida del paciente (Fig. 6). Fig. 6. Length bias. Fuente: NCI (www.cancer.gov/NLST) (113). 90 INFORMES, ESTUDIOS E INVESTIGACIÓN • Sobrediagnóstico: consiste en el diagnóstico de lesiones de pequeño tamaño y con crecimiento lento que podrían permanecer asintomáticas durante toda la vida del paciente si no hubiera sido detectado por el programa de cribado (112) (Fig. 7). Podemos distinguir dos tipos de sobrediagnóstico (114): —— Tipo I: detecta la enfermedad preclínica que no progresa o que está en regresión. —— Tipo II: detecta la enfermedad preclínica que progresa pero no lo suficientemente rápido para que se aprecien síntomas antes de que el paciente se muera. Es más prevalente en pacientes con tumores de crecimiento lento y corta expectativa de vida debido a la edad y la morbilidad. Fig. 7. Sobrediagnóstico. Fuente: NCI (www.cancer.gov/NLST) (113). Se ha comprobado que el sobrediagnóstico está presente en muchos estudios. El número de falsos positivos es mayor para la tomografía computarizada que para la radiografía de tórax y es mayor aún en el cribado basal que en los sucesivos tests (5-50 % vs. 3-12 %, respectivamente) (115). En el caso particular del cáncer de pulmón es muy difícil de eliminar este sesgo (76). Por ejemplo, la tasa de tuberculosis en España es muy superior al resto de los países desarrollados ya que ocupa el noveno puesto respecto a otros países europeos. Según datos de la SEPAR (Sociedad Española de Neumología y Cirugía Torácica) se diagnostican unos 13.000 nuevos casos anuales, lo que supone una incidencia de unos 30 casos nuevos anuales por 100.000 Cribado de cáncer de pulmón 91 habitantes (116). Esto implicaría que en áreas con alta prevalencia de la enfermedad habría más falsos positivos, obligando a realizar pruebas invasivas innecesarias. Se sabe que la mortalidad y morbilidad debidas a complicaciones por la realización de intervenciones quirúrgicas en pacientes con síntomas son 1,3-11,6 % y 8,8-44 %, respectivamente (97). Estos porcentajes son realmente elevados y añadirán riesgos a los falsos positivos. 5.3. Discusión de los resultados de seguridad No hay muchos estudios que evalúen la seguridad del cribado de cáncer de pulmón. Solo hemos podido encontrar una revisión sistemática que consideró que sería necesario evaluar también las intervenciones en individuos sanos, los riesgos de la exposición a la radiación o la ansiedad generada en el período de espera de los resultados de las pruebas (73). También hay que considerar que el hecho de realizar pruebas de cribado repetidamente puede aumentar el número de casos detectados, ya que al someter a los pacientes a radiación, ésta puede aumentar la incidencia de cáncer de pulmón. Esto indica que en el propio programa de cribado, tanto el test basal como los sucesivos, pueden influir en el número de casos detectados debido a que la radiación es capaz de generar alteraciones en el ADN que podrían favorecer el desarrollo de un cáncer. Este riesgo es parte de los programas de cribado e incluso podría tener un efecto sinérgico con el tabaco (117, 118). Estudios recientes describen un aumento de riesgo anual del 1,8 % (en población de riesgo sometida a tomografía de baja dosis durante 20-25 años) (119). Sin embargo, hay que tener en cuenta que la dosis de radiación es diferente dependiendo del tipo de prueba. Así, nos encontramos con valores de 0,06-0,25 mSv para radiografía de tórax y de 0,3-0,55 mSv para LDCT. Por otro lado, se sabe que la tomografía computarizada multicorte (TCMC) usa menor radiación que la tomografía computarizada convencional. La dosis de radiación de esta prueba es menor que la de la tomografía computarizada convencional incluso si la TCMC es empleada anualmente durante un período de 4 años (120). En cualquier caso, si se demostrase la eficacia de una prueba de cribado para el cáncer de pulmón, el potencial beneficio superaría los riesgos de cáncer debidos a la radiación. 92 INFORMES, ESTUDIOS E INVESTIGACIÓN 5.4. Discusión de los costes Es muy complicado obtener conclusiones generales debido a que cada estudio emplea diferentes unidades (años de vida ganados (AVG) o años de vida ganados ajustados por calidad de vida (QALY)) por lo que en nuestro análisis se han reflejado únicamente las conclusiones finales de los cuatro estudios analizados. Por otra parte, es difícil extrapolar los datos ya que la moneda es casi siempre dólares y no tiene el mismo valor actualmente que en el momento de realizar el estudio y además se han producido cambios en los costes de las pruebas. Lo ideal sería poder comparar un grupo cribado frente a otro sin cribar para analizar con mayor claridad el coste-efectividad de la prueba empleada. Sin embargo, esto solo ocurre en dos de los estudios incluidos (80, 81). Las estimaciones de los costes son también muy dispares; esto se debe al tiempo de seguimiento, ya que las variables y supuestos considerados son muy diferentes dependiendo del estudio (121). Solamente uno de los estudios incluidos de coste-efectividad considera que el cribado de cáncer de pulmón es coste-efectivo ya que se observa una hipotética reducción de la mortalidad en un 18 % en el grupo cribado. El coste para obtener este beneficio es de unos 3.000 $ americanos por persona (82). En el resto de los estudios se observó un aumento del coste en el grupo cribado por lo que se concluyó que estos programas solo se consideran coste-efectivos en poblaciones de alto riesgo de desarrollar cáncer de pulmón o si los costes de la LDCT se reducen notablemente. Uno de los estudios tiene en cuenta el lead-time bias y en este caso el coste es aún mayor (80) ya que con ello también se adelantará el tratamiento (67). Lo que se busca con estos programas de cribado no es solo aumentar la supervivencia sino también que la calidad de vida sea lo mejor posible, ya que no tendría sentido vivir más tiempo con mala calidad de vida. En el estudio de Marshall y cols. se considera que hay gran incertidumbre sobre los beneficios potenciales de la tomografía computarizada ya que un exceso de radiación puede ser perjudicial viéndose reducidos los efectos del cribado por la escasa calidad de vida. En este mismo estudio se considera que cuanta más alta es la incidencia más coste-efectivo será el cribado (80). En cualquier caso, mientras no se disponga de una prueba de cribado efectiva, no tiene mucho sentido analizar su coste-efectividad. Cribado de cáncer de pulmón 93 5.5. Discusión de los resultados de contextualización La cantidad de personas susceptibles de ser cribadas en España es muy elevada. Según las estimaciones realizadas, habría casi 1.300.000 españoles susceptibles de ser cribados en un programa de detección precoz del cáncer de pulmón. Las diferencias en cuanto al número de sujetos a cribar son grandes en números absolutos entre las diferentes Comunidades Autónomas, lo que es lógico ya que habrá más cantidad de fumadores en las Comunidades Autónomas de más población y menos en las de menos población. En términos relativos, las Comunidades Autónomas con mayor porcentaje de hombres y mujeres susceptibles de ser cribados son respectivamente Ceuta y Melilla (24,74%) y Cantabria (9,41%). Entre las diferentes Comunidades Autónomas no hay grandes diferencias en los porcentajes de población susceptible de ser cribada indicando por tanto que previsiblemente no habría un mayor beneficio de implantar un hipotético cribado en unas Comunidades Autónomas frente a otras. En cuanto a las cifras obtenidas, no dejan de ser una estimación más o menos válida, aunque tiene limitaciones. Una de ellas es que la información correspondiente al hábito tabáquico de las personas entre 50 y 74 años es una estimación, ya que no se ha podido obtener esta información desglosada por Comunidades Autónomas. El porcentaje de fumadores entre esas edades se ha estimado multiplicando el porcentaje de fumadores para todas las edades en cada Comunidad Autónoma por el porcentaje de sujetos que fuman más de 20 cig/día (también para todas las edades). Es previsible, y así lo indican los datos de intensidad del consumo de tabaco para toda España, que entre 50 y 74 años haya menos fumadores y de menos intensidad que si se considera a la población mayor de 18 años, por lo que el número de sujetos a cribar va a estar sobreestimado, posiblemente en torno a un 10%, si se tienen en cuenta los descensos en la intensidad del consumo por edad para toda la población española (ver tablas 13 y 14). Se ha indicado que aproximadamente un 15% de todos los grandes fumadores desarrollarán cáncer de pulmón (12). Se podría haber hecho este cálculo con los individuos susceptibles de cribado para estimar el número de casos que se podrían detectar en cada Comunidad Autónoma, pero se ha optado por no hacerlo ya que no serían unos datos muy robustos. 94 INFORMES, ESTUDIOS E INVESTIGACIÓN 5.5.1. Aspectos organizativos A pesar de que se ha indicado que el cribado del cáncer de pulmón con tomografía computarizada no ha demostrado mejorar la mortalidad por esta enfermedad, se ha considerado interesante hacer una estimación del número de pacientes anuales que podrían ser cribados con LDCT en un tomógrafo dedicado a tal efecto. Radiólogos consultados han indicado que durante una jornada podrían ser explorados unos 20 pacientes con una tomografía computarizada sin contraste con la finalidad de detectar nódulos pulmonares en un programa de cribado de cáncer de pulmón. Asumiendo un doble turno, esto supondría 40 pacientes diarios. Un año tiene 220 días laborables aproximadamente, por lo que durante un año podrían explorarse 220 * 40 = 8.800 pacientes. Este número de pacientes, a pesar de parecer grande, no lo es en términos relativos si se tiene en cuenta el número de pacientes en riesgo que presenta cada Comunidad Autónoma (ver sección de resultados de contextualización). Por poner un ejemplo, en Galicia existen unas 76.000 personas para cribar. Asumiendo un cribado bianual se cribarían con cada tomógrafo dedicado 17.600 personas. Esto implica que harían falta al menos 4,3 tomógrafos, o más bien 5, para realizar el cribado de cáncer de pulmón. A todo este coste de material, estructuras, personal dedicado, etc., habría que sumarle el coste adicional del manejo de falsos positivos que, asumiendo que solo fuese un 5 %, significarían un total de 1.900 falsos positivos anuales (38.000 personas cribadas en un año x 0.05), algo tremendamente difícil de manejar cuando se derivasen a los hospitales para hacerles las pruebas complementarias. Otro aspecto muy importante a tener en cuenta en un posible cribado del cáncer de pulmón sería cómo se localizan los fumadores de más de 20 cigarrillos/día entre 50 y 74 años. No hay ninguna base de datos que identifique a esas personas dentro de un marco poblacional. La única posibilidad sería a través de historias clínicas hospitalarias o de historias médicas de empresa. La localización de esos fumadores sería muy difícil y no todos ellos desearán participar en un programa de cribado de cáncer de pulmón. Este aspecto logístico también complicaría la realización de un programa de cribado, siendo además la participación elevada un elemento clave en el éxito de cualquier programa de cribado. A pesar de esto, el hecho de que les sea detectado un cáncer de pulmón disminuye la participación por el miedo de los propios pacientes. De todos los estudios incluidos solo uno recupera la información correspondiente al grado de participación durante el seguimiento, siendo ésta del 99 % (76). Cribado de cáncer de pulmón 95 Los costes económicos y organizativos del cribado de cáncer de pulmón indican que habría que ser muy cuidadoso a la hora de plantearlo. Incluso si se demostrase la efectividad de la LDCT sería necesario un estudio muy riguroso de coste/beneficio o de coste/utilidad para ver cuál sería el valor añadido del cribado de cáncer de pulmón. No debemos olvidar que quizá sería mucho más beneficioso para la población invertir el dinero del cribado (varios millones de euros) en la promoción del abandono del tabaco y evitar su inicio en los jóvenes. Además de evitar cáncer de pulmón se evitarían enfermedades respiratorias y cardiovasculares, que probablemente generarán un beneficio mucho mayor a las personas y al sistema sanitario que si se detecta precozmente cualquier enfermedad provocada por el tabaco. 5.6. Discusión de la periodicidad del cribado Para poder tratar correctamente un cáncer y realizar un programa de cribado adecuado, se debe considerar el tiempo de duplicación de un tumor. En los programas de cribado, se parte de la hipótesis de que los nódulos que crecen rápidamente son los que causan la enfermedad. Este tiempo puede ayudar a ver las diferencias entre la detección de un cáncer de pulmón con un programa de cribado y con la práctica clínica habitual. Este tipo de detección es útil para evaluar si los tumores detectados por LDCT tienen un comportamiento tan agresivo como los detectados esporádicamente (por lo general detectados en estadíos avanzados) (68). Según estudios publicados se producen 20 divisiones celulares hasta que el tumor tiene un tamaño de 1 mm, 22 divisiones hasta que es visible, 28 hasta que es claramente visible con LDCT y entre 35 y 40-41 divisiones para que sea clínicamente aparente y letal, alcanzando un tamaño de 100 mm (68). Para que se produzcan estas divisiones se requieren 40 días. Así, para que el tumor sea detectable por LDCT (22 divisiones) transcurrirán 880 días (2,4 años), para que sea clínicamente aparente (35 divisiones) transcurrirán 3,8 años y para las 40-41 divisiones transcurrirán 4,6 años (68). Este dato indicaría que la periodicidad del cribado adecuada sería de 2 años. 96 INFORMES, ESTUDIOS E INVESTIGACIÓN 6. CONCLUSIONES No existe una prueba de cribado de cáncer de pulmón que disminuya la mortalidad de los sujetos cribados ni aumente la proporción de curaciones, por lo que no se recomienda, en la actualidad, realizar un programa de cribado para el cáncer de pulmón. La modalidad de cribado más adecuada para el cáncer de pulmón sería el cribado selectivo en fumadores. Existe controversia acerca de las características que deberían reunir los fumadores para ser incluidos en un programa de cribado. De todas las pruebas disponibles, las de imagen son las más adecuadas en el momento actual para un hipotético cribado. De entre ellas, la LDCT es la que ofrece mayor sensibilidad y especificidad, aunque la gran mayoría de las lesiones detectadas en estudios de cribado mediante LDCT no son malignas, suponiendo un incremento en procedimientos diagnósticos y quirúrgicos innecesarios. Ni la radiografía de tórax ni otras pruebas biológicas tienen la suficiente validez para ser utilizadas como pruebas de cribado del cáncer de pulmón. Las pruebas de imagen suponen la exposición a radiación, por lo que podrían aumentar el riesgo de cáncer a largo plazo. Se debe ser cuidadoso cuando se realizan pruebas de imagen repetitivas y valorar adecuadamente si son realmente necesarias. Los estudios publicados sobre cribado de cáncer de pulmón presentan deficiencias metodológicas, y no puede descartarse la presencia de sesgos que afecten a los resultados. Cribado de cáncer de pulmón 97 7. RECOMENDACIONES La mejor manera de evitar el cáncer de pulmón es no fumar. Si no existiese el tabaquismo, no sería necesario plantearse un cribado para esta enfermedad. Sería seguramente más útil invertir los recursos de un programa de cribado de cáncer de pulmón en programas de prevención y abandono del tabaquismo bien diseñados. Para conocer la verdadera eficacia de las pruebas disponibles para el cribado de cáncer de pulmón son necesarios ensayos aleatorizados con grupo control, bien diseñados, con un seguimiento amplio y homogéneo y con puntos finales bien definidos. Los estudios NELSON y National Lung Screening Trial (NLST) ofrecerán una buena información para conocer la eficacia del cribado con tomografía computarizada de baja dosis (LDCT) en población belga y holandesa y estadounidense. Es necesario conocer con más detalle qué características de los fumadores serían las más adecuadas para incluirlos en un programa de cribado de cáncer de pulmón, tanto en lo que se refiere al número de cigarrillos diarios, a la duración del hábito como a los años de abstinencia en exfumadores. Para conocer la efectividad de un hipotético programa de cribado en España es necesaria la existencia de buenos datos sobre el consumo de tabaco de la población a nivel nacional, desglosados por Comunidades Autónomas, por intensidad de consumo de tabaco, por sexo y edad. Las fuentes de información existentes en la actualidad no han sido diseñadas específicamente con ese propósito. También sería muy útil disponer de información unificada de base poblacional sobre mortalidad e incidencia del cáncer de pulmón a nivel nacional y autonómico. Sería conveniente revisar este informe en 2011, cuando se disponga de nuevos datos sobre estudios publicados y también sobre la efectividad de las nuevas pruebas biológicas disponibles o de nuevas pruebas de imagen. Cribado de cáncer de pulmón 99 Bibliografía (1) Ferlay J, Autier P, Boniol M, Colombet M, Boyle P. Estimates of the cancer incidence and mortality in Europe in 2006. Ann Oncol. 2006;18(3):581-92. (2) Ries LAG, Melbert D, Krapcho M, Stinchcomb DG, Howlader N, Horner MJ, et al. SEER Cancer Statistics Review, 1975-2005 [Internet]. Bethesda (MD): National Cancer Institute; 2008 [citado nov 2008]. Disponible en: http://seer.cancer.gov/csr/1975_2005/ (3) Jemal A, Siegel R, Ward E, Murray T, Xu J, Thun MJ. Cancer statistics, 2007. CA Cancer J Clin. 2007;57(1):43-66. (4) Parkin DM, Bray F, Ferlay J, Pisani P. Global cancer statistics, 2002. CA Cancer J Clin. 2005;55(2):74-108. (5) López-Abente G, Pollán M, Aragonés N, Pérez Gómez B, Hernández Barrera V, Lope V, et al. Situación del cáncer en España: incidencia. An Sist Sanit Navar. 2004;27(2):165-73. (6) Sánchez De Cos Escuín J. El cáncer de pulmón en España. Epidemiología, supervivencia y tratamiento actuales. Arch Bronconeumol. 2009. [Epub ahead of print] (7) López-Abente G, Pollán M,Aragonés N, Pérez-Gómez B. Informe sobre la salud de los españoles. Cáncer. Información disponible a diciembre de 2003 [Internet]. Madrid: Centro Nacional de Epidemiología; 2003 [citado 12 mar 2008]. Disponible en: www.isciii.es/htdocs/pdf/saludcancer-2003.pdf. (8) Centro Nacional de Epidemiología (ISCIII). Servidores interactivos de información epidemiológica. Ariadna: Mortalidad por cáncer y otras causas [Internet]. Madrid: Centro Nacional de Epidemiología; [citado 25 jun 2008]. Disponible en: http://193.146.50.130/ariadna.php. (9) Sánchez-Hernández I, Izquierdo-Alonso JL, Almonacid-Sánchez C. Situación epidemiológica y pronóstica del cáncer de pulmón en nuestro medio. Arch Bronconeumol. 2006;42(11):594-9. (10) Brenner H, Francisci S, de Angelis R, Marcos-Gragera R, Verdecchia A, Gatta G, et al. Long-term survival expectations of cancer patients in Europe in 2000-2002. Eur J Cancer. 2009;45(6):1028-41. Cribado de cáncer de pulmón 101 (11) Ruano-Raviña A, Figueiras A, Barros-Dios JM. Lung cancer and related risk factors: an update of the literature. Public Health. 2003;117(3):149-56. (12) Ruano-Raviña A, Figueiras A, Loidi L, Barros-Dios JM. GSTM1 and GSTT1 polymorphisms, tobacco and risk of lung cancer: a case-control study from Galicia, Spain. Anticancer Res. 2003;23(5b):4333-7. (13) World Health Organization; International Agency for Research on Cancer. Tobacco Smoke and Involuntary Smoking [Internet]. Geneva: World Health Organization; 2002. IARC Monographs 83. [actualizada 22 jul 2002; citado 15 mar 2008] Disponible en: monographs.iarc.fr/ ENG/Monographs/vol83/volume83.pdf. (14) Doll R, Peto R, Wheatley K, Gray R, Sutherland I. Mortality in relation to smoking: 40 years’ observations on male British doctors. BMJ. 1994;309(6959):901-11. (15) Ruano-Raviña A, Figueiras A, Montes-Martínez A, Barros-Dios JM. Dose-response relationship between tobacco and lung cancer: new findings. Eur J Cancer Prev. 2003;12(4):257-63. (16) Hecht SS, Murphy SE, Carmella SG, Li S, Jensen J, Le C, et al. Similar uptake of lung carcinogens by smokers of regular, light, and ultralight cigarettes. Cancer Epidemiol Biomarkers Prev. 2005;14(3):693-8. (17) Ruano-Raviña A, Pérez-Ríos M, Barros-Dios JM. Tobacco-related cancers. En: Schwabb M, ed. Cancer Encyclopedia. Heidelberg: Springer-Verlag; 2009. (18) Sasco AJ, Secretan MB, Straif K. Tobacco smoking and cancer: a brief review of recent epidemiological evidence. Lung Cancer. 2004;45 Suppl 2:S3-9. (19) Finette BA, O’Neill JP, Vacek PM, Albertini RJ. Gene mutations with characteristic deletions in cord blood T lymphocytes associated with passive maternal exposure to tobacco smoke. Nat Med. 1998;4(10):114451. (20) ParsonsWD,Carmella SG,Akerkar S,Bonilla LE,Hecht SS.A metabolite of the tobacco-specific lung carcinogen 4-(methylnitrosamino)-1(3-pyridyl)-1-butanone in the urine of hospital workers exposed to 102 INFORMES, ESTUDIOS E INVESTIGACIÓN environmental tobacco smoke. Cancer Epidemiol Biomarkers Prev. 1998;7(3):257-60. (21) Anderson KE, Carmella SG, Ye M, Bliss RL, Le C, Murphy L, et al. Metabolites of a tobacco-specific lung carcinogen in nonsmoking women exposed to environmental tobacco smoke. J Natl Cancer Inst. 2001;93(5):378-81. (22) Hecht SS. Human urinary carcinogen metabolites: biomarkers for investigating tobacco and cancer. Carcinogenesis. 2002;23(6):907-22. (23) Bain C, Feskanich D, Speizer FE, Thun M, Hertzmark E, Rosner BA, et al. Lung cancer rates in men and women with comparable histories of smoking. J Natl Cancer Inst. 2004;96(11):826-34. (24) Instituto Nacional de Estadística (INE). Estilos de vida y prácticas preventivas. Cifras relativas: Consumo de tabaco [Base de datos en internet] Madrid: Instituto Nacional de Estadística (INE); 2006 [citado 25 jun 2008] Disponible en: http://www.ine.es/jaxi/menu. do?type=pcaxis&path=/t15/p419/a2006/p07/&file=pcaxis. (25) Darby S, Hill D, Auvinen A, Barros-Dios JM, Baysson H, Bochicchio F, et al. Radon in homes and risk of lung cancer: collaborative analysis of individual data from 13 European case-control studies. BMJ. 2005;330(7485):223. (26) Kogevinas M, Rodríguez Suárez MM, Tardón A, Serra C. Cáncer laboral en España. Barcelona: Institut Municipal d’Investigació Médica, Universitat Pompeu Fabra, Universidad de Oviedo; 2005. (27) Kleinerman R, Wang Z, Lubin J, Zhang S, Metayer C, Brenner A. Lung cancer and indoor air pollution in rural china. Ann Epidemiol. 2000;10(7):469. (28) Donaldson MS. Nutrition and cancer: a review of the evidence for an anti-cancer diet. Nutr J. 2004;3:19. (29) Ruano-Raviña A, Figueiras A, Barros-Dios JM. Type of wine and risk of lung cancer: a case-control study in Spain. Thorax. 2004;59(11):981-5. (30) Mao Y, Hu J, Ugnat AM, Semenciw R, Fincham S. Socioeconomic status and lung cancer risk in Canada. Int J Epidemiol. 2001;30(4):80917. Cribado de cáncer de pulmón 103 (31) Hussain SK, Lenner P, Sundquist J, Hemminki K. Influence of education level on cancer survival in Sweden. Ann Oncol. 2008;19(1):156-62. (32) Menvielle G, Boshuizen H, Kunst AE, Dalton SO, Vineis P, Bergmann MM, et al. The role of smoking and diet in explaining educational inequalities in lung cancer incidence. J Natl Cancer Inst. 2009;101(5):321-30. (33) Blot W, Fraumeni J. Cancers of the lung and pleura. En: Schottenfeld D y Fraumeni JF Jr e, ed. Cancer Epidemiology and Prevention. 2ª ed. New york: Oxford University Press; 1996. p. 637-65. (34) Donado, JR, Paz-Ares L. Coordinadores. Diagnóstico y tratamiento. Cáncer de pulmón [Internet]. Madrid: Fundación Médica Mutua Madrileña; 2007 [citado 20 mar 2009]. Disponible en: http://www. seom.org/seomcms/images/stories/recursos/sociosyprofs/colectivos/ grupocooperativo/2006/oncosur/guia_clinica_oncosur_cancerpulmon. pdf (35) Rami-Porta R, Crowley JJ, Goldstraw P. The revised TNM staging system for lung cancer. Ann Thorac Cardiovasc Surg. 2009;15(1):4-9. (36) Agència d´Avaluació de Tecnología i Recerca Médiques. Oncoguía de pulmón. OG02/2003 Noviembre 2003. [Base de datos en internet] Barcelona: Agència d´Avaluació de Tecnología i Recerca Médiques; 2003 [citado 10 mar 2009]. Disponible en: http://www.gencat.cat/salut/ depsan/pdf/og0302es.pdf (37) Gift AG, Stommel M, Jablonski A, Given W. A cluster of symptoms over time in patients with lung cancer. Nurs Res. 2003;52(6):393-400. (38) Schreiber G, McCrory DC. Performance characteristics of different modalities for diagnosis of suspected lung cancer: summary of published evidence. Chest. 2003;123(1 Suppl):115S-28S. (39) Ramí Porta R, Duque Medina J, Hernández Hernández J, López Encuentra A, Sánchez de Cos Escuín J. Diagnóstico y estadificación del carcinoma broncogénico. Barcelona: SEPAR; 2001 [citado 09 jun 2009]. Disponible en: http://www.separ.es/doc/publicaciones/ normativa/rec18.pdf 104 INFORMES, ESTUDIOS E INVESTIGACIÓN (40) Rivera MP, Mehta AC. Initial diagnosis of lung cancer: ACCP evidencebased clinical practice guidelines (2nd edition). Chest. 2007;132(3 Suppl):131S-48S. (41) Gould MK, Fletcher J, Lanettoni MD, Lynch WR, Midthun DE, Naidich DP, et al. Evaluation of patients with pulmonary nodules: when is it lung cancer? Chest. 2007;132(3 supl):108S-30S (42) MacMahon H, Austin JH, Gamsu G, Herold CJ, Jett JR, Naidich DP, et al. Guidelines for management of small pulmonary nodules detected on CT scans: A statement from the Fleischner Society. Radiology. 237(2):395-400. (43) Henschke CI, Yankelevitz DF, McCauley DI, Libby DM, Pasmantier MW, Smith JP. Guidelines for the use of spiral computed tomography in screening for lung cancer. Eur Respir J Suppl. 2003;39:45s-51s. (44) Prakash UB, Reiman HM. Comparison of needle biopsy with cytologic analysis for the evaluation of pleural effusion: analysis of 414 cases. Mayo Clin Proc. 1985;60(3):158-64. (45) Varela-Lema L, Fernández Villar A, Ruano-Raviña A. Effectiveness and safety of EBUS-TBNA: a systematic review. Eur Respir J. 2009;33(5):1156-64. (46) Salleras L, Domínguez A, Fores MD. Los métodos de la medicina clínica preventiva (III). Cribados. Med Clin (Barc). 1994;102 Suppl 1:26-34. (47) Cerdá Mota T. Programa de cribado: características y condiciones para su puesta en marcha. Medicine. 2003;8(118):6312-17. (48) Wilson JMG, Jungner G. Principles and practice of screening for disease. Genéve: World Health Organization; 1968. (49) Cerdá Mota T, Ascunce Elizaga N. Coordinadoras. Implantación y Evaluación de Programas Poblacionales de Cribado. Madrid; Sociedad Epañola de Epidemiología, 2006. (50) Muir Gray JA. Atención sanitaria basada en la evidencia. Madrid: Churchill Livingstone. 1997. Cribado de cáncer de pulmón 105 (51) Díaz-Rubio R. Coordinador. Estrategia en cáncer de pulmón del sistema nacional de salud [Internet]. Madrid. Ministerio de Sanidad y Consumo; 2006 [citado 20 mar 2009] Disponible en: http://www.gencat. cat/salut/depsalut/pdf/estratcancersns.pdf. (52) Ramírez Giraldo JC, Arboleda Clavijo C, McCollough CH. Tomografía computerizada por rayos X: fundamentos y actualidad. Biomedica. 2008;2(4):54-72. (53) Antona Rodríguez MJ. Tomografía axial computerizada de tórax: principales patrones radiológicos. Papel de la RNM en el estudio de la patología torácica. Neumosur. 2006;18(Supl 1):13-7. (54) Varela Lema M. Broncoscopia de autofluorescencia para el diagnóstico precoz de cáncer de pulmón en pacientes de riesgo [Internet]. Santiago de Compostela: Axencia de Avalicación de Tecnologías Sanitarias, Avalia-t; 2008 [citado 15 jun 2009] Informe Nº.: FT 2008/01. Disponible en: http://www.sergas.es/MostrarContidos_N3_T02. aspx?IdPaxina=60536&uri=http://www.sergas.es/gal/Servicios/docs/ AvaliacionTecnoloxias/FT2008_01%20broncoscopia%20de%20 autofluorescencia.pdf&hifr=1000&seccion=0 (55) Mazzone PJ, Hammel J, Dweik R, Na J, Czich C, Laskowski D, et al. Diagnosis of lung cancer by the analysis of exhaled breath with a colorimetric sensor array. Thorax. 2007;62(7):565-8. (56) Montuschi P, Barnes PJ. Analysis of exhaled breath condensate for monitoring airway inflammation. Trends Pharmacol Sci. 2002;23(5):232-7. (57) Dwyer TM. Sampling airway surface liquid: non-volatiles in the exhaled breath condensate. Lung. 2004;182(4):241-50. (58) Garey KW, Neuhauser MM, Robbins RA, Danziger LH, Rubinstein I. Markers of inflammation in exhaled breath condensate of young healthy smokers. Chest. 2004;125(1):22-6. (59) Carpagnano GE, Foschino-Barbaro MP, Resta O, Gramiccioni E, Carpagnano F. Endothelin-1 is increased in the breath condensate of patients with non-small-cell lung cancer. Oncology. 2004;66(3):180-4. (60) Kharitonov SA, Barnes PJ. Exhaled markers of pulmonary disease. Am J Respir Crit Care Med. 2001;163(7):1693-722. 106 INFORMES, ESTUDIOS E INVESTIGACIÓN (61) Horvath I, Hunt J, Barnes PJ, Alving K, Antczak A, Baraldi E, et al. Exhaled breath condensate: methodological recommendations and unresolved questions. Eur Respir J. 2005;26(3):523-48. (62) Machado RF, Laskowski D, Deffenderfer O, Burch T, Zheng S, Mazzone PJ, et al. Detection of lung cancer by sensor array analyses of exhaled breath. Am J Respir Crit Care Med. 2005;171(11):1286-91. (63) Petricoin EF, Liotta LA. Clinical applications of proteomics. J Nutr. 2003;133(7 Suppl):2476S-84S. (64) Rahman SM, Shyr Y, Yildiz PB, Gonzalez AL, Li H, Zhang X, et al. Proteomic patterns of preinvasive bronchial lesions. Am J Respir Crit Care Med. 2005;172(12):1556-62. (65) Recomendación del consejo de 2 de diciembre de 2003 sobre el cribado del cáncer. L327/2003 de 2 de diciembre de 2003. Diario Oficial de la Unión Europea, nº 878, (2 de diciembre de 2003). (66) Black WC. Computed tomography screening for lung cancer: review of screening principles and update on current status. Cancer. 2007;110(11):2370-84. (67) Aberle DR, Brown K. Lung cancer screening with CT. Clin Chest Med. 2008;29(1):1-14, v. (68) Bach PB, Silvestri GA, Hanger M, Jett JR. Screening for lung cancer: ACCP evidence-based clinical practice guidelines (2nd edition). Chest. 2007;132(3 Suppl):69S-77S. (69) Yau G, Lock M, Rodrigues G. Systematic review of baseline low-dose CT lung cancer screening. Lung cancer. 2007;58(2):161-70. (70) Black C, de Verteuil R, Walker S, Ayres J, Boland A, Bagust A, et al. Population screening for lung cancer using computed tomography, is there evidence of clinical effectiveness? A systematic review of the literature. Thorax. 2007;62(2):131-8. (71) Hunt I, Siva M, Southon R, Treasure T. Does lung cancer screening with low-dose computerised tomography (LDCT) improve diseasefree survival? Interact Cardiovasc Thorac Surg. 2006;5(5):612-5. Cribado de cáncer de pulmón 107 (72) Hunt I, Siva M, Southon R, Treasure T. Does lung cancer screening with chest X-ray improve disease-free survival? Interact Cardiovasc Thorac Surg. 2006;5(4):483-7. (73) Vidal Serrano S. Cribado de cáncer de pulmón con TC de tórax: revisión sistemática. Med Clin (Barc). 2007;15(129):582-7. (74) Toyoda Y, Nakayama T, Kusunoki Y, Iso H, Suzuki T. Sensitivity and specificity of lung cancer screening using chest low-dose computed tomography. Br J Cancer. 2008;98(10):1602-7. (75) Blanchon T, Brechot JM, Grenier PA, Ferretti GR, Lemarie E, Milleron B, et al. Baseline results of the Depiscan study: a French randomized pilot trial of lung cancer screening comparing low dose CT scan (LDCT) and chest X-ray (CXR). Lung Cancer. 2007;58(1):50-8. (76) Marcus PM, Bergstralh EJ, Zweig MH, Harris A, Offord KP, Fontana RS. Extended lung cancer incidence follow-up in the Mayo Lung Project and overdiagnosis. J Natl Cancer Inst. 2006;98(11):748-56. (77) Melamed MR. Lung cancer screening results in the National Cancer Institute New York study. Cancer. 2000;89(11 Suppl):2356-62. (78) Fujikawa A, Takiguchi Y, Mizuno S, Uruma T, Suzuki K, Nagao K, et al. Lung cancer screening - Comparison of computed tomography and X-ray. Lung Cancer. 2008;61(2):195-201. (79) Harbour R, Miller J, for the Scottish Intercollegiate Guidelines Network Grading Review Group. A new system for grading recommendations in evidence based guidelines. BMJ. 2001;323(7308):334-6. (80) Marshall D, Simpson KN, Earle CC, Chu C. Potential cost-effectiveness of one-time screening for lung cancer (LC) in a high risk cohort. Lung Cancer. 2001;32(3):227-36. (81) Manser R, Dalton A, Carter R, Byrnes G, Elwood M, Campbell DA. Cost-effectiveness analysis of screening for lung cancer with low dose spiral CT (computed tomography) in the Australian setting. Lung Cancer. 2005;48(2):171-85. (82) Caro JJ, Klittich WS, Strauss G. Could chest X-ray screening for lung cancer be cost-effective? Cancer. 2000;89(11 Suppl):2502-5. 108 INFORMES, ESTUDIOS E INVESTIGACIÓN (83) Wisnivesky JP, Mushlin AI, Sicherman N, Henschke C. The costeffectiveness of low-dose CT screening for lung cancer: preliminary results of baseline screening. Chest. 2003;124(2):614-21. (84) Brawner EJ, Patrick Nana-Sinkam S, Jett JR. Lung cancer screening in 2008: A review and update. Respiratory Medicine CME. 2008;1(1):2-9. (85) Bellomi M, Rampinelli C, Funicelli L, Veronesi G. Screening for lung cancer. Cancer Imaging. 2006;6:S9-12. (86) Coche E. Screening for lung cancer with low-dose CT. JBR-BTR. 2008;91(1):1-5. (87) Ravenel JG, Costello P, Silvestri GA. Screening for lung cancer. AJR Am J Roentgenol. 2008;190(3):755-61. (88) Melamed MR, Flehinger BJ, Zaman MB, Heelan RT, Perchick WA, Martini N. Screening for early lung cancer. Results of the Memorial Sloan-Kettering study in New York. Chest. 1984;86(1):44-53. (89) Frost JK, Ball WC, Jr., Levin ML, Tockman MS, Baker RR, Carter D, et al. Early lung cancer detection: results of the initial (prevalence) radiologic and cytologic screening in the Johns Hopkins study. Am Rev Respir Dis. 1984;130(4):549-54. (90) Sobue T, Moriyama N, Kaneko M, Kusumoto M, Kobayashi T, Tsuchiya R, et al. Screening for lung cancer with low-dose helical computed tomography: anti-lung cancer association project. J Clin Oncol. 2002;20(4):911-20. (91) Nawa T, Nakagawa T, Kusano S, Kawasaki Y, Sugawara Y, Nakata H. Lung cancer screening using low-dose spiral CT: results of baseline and 1-year follow-up studies. Chest. 2002;122(1):15-20. (92) Fontana RS, Sanderson DR, Woolner LB, Taylor WF, Miller WE, Muhm JR. Lung cancer screening: the Mayo program. J Occup Med. 1986;28(8):746-50. (93) Twombly R. Lung cancer screening debate continues despite international CT study results. J Natl Cancer Inst. 2007;99(3):190-5. Cribado de cáncer de pulmón 109 (94) Godtfredsen N, Prescott E, Osler M. Effect of Smoking Reduction on Lung Cancer Risk. JAMA. 2005;294(12):1505-10. (95) Waldman MJ, Neher JO, Harper A, Huber TE. Clinical inquiries. Does screening reduce lung cancer mortality? J Fam Pract. 2008;57(1):49-50. (96) Bach PB. Is our natural-history model of lung cancer wrong? Lancet Oncol. 2008;9(7):693-7. (97) U.S. Prevention Services Task Force. Lung cancer screening: recommendation statement. Ann Intern Med. 2004;140(9):738-9. (98) Benjamin MS, Drucker EA, McLoud TC, Shepard JA. Small pulmonary nodules: detection at chest CT and outcome. Radiology. 2003;226(2):489-93. (99) Bastarrika G, Garcia-Velloso MJ, Lozano MD, Montes U, Torre W, Spiteri N, et al. Early lung cancer detection using spiral computed tomography and positron emission tomography. Am J Respir Crit Care Med. 2005;171(12):1378-83. (100)Gierada DS, Pilgram TK, Ford M, Fagerstrom RM, Church TR, Nath H, et al. Lung cancer: Interobserver agreement on interpretation of pulmonary findings at low-dose CT screening. Radiology. 2008;246(1):265-72. (101)Smith R, Cokkinides V, Brawley O. Cancer screening in the United States, 2009: a review of current American Cancer Society guidelines and issues in cancer screening. CA Cancer J Clin. 2009;59(1):27-41. (102)Tockman MS, Gupta PK, Myers JD, Frost JK, Baylin SB, Gold EB, et al. Sensitive and specific monoclonal antibody recognition of human lung cancer antigen on preserved sputum cells: a new approach to early lung cancer detection. J Clin Oncol. 1988;6(11):1685-93. (103)Mao L, Hruban RH, Boyle JO, Tockman M, Sidransky D. Detection of oncogene mutations in sputum precedes diagnosis of lung cancer. Cancer Res. 1994;54(7):1634-7. (104)Palmisano WA, Divine KK, Saccomanno G, Gilliland FD, Baylin SB, Herman JG, et al. Predicting lung cancer by detecting aberrant promoter methylation in sputum. Cancer Res. 2000;60(21):5954-8. 110 INFORMES, ESTUDIOS E INVESTIGACIÓN (105)Tsou JA, Hagen JA, Carpenter CL, Laird-Offringa IA. DNA methylation analysis: a powerful new tool for lung cancer diagnosis. Oncogene. 2002;21(35):5450-61. (106)Anglim PP, Alonzo TA, Laird-Offringa IA. DNA methylation-based biomarkers for early detection of non-small cell lung cancer: an update. Mol cancer. 2008;7:81. (107)Gazdar AF, Minna JD. Molecular detection of early lung cancer. J Natl Cancer Inst. 1999;91(4):299-301. (108)Fong KM, Sekido Y, Minna JD. Molecular pathogenesis of lung cancer. J Thorac Cardiovasc Surg. 1999;118(6):1136-52. (109)Tockman MS, Mulshine JL. Sputum screening by quantitative microscopy: a new dawn for detection of lung cancer? Mayo Clin Proc. 1997;72(8):788-90. (110)Phillips M, Gleeson K, Hughes J, Greenberg J, Cataneo RN, Baker L, et al. Volatile organic compounds in breath as markers of lung cancer: a cross-sectional study. Lancet. 1999;353(9168):1897-8. (111)Baryshnikova E, Destro A, Infante MV, Cavuto S, Cariboni U, Alloisio M, et al. Molecular alterations in spontaneous sputum of cancer-free heavy smokers: results from a large screening program. Clin Cancer Res. 2008;14(6):1913-9. (112)Black C, Bagust A, Boland A, Walker S, McLeod C, De Verteuil R, et al. The clinical effectiveness and cost-effectiveness of computed tomography screening for lung cancer: systematic reviews. Health Technol Assess. 2006;10(3):iii-iv, ix-x, 1-90. (113)National Cancer Institute (NCI). What is NLST? [Internet]. Bethesda (MD): National Cancer Institute; 2008 [citado 2 jul 2008]; Disponible en: www.cancer.gov/NLST. (114)Black WC. Randomized clinical trials for cancer screening: Rationale and design considerations for imaging tests. Am J Clin Oncol. 2006;24(20):3252-60. (115)Humphrey LL, Teutsch S, Johnson M. Lung cancer screening with sputum cytologic examination, chest radiography, and computed Cribado de cáncer de pulmón 111 tomography: an update for the U.S. Preventive Services Task Force. Ann Intern Med. 2004;140(9):740-53. (116)World Health Organization. Global tuberculosis control: surveillance, planning, financing [Internet]. Geneva: World Health Organization; 2007 [citado 17 jun 2009] WHO Report 2007. WHO/HTM/TB/ 2007.376. Disponible en: http://www.who.int/tb/publications/global_ report/2007/en/index.html. (117)Tokarskaya ZB, Scott BR, Zhuntova GV, Okladnikova ND, Belyaeva ZD, Khokhryakov VF, et al. Interaction of radiation and smoking in lung cancer induction among workers at the Mayak nuclear enterprise. Health Phys. 2002;83(6):833-46. (118)Neugut AI, Murray T, Santos J, Amols H, Hayes MK, Flannery JT, et al. Increased risk of lung cancer after breast cancer radiation therapy in cigarette smokers. Cancer. 1994;73(6):1615-20. (119)Brenner DJ. Radiation risks potentially associated with lowdose CT screening of adult smokers for lung cancer. Radiology. 2004;231(2):440-5. (120)Mascalchi M, Belli G, Zappa M, Picozzi G, Falchini M, Della Nave R, et al. Risk-benefit analysis of X-ray exposure associated with lung cancer screening in the Italung-CT trial. AJR Am J Roentgenol. 2006;187(2):421-9. (121)Mahadevia PJ, Fleisher LA, Frick KD, Eng J, Goodman SN, Powe NR. Lung cancer screening with helical computed tomography in older adult smokers: a decision and cost-effectiveness analysis. JAMA. 2003;289(3):313-22. 112 INFORMES, ESTUDIOS E INVESTIGACIÓN ANEXOS ANEXO A Estrategia de búsqueda La revisión bibliográfica se ha realizado en febrero-marzo de 2008 y para ello se ha llevado a cabo una estrategia de búsqueda en las bases de datos que se mencionan a continuación. Además, se han realizado actualizaciones periódicamente. La última actualización se realizó en enero de 2009. 1. BASES DE DATOS ESPECIALIZADAS EN REVISIONES SISTEMÁTICAS Cochrane Library Plus y base de datos del NHS Centre for Reviews and Dissemination. En esta última se incluyen las bases de datos HTA (Health Technology Assessment) —que contiene informes de evaluación—, DARE —que contienen revisiones de efectividad— y la NHSEED —con documentos de evaluación económica—. Cochrane Library Plus: #1. MASS SCREENING término simple (MeSH) #2. LUNG NEOPLASMS término simple (MeSH) #3. #1 AND #2 #4. (lung and neoplasm*) OR (lung and cancer) #5. screen*: ti OR screen*:ab #6. #4 AND #5 #7. #3 OR #6 #8. mam*: ti OR mam*:ab OR prostat*:ti OR melanom*:ti #9. #7 NOT #8 Límites: 2003-actualidad CRD Databases (HTA, DARE): #1 lung AND cancer # 2 lung AND neoplasm* # 3 #1 OR #2 # 4 screen*: ti # 5 early:ti AND diagnos*:ti Cribado de cáncer de pulmón 115 # 6 early:ti AND detect*:ti # 7 #4 OR #5 OR #6 # 8 #3 AND #7 #9 MeSH Lung Neoplasms EXPLODE 1 #10 MeSH Mass Screening EXPLODE 1 2 3 4 5 6 7 #11 #9 AND #10 #12 #8 OR #11 RESTRICT YR 2000-2008 AHRQ: #1. “lung cancer” NEAR screening” 2. BASES DE DATOS ESPECÍFICAS DE GPC Tripdatabase: #1. lung OR pulmon #2. (cancer or neoplas* or tumor* or tumour* or carcino*):ti #3. (screen* or “early diagnos*” or “early detect*”):ti #4. #1 AND #2 AND #3 3. BASES DE DATOS GENERALES MEDLINE (PUBMED): #1. “Lung Neoplasms”[Mesh] #2. “Neoplasms”[Mesh] OR neoplas*[TIAB] OR cancer*[TIAB] OR disease*[TIAB] OR malignan*[TIAB] OR tumor*[TIAB] OR tumour*[TIAB] OR carcino*[TIAB] OR adenocarcin*[TIAB] #3. “Lung”[Mesh] #4. #2 AND #3 #5. #1 OR #4 #6. “Mass Screening”[Mesh] OR “Early Diagnosis”[Mesh] #7. #5 AND #6 Limits: 2000 to 2008, English, French, Italian, Spanish, Portuguese Exclusión de artículos de opinión #8. ((“Lung Neoplasms”[Mesh] OR ((“Neoplasms”[Mesh] OR neoplas*[TIAB] OR cancer*[TIAB] OR disease*[TIAB] OR malignan*[TIAB] OR tumor*[TIAB] OR tumour*[TIAB] OR carcino*[TIAB] OR adenocarcin*[TIAB]) AND “Lung”[Mesh])) 116 INFORMES, ESTUDIOS E INVESTIGACIÓN AND (“Mass Screening”[Mesh] OR “Early Diagnosis”[Mesh])) AND systematic[sb] Limits: Publication Date from 2003 to 2008, English, French, Italian, Spanish, Portuguese #9. #7 OR #8 EMBASE (OVID): #1. Lung Cancer/ #2. LUNG/ #3. Neoplasm/ #4. (neoplas* or cancer* or tumo?r* or carcino* or adenocarcino* or malignan* or disease*).ab,ti. #5. #3 or #4 #6. #2 and #5 #7. #1 or #6 #8. Mass Screening/ #9. Early Diagnosis/ #10. #8 or #9 #11. #6 and #10 #12. meta analysis/ or outcomes research/ or randomized controlled trial/ or practice guideline/ #13. #11 and #12 Límite: 2000-actualidad #14. “systematic review”/ #15. #11 and #14 Límite: 2003-actualidad #16. #13 OR #15 ISI Web of Knowledge: #1. Topic= (LUNGTUMORS OR LUNGTUMOURS OR LUNGCANCER OR LUNGCANCERS OR LUNGNODULES OR LUNGSCANCER OR LUNGADENOCARCINOMA OR LUNGCARCINOMAS OR LUNGCARCINOMO OR LUNGDISEASE OR LUNGDISEASES) #2. Title= (lung or pulmon) #3. Title= (neoplas* or cancer* or tum?r* or carcino* or adenocarcino*) #4. #2 AND #3 #5. #1 OR #4 #6. Topic= (SCREENING OR MASSSCREENING OR EARLYDIAGNOSIS) #7. #5 AND #6 #8. Topic=LUNGCANCERSCREENING #9. #7 OR #8 Cribado de cáncer de pulmón 117 Limits: English, Spanish, French, Portuguese, Italian 1995Exclusión de artículos de opinión IME: #1. Campos básicos= ‘’diagnostico precoz’’, Descriptores=’’cancer de pulmón’’ #2. Campos básicos= ‘’cribado’’, Campos básicos=’’cancer de pulmón’’ Límites: 1995- 4. PÁGINAS ESPECIALIZADAS National Cancer Institute: Búsqueda manual a través del índice. National Cancer Institute (Canadá): #1. “early detection” “lung cancer” #2. screening “lung cancer” 118 INFORMES, ESTUDIOS E INVESTIGACIÓN ANEXO B Estudios incluidos • Bach PB, Silvestri GA, Hanger M, Jett JR. Screening for lung cancer: ACCP evidence-based clinical practice guidelines (2nd edition). Chest. 2007;132(3 Suppl):69‑77. • Yau G, Lock M, Rodrigues G. Systematic review of baseline low-dose CT lung cancer screening. Lung Cancer. 2007;58(2):161-70. • Black C, De Verteuil R, Walker S, Ayres J, Boland A, Bagust A, et al. Population screening for lung cancer using computed tomography, is there evidence of clinical effectiveness? A systematic review of the literature. Thorax. 2007;62(2): 131-8. • Vidal Serrano S, Mendez AL. Cribado de cancer de pulmon con TC de torax: revision sistemática. Med Clin (Barc.) 2007;129(15):582-7. • Hunt I, Siva M, Southon R, Treasure T. Does lung cancer screening with low-dose computerised tomography (LDCT) improve diseasefree survival? Interact CardioVasc Thorac Surg. 2006;5(5):612-5. • Hunt I, Siva M, Southon R, Treasure T. Does lung cancer screening with chest X-ray improve disease-free survival? Interact CardioVasc Thorac Surg. 2006;5(4):483-7. • Toyoda Y, Nakayama T, Kusunoki Y, Iso H, Suzuki T. Sensitivity and specificity of lung cancer screening using chest low-dose computed tomography. Br J Cancer. 2008;98(10):1602-7. • Fujikawa A, Takiguchi Y, Mizuno S, Uruma T, Suzuki K, Nagao K, et al. Lung cancer screening - Comparison of computed tomography and X-ray. Lung Cancer. 2008;61(2):195-201. • Blanchon T, Brechot JM, Grenier PA, Ferretti GR, Lemarie E, Milleron B, et al. Baseline results of the Depiscan study: a French randomized pilot trial of lung cancer screening comparing low dose CT scan (LDCT) and chest X-ray (CXR). Lung Cancer. 2007;58(1):50-8. Cribado de cáncer de pulmón 119 • Marcus PM, Bergstralh EJ, Zweig MH, Harris A, Offord KP, Fontana RS. Extended lung cancer incidence follow-up in the Mayo Lung Project and overdiagnosis. J Natl Cancer Inst. 2006;98(11):748-56. • Melamed MR. Lung cancer screening results in the National Cancer Institute New York study. Cancer. 2000;89(11 Suppl):2356-62. 120 INFORMES, ESTUDIOS E INVESTIGACIÓN ANEXO C Estudios excluidos Cita Causa de exclusión Adelaide Health Technology Assessment. Screening for lung cancer utilising computed tomography. Update: February 2008. [monografía en internet]. Adelaide: Adelaide Health Technology Assessment; 2008 [citado 3 mar 2008]. Disponible en http:// www.horizonscanning.gov.au. Diseño del estudio Waldman MJ, Neher JO, Harper A, Huber TE. Clinical inquiries. Does screening reduce lung cancer mortality? J Fam Pract. 2008;57(1):49-50 Tipo de estudio (comentario) Manser RL, Irving LB, Stone C, Byrnes G, Abramson M, Campbell D. Cribaje (screening) para el cáncer de pulmón (Revisión Cochrane traducida) [Base de datos en internet]. Oxford: Update Software Ltd; 2003 [actualizado 21 nov 2003; citado 17 jun 2009]. Disponible en: http://212.169.42.7/ newgenClibPlus/pdf/CD001991.pdf Actualizado por última vez en 2003 Conrad DH, Goyette J, Thomas PS. Proteomics as a method for early detection of cancer: a review of proteomics, exhaled breath condensate, and lung cancer screening. J Gen Intern Med. 2008;23 (Suppl 1):78-84 Tipo de estudio (revisión narrativa) Spiro SG. Ensuring the right PET scan for the right patient. Lung Cancer. 2008;59(1):48-56 No es objeto de estudio Gómez M. Lung cancer screening. Am J Med Sci. 2008;335(1):46-50 Tipo de estudio (revisión narrativa) Bach PB. Lung cancer screening. J Natl Compr Canc Netw. 2008;6(3):271-5 Tipo de estudio (revisión narrativa) Smith JJ, Berg CD. Lung cancer screening: promise and pitfalls. Semin Oncol Nurs. 2008;24(1):9-15 Tipo de estudio (revisión narrativa) Coche E. Screening for lung cancer with low-dose CT. JRBBTR. 2008;91(1):1-5 Tipo de estudio (revisión narrativa) Bach P. Is our natural-history model of lung cancer wrong? Lancet Oncol. 2008;9(7):693-7 No es objeto de estudio Bach PB. Lung cancer screening. J Natl Compr Canc Netw. 2008;6(3):271-5 Tipo de estudio (revisión narrativa) Ravenel JG, Costello P, Silvestri GA. Screening for lung cancer. Am J Roentgenol. 2008;190(3):755-61 Tipo de estudio (revisión narrativa) Twombly R. Lung cancer screening trial financed by tobaccofunded foundation, sparks debate. J Natl Cancer Inst. 2008;100(10):690-1 Tipo de estudio (editorial) Cribado de cáncer de pulmón 121 Cita Causa de exclusión Aberle DR, Brown K. Lung cancer screening with CT. Clin Chest Med. 2008;29(1):1-14 No especifica las bases de datos de recogida de los estudios Henschke CI. CT screening for lung cancer: Update 2007. Oncologist. 2008;13(1):65-78 No tiene control Ferretti G, Jankowski A, Calizzano A, Moro-Sibilot D, Vuillez J. Imagerie radiologique et TEP Scanner dans les cancers du poumon. J Radiol. 2008;89(3 Pt 2):387-400 No es objeto de estudio Tipo de estudio (carta el editor) Tipo de estudio (revisión narrativa) Baryshnikova E, Destro A, Infante MV, Cavuto S, Cariboni U, Alloisio M, et al. Molecular alterations in spontaneous sputum of cancer-free heavy smokers: Results from a large screening program. Clin Cancer Res. 2008;14(6):1913-9 No tiene control Spiro SG. Ensuring the right PET scan for the right patient. Lung Cancer. 2008; 59(1):48-56 No es objeto de estudio Brower, V. Biomarker studies abound for early detection of lung cancer. J Natl Cancer Inst. 2009;101(1):11-3. Tipo de estudio (editorial) Anglim PP, Alonzo TA, Laird-Offringa IA. DNA methylationbased biomarkers for early detection of non-small cell lung cancer: an update. Mol Cancer. 2008;7:81 Tipo de estudio (revisión narrativa) Dubey, S. Powell CA. Update in lung cancer 2007. Am J Respir Crit Care Med. 2008;177(9):941-6 Tipo de estudio (revisión narrativa) Sone S, Nakayama T, Honda T, Tsushima K, Li F, Haniuda M, et al. CT findings of early-stage small cell lung cancer in a lowdose CT screening programme. Lung Cancer. 2007;56(2):20715. No tiene control Tamaño muestral (N=5) Black WC. Computed tomography screening for lung cancer: review of screening principles and update on current status. Cancer. 2007;110(11):2370-84 Revisión sistemática (no especifica las bases de datos de recogida de los estudios) William CB. Computed tomographic screening for lung cancer: individualising the benefit of the screening. Eur Respir J. 2007;30(5):843-7. No tiene control Welch HG, Woloshin S, Schwartz LM, Gordis L, Gotzsche PC, Harris R, et al. Overstating the evidence for lung cancer screening: the International Early Lung Cancer Action Program (I-ELCAP) study. Arch Intern Med. 2007;167(21):2289-95 No tiene control Bach PB, Jett JR, Pastorino U, Tockman MS, Swensen SJ, Begg CB. Computed tomography screening and lung cancer outcomes. JAMA. 2007;297(9):953-61. Erratum in: JAMA. 2007;298(5):518 No tiene control Taylor KL, Cox LS, Zincke N, Mehta L, McGuire C, Gelmann E. Lung cancer screening as a teachable moment for smoking cessation. Lung Cancer. 2007;56(1):125-34 No es objeto de estudio 122 INFORMES, ESTUDIOS E INVESTIGACIÓN Cita Causa de exclusión Silvestri GA, Nietert PJ, Zoller J, Carter C, Bradford D. Attitudes towards screening for lung cancer among smokers and their non-smoking counterparts. Thorax. 2007;62(2):126-30 No es objeto de estudio Miser WF. Cancer screening in the primary care setting: the role of the primary care physician in screening for breast, cervical, colorectal, lung, ovarian, and prostate cancers. Prim Care. 2007;34(1):137-67 No es objeto de estudio (no es cribado de cáncer de pulmón específicamente) Kloecker GH, Studts JL, Laber DA, Bousamra M. Lung cancer in the US and in Kentucky. J Ky Med Assoc. 2007;105(4):15964 No es objeto de estudio Clark KW, Gierada DS, Moore SM, Maffitt DR, Koppel P, Phillips SR, et al. Creation of a CT Image Library for the Lung Screening Study of the National Lung Screening Trial. J Digit Imaging. 2007;20(1):23-31 No es objeto de estudio Yankelevitz DF. Screening for a cancer: acting on social responsibility. Am J Roentgenol. 2007;188(5):1171-2 Tipo de estudio (comentario) Simon BM. Lung cancer diagnosis in primary care. Nurse Pract. 2007;32(1):43-9 No es objeto de estudio Lee P, Sutedja TG. Lung cancer screening: has there been any progress? Computed tomography and autofluorescence bronchoscopy. Curr Opin Pulm Med. 2007;13(4):243-8 Tipo de estudio (revisión narrativa) Mazzone PJ, Hammel J, Dweik R, Na J, Czich C, Laskowski D, et al. Diagnosis of lung cancer by the analysis of exhaled breath with a colorimetric sensor array. Thorax. 2007;62(7):565-8 Tipo de estudio (caso control) New York Early Lung Cancer Action Project Investigators. CT Screening for lung cancer: diagnoses resulting from the New York Early Lung Cancer Action Project. Radiology. 2007;243(1):239-49 No tiene control Callol L, Roig F, Cuevas A, de Granda JI, Villegas F, Jareno J, et al. Low-dose CT: a useful and accessible tool for the early diagnosis of lung cancer in selected populations. Lung Cancer. 2007;56(2):217-21 No tiene control Jin SM, Choi SH, Yoo CG, Kim YW, Han SK, Shim YS, et al. Small solid noncalcified pulmonary nodules detected by screening chest computed tomography. Respir Med. 2007;101(9):1880-4 No tiene control Roberts HC, Patsios D, Paul NS, McGregor M, Weisbrod G, Chung T, et al. Lung cancer screening with low-dose computed tomography: Canadian experience. Can Assoc Radiol J. 2007;58(4):225-35 No tiene control Twombly R. Lung cancer screening debate continues despite international CT study results. J Natl Cancer Inst. 2007;99(3):190-5 Tipo de estudio (editorial) Cribado de cáncer de pulmón 123 Cita Causa de exclusión Paci E. Observational, one-arm studies and randomized population-based trials for evaluation of the efficacy of lung cancer screening. J Thorac Oncol. 2007;2(5 Suppl):S45-6 Tipo de estudio (suplemento) Smith RA, Cokkinides V, Brawley OW. Cancer screening in the United States, 2008: A review of current American Cancer Society guidelines and cancer screening issues. CA Cancer J Clin. 2008;58(3):161-79 No es objeto de estudio (cáncer en general) van de Wiel JC, Wang Y, Xu DM, van der Zaag-Loonen HJ, van der Jagt EJ, van Klaveren RJ, et al. Neglectable benefit of searching for incidental findings in the Dutch-Belgian lung cancer screening trial (NELSON) using low-dose multidetector CT. Eur Radiol. 2007;17(6):1474-82 No es objeto de estudio Carter D, Vázquez M, Flieder DB, Brambilla E, Gazdar A, Noguchi M, et al. Comparison of pathologic findings of baseline and annual repeat cancers diagnosed on CT screening. Lung Cancer. 2007;56(2):193-9 No tiene control Hampton T. New screening techniques show potential for early detection of lung cancer. JAMA. 2007;298(17):1997 Tipo de estudio (revisión narrativa) No es objeto de estudio van Iersel CA, de Koning HJ, Draisma G, Mali WP, Scholten ET, Nackaerts K, et al. Risk-based selection from the general population in a screening trial: selection criteria, recruitment and power for the Dutch-Belgian randomised lung cancer multi-slice CT screening trial (NELSON). Int J Cancer. 2007;120(4):868-74 No es objeto de estudio Cassidy A, Duffy SW, Myles JP, Liloglou T, Field JK. Lung cancer risk prediction: a tool for early detection. Int J Cancer. 2007;120(1):1-6 No es objeto de estudio Pinsky PF, Miller A, Kramer BS, Church T, Reding D, Prorok P, et al. Evidence of a healthy volunteer effect in the prostate, lung, colorectal, and ovarian cancer screening trial. Am J Epidemiol. 2007;165(8):874-81 No es objeto de estudio Kemp RA, Reinders DM, Turic B. Detection of lung cancer by automated sputum cytometry. J Thorac Oncol. 2007;2(11):9931000 Población de estudio (población con posibilidad de riesgo de cáncer de pulmón) Xu DM, Gietema H, de Koning H, Vernhout R, Nackaerts K, Prokop M, et al. Nodule management protocol of the NELSON randomised lung cancer screening trial. Lung Cancer. 2006;54(2):177-84 No es objeto de estudio Smith RA. Cancer screening in the USA. J Med Screen. 2006;13 (Suppl 1):S48-53 Shaipanich T, McWilliams A, Lam S. Early detection and chemoprevention of lung cancer. Respirology. 2006;11(4):36672 124 Tipo de estudio (suplemento) No es objeto de estudio Tipo de estudio (revisión narrativa) INFORMES, ESTUDIOS E INVESTIGACIÓN Cita Causa de exclusión Petersen RP, Harpole DH. Computed tomography screening for the early detection of lung cancer. J Natl Compr Canc Netw. 2006;4(6):591-4 Tipo de estudio (revisión narrativa) Read C, Janes S, George J, Spiro S. Early lung cancer: screening and detection. Prim Care Respir J. 2006;15(6):332-6 Tipo de estudio (revisión narrativa) Horng MS. Annual CT screening for lung cancer may significantly improve survival. N Engl J Med. 2006;355:1763-71 No tiene control Henschke CI, Yankelevitz DF, Miettinen OS. Computed tomographic screening for lung cancer: the relationship of disease stage to tumor size. Arch Intern Med. 2006;166(3):321-5 No tiene control McWilliams AM, Mayo JR, Ahn MI, MacDonald SL, Lam SC. Lung cancer screening using multi-slice thin-section computed tomography and autofluorescence bronchoscopy. J Thorac Oncol. 2006;1(1):61-8 No tiene control Pinsky PF, Freedman M, Kvale P, Oken M, Caporaso N, Gohagan J. Abnormalities on chest radiograph reported in subjects in a cancer screening trial. Chest. 2006;130(3):688-93 No tiene control MacRedmond R, McVey G, Lee M, Costello RW, Kenny D, Foley C, et al. Screening for lung cancer using low dose CT scanning: results of 2 year follow up. Thorax. 2006;61(1):54-6 No tiene control No es objeto de estudio Incluido en revisiones posteriores Shaham D, Breuer R, Copel L, Agid R, Makori A, Kisselgoff D, et al. Computed tomography screening for lung cancer: applicability of an international protocol in a single-institution environment. Clin Lung Cancer. 2006;7(4):262-7 No es objeto de estudio Smith RA, Cokkinides V, Eyre HJ. American Cancer Society guidelines for the early detection of cancer. CA Cancer J Clin. 2006;56(1):11-25 No es objeto de estudio Black WC. Randomized clinical trials for cancer screening: Rationale and design considerations for imaging tests. J Clin Oncol. 2006;24(20):3252-60 Mascalchi M, Belli G, Zappa M, Picozzi G, Falchini M, Della Nave R, et al. Risk-benefit analysis of X-ray exposure associated with lung cancer screening in the Italung-CT trial. Am J Roentgenol. 2006;187(2):421-9 No es objeto de estudio Tipo de estudio (revisión narrativa) No es objeto de estudio Black C, Bagust A, Boland A, Walker S, McLeod C, De Verteuil R, et al. The clinical effectiveness and cost-effectiveness of computed tomography screening for lung cancer: systematic reviews. Health Technol Assess. 2006;10(3):iii-iv, ix-x, 1-90 Incluido en revisiones posteriores Field JK, Smith DL, Duffy S, Cassidy A. The Liverpool Lung Project research protocol. Int J Oncol. 2005;27(6):1633-45 No es objeto de estudio Cribado de cáncer de pulmón 125 Cita Causa de exclusión Gohagan JK, Marcus PM, Fagerstrom RM, Pinsky PF, Kramer BS, Prorok PC, et al. Final results of the Lung Screening Study, a randomized feasibility study of spiral CT versus chest X-ray screening for lung cancer. Lung Cancer. 2005;47(1):9-15 Incluido en revisiones posteriores Abe Y, Hanai K, Nakano M, Ohkubo Y, Hasizume T, Kakizaki T, et al. A computer-aided diagnosis (CAD) system in lung cancer screening with computed tomography. Anticancer Res. 2005;25(1B):483-8 No tiene control No es objeto de estudio Kanashiki M, Sairenchi T, Saito Y, Ishikawa H, Satoh H, Sekizawa K. Body mass index and lung cancer: a case-control study of subjects participating in a mass-screening program. Chest. 2005;128(3):1490-6 Tipo de estudio (caso-control) Mulshine JL. Clinical issues in the management of early lung cancer. Clin Cancer Res. 2005;11(13 Pt 2):4993s-8s No es objeto de estudio Mulshine JL. Current issues in lung cancer screening. Oncology (Williston Park). 2005;19(13):1724-30 No tiene control Tipo de estudio (suplemento) Mulshine JL. New developments in lung cancer screening. J Clin Oncol. 2005;23(14):3198-202 Tipo de estudio (revisión narrativa) Rossi A, Maione P, Colantuoni G, Gaizo FD, Guerriero C, Nicolella D, et al. Screening for lung cancer: New horizons? Crit Rev Oncol Hematol. 2005;56(3):311-20 Tipo de estudio (revisión narrativa) Smith RA, Cokkinides V, Eyre HJ. American Cancer Society guidelines for the early detection of cancer. CA Cancer J Clin. 2005;55(1):31-44 Oken MM, Marcus PM, Hu P, Beck TM, Hocking W, Kvale PA, et al. Baseline chest radiograph for lung cancer detection in the randomized Prostate, Lung, Colorectal and Ovarian Cancer Screening Trial. J Natl Cancer Inst. 2005;97(24):1832-9 Novello S, Fava C, Borasio P, Dogliotti L, Cortese G, Crida B, et al. Three-year findings of an early lung cancer detection feasibility study with low-dose spiral computed tomography in heavy smokers. Ann Oncol. 2005;16(10):1662-6 Chong S, Lee KS, Chung MJ, Kim TS, Kim H, Kwon OJ, et al. Lung cancer screening with low-dose helical CT in Korea: experiences at the Samsung Medical Center. J Korean Med Sci. 2005;20(3):402-8 No es objeto de estudio (es cribado general, no cáncer de pulmón) Hay versión posterior No tiene control Incluido en revisiones posteriores No tiene control Incluido en revisiones posteriores No tiene control Incluido en revisiones posteriores No es objeto de estudio Xing S, Khanavkar B, Nakhosteen JA, Atay Z, Jöckel KH, Marek W, RIDTELC Lung Study Group. Predictive value of image cytometry for diagnosis of lung cancer in heavy smokers. Eur Respir J. 2005;25(6):956-63 No tiene control Brant-Zawadzki MN. The role of computed tomography in screening for cancer. Eur Radiol. 2005;15 (Suppl 4):D52-4 No tiene control 126 INFORMES, ESTUDIOS E INVESTIGACIÓN Cita Bastarrika G, García-Velloso MJ, Lozano MD, Montes U, Torre W, Spiteri N, et al. Early lung cancer detection using spiral computed tomography and positron emission tomography. Am J Respir Crit Care Med. 2005;171(12):1378-83 Cardinale L, Cortese G, Borasio P, Dogliotti L, Ferraris F, Novello S, et al. Low dose CT in early lung cancer diagnosis: Prevalence data. Radiol Med (Torino). 2005;110(5-6):532-43 Swensen SJ, Jett JR, Hartman TE, Midthun DE, Mandrekar SJ, Hillman SL, et al. CT screening for lung cancer: five-year prospective experience. Radiology. 2005;235(1):259-65 Jett JR. Limitations of screening for lung cancer with low-dose spiral computed tomography. Clin Cancer Res. 2005;11(13 Pt 2):4988s-92s Machado RF, Laskowski D, Deffenderfer O, Burch T, Zheng S, Mazzone PJ, et al. Detection of lung cancer by sensor array analyses of exhaled breath. Am J Respir Crit Care Med. 2005;171(11):1286-91. Bastarrika G, García-Velloso MJ, Lozano MD, Montes U, Torre W, Spiteri N, et al. Early lung cancer detection using spiral computed tomography and positron emission tomography. Am J Respir Crit Care Med. 2005;171(12):1378-83 Causa de exclusión No tiene control Incluido en revisiones posteriores No tiene control No tiene control Incluido en revisiones posteriores No tiene control Tipo de estudio (caso-control) Tamaño poblacional (N < 100) No tiene control Incluido en revisiones posteriores Strauss GM, Dominioni L, Jett JR, Freedman M, Grannis FW. Como international conference position statement: lung cancer screening for early diagnosis 5 years after the 1998 Varese conference. Chest. 2005;127(4):1146-51 Tipo de estudio (conferencia de expertos) Pinsky PF, Marcus PM, Kramer BS, Freedman M, Nath H, Kvale P, et al. Diagnostic procedures after a positive spiral computed tomography lung carcinoma screen. Cancer. 2005;103(1):157-63 No es objeto de estudio Haussinger K, Becker H, Stanzel F, Kreuzer A, Schmidt B, Strausz J, et al. Autofluorescence bronchoscopy with white light bronchoscopy compared with white light bronchoscopy alone for the detection of precancerous lesions: A European randomised controlled multicentre trial. Thorax. 2005;60;496503 Manser RL, Irving LB, de Campo MP, Abramson MJ, Stone CA, Pedersen KE, et al. Overview of observational studies of lowdose helical computed tomography screening for lung cancer. Respirology. 2005;10(1):97-104 Diederich S, Thomas M, Semik M, Lenzen H, Roos N, Weber A, et al. Screening for early lung cancer with low-dose spiral computed tomography: results of annual followup examinations in asymptomatic smokers. Eur Radiol. 2004;14(4):691-702 Cribado de cáncer de pulmón Sólo detecta lesiones preinvasivas con broncoscopia de luz blanda. Tipo de estudio (comunicado) Incluye estudios sin control No tiene control Incluido en revisiones posteriores 127 Cita Causa de exclusión MacRedmond R, McVey G, Lee M, Costello RW, Kenny D, Foley C, et al. Screening for lung cancer using low dose CT scanning. Thorax. 2004;59(3):237-41 No tiene control Incluido en revisiones posteriores Travis K. Lung cancer screening for all? Not yet, panel says. J Natl Cancer Inst. 2004;96(12):900-1 Tipo de estudio (comentario) Lafata JE, Simpkins J, Lamerato L, Poisson L, Divine G, Johnson CC. The economic impact of false-positive cancer screens. Cancer Epidemiol Biomarkers Prev. 2004;13(12):2126-32 No es objeto de estudio Chanin TD, Merrick DT, Franklin WA, Hirsch FR. Recent developments in biomarkers for the early detection of lung cancer: perspectives based on publications 2003 to present. Curr Opin Pulm Med. 2004;10(4):242-7 No es objeto de estudio Tipo de estudio (revisión narrativa) Humphrey LL, Teutsch S, Johnson M; U.S. Preventive Services Task Force. Lung cancer screening with sputum cytologic examination, chest radiography, and computed tomography: an update for the U.S. Preventive Services Task Force. Ann Intern Med. 2004;140(9):740-53 Revisión publicada antes del 1 enero de 2005 van Meerbeeck JP, Tournoy KG. Screening and diagnosis of NSCLC. Ann Oncol. 2004;15 (Suppl 4):iv65-70 Revisión sistemática anterior al 1 de enero de 2005 Henschke CI, Yankelevitz DF, Naidich DP, McCauley DI, McGuinness G, Libby DM, et al. CT screening for lung cancer: suspiciousness of nodules according to size on baseline scans. Radiology. 2004;231(1):164-8. Epub 2004 Feb 27 No es objetivo de estudio Stanzel F. Fluorescent bronchoscopy: contribution for lung cancer screening? Lung Cancer. 2004;45(Suppl 2):S29-37 Tipo de estudio (revisión narrativa) National Horizon scanning Centre. Breath test for lung cancer screening 2004.- national horizon centre [monografía en Internet]. Birmingham: National Horizon Scanning Centre; 2004 [citado 9 oct 2008]. Disponible en: Tipo de estudio (caso-control) http://www.sst.dk/publ/publ2004/Tidlig_varsling_ kommenteret_breathtest_juli.pdf Hilbe W, Dirnhofer S, Greil R, Wöll E. Biomarkers in non-small cell lung cancer prevention. Eur J Cancer Prev. 2004;13(5):42536 Vassallo F, Imperatori A, Rovera F, Pericelli A, Antonini C, Dominioni L. The PRE.DI.CA. project for radiographic lung cancer screening in cigarette smokers. Rays. 2004;29(4):383-5 Gohagan J, Marcus P, Fagerstrom R, Pinsky P, Kramer B, Prorok P, et al. Baseline findings of a randomized feasibility trial of lung cancer screening with spiral CT scan vs chest radiograph: the Lung Screening Study of the National Cancer Institute. Chest. 2004;126(1):114-21 128 Tipo de estudio (revisión narrativa) No tiene control Incluido en revisiones posteriores INFORMES, ESTUDIOS E INVESTIGACIÓN Cita Church TR. Chest radiography as the comparison for spiral CT in the National Lung Screening Trial. Acad Radiol. 2003;10(6):713-5 Causa de exclusión Tipo de estudio (comentario) Es publicado antes del 1 de enero de 2004 y evalúa tomografía computarizada Bach PB, Kelley MJ, Tate RC, McCrory DC. Screening for lung cancer: a review of the current literature. Chest. 2003;123(Suppl 1):72S-82S Tipo de estudio (revisión narrativa) Thunnissen FB. Sputum examination for early detection of lung cancer.J Clin Pathol. 2003;56:805-10 Tipo de estudio (revisión narrativa) Henschke CI, Yankelevitz DF, McCauley DI, Libby DM, Pasmantier MW, Smith JP. Guidelines for the use of spiral computed tomography in screening for lung cancer. Eur Respir J. 2003;21(Suppl 39):45s-51s Tipo de estudio (revisión narrativa) No tiene control Bepler G, Carney DG, Djulbegovic B, Clark RA, Tockman M. A systematic review and lessons learned from early lung cancer detection trials using low-dose computed tomography of the chest. Cancer Control. 2003;10(4):306-14 Revisión sistemática anterior al 1 de enero de 2005 Koinuma N. The economic evaluation of lung cancer screening using a system model. Japanese Journal of Lung Cancer. 2003;43(7):1018-1027 Idioma (Japonés) Pastorino U, Bellomi M, Landoni C, De Fiori E, Arnaldi P, Picchio M, et al. Early lung-cancer detection with spiral CT and positron emission tomography in heavy smokers: 2-year results. Lancet. 2003;362(9384):593-7 No tiene control Wisnivesky JP, Mushlin AI, Sicherman N, Henschke C. The cost-effectiveness of low-dose CT screening for lung cancer: preliminary results of baseline screening. Chest. 2003;124(2):614-21 No tiene control Li F, Sone S, Abe H, MacMahon H, Doi K. Low-dose computed tomography screening for lung cancer in a general population: characteristics of cancer in non-smokers versus smokers. Acad Radiol. 2003;10(9):1013-20 No tiene control Li F, Sone S, Abe H, MacMahon H, Doi K. Low-dose computed tomography screening for lung cancer in a general population: characteristics of cancer in non-smokers versus smokers. Acad Radiol. 2003;10(9):1013-20 No tiene control Marcus PM. Conflicting evidence in lung cancer screening: randomized controlled trials versus case-control studies. Lung Cancer. 2003;41(1):37-9 No es objeto de estudio Sobue T, Moriyama N, Kaneko M, Kusumoto M, Kobayashi T, Tsuchiya R, et al. Screening for lung cancer with low-dose helical computed tomography: anti-lung cancer association project. J Clin Oncol. 2002;20(4):911-20 No tiene control Cribado de cáncer de pulmón 129 Cita Causa de exclusión Blanchon T, Lukasiewicz-Hajage E, Lemarié E, Milleron B, Bréchot JM, Flahault A; Groupe Dépiscan. Depiscan, un projet pilote pour evaluer le depistage du cancer broncho-pulmonaire par le scanner helicoidal a faible dose Rev Mal Respir. 2002;19(6):701-5 Es publicado antes del 1 de enero de 2004 y evalúa tomografía computarizada y radiografía de tórax Nawa T, Nakagawa T, Kusano S, Kawasaki Y, Sugawara Y, Nakata H. Lung cancer screening using low-dose spiral CT: results of baseline and 1-year follow-up studies. Chest. 2002;122(1):15-20 No tiene control Es publicado antes del 1 de enero de 2004 y evalúa tomografía computarizada Henschke CI, Naidich DP, Yankelevitz DF, McGuinness G, McCauley DI, Smith JP, et al. Early lung cancer action project: initial findings on repeat screenings.Cancer. 2001;92(1):153-9 No tiene control Sone S, Li F, Yang ZG, Honda T, Maruyama Y, Takashima S, et al. Results of three-year mass screening programme for lung cancer using mobile low-dose spiral computed tomography scanner. Br J Cancer. 2001;84(1):25-32 No tiene control Henschke CI, Naidich DP, Yankelevitz DF, McGuinness G, McCauley DI, Smith JP, et al. Early lung cancer action project: initial findings on repeat screenings. Cancer. 2001;92(1):153-9 No tiene control Es publicado antes del 1 de enero de 2004 y evalúa tomografía computarizada y radiografía de tórax Okamoto N. Cost-effectiveness of lung cancer screening in Japan. Cancer. 2000;89(11 Suppl):2489-93 Incluido en revisiones posteriores Dominioni L, Imperatori A, Rovera F, Ochetti A, Paolucci M, Dionigi G. Lung cancer screening in cigarette smokers in the province of Varese, Italy. Cancer. 2000;89(11 Suppl):2345-8 No tiene control Marcus PM, Bergstralh EJ, Fagerstrom RM, Williams DE, Fontana R, Taylor WF, et al. Lung cancer mortality in the Mayo Lung Project: impact of extended follow-up. J Natl Cancer Inst. 2000;92(16):1308-16 Kubik AK, Parkin DM, Zatloukal P. Czech Study on Lung Cancer Screening: post-trial follow-up of lung cancer deaths up to year 15 since enrolment. Cancer. 2000;89(11 Suppl):2363-8 Patz EF, Goodman PC, Bepler G. Screening for lung cancer. N Engl J Med. 2000;343(22):1627-33 130 Hay un estudio posterior de 2006 Incluido en revisiones posteriores Es publicado antes del 1 de enero de 2004 Incluido en revisiones posteriores Tipo de estudio (revisión narrativa) INFORMES, ESTUDIOS E INVESTIGACIÓN Cribado de cáncer de pulmón 131 2007 (68) - Medline American College of Chest Physicians, -Lista de referencias de artículos relevantes de “Thoracic Oncology NetWork” Bases de datos revisadas Institución, año -Estudios que aportan información de la base teórica del cribado o su comportamiento clínico y que analizan nuevas pruebas de cribado -Pacientes cribados entre 2002 y 2005 Criterios de inclusión -Evaluar la efectividad del cribado con LDCT en pacientes de alto riesgo asintomáticos, sin historia previa de cáncer de pulmón, ≥ 40 años, ≥ 10-20 PY) frente a radiografía de tórax Objetivo -No se especifica Nº estudios ANEXO D. Revisiones sistemáticas incluidas -El cribado es eficiente y coste-efectivo solamente en población de riesgo -Se recomienda un cribado con LDCT en casos muy concretos -No se recomiendan radiografía de tórax ni citología simple o seriada para el cribado de cáncer de pulmón -LDCT detecta tumores de crecimiento lento y poco agresivos -El conocimiento del tiempo de duplicación del tumor puede ayudar a determinar la extensión y comportamiento biológico del tumor -Ninguna de las pruebas de cribado reduce la mortalidad a pesar de que sí hay mejor supervivencia y pueden servir para detectar tumores en estadíos tempranos -LDCT detecta tumores de tamaño muy pequeño y en estadíos tempranos (sobre todo en estadío I), además es tres veces más sensible que radiografía de tórax Conclusiones -Problema: identificar exactamente la población de riesgo. Es difícil verificar si LDCT es factible o no como pruebas de cribado debido a la inexistencia de estudios con grupo control -No incluyen datos de sobrediagnóstico -No se llevó a cabo una valoración de la calidad de los estudios -No se hace una búsqueda muy exhaustiva, ya que solo se busca en Medline -La supervivencia solo se analiza en los casos de cáncer de pulmón detectados con el cribado Comentarios 2++ Nivel de calidad 132 INFORMES, ESTUDIOS E INVESTIGACIÓN -Se revisan artículos y referencias relacionados y libros de texto de cáncer de pulmón y de radiología -Para abstracts: RSNA (20032005) y ECR (2001-2006) -Para estudios de 1966 a mayo de 2006: MEDLINE, EMBASE, Cochrane Library CINAHL -Se buscan revisiones de cribado de cáncer de pulmón con radiografía de tórax o tomografía computarizada. London Health Sciences Centre, 2007 (69) Bases de datos revisadas Institución, año -Estudios que incluyen población de riesgo basada en exposiciones ocupacionales -Estudios que solo aportan el abstract Criterios de exclusión: -Estudios prospectivos y retrospectivos que evalúan el cribado de cáncer de pulmón en población de riesgo. Los estudios deben tener al menos un cribado basal con tomografía computarizada de baja dosis e incluir el número de casos detectados Criterios de inclusión: Criterios de inclusión -Evaluar la factibilidad de LDCT en población de riesgo (≥40 años, fum de > 1 PY, exfum, principalmente hombres) frente a radiografía de tórax Objetivo (1966-2006) -22 estudios Nº estudios -Se detectan valores muy dispares de falsos positivos (de 8 a 761 dependiendo del estudio) -Se estiman los valores medios en 9 estudios de sensibilidad, especificidad, valor predictivo positivo y valor predictivo negativo (81 %, 81 %, 8 % y 99 %, respectivamente) -Un programa de cribado con LDCT sería rentable en una población de riesgo -No hay una relación entre el estadío temprano y que el nódulo sea pequeño -La LDCT es capaz de detectar hasta un 80 % de tumores en estadíos tempranos en el cribado basal -La exactitud de la LDCT depende del médico y del umbral entre las lesiones sospechosas y no sospechosas -La LCDT presenta valores altos de sensibilidad y especificidad, detecta más nódulos no calcificados en estadíos tempranos que radiografía de tórax y otras pruebas, pero no disminuye la mortalidad ni morbilidad Conclusiones -A pesar de que se recogen estudios hasta 2006, también se incluyen datos muy antiguos (desde 1966) -No se llevó a cabo una valoración de la calidad de los estudios Comentarios 2++ Nivel de calidad Cribado de cáncer de pulmón 133 - MEDLINE, EMBASE, Cochrane Database of Systematic Reviews, Cochrane CENTRAL Register of Controlled Clinical Trials, NHS, EED, HTA database, DARE, Bandolier, Health Management Information Consortium, American Society of Clinical Oncology, Research Findings Register, National Horizon Scanning Centre, SCI, Web of Science Proceedings, National Research Register and INAHTA Aberdeen Health Technology Assessment Group, 2007 (70) Bases de datos revisadas Institución, año -Estudios que emplean otras pruebas diferentes a tomografía computarizada o que emplean tomografía computarizada como prueba de diagnóstico o estadificación Criterios de exclusión: -Estudios de cualquier procedencia geográfica y sin restricción de edad, sexo o hábito tabáquico -Revisiones como fuente de información de estudios primarios -Estudios publicados entre enero de 1994 y enero de 2005 -Estudios en cualquier idioma -Estudios sobre cribado de cáncer de pulmón con tomografía computarizada Criterios de inclusión: Criterios de inclusión -Evaluar la efectividad clínica del cribado con LDCT en población de riesgo (≥40, fum, no fum, ≥10 PY) Objetivo -12 estudios (2 ensayos clínicos aleatorizados + 10 estudio sin grupo de comparación) Nº estudios -Este tipo de estudios solo puede aportar un mejor entendimiento de la historia natural de los nódulos y casos de cáncer de pulmón detectados con tomografía computarizada -A pesar de que la tomografía computarizada detecta muchos tumores en estadíos tempranos, no se puede obtener evidencia clara de que un programa de cribado con tomografía computarizada sea efectivo, ya que no hay reducción de la mortalidad Conclusiones -No incluyen datos de sobrediagnóstico -La selección de los estudios la realizan dos investigadores -Muchos estudios incluidos no tienen grupo control, lo que dificulta la determinación del efecto del programa de cribado -La duración del seguimiento es en la mayoría de los estudios menor de 2 años -Ninguno de los estudios informa sobre la representatividad de las muestras (incluyen pacientes voluntarios, por lo que es difícil evaluar si son o no representativas) Comentarios 2++ Nivel de calidad 134 INFORMES, ESTUDIOS E INVESTIGACIÓN 2007 (73) -Bases de datos de CRD Agencia de Evaluación de Tecnologías Sanitarias de Andalucía, -INAHTA y otros organismos o instituciones relacionados -Bases de datos médicas: MEDLINE, PreMEDLINE, EMBASE y Cochrane Library Bases de datos revisadas Institución, año -Estudios en inglés, español, francés, italiano o portugués -Estudios que evalúen la efectividad del cribado con LDCT en población de riesgo (adultos asintomáticos con riesgo de desarrollar cáncer de pulmón) principalmente en términos de mortalidad (general o específica), supervivencia o prevalencia y/o incidencia de la enfermedad -Revisiones sistemáticas y cualquier estudio primario (ensayo clínico, análisis económico, cohortes,…) Criterios de inclusión -Evaluar la efectividad de la LDCT en población de riesgo (≥40, asintomáticos, exfum, fum de ≥10 PY) Objetivo -12 estudios (11 de cribado con LDCT+1 costeefectividad de LDCT) Nº estudios -El porcentaje de falsos positivos para el cribado con LDCT es muy elevada, oscila entre 87,9 % y 96 % -No se considera costeefectivo, ya que no hay reducción de la mortalidad, de la tasa de falsos positivos ni del coste económico de las pruebas realizadas ni aumento de la adherencia -La LDCT es capaz de detectar tumores en estadíos tempranos y, por tanto, con mejor pronóstico, pero no hay evidencia de un cambio en el pronóstico de la enfermedad Conclusiones -Período de seguimiento < 5 años -La valoración de la calidad de los estudios fue realizada por dos investigadores empleando la lista de comprobación del National Institute for Health and Clinical Excellence para las revisiones sistemáticas y la lista de comprobación del CRD para estudios originales Comentarios 2++ Nivel de calidad Cribado de cáncer de pulmón 135 2006 (71) -MEDLINE (1966- Feb 2006) y EMBASE (1980Feb 2006) Interactive Cardio Vascular and Thoracic Surgery, -Cochrane Central Register of Controlled Trials Bases de datos revisadas Institución, año -Estudios únicamente en inglés -Estudios que evalúen el cribado de cáncer de pulmón en población de riesgo con radiografía de tórax o tomografía computarizada Criterios de inclusión -Evaluar la mejora o no de la supervivencia con LDCT en población asintomática de bajo y alto riesgo (fum, exfum, expuestos a asbestos, hombres y mujeres, >40 años) Objetivo -354 artículos (solo 9 incluidos:3 revisiones sistemáticas + 4 estudios de cohortes + 1 revisión no sistemática + 1 estudio retrospectivo) Nº estudios -No hay evidencia de reducción de la mortalidad a pesar de que sí se observa mejor supervivencia -La LDCT detecta tres veces más nódulos y tumores en estadíos más tempranos que radiografía de tórax -La prevalencia usando LDCT oscila entre el 0,40 y el 2,70 % Conclusiones - Solo se consideran estudios en inglés -A pesar de que se recogen estudios hasta 2006, también se incluyen datos muy antiguos (desde 1966) -El tiempo de seguimiento es muy corto, la población no es representativa y no se valora el impacto de la tomografía computarizada -No se llevó a cabo una valoración de la calidad de los estudios -No se especifican claramente los criterios de inclusión y exclusión Comentarios 2++ Nivel de calidad 136 INFORMES, ESTUDIOS E INVESTIGACIÓN 2006 (72) -MEDLINE (1966- Feb 2006) y EMBASE (1980Feb 2006) Interactive Cardio Vascular and Thoracic Surgery, -Cochrane Central Register of Controlled Trials Bases de datos revisadas Institución, año -Estudios únicamente en inglés -Estudios que evalúen el cribado de cáncer de pulmón en población de riesgo con radiografía de tórax o tomografía computarizada Criterios de inclusión -Evaluar la mejora de supervivencia con radiografía de tórax en población de alto riesgo (asintomáticos, fum, 40-45 años) Objetivo -136 artículos (10 relevantes: 7 ensayos clínicos aleatorizados + 1 revisión sistemática con metanálisis+1 revisión no sistemática+1 revisión sistemática) Nº estudios -No hay evidencia para realizar un cribado de cáncer de pulmón con radiografía de tórax con o sin citología como prueba de cribado -Hay sobrediagnóstico -Mayor detección en el grupo de mayor intensidad de radiación -Se observó aumento de mortalidad (11 %) debido a la radiación -Mayor incidencia de cáncer de pulmón, tasa de operaciones quirúrgicas y mejor supervivencia en el grupo cribado con mayor intensidad, pero no hay reducción de la mortalidad en ningún caso Conclusiones - Solo se consideran estudios en inglés -A pesar de que se recogen estudios hasta 2006, también se incluyen datos muy antiguos (desde 1966) -No se llevó a cabo una valoración de la calidad de los estudios -No se especifican claramente los criterios de inclusión y exclusión Comentarios 2++ Nivel de calidad Cribado de cáncer de pulmón 137 (Japón) (74) Toyoda y cols., 2008 Autor, año (país) -Reclutados desde agosto de 1998 a mayo de 2002 -18.070 pacientes -Ensayo clínico Diseño, tamaño muestral y tiempo de seguimiento -Edad: 40-80 años -Fum actuales, exfum, no fum -Hombres y mujeres Características de los sujetos incluidos -Citología de esputo adicional en ambos brazos -Radiografía de tórax: 13.381 pacientes -LDCT: 4.689 pacientes Intervención y grupo de comparación -LDCT tiene mayor sensibilidad y menor especificidad que radiografía de tórax -Mayor sobrediagnóstico en el brazo cribado con LDCT -Ambas pruebas presentan mejor rendimiento para no fumadores -Sensibilidad mayor para adenocarcinoma que para no adenocarcinoma -Especificidad más elevada en los test sucesivos que en el basal -Sensibilidad y especificidad de 88,9 % y 92,6 % para LDCT y 78,3 % y 97,0 % para radiografía de tórax Resultados -No evalúa supervivencia ni mortalidad Supervivencia -Para comparar LDCT con radiografía de tórax se asume que la fase preclínica detectable es de 1 año (LDCT detecta tumores de crecimiento lento) -Se diagnostican muchos nódulos con LDCT, aunque luego no son confirmados patológicamente -Sensibilidad basal está afectada por el length bias y el sobrediagnóstico Principales limitaciones del estudio 1- Nivel de calidad ANEXO E. Estudios primarios incluidos sobre cribado de cáncer de pulmón 138 INFORMES, ESTUDIOS E INVESTIGACIÓN Blanchon y cols., 2007 (Francia) (75) Fujikawa y cols., 2008 (Japón) (78) Autor, año (país) -2 años de cribado -Asintomáticos -765 pacientes (brazo cribado: 385 pacientes; brazo control: 380 pacientes) -Consumo medio de ≥ 15 cigarrillos/día al menos durante 20 años -Fum habituales o exfum (desde hace menos de 15 años) -Edad media: 56 años -71 % hombres y 29 % mujeres -≥40 años -Población general Características de los sujetos incluidos -Ensayo clínico aleatorizado -Reclutados desde 2001 hasta 2004 -26.025 pacientes -Ensayo clínico Diseño, tamaño muestral y tiempo de seguimiento -Ambos tipos de cribado son realizados al inicio del programa de cribado y anualmente durante 2 años -LDCT detecta hasta 10 veces más nódulos no calcificados (NCN) con que radiografía de tórax -Más anormalidades con LDCT que con radiografía de tórax - Solo se detectan tumores en estadíos avanzados en el brazo cribado con LDCT -Se detectan más casos de cáncer con LDCT que con radiografía de tórax (2,4 % frente a 0,3 %) y, además, en estadíos más tempranos (3 frente a 1) -Más casos detectados en mujeres en el brazo de LDCT y más adenocarcinomas -LDCT: 3.305 con resultado negativo en la radiografía -LDCT frente a radiografía de tórax -LDCT detecta más casos de cáncer en estadíos más tempranos y siempre en el cribado basal Resultados -Radiografía de tórax: 22.720 pacientes durante 4 años Intervención y grupo de comparación -No evalúa ni supervivencia ni mortalidad -Mayor supervivencia en el grupo cribado con LDCT, tanto los tratados con cirugía como los no tratados Supervivencia -La proporción de tumores en estadíos tardíos es mayor en el cribado inicial posiblemente debido a que se hayan incluido fumadores severos y con síntomas -No hay cribados intermedios para determinar la mortalidad y la incidencia del cáncer de pulmón -No hay igualdad en la periodicidad del cribado -Poblaciones de cada brazo con características diferentes Principales limitaciones del estudio 1- 1- Nivel de calidad Cribado de cáncer de pulmón 139 (Nueva York) (77) Melamed y cols., 2000 (EE.UU.) (76) Marcus y cols., 2006 Autor, año (país) -Fum de cigarrillos -Fumadores (≥ 1 paquete/ día) -≥ 45 años -10.040 hombres -5-8 años de cribado + 2 de seguimiento -Hombres -Ensayo clínico -6 años de cribado + 1,5 años de seguimiento poscribado -Hombres -9.211 pacientes (brazo cribado: 4.618 pacientes; brazo control: 4.593 pacientes) Características de los sujetos incluidos -Ensayo clínico Diseño, tamaño muestral y tiempo de seguimiento -Citología de esputo -Radiografía de tórax + citología de esputo -Radiografía de tórax -Brazo control: recomendación de radiografía de tórax + citología de esputo anual -Brazo cribado: radiografía de tórax + citología de esputo cada 4 meses Intervención y grupo de comparación -En población de riego la citología de esputo no aumenta la supervivencia, pero sí el número de casos de cáncer detectados en estadíos tempranos -Ambas pruebas se complementan a la hora de detectar cáncer de pulmón -La citología de esputo detecta más carcinomas epidermoides en estadío temprano -La radiografía de tórax es más efectiva para adenocarcinomas periféricos -Mayor número de casos diagnosticados en el brazo cribado -Mortalidad similar en ambos brazos Resultados -No hay reducción de mortalidad -Mayor supervivencia de la población cribada frente a la no cribada (35 % frente a 13 %) -Mayor supervivencia en el brazo cribado Supervivencia -No se reflejan los falsos positivos -El diseño del estudio no permite observar reducción de la mortalidad al no comparar un grupo cribado con radiografía de tórax frente a un grupo control sin ningún tipo de cribado -A pesar de que las muestras se recogen con máxima precisión son de años atrás y de diferentes fuentes de información, por lo que pueden ser poco fiables Principales limitaciones del estudio 1- 1- Nivel de calidad ANEXO F Niveles de evidencia (SIGN) Nivel de evidencia Tipo de estudio 1++ Meta-análisis de gran calidad, revisiones sistemáticas de ensayos clínicos aleatorizados o ensayos clínicos aleatorizados con muy bajo riesgo de sesgos. 1+ Meta-análisis bien realizados, revisiones sistemáticas de ensayos clínicos aleatorizados o ensayos clínicos aleatorizados con bajo riesgo de sesgos. 1- Meta-análisis, revisiones sistemáticas de ensayos clínicos aleatorizados o ensayos clínicos aleatorizados con alto riesgo de sesgos. Revisiones sistemáticas de alta calidad de estudios de cohortes o de casos y controles, o 2++ Estudios de cohortes o de casos y controles de alta calidad, con muy bajo riesgo de confusión, sesgos o azar y una alta probabilidad de que la relación sea causal. 2+ Estudios de cohortes o de casos y controles bien realizados, con bajo riesgo de confusión, sesgos o azar y una moderada probabilidad de que la relación sea causal. 2- Estudios de cohortes o de casos y controles con alto riesgo de confusión, sesgos o azar y una significante probabilidad de que la relación no sea causal. 3 Estudios no analíticos (observaciones clínicas y series de casos). 4 Opiniones de expertos. 140 INFORMES, ESTUDIOS E INVESTIGACIÓN P.V.P.: 10 euros