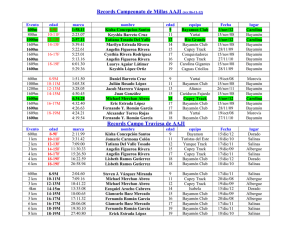
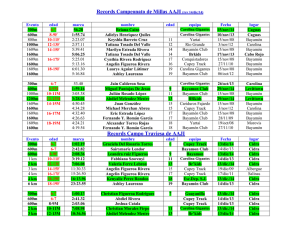
Diagramas
Anuncio

Química Inorgánica-63.13- Dra.Silvia E. Jacobo Diagrama de Látimer a ) En solución ácida ClO4 - 1,19 ClO3- 1,21 HClO2 1,63 Cl2 1,36 Cl - 1,46 b ) En solución básica ClO4- 0,37 ClO3- 0,33 ClO2- 0,66 0,50 ClO - 0,40 Cl2 0,89 1,36 Cl- Química Inorgánica-63.13- Dra.Silvia E. Jacobo Diagrama de Frost 10 HClO4 pH= 0 8 pH= 14 HClO3 6 nEV HClO2 4 - HClO 2 - ClO3 - ClO2 Cl2 0 ClO4 - ClO - Cl -2 -1 0 1 2 3 4 n° oxidación 5 6 7 Química Inorgánica-63.13- Dra.Silvia E. Jacobo Diagrama de Frost 6 5 HMnO4 H2MnO4 4 nE / V 3 2 1 Mn o 0 MnO2 O2 -1 Mn H2O2 -2 Mn H2O -3 -2 -1 0 1 2 3+ 2+ 3 4 n°de oxidación 5 6 7 Química Inorgánica-63.13- Dra.Silvia E. Jacobo Diagrama de Frost HNO3 7 6 E. Libre (V.mol e-) 5 Condiciones básicas HNO2 4 Condiciones ácidas NH2OH 3 N2H4 2 NO3 - NH3OH+ NO2- 1 NH3 N2H5+ 0 NH4+ N2 -1 6 5 4 3 2 1 0 -1 Estados de oxidación -2 -3 -4