DIARREA EN PACIENTES HIV DE ORIGEN PARASITARIO
Anuncio

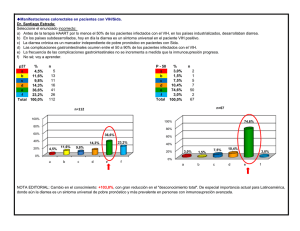
Juan Carlos Abuin Ricardo Darío Marino DIARREAS DE ORIGEN PARASITARIO EN PACIENTES HIV El creciente número de pacientes inmunocomprometidos exige al medico conocer los problemas que con más frecuencia afectan a este tipo de población. Dentro de este grupo se encuentran los enfermos afectados por el virus de la inmunodeficiencia humana (HIV) , siendo el síndrome diarreico una de las complicaciones más frecuentes que padecen estos pacientes, incluso, en algunos casos, pudiendo desencadenar la muerte de estos individuos.(1) Diversos autores coinciden en que más de la mitad de los individuos con SIDA presentan episodios de diarrea en el transcurso de su enfermedad. Su frecuencia depende del grado de inmunodepresión superando el 30% en los países desarrollados y el 90% en los países subdesarrollados. Se considera que en los países clasificados como de tercer mundo la presentación del síndrome diarreico en el SIDA es particularmente frecuente como consecuencia de la limitada accesibilidad al tratamiento con antiretrovirales. Se debe asociar a este factor la frecuente presencia de diversos agentes infecciosos, comunes en estos países, junto a la deficiencia alimentaria y sanitaria. Al estudiar el síndrome diarreico es conveniente recordar que las enfermedades que comprometen el sistema inmune por sí mismas suelen causar diarrea. Siendo la enteropatía asociada a HIV una de las causas en esta población. Los pacientes afectados por el virus HIV presentan distintos tipos de infecciones oportunistas , entre ellas las parasitarias. Estos agentes parasitarios fueron surgiendo a medida que la pandemia por el HIV avanzaba , por la sospecha de los profesionales que atendían a esta población y que no encontraban la causa de la afección que presentaban. Se debió ,en el caso de las parasitosis, recurrir a otra disciplina como la medicina veterinaria .Esta permitió estudiar nuevas zoonosis parasitarias que en los animales con trastornos inmunológico producían casos similares. Es así como se comenzaron a utilizar nuevas técnicas diagnósticas que permitirían hallar estos agentes, sobre todo a nivel del grupo de los coccidios , protozoarios que son las principales causantes de diarrea no solo en los pacientes HIV sino en otro tipo de inmunodepresión . Dado el alto impacto de las parasitosis, entre ellas las entéricas , dentro de esta población se ha dedicado especial atención al estudio y normatización del diagnóstico. Los parásitos del tracto gastrointestinal pueden comportarse como agentes patógenos produciendo sintomatología gastrointestinal o como “ comensales”, término que se encuentra actualmente en discusión porque dependería dicha característica del estado inmunitario del individuo parasitado. Algunos parásitos se asocian también a patología alérgica (dermatológica o respiratoria), pudiendo actuar como factor agravante de la misma, o bien ser iniciadores del mecanismo alérgico. Las giardiasis y actualmente el Blastocystis hominis, son los protozoarios asociados más frecuentemente a estos cuadros. En los pacientes inmunocomprometidos, las parasitosis intestinales, presentan compromiso un sistémico como son gastroenteritis secretorias con abundante pérdida de líquidos y electrolitos y el síndrome de mala absorción : caracterizado por pérdida de peso, desnutrición e hipovitaminosis. En algunas de estas etiologías se puede también observar alteraciones del metabolismo hepático y de la vía biliar (colecistitis alitiásicas). En general el número de elementos parasitarios es elevado y el curso clínico que adopta es más prolongado, con eventuales remisiones periódicas y frecuentes fracasos terapéuticos. El diagnóstico se basa en el hallazgo del agente etiológico, el cual, con el uso de nuevas técnicas de concentración, coloraciones especiales y la utilización de microscopía de avanzada permiten, en la actualidad, aumentar la sensibilidad y especificidad del mismo. Problemas tales como la falta de tratamiento efectivo para determinados patógenos, la emergencia de nuevos agentes oportunistas y el aumento de los patrones de resistencia a drogas continúan planteándonos un desafío en este grupo poblacional. Fisiopatogenia del síndrome diarreico parasitario en los pacientes HIV + El sistema inmune de la mucosa gastrointestinal juega un papel esencial en la fisiopatogenia de la infección por el HIV. Puede ser la puerta de entrada del virus HIV-1 y un sitio de infección y destrucción de linfocitos CD4.Se ha demostrado una marcada reducción en el número de células T CD4+ de la población linfocitaria de la mucosa, acompañada de un incremento de las células T CD8+, que en ocasiones supera a lo hallado en la sangre periférica. La inmunodepresión de los órganos linfoides durante la infección crónica finalmente predispone al desarrollo de infecciones oportunistas, entre ellas las parasitarias.(1)(2)(3)(4) Los parásitos pueden alterar la pared intestinal y producir diarrea, con mecanismos de daño diverso como lo es por acción de enzimas, un traumatismo directo, la obstrucción del área de absorción, taponamiento de un conducto, producción de ulceraciones, liberación de productos tóxicos, etc. Los agentes parasitarios, de acuerdo a los grandes avances en el conocimiento de la etiopatogenia de la diarrea y de acuerdo a las características clínicas que produce se han podido clasificar en tres patrones clínicos(1): 1-Diarrea aguda líquida o acuosa (Mecanismo no inflamatorio, acción de enterotoxinas o de adherencia) Ej. Cryptosporidium spp. 2-Diarrea con sangre (Mecanismo inflamatorio, resultado de la invasión inflamatoria de la mucosa colónica producida por el parásito y/o la acción de citotoxinas) . Este patrón es el menos observado en esta población por el estado de inmunodepresión. Ejemplo : Ameba histolytica 3-Diarrea persistente (diarrea que se prolonga más de 14 días y que inicia con un proceso infeccioso agudo) Es el patrón más frecuente de observar . Causada por la gran mayoría de las parásitos que afectan a los pacientes HIH/SIDA Ejemplo : Cryptosporidium spp., Giardia lamblia, Strongyloides stercoralis. Principales agentes parasitarios que producen un sindrome diarreico en pacientes HIV/SIDA Diversos son los agentes parasitarios que provocan un síndrome diarreico en pacientes afectados por HIV/SIDA. La siguiente clasificación, basada en la relación parásito / huésped inmunodeprimido, con manifestaciones clínicas los agrupa en 3 grandes grupos: A. Marcadores de SIDA 1. 2. 3. 4. 5. 6. Cryptosporidium spp. Isospora belli Cyclospora cayetanensis Microsporidium spp. Sarcocystis spp. Strongyloides stercoralis B. Marcadores Potenciales 1. Giardia lamblia 2. Blastocystis hominis 3. Entamoeba histolytica 4. Dientamoeba fragilis No incluidos en los grupos anteriores (ej. C. No Reconocidos como Oportunistas E. coli, etc. ) El primer grupo está integrado por los parásitos que producen un compromiso sistémico , que incluso puede ocasionar la muerte debido a la descompensación en su estado general. El segundo esta integrado por aquellos agentes que producen manifestaciones clínicas importantes como diarrea pero sin un compromiso sistémico. En este grupo se ha observado que ante el tratamiento antiparasitario los pacientes que no han respondido a un primer esquema terapéutico , debieron repetir una nueva serie , misma dosis, lográndose la resolución del cuadro y la negativización del examen parasitológico. El último grupo es aquel en el cual los pacientes inmunocomprometidos parasitados no han presentado diferencias clínicas con la población inmunocompetente. Se menciona , a continuación, a los principales causantes del síndrome diarreico de causa parasitaria: Cryptosporidium spp El Cryptosporidium es un protozoario que puede causar diarrea severa en pacientes con SIDA o neutropénicos , y moderada y generalmente autolimitada en su evolución en pacientes inmunocompetentes. Este protozoario Coccidio fue comunicado por primera vez como causante de patologías en humanos en 1976. En 1981-82 se identificó Cryptosporidium en 47 pacientes con SIDA en USA y se descubrió que era capaz de causar enteritis grave. Existen distintas especies de Cryptosporidium: (5) A. .C.parvum Afecta humanos y ganado bovino B. .C. muris Afecta ratones y ganado vacuno C. .C.baileyi D. .C.meleagridis Afectan aves Si bien pudieran existir infecciones cruzadas se considera a Cryptosporidium parvum la especie predominante en el ser humano. No obstante se sigue informando como Cryptosporidium spp en los laboratorios donde no se puede realizar tipificación de especie. Este Coccidio desarrolla todo su ciclo en un único huésped. El Cryptosporidium puede trasmitirse de los animales a los seres humanos (zoonosis parasitaria) y entre los humanos (6) siendo una causa descripta de infección intranosocomial parasitaria. La contaminación con heces de animales conteniendo ooquistes maduros en aguas y alimentos es la fuente de infección más probable. La cloración del agua no destruye el ooquiste maduro, lo mismo que el hipoclorito y la iodopovidona, sí, el formol al 10% y la congelación. Ciclo Vital El ciclo de este parásito comienza con la ingestión de ooquistes maduros el cual contiene cuatro esporozoítos (se discute la existencia de un mecanismo inhalatorio). La dosis infectiva en un paciente adulto es de10² ooquiste como mínimo. Algunos autores refieren que se necesita menor cantidad de ooquistes para producir la infectación. Luego se produce la desenquistación por disolución de la membrana del ooquiste y penetración de los esporozoitos en la célula epitelial donde se transforman en trofozoitos. Comienza la multiplicación asexual – merogonia - con producción de merontes tipo 1 (8 en total) los cuales invaden otras células y reinician la merogonia dando merontes tipo 2 (4 en total). Esto merontes tipo 2 forman micro y macro gametos que al unirse forman por último el ooquiste, el cual madura y puede infectar a un nuevo huésped o reinfectar al mismo. Anatomía patológica y patogenia El yeyuno es el sitio mayormente afectado.(5) Clásicamente los cambios que a este nível se describen son: - Aplastamiento y pérdida de las microvellosidades Elongación de las criptas Infiltrado inflamatorio de la lámina propia La microscopía electrónica revela al Cryptosporidium, en estadios endógenos -entre las microvellosidades y encerrado en una vacuola parasitófora justo por debajo de la célula huesped - en una posición intracelular aunque extracitoplasmática. (7) Se han sugerido respecto de la fisiopatología de la diarrea por Cryptosporidium mecanismos secretorios, humorales , enterotoxigénicos y la destrucción mecánica del ribete en cepillo. Clínica La gravedad y duración de la enfermedad depende del estado inmunitario del paciente. a- Pacientes inmunocomprometidos La inmunidad celular y humoral parecen estar involucradas en el control de la infección por Cryptosporidium , por lo cual puede observarse estas formas no sólo en pacientes con SIDA sino también en aquellos con diabetes, hemopatías, inmunodeficiencias congénitas, transplantados, tratamientos con corticoides , etc. (6) Los síntomas son más intensos y de larga duración . - Diarrea acuosa (generalmente crónica, con pérdida de agua y electrolitos) - Dolor abdominal cólico - Anorexia y pérdida de peso - Nauseas, vómitos - Mialgias - Sindrome de malabsorción con esteatorrea y alteraciones de test funcionales. (8) En pacientes con SIDA se ha descripto la forma diseminada con localización pulmonar y en la vía biliar. (6) En concomitancia con crytposporidiosis severa se ha visualizado el gérmen en esputo, lavado broncoalveolar, aspirado traqueal y tejido pulmonar, pero, y a pesar de haberse reportado casos de infección respiratoria con hipoxia (9), el significado clínico del Cryptosporidium en pulmón es motivo de controversia. En los cuadros de colangitis y colecistitis alitiásica frecuentemente se lo encuentra asociado al CMV(10). Estos pacientes suelen presentar dolor en hipocondrio derecho con FAL y δ GT elevadas. Las transaminasas y los niveles de bilirrubinemia permanecen dentro del rango normal. b- Paciente inmunocompetente El período de incubación es de 3-12 días Formas clínicas: 1- Asintomática 2- Síndrome dispéptico 3- Diarrea aguda, (acuosa, sin moco, ni pus ni sangre) generalmente se autolimita en 14 días. (Diarrea del viajero?) 4- Diarrea crónica (25% de los casos) La mayoría de los casos no requieren más tratamiento que el soporte hídrico. La desaparición del Cryptosporidium ocurre entre 4 y 6 semanas. (5) Diagnóstico Se basa en la búsqueda de los ooquistes en materia fecal - Tinción de kinyoun - Tinción de auramina rodamina La eliminación de ooquistes es intermitente, por lo cual se deben obtener un mínimo de 2 muestras - IFD con anticuerpos monoclonales anticryptosporidium Este método es utilizado básicamente para mensurar la excreción de ooquistes por materia fecal, ya que generalmente existe una correlación entre el número de ooquistes y la cantidad de microorganismos observados en la biopsia. (11) - Técnicas de concentración o flotación que permitan optimizar la detención de ooquistes en materia fecal. - ELISA Se han detectado anticuerpos IgG e IgM en el 95% de los pacientes con SIDA y Cryptosporidium. Si bien no sirve para el diagnóstico de enfermedad aguda, este método es útil para estudios epidemiológicos. - Biopsia de intestino Habitualmente se colorea con metenamina plata o inmunoperoxidasa. Tratamiento. Todos los tratamientos para la diarrea por Crytposporidium han dado pobres resultados incluyendo el uso de antidiarreicos , antimicrobianos y antiparasitarios. La terapéutica antiretroviral al mejorar el estado inmunológico del paciente ha logrado revertir esta situación. La reposición hidroelectrolítica, sobre todo en el caso de diarrea graves es prioritaria. La espiramicina (2-3 gr./día) no ha resultado efectiva en comparación al placebo (12), probablemente por el reservorio biliar de Cryptosporidium y su baja disponibilidad por vía oral. Inclusive algunos pacientes han desarrollado diarrea de otras características con este antibiótico, probablemente asociada al desarrollo de disbacteriosis. Según estudios (13) (14), la paromomicina, un aminoglucósido administrado por vía oral, ha logrado en pacientes con Sida una mejoría en la sintomatología y disminuyó considerablemente el crecimiento del microorganismo, por sobre el placebo. La dosis utilizada fue de 2 gramos por 4 semanas y 1 gramo las 4 semanas posteriores (15). Se ha utilizado en ensayos, azitromicina (16) ,que presenta buena concentración biliar y una eficacia aceptable según algunos autores, lactobin-R (17) (calostro bovino inmune comercial), octeocride (6), un análogo de somatostatina que disminuye la secreción esplácnica, etc. Debido a la alta resistencia del ooquiste es fundamental el lavado de manos y las normas de bioseguridad al manejar estos pacientes. Microsporidium spp. El filum Microsporidia consta de 80 géneros y 700 especies. Se denominan genéricamente Microsporidium y a la enfermedad que producen microsporidiosis. Su importancia en patología humana no fue descripta hasta la aparición del SIDA, y en rigor de verdad solo fueron comunicados muy pocos casos en pacientes no HIV (18). Los géneros mas frecuentemente implicados en patología humana intestinal son: Enterocytozoon bieneusi ( E. bieneusi ) y Encephalitozoon intestinalis ( E. intestinalis ) Ciclo vital: Son protozoarios de ciclo intracelular obligatorio que forman esporas de 1-2 micrones . Estos constituyen los elementos infectantes, los cuales penetran por vía digestiva a partir de la contaminación fecal - oral de aguas y alimentos. Se ha postulado como otra probable vía de transmisión la transplacentaria. Dentro del citoplasma de la célula epitelial intestinal sufre un proceso de reproducción asexual (merogonia) y sexual (gametogonia) dando origen a una nueva generación de esporas. Estos pueden diseminarse por sangre (libremente o en el interior de macrófagos) o linfa a diferentes órganos. La eliminación se realiza de acuerdo a la diseminación por materia fecal, orina, etc. Las esporas permanecen viables 4 meses promedio (18). El Microsporidium spp estimula la producción de anticuerpos, pero la respuesta microbicida es básicamente celular. Clínica: Las formas que afectan el tracto digestivo pueden producir diarrea crónica y afectar la vía biliar dando origen a colangitis. Otros pueden producir trastornos urinarios, conjuntivitis, sinusitis, bronquitis, hepatitis (19) y peritonitis. Habitualmente estos pacientes tienen recuentos de células CD4 menores a 50-100 mm³ , la infección tiende a autolimitarse con la elevación del número de células CD4 tras la administración de antiretrovirales. Aproximadamente un tercio de los pacientes infectados con Mycropsporidium spp. tienen concomitantemente otro patógeno, lo que dificulta su valoración como real agente etiológico. Un estudio de Rabeneck y col (20) comparó biopsias de pacientes HIV+, 55 con diarrea y 51 sin diarrea , y no halló diferencias significativas en infección por Microsporidium spp en ambos grupos , por lo cual sugiere que un estadio de portación precede a la enfermedad diarreica. Diagnóstico: Depende de la demostración morfológica del parásito, ya que faltan más ensayos clínicos para tener test serológicos y sondas moleculares confiables. La tinción tricrómica modificada por Weber y la tinción con fluorocromo Uvitex 2B, son usadas para la detección de esporas de este parásito tanto en extendidos de materia fecal como en aspirados duodenales básicamente en pacientes HIV+, con resultados comparables al diagnóstico por biopsia (21). La identificación definitiva de especie se realiza por microscopía electrónica y /o inmunofluorescencia con anticuerpos monoclonales (22). Tratamiento: Se utiliza el albendazol a 400 mg 2 veces por día durante 30 días para la forma E. intestinalis. La misma droga es efectiva para el E. hellem y E.cuniculi. La microsporidiosis diseminada debe ser considerada como una infección oportunista en el paciente con SIDA, particularmente si presenta: fiebre, dolor abdominal, diarrea y síntomas urinarios u oculares. Isospora belli La isosporidiosis humana es una infección del tracto gastrointestinal producida por un protozoario del grupo de los coccidios, llamado Isospora belli, del cual el ser humano es el único huésped definitivo.(6) Ciclo vital: La ingestión de los ooquistes de Isospora belli madurados en el medio ambiente determinan la infección, produciéndose luego la liberación de los esporozoitos que invadirán el epitelio intestinal. Se cumple en este la fase sexuada y asexuada del parásito para terminar dando origen a nuevos ooquistes no esporulados que son eliminados con las heces. Anatomía patológica del intestino delgado: En la infección intestinal por Isospora belli se observa aplastamiento y pérdida de microvellosidades, elongación de las criptas e infiltrado inflamatorio a nivel de la lámina propia. En el interior de los enterocitos, por microscopía electrónica, se evidencian vacuolas citoplasmáticas con microorganismos en su interior. Se ha documentado compromiso extraintestinal de ganglios linfáticos en pacientes con SIDA aunque este hallazgo es muy raro (23). Se desconocen con certeza los mecanismos por los cuales la Isospora belli produce diarrea. Clínica: En pacientes inmunocompetentes la infección varía desde cuadros asintomáticos a diarrea aguda autolimitada. En cambio en inmunocomprometidos pueden presentar: -Diarrea acuosa (desde autolimitada hasta crónica, sin moco, pus ni sangre). -Dolor abdominal crónico, hipertermia. -Anorexia y pérdida de peso -Malabsorción (generalmente asociada a las formas graves). La diarrea cursa con gran tendencia a la cronicidad y a las recidivas. Cursa siempre con eosinofilia, en ocasiones altas, aunque de acuerdo a la inmunodepresión puede presentar an-eosinofilia ,siendo en estos casos un índice de mal pronóstico Diagnóstico: Se basa en la visualización directa de ooquistes en muestras de materia fecal o con tinción de Kinyoun. Al igual que en la crytposporidiosis, la liberación de ooquistes se realiza en forma intermitente por lo cual se debe obtener más de una muestra. Los métodos de concentración pueden ser útiles para aumentar el rendimiento diagnóstico. Tratamiento: Contrariamente a la criptosporidiosis, la isosporidiosis responde rápidamente al tratamiento. Se puede lograr la curación clínica y parasitológica dentro de la semana de tratamiento con cotrimoxazol (160 mg de trimetroprima y 800 mg de sulfametoxazol durante 10 días). Inclusive las recidivas de los pacientes HIV positivo responden favorablemente a este tratamiento (5). La profilaxis secundaria en pacientes con SIDA permanece en controversia. Existen comunicaciones de tratamiento con pirimetamina, roxitromicina, metronidazol, quinacrina , nitrofurantoina. (24) y quinolonas (Ciprofloxacina) Cyclospora cayetanensis La cyclosporosis es la infección producida por la Cyclospora cayetanensis, coccidio que provoca un síndrome diarreico prolongado en pacientes inmunocompetentes e inmunocomprometidos. Basado en su morfología y en sus afinidades tintoriales , lo cual hizo dificil su clasificación, se propuso llamarlo Cyanobacterium-like o Coccidian-like body. Hasta el presente, se desconoce gran parte de su ciclo evolutivo y de su epidemiología. (25) Anatomía patológica: En la infección por Cyclospora se han observado varios cambios histológicos: - Inflamación aguda y crónica Alteraciones de la superficie epitelial - Diversos grados de atrofia de vellosidades Hiperplasia de las criptas La patogenia del daño intestinal aún no se ha establecido Clínica La sintomatología de la cyclosporosis es similar a la de los otros coccidios y microsporidios intestinales: malestar general y fiebre de 1 a 2 días al inicio, síndrome diarreico - entérico de magnitud y duración variables. Tiende a ser una infección autolimitada en el paciente inmunocompetente y de evolución prolongada en inmunodeprimidos. Diagnóstico: Los ooquistes de Cyclospora cayetanensis se observan con el microscopio óptico como esferas no refráctiles de 8 a 10 micrones de diámetro. Pero el diagnóstico de certeza se realiza mediante la tinción de Kinyoun y Visvesvara. También presentan una fuerte auto - fluorescencia cuando se las observa con luz ultravioleta. Tratamiento: Se trata la cyclosporosis con cotrimoxazol (trimetroprima 160 mg y sulfametoxazol 800 mg) 2 veces al día durante 7 días, obteniéndose una rápida respuesta terapéutica y una negativización del exámen coproparasitológico. Otros agentes: Blastocystis hominis: produce en esta población diarrea, generalmente líquida y excepcionalmente disentérica, acompañándose de dolor abdominal, náuseas, fiebre y eosinofilia. (26) Giardia lamblia: Aunque los pacientes con SIDA tengan una respuesta inmune alterada al parásito, no existe evidencia que en estos pacientes la diarrea sea más severa o prolongada como ocurre con otros protozoarios. (27) Ameba histolytica: Los pacientes con SIDA no parecen tener un riesgo aumentado de desarrollar amebiasis grave. (28) Por contraste, aquellos pacientes en los cuales su inmunocompromiso se relaciona con quimio terapia, corticoides y transplante tienen un gran riesgo de desarrollar colitis fulminante. (5) Strongyloides stercoralis: Esta geohelmintiasis puede producir en pacientes con SIDA cuadros diarreicos importantes e hiperinfección (5). Esta última puede producir sepsis por bacilos gram negativos que es la mayor causa de muerte en estos pacientes. (29) . El ciclo de autoinfección juega un importante protagonismo en esta población. Se debe insistir en la búsqueda de esta agente parasitario dado que a veces no es diagnosticado con el primer examen parasitológico . La terapéutica en las infecciones diseminadas presenta algunas modificaciones con respecto a la dosis y el tiempo de empleo , con respecto a los pacientes inmunocompetentes:. Tiabendazol en dosis de 50 mg/kg/día durante 7 a 10 días, albendazol 800 mg/día por 5 días o ivermectina 0,2 mg/kg durante 2 días. Se debe evaluar clínicamente al paciente y realizar exámenes parasitológicos para decidir , de acuerdo a los resultados , realizar una nueva serie de antiparasitarios. Métodos Diagnósticos Existen diversos métodos diagnósticos utilizados para el hallazgo de los distintos agentes etiológicos parasitarios que afectan el tracto gastrointestinal. Los empleados en la Sección Parasitología del Hospital de Infecciosas F. J. Muñiz, que han permitido contar con datos de prevalencia en la población HIV+ son normativas en forma parcial y total en varios centros asistenciales. Se detalla a continuación las mismas: Normatización diagnóstica de las parasitosis intestinales. Muestras a analizar: 1-Muestras seriadas de materia fecal conservadas en S.A.F. (acetato de sodio, ácido acético y formol). 2-Muestra fresca de materia fecal. 3-Escobillado anal o Test de Graham. 4-Material obtenido de zona duodenal por Enterotest o sondaje duodenal. Métodos diagnósticos: 1-Técnica de Tellemann (Concentración por centrifugación). 2-Técnica de Willis (Flotación en solución sobresaturada de Cl Na) 3-Observación directa (Examen en fresco-seriado-escobillado,etc) 4-Técnica de Baermann (Para diagnostico de Strongyloidosis). Diagnóstico coproparasitológico en diarreas en pacientes HIV/SIDA. -Muestras seriadas de materia fecal recolectadas en S.A.F. -Muestra fresca de materia fecal recolectada en solución fisiológica. -Enterotest o sondaje duodenal. Efectuar: 1-Observación directa - Giardias, Amebas, Helmintos , Isospora, otros coccidios , etc. 2-Técnica de Tellemann _ Tinción de Kinyoun (Cryptosporidium-Cyclospora-etc). _Tinción de Visvesvara (Cyclospora) * _Tinción de Wright-Giemsa (Dientamoeba fragilis).* _Tinción de Gram-Cromotrope (Microsporidium)* Tricromicas de Weber o Didier o Ryan Tinción tricromica de Wheatley (Amebiasis) Observaciones: Sugerimos investigar siempre Dientamoeba fragilis si el paciente presenta Enterobiosis o Ascariosis, aunque no presente diarrea. *Técnicas empleadas en nuestro servicio de parasitología con modificaciones, presentando óptimos resultados coincidiendo con los autores 3-Cryptosporidium: buscar además en A- Esputo o L.B.A B- Sondaje duodenal C- En caso de colecistectomia explorar Vesícula con coloraciones. 4-Cyclospora: Buscar ídem a A-B y C ( Autofluorescencia en microscopía de fluorescencia). Observaciones: Es necesario buscar cadena epidemiológica: Animales domésticos como perros, gatos , aves , etcétera. Diagnostico de Strongiloidosis Si las pruebas de concentración en materia fecal dan positivas para Strongyloides stercolaris (S.s) en pacientes HIV+ /SIDA u otros inmunocomprometidos, buscar además en : ESPUTO L.B.A ORINA Sangre por técnica de KNOTT* LCR Si existe importante sospecha de STRONGILOIDOSIS, y presenta por lo menos tres exámenes de materia fecal negativos, se debe efectuar técnica de Baermann. Si se cuenta con Enterotest efectuar dicha técnica. *En la sección parasitología se efectúa esta técnica en forma similar que para filariasis. Prevalencia En un estudio realizado en el Hospital de Enfermedades Infecciosas Francisco J. Muñiz sobre prevalencia de enteroparasitosis en pacientes VIH + (internados y ambulatorios ) se concluye, que el índice de positividad sobre 2463 pacientes cuyas muestras fueron remitidas al Servicio de Parasitología durante 1993-1996 fue de 32.5% ( 800 ). La prevalencia fue la siguiente : Parásitos oportunistas (marcadores) : Cryptosporidium spp. 37.6%, Isospora belli 3.5%. Parásitos potencialmente oportunistas : Blastocystis hominis 37.6 %, Giardia lamblia 17.8 %, Endolimax nana 9.7 %. Parásitos de repercución incierta : Strongyloides stercoralis 2.5 %, otros 5.5 %.(30) Estos pacientes presentaban diarrea o no, pero tenían como antecedente haber padecido este síntoma durante la evolución de la enfermedad. En estas series no fueron consideradas las diarreas por parásitos del filum Microsporidia y otros coccidios como Cyclospora, debido a que en ese período no se utilizaban técnicas especiales para su diagnóstico. En la actualidad la incorporación de técnicas rápidas y sencillas de tinciones ha permitido diagnosticar éstos últimos agentes. Informes preliminares refieren que pacientes SIDA afectados con síndrome diarreico presentan como causa una parasitosis intestinal en el 56.7 % de los casos (se evaluó un grupo de 37 pacientes ). Este índice de parasitación se ha logrado por la incorporación de técnicas tricrómicas y Gram cromotrope para el diagnóstico de Microsporidium y Visvesvara para Cyclospora cayetanensis. Los principales agentes hallados en este estudio fueron Microsporidium spp. (38%- 8 pacientes) y Cryptosporidium spp (33%- 7 pacientes). Se ha observado la presencia de un poliparasitismo (Cryptosporidium, Microsporidium, Cyclospora cayetanesis.) Estos resultados corresponden al primer trimestre de 1999 y fueron realizados en el servicio de parasitología del Hospital Muñiz.(31) En este nosocomio se han efectuado también diversos estudios de prevalencia en la población internada con SIDA, donde se destaca la estadística referida a pacientes femeninas durante el período 1990-94 parasitadas con Cryptosporidium spp (12,24%) e Isospora belli (2,55) sobre un número de 196 pacientes, hallándose Blastocystis hominis (71,87%) como agente parasitario más frecuentemente identificado. (32) Los estudios realizados en otros centros asistenciales como el Hospital Rawson de Córdoba y el Instituto de Infectología Emilio Ribas/Hospital de San Pablo Brasil , refieren un índice de parasitación entre el 40% y el 57%. Siendo los protozoarios intestinales los que ocupan los primeros lugares al igual que en el Hospital Muñiz Hospital Rawson, Córdoba (1996-97) N: 75 pacientes. Positivos 43 (57%) Blastocystis hominis Cryptosporidium spp Giardia lamblia Endolimax nana Chilomastix mesnilli Cyclospora cayetanensis 25,3% 24% 17,3% 10,6% 2,6% 1,3% Instituto Emilio Ribas- Hospital San Pablo, Brasil (1998)Dr Sergio CIMERMAN 200 muestras. Positivas: 80 (40%) Giardia Lamblia Entamoeba coli Cryptosporidium spp Endolimax nana Isospora belli Blastocytis hominis 16% 13% 7% 3,5% 2% 0,5% Conclusión Varios agentes infecciosos pueden producir enfermedad gastrointestinal y en particular diarrea en los pacientes con enfermedad por HIV. Las parasitosis entéricas son comunes dentro de esta población, adoptando características especiales respecto de la población general, no solo en los aspectos clínicos de las mismas sino también en su etiología. Agentes inocuos en la mayoría de los casos para el hospedero inmunocompetente plantean un verdadero desafío diagnóstico y terapéutico. Los clásicos exámenes en fresco y seriado de materia fecal procesados con técnicas de concentración adecuadas, permiten a través de la observación directa y el empleo de tinciones permanentes llegar al diagnóstico etiológico en la mayoría de los casos. El tratamiento de estas parasitosis en este grupo poblacional permanece todavía como un punto a resolver. La mayoría de los autores coinciden que las fallas de tratamiento y el alto índice de recaídas son el denominador común en estos pacientes. El empleo de la terapéutica combinada antiretroviral que permite disminuir la carga viral y aumentar las células involucradas en la inmunidad actuaría disminuyendo el índice de parasitación en el tracto gastrointestinal , en esta población como se ha observado en últimos estudios. BIBLIOGRAFIA 1- ROMERO CABELLO, R; HERRERA BENAVENTE, I: Síndrome Diarreico Infeccioso Cap 6-40 Edic 2002 Edit Medica Panamericana 2- GIULIODORO, N.: Características De Las “Inmunología”, 1990, Unidad Temática 3, P. 47, Mem Editora. Poblaciones Linfocitarias, En 3- SCOTT, D.: Organización Y Aspectos Celulares De La Respuesta Y La Regulación Inmunitarias, En Microbiología, Zinsser, 1995, Cap. 13, P. 344-65 Panamericana. 4- MATTEWSON, J. J. Y Col.: Intestinal Secretory Iga Immune Response Against Human Immunideficiency Virus Among Infected Patients Wiyh Acute And Chronic Diarrhea, J. Infect, Dis., RESTREPO, M.: Parasitosis Humanas, 2da. De, 1994, CIB. 5- BOTERO, D., RESTREPO, M.: Parasitosis Humanas, 2da. De, 1994, CIB. 6- RUBIN, R.; YOUNG, L.: Clinical Approach To Infection In The Compromised Host, Third Edition, 1994, Plenum Medical Book Company. New York And London. 7- SOAVE, R.; WEIKEL, C.: Cryptosporidium Y Otros Protozoarios Incluyendo Isospora, Sarcocystis, Balantidium Coli Y Blastocystis, En Enfermedades Infecciosas Principios Y Práctica, Mandel-Douglas Bennett, 3ra. Edición, Cap. P. 2253-61, Panamericana. 8- O’DONOGHUE, P.: Cryptosporidium And Crytpospordiosis In Man And Animals, Int. J. Paras, 1995, Vol 25 Nº2, P. 139-95. 9- MOHRI, H. Y Col., Case Report: Inhalation Therapy Of Paromomycin Is Effective For Respiratory Infection And Huypoxia By Cryptosporidium With AIDS, Am. J. Med. Sci., 1995, Jan. 309 (1), P. 60-2 10- GILLEN, A.: Illustrating Crytposporidium As A Newly Recognized Threat To Clean Water, The Am. Biology Teacher, 1995, Vol. 57, Nº 8, Nov/Dec. 11- GOODGAME, R. W. Y Col.: Intensity Of Infection In AIDS- Associated Cryptosporidiosis, J. Infect. Dis., 1993 Mar., 167 (3), P. 704-9. 12- Mc Anulty, J. M. Y Col.: A Community –Wide Outbreak Of Cryptosporidiosis Associated With Swimming At A Wave Pool, JAMA, 1994, 272: 1597-1600. 13- TZIPORI S. Y Col.: Paromomycin Treatment Against Cruptosporidiosis In Patients With AIDS, JID, Apr. 1995, 171 (4), 1069. 14- VERDON, R. Y Col.: Paromomycin For Crytposporidiosis In AIDS, JID, Apr. 1995, 171 (4), 1070. 15- FICHTENBAUN, C. J. Y Col.: Use Of Paromomycin For Treatment Of Cryptosporidiosis In Patients With AIDS, CID, 1993, 16: 298, 300. 16- NEILL, M. A. Y Col.: Cryptosporidiosis: An Unrecognized Cause Of Diarrhea In Ederly Hospitalized Patients, CID, 1996, 22:168-170 17- SHIELD, J. Y Col.: Bovine Colostrum Inmunoglobulin Cryptosporidiosis In AIDS, Arch. , Dis. Child, 1993 Oct. 69 (4), P. 451-3. Concentrated For 18- BRYAN, R.: Microsporidia, En Enfermedades Infecciosas Principios Y Práctica, Mandell-Douglas-Bennett, 3ra. Edición, Cap. 261, 2262-65, Panamericana. 19- CALI, A.: General Microsporidian Features And Recent Findings On AIDS Isolates, J. Protozoo, 1991, 38 (6), P. 625-30. 20- LECUIT, M.: Use Of Albendazole For Disseminated Microsporidian Infection In A Patient With AIDS, CID, 1994, 19: 332-3. 21- DE GIROLAMI, P. C. Y Col.: Diagnosis Of Intestinal Microsporidiosis By Examination Of Stool And Duodenal Aspirate With Weber’s Modified Trichrome And Uvitex 2B Strains, J. Clin. Microbiol. 1995, Apr. 33 (4), P. 805-10. 22- KOTIER, D. P. Y Col.: Light Microscopic Diagnosis Of Microsporidiosis In Patients With AIDS, Am. J. Gastroenterol., 1994, Apr. 89 (4), P. 540-4. 23- CAMARENA, J. J. Y Col.: Coccidios Intestinales, En Enfermedades Infecciosas Y Microbiología Clínica, Perea E. J., 1992, Vol. 2, Cap. 85, P. 1031-2. 24- FAIRA, J. A. Y Col.: Human Isosporidiasis Caused By Isospora Belli, Rev. Inst. Med. Trop. Sao Paulo, 1983, 251: 47-9. 25- ATIAS, A.: Parasitología Médica. 4ta. Edic. 1998. Mediterraneo. 26- MILLER, R.; MINSHEW, B.: Blastocystis Hominis: An Organism Of Serach Of A Disease, Rev. Inf. Dis., 1988, Sep.- Oct. Vol. 10, Nº5. 27- MARTINEZ MARTINEZ, L.: Flagelados Y Ciliados De Cavidades Naturales, En Enfermedades Infecciosas Y Microbiología Clínica, Perea E. J., 1992, Vol. 2, Cap. 78 P. 959. 28- RUBIN, R.; YOUNG, L.: Clinical Approach To Infection In The Compromised Host. Third Edition 1994, Plenum Medical Book Company. New York And London. 29- MAHMOUD, A.: Nematodos Intestinales (Vermes Cilíndrico) En Enfermedades Infecciosas. Principios Y Práctica, Mandell,-Douglas-Bernett, Cap. 263, P. 2271-72, Panamericana. 30- ABUIN, J. C. Y Col.: Prevalencia De Enteroparasitosis En Pacientes HIV+. Libro De Resúmenes. XIII Congreso Latinoamericano De Parasitología. La Habana, Cuba, 1997 P. 248-49. 31-ABUIN,J.C:Enteroparasitosis En SIDA. Libro De Resúmenes .3 Congreso Argentino De Parasitología. Mar Del Plata 2000,Pag144-147. 32- BELLEGARDE E.; MACIAS J. Y Col.: Libro De Resúmenes. Ier Congreso Latinoamericano De Zoonosis Bs. As. 1995, P. 167.