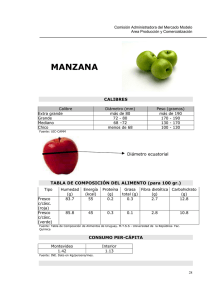
Malus domestica
Anuncio

XII CONGRESO NACIONAL DE CIENCIA Y TECNOLOGIA DE ALIMENTOS Jueves 27 y Viernes 28 de Mayo de 2010 Guanajuato, Gto. División Ciencias de la Vida Campus Irapuato-Salamanca ESTUDIO DE LA CONCENTRACIÓN DE QUERCETINA EN LAS VARIEDADES DE MANZANA (Malus domestica) FUJI, RED DELICIUS Y DELICIA a* a b a Navarro Cruz A. R. , Vera López O. , Muñoz Bedolla R. , Melgoza Palma N. , Lazcano a a a Hernández M. , Gómez Crisóstomo M. R. , Romero Vázquez M. b Departamento de Análisis Clínicos, Facultad de Ciencias Químicas, Benemérita Universidad Autónoma de Puebla, 14 Sur y San Claudio, Ciudad Universitaria, C.P. 72570, Puebla, Puebla a Departamento de Bioquímica-Alimentos, Facultad de Ciencias Químicas, Benemérita Universidad Autónoma de Puebla, 14 Sur y San Claudio, Ciudad Universitaria, C.P. 72570, Puebla, Puebla * rnavarro@siu.buap.mx RESUMEN: El estudio de los antioxidantes en frutas ha tomado mucho énfasis en la actualidad, particularmente la quercetina a la cual se le han atribuido múltiples beneficios para la salud. Entre las frutas que más se consumen en México por su accesibilidad, costo y versatilidad, se encuentra la manzana la cual presenta gran cantidad de antioxidantes -entre ellos quercetina- por lo que surge el interés de investigar el contenido de ésta en dichos frutos. El objetivo del presente trabajo fue realizar la evaluación del contenido de quercetina de tres variedades de manzana (Fuji, Red Delicious y Delicia), por medio del método de Espectrofotometría de luz visible. Se realizó la identificación de los flavonoides presentes en las diferentes muestras por medio de la reacción de Shinoda, y se determinó que la mayor concentración de flavonoides (contenido total de quercetina) se encuentra en la cáscara de la manzana mientras que la concentración en pulpa de manzana es mínima. En cuanto a las concentraciones de quercetina en las manzanas, la manzana Fuji presentó 0.29-1.65 mg/g, la Red Delicious 0.39-1.21 mg/g y la variedad Delicia 0.32-1.31 mg/g. De acuerdo con los datos anteriores, el contenido de quercetina puede considerarse igual en las diferentes variedades analizadas. ABSTRACT: The study of antioxidants in fruits has taken a strong emphasis now, particularly quercetin which have been attributed to many health benefits. Among the most consumed fruit in Mexico for its accessibility, cost and versatility, is the apple which has a large amount of antioxidants, including quercetin- hence the interest of investigating the contents into this fruit. The aim of this study was the assessment of the quercetin content of three varieties of apples (Fuji, Red Delicious and Delicious), by the method of visible light spectrophotometry. Was conducted to identify the flavonoids present in different samples by the reaction Shinoda, and determined that the highest concentration of flavonoids (total content of quercetin) was found in the peel of the apple while the concentration in pulp Apple is minimal. In relation to concentrations of quercetin in apples, Fuji apple presented 0.29-1.65 mg / g, the Red Delicious 0.39-1.21 mg / g range 0.32-1.31 Delicia mg / g. According to previous data, the content of quercetin can be considered equal in the different varieties. Palabras clave: Quercetina, antioxidantes, manzana FH1151 División Ciencias de la Vida Campus Irapuato-Salamanca XII CONGRESO NACIONAL DE CIENCIA Y TECNOLOGIA DE ALIMENTOS Jueves 27 y Viernes 28 de Mayo de 2010 Guanajuato, Gto. INTRODUCCIÓN: Los flavonoides son pigmentos naturales presentes en los vegetales y que protegen al organismo del daño producido por agentes oxidantes, como los rayos ultravioletas, la polución ambiental, sustancias químicas presentes en los alimentos, etc. El organismo humano no puede producir estas sustancias químicas protectoras, por lo que deben obtenerse mediante la alimentación o en forma de suplementos. Están ampliamente distribuidos en plantas, frutas, verduras y en diversas bebidas y representan componentes sustanciales de la parte no energética de la dieta human. Estos compuestos fueron descubiertos por el premio Nobel Szent-György, quien en 1930 aisló de la cáscara del limón una sustancia, la citrina, que regulaba la permeabilidad de los capilares. Los flavonoides se denominaron en un principio vitamina P (por permeabilidad) y también vitamina C2 (porque se comprobó que algunos flavonoides tenían propiedades similares a la vitamina C). Sin embargo, el hecho de que los flavonoides fueran vitaminas no pudo ser confirmado, y ambas denominaciones se abandonaron alrededor de 1950. Se estima que el número de flavonoides conocidos por la diversidad de su arquitectura molecular es de alrededor de 5000 sustancias entre los que se pueden destacar: 1. Citroflavonoides: quercitina, hesperidina, rutina, naranjina y limoneno. La quercetina es un flavonoide amarillo-verdoso presente en cebollas, manzanas, brócoles, cerezas, uvas o repollo rojo. 2. Flavonoides de la soja o isoflavonoides: están presentes en los alimentos con soja tales como porotos, tofu, tempeh, leche, proteína vegetal texturizada, harina, miso. 3. Proantocianidinas se localizan en las semillas de uva, vino tinto y extracto de corteza del pino marino. 4. Antocianidinas: son pigmentos vegetales responsables de los colores rojo y rojo-azulado de las cerezas. 5. Ácido elágico: es un flavonoide que se encuentra en frutas como la uva y en verduras. 6. Catequina: el té verde y negro son buenas fuentes. 7. Kaemferol: aparece en puerros, brócoles, rábano, endibias y remolacha roja. Las estructuras básicas de los principales grupos flavonoides (flavanos, flavonoles, flavonas, antocianidinas ),(figura 1). Las diferencias entre grupos se han establecido por el grado de aromaticidad, el ordenamiento y el número de hidroxilos sustitutos, así como la extensión y tipo de glicosilación de estos grupos. El sitio de glicosilación preferida es en la posición 3 y la glucosa constituye el residuo más usual. Otros residuos son galactosa, xilosa, etcétera. FH1152 División Ciencias de la Vida Campus Irapuato-Salamanca XII CONGRESO NACIONAL DE CIENCIA Y TECNOLOGIA DE ALIMENTOS Jueves 27 y Viernes 28 de Mayo de 2010 Guanajuato, Gto. FIGURA 1. Flavonoides, estructuras básicas y tipos Los flavonoides contienen en su estructura química un número variable de grupos hidroxilo fenólicos y excelentes propiedades de quelación del hierro y otros metales de transición, lo que les confiere una gran capacidad antioxidante. Tres características estructurales son importantes para su función: a) La presencia en el anillo B de la estructura catecol u O-dihidroxi; b) La presencia de un doble enlace en posición 2,3; c) La presencia de grupos hidroxilo en posición 3 y 514. La quercetina presenta las tres características mientras que la catequina solo presenta la segunda y la diosmetina la primera. Además de sus conocidos efectos antioxidantes, los flavonoides presentan otras propiedades que incluyen la estimulación de las comunicaciones a través de las uniones en hendidura, el impacto sobre la regulación del crecimiento celular y la inducción de enzimas de destoxificación tales como las monooxigenasas dependientes de citocromo P-450, entre otra. Aunque los hábitos alimenticios son muy diversos en el mundo, el valor medio de ingesta de flavonoides se estima como 23 mg/día, siendo predominantes los flavonoles especialmente la quercetina. Las fuentes alimenticias principales de los flavonoles son, entre otras, el té negro, las cebollas, las manzanas, la pimienta negra —que contiene cerca de 4 g/kg de quercetina—, y bebidas alcohólicas como vino y cerveza. La ingesta promedio de flavonoles y flavonas se sitúa entre los 20 y 26 mg/día. Excede, por tanto, a la de otros antioxidantes en la dieta, tales como el beta-caroteno (2-3 mg/día) y la vitamina E (7-10 mg/día) y es igual aproximadamente a un tercio de la vitamina C (70-100 mg/día). En estudios epidemiológicos se ha demostrado que con el consumo incrementado de frutas y vegetales se experimenta una reducción del 50% en el riesgo de cánceres digestivos y de las vías respiratorias. La capacidad de los polifenoles vegetales para actuar como antioxidantes en los sistemas biológicos fue ya reconocida en los años treinta; sin embargo, el mecanismo antioxidante fue ignorado en gran medida hasta hace poco tiempo. El creciente interés en los flavonoides se debe a la apreciación de su amplia actividad farmacológica. En experimentos in vitro se ha confirmado el papel protector de la quercetina, la cual ejerce efectos de inhibición frente a células cancerígenas en humanos: en colon, glándula mamaria y ovario, en región gastrointestinal y en la leucemia. FH1153 División Ciencias de la Vida Campus Irapuato-Salamanca XII CONGRESO NACIONAL DE CIENCIA Y TECNOLOGIA DE ALIMENTOS Jueves 27 y Viernes 28 de Mayo de 2010 Guanajuato, Gto. METODOLOGÍA: Obtención y preparación de la muestra Las muestras de manzanas fueron obtenidas de tres diferentes puntos de la ciudad de Puebla. Fueron utilizadas las manzanas que presentaban mayor maduración así como coloración rojiza obteniendose de manera aleatoria por selección organoleptica, de las variedades Red Delicious, Fuji y Delicia. De las manzanas se tomó una muestra de cáscara con la ayuda de un pelador quitando la capa de pulpa adherida a la piel. Se pesó 1 gramo de cáscara con ayuda de la balanza analítica. Protegiendo de la luz se colocó 1 gramo de cáscara de manzana más 10 mL de alcohol absoluto en el mortero y se molió. Identificación de flavonoides por reacción de Shinoda Tomando una alícuota de la molienda anterior se colocó en un tubo de ensayo y se agregó de dos a tres virutas de magnesio y unas gotas de ácido clorhídrico concentrado, observando la coloración característica (azul magenta, violeta o rojo) en presencia de flavonoides o incolora en ausencia de estos. Se utilizó como control negativo agua destilada. Extracción alcohólica En un embudo de separación previamente forrado de papel negro para evitar el paso de la luz se colocaron 10 mL de muestra obtenida en la molienda, agregando 2.5 mL de agua y 7.5 mL de cloroformo, se tapó y se agitó vigorosamente permitiendo la salida de gas y a continuación dejando en reposo de forma vertical hasta la separación de fases, cada una de estas fases fueron obtenidas de la extracción con ayuda de un embudo de plástico y papel filtro, la fase cloroformica fue filtrada para retener las partículas grandes y así evitar variaciones en la lectura. Lectura Se colocaron 1.5 mL de la fase cloroformica, 0.5 mL de acetato de potasio 1M, 0.5 mL de nitrato de aluminio 10% y 7.5 mL de alcohol etílico absoluto. Se tomó una alícuota y colocándola en una celda de cuarzo se llevó a lectura en el espectrofotómetro a 415 nm anotando los resultados. Las absorbancias obtenidas en las determinaciones fueron interpoladas para poder determinar la concentración por medio de una curva de calibración de un estándar de quercetina. Los estudios UV-Vis fueron realizados utilizando celdas de cuarzo de 3 mL de capacidad, 1 cm de paso de luz, a temperatura ambiente, en un tiempo máximo de 60 segundos por lectura. Análisis de datos Los datos que se obtuvieron durante la lectura se analizaron mediante el método de Análisis estadístico de Kruskal Wallis. . FH1154 División Ciencias de la Vida Campus Irapuato-Salamanca XII CONGRESO NACIONAL DE CIENCIA Y TECNOLOGIA DE ALIMENTOS Jueves 27 y Viernes 28 de Mayo de 2010 Guanajuato, Gto. RESULTADOS Y DISCUSIÓN: Los extractos obtenidos fueron óptimos para la realización del ensayo, ya que por las propiedades de polaridad de los flavonoides y los solventes utilizados se facilitó la extracción correcta de los mismos. Al realizar una comparación de la concentración de quercetina en los lotes de manzana Fuji se observa según el estudio estadístico de la concentración que no hay diferencias significativas entre los lotes, esto se puede deber a que las manzanas son provenientes de lugares cercanos lo que permite una mejor conservación de sus propiedades entre ellas la concentración de flavonoides. De la misma manera al comparar los lotes de la manzana Red Delicious se observa que no hay diferencias en la concentración de quercetina. En los lotes de manzana Delicia la concentración de quercetina no tiene diferencias significativas pudiendo deberse a las condiciones en que se mantiene la fruta en un supermercado. Se observó que la concentración de flavonoides expresada como concentración total de quercetina no varía entre especies de manzana ni entre lotes ya que al realizar el análisis estadístico de Kruskal Wallis se notó que no existen diferencias significativas en las concentraciones de quercetina de las diferentes especies de manzana. Por lo anterior se puede decir que para estos lotes no importan las condiciones de transporte, condiciones y tiempo de almacenamiento en la concentración de flavonoides, del mismo modo no importa la especie de la manzana ya que las concentraciones son similares. En la figura 1 se muestran las concentraciones determinadas de quercetina. Con la finalidad de determinar si la mayor concentración de quercetina se encontraba en cáscara o en pulpa, se probaron los extractos de cáscara sola y cáscara con pulpa, se determinó que la mayor concentración de flavonoides (contenido total de quercetina) se encuentra en la cáscara de la manzana mientras que la concentración en pulpa de manzana es mínima. FH1155 XII CONGRESO NACIONAL DE CIENCIA Y TECNOLOGIA DE ALIMENTOS Jueves 27 y Viernes 28 de Mayo de 2010 Guanajuato, Gto. División Ciencias de la Vida Campus Irapuato-Salamanca CON PULPA 1.4 SIN PULPA 1.2 CONCENTRACIÓN 1 0.8 0.6 0.4 0.2 0 FUJI RED DELICIOUS DELICIA Figura 1. Comparación de concentración de quercetina en manzana con pulpa y sin pulpa. CONCLUSIONES: La mezcla más adecuada para la extracción de la quercetina fue una solución de cloroformo-alcohol ya que facilitó la extracción y evitó pérdidas significativas. Fue posible la identificación cualitativa de los flavonoides por medio de la reacción de Shinoda. No existió diferencia significativa en la concentración de flavonoides si se considera el fruto completo o únicamente la cáscara, no hubo diferencia en la concentración tampoco entre los tres tipos de manzana y tampoco parece ser importante el lugar de compra. Además, de acuerdo con las concentraciones determinadas, con el consumo de 12 manzanas diariamente se puede cubrir las ingestas diarias más probablemente recomendadas de quercetina. REFERENCIAS: Bors W, Heller W, Michel C, y col.: Flavonoids and polyphenols: chemistry and biology. In Handbook of Antioxidants (eds. Packer L, and Cadenas E), pp 409-466, Marcel Dekker Inc., 1996. New York. FH1156 División Ciencias de la Vida Campus Irapuato-Salamanca XII CONGRESO NACIONAL DE CIENCIA Y TECNOLOGIA DE ALIMENTOS Jueves 27 y Viernes 28 de Mayo de 2010 Guanajuato, Gto. Rice-Evans CA, Miller NJ, Paganga J: Structure antioxidant activity relationships of flavonoids and phenolic acids. Free Rad Biol Med 1996; 20: 933-956. Ross JA y Kasum CM: Dietary flavonoids: Bioavailability, metabolic effects, and safety. Ann. Rev Nutr, 2002, 22:19-34. Havsteen B: Flavonoids. A class of natural products of high pharmacological potency. Biochem Pharmacol, 1983, 32:1141-1148. Pace-Asciak CR, Hahn S, Diamandis EP, Soleas G y Goldberg DM.: The red wine phenolics transresveratrol and quercitin block human platelet aggregation in eicosanoid synthesis: implication for protection against coronary heart disease. Clin Chim Acta, 1995, 235:207-219. Jang M, Cai L, Udeani GO y cols.: Cancer chemopreventive activity of resveratrol, a natural product derived from grapes. Science, 1997, 275:218-221. Stahl W, Ale-Agha N y Polidori MC: Non-antioxidant properties of carotenoids. Biol Chem, 2002, 383:553-558. Hertog MGL, Hollman PCH y Putte van de B: Content of potentially anticarcinogenic flavonoids of tea, infusions, wines, and fruit juices. J Agric Food Chem, 1996, 41:1242-1246. Rimm ER, Katan MB, Ascherio A, Stampfer M y Willet W.: Relation between intake of flavonoids and risk for coronary heart disease in male health professionals. Ann Intern Med, 1996, 125:384389. Hollman PCH y Katan MB: Absortion, Metabolism, and Bioavailabiliy of Flavonoids. En: Flavonoids in Health and Disease. Ed. Marcel Dekker, INC. New York, 1998, 22:483-522. Manach C, Texier O, Morand C y cols.: Compartion of the bioavailability of quercetin and catequin in rats. Free Rad Biol Med, 1999, 27:1259-1266. Rice-Evans CA, Miller NJ y Paganga J: Structure antioxidant activity relationships of flavonoids and phenolic acids. Free Rad Biol Med, 1996, 20:933-956. Cody V, Middleton E, Harborne JB y cols.: Plant flavonoids in biology and medicine. Biochemical, pharmacological and structure-activity relatioships. Alan R Liss, New York, 1998. Teofili L, Pierlli L y Lovino MS.: The combination of quercetin and cytosine arabinoside synergistically inhibits leukemic cell growth. Leukemia Res, 1992, 16:497-503. FH1157