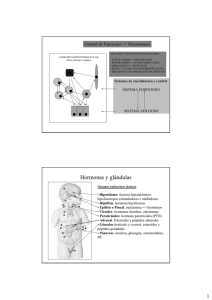
SISTEMA ENDOCRINO
Anuncio

FACULTAD DE CIENCIAS VETERINARIAS Y AMBIENTALES FISIOLOGÍA VETERINARIA SISTEMA ENDOCRINO APUNTES TEÓRICOS – 20 AÑO PROFESOR TITULAR PABLO VALLEJOS PROFESOR ADJUNTO DIEGO GRILLI JTP ANAMARIA GIANOLINI M. VERÓNICA SABATINI 2015 SISTEMA ENDOCRINO INTRODUCCION El organismo esta regulado por dos grandes sistemas que interaccionan entre si coordinando y controlando las funciones del cuerpo, estos son, el Sistema Nervioso que se encarga de las actividades que requieren un control rápido ( milisegundos a segundos) y el Sistema Endocrino cuyas acciones son lentas y sus efectos duran de minutos a días. Así tenemos diferentes tipos de mensajeros que funcionan como medios de comunicación entre dos o más células y son los siguientes: Neurotransmisores: son liberados por los axones terminales de las neuronas en las uniones sinápticas y actúan localmente. Sustancias Endocrinas: son producidas por glándulas o tejidos especializados y secretadas al torrente sanguíneo. Su función la ejercen en células diana ubicadas en diferentes lugares del organismo. Sustancias Neuroendocrinas: secretadas por neuronas hacia la sangre su lugar de acción es en diferentes células del organismo. Sustancias Paracrinas: son secretadas al líquido intersticial e influyen sobre células adyacentes. Sustancias Autocrinas: secretadas al intersticio pero actúan sobre las mismas células que las fabrican. Citocinas: secretadas al intersticio pero pueden funcionar como agentes paracrinos, autocrinos o endocrinos. El sistema endocrino comprende el conjunto de órganos y tejidos que permiten coordinar y regular procesos fisiológicos a través de la producción de verdaderos MENSAJEROS QUIMICOS llamados HORMONAS que intervienen en la regulación de casi todas las funciones incluidos metabolismo, crecimiento y desarrollo, equilibrio hidro-electrolítico, reproducción y comportamiento. HORMONAS: definición actual. “Compuestos químicos secretados en mínimas concentraciones al torrente sanguíneo por glándulas de secreción interna, y que actúan en células distantes al lugar de origen, donde se unen a receptores específicos y producen una respuesta biológica.” ORGANOS ENDOCRINOS CLÁSICOS: Hipotálamo, hipófisis, gl. pineal, tiroides, paratirotdes, páncreas endocrino, adrenales, gónadas. ORGANOS ENDOCRINOS NO CLÁSICOS: Cerebro, pulmón, corazón, hígado, riñón, tracto gastrointestinal, endotelio. CLACIFICACION DE LAS HORMONAS Las hormonas se pueden clasificar de diferentes maneras: 1. Según su naturaleza química y solubilidad (proteicas, esteroideas, amínicas y ácidos grasos cíclicos). 2. Según la ubicación de los receptores y la naturaleza de la señal utilizada: A) Grupo I, hormonas que se fijan a receptores intracelulares. B) Grupo II, hormonas que se fijan a receptores localizados en la superficie celular. NATURALEZA QUÍMICA DE LAS HORMONAS De acuerdo con su naturaleza química, las hormonas pueden clasificarse en cinco categorías: 1. Esteroides: Químicamente derivan del colesterol. A este grupo pertenecen glucocorticoides, aldosterona y andrógenos de la corteza adrenal, estrógenos y progesterona del ovario, testosterona del testículo y 1,25 dihidroxicolecalciferol D3, metabolito activa de vitamina D3. Su naturaleza es lipófila por lo que estas hormonas atraviesan con facilidad las membranas celulares. No se almacenan en el citosol excepto la vitamina D. Su síntesis implica la presencia de un conjunto enzimático (P450) dependiente del Calcio iónico presente en las células glandulares, que hidrolizan la molécula de colesterol. En sangre deben ser transportadas en asociación con proteínas. 2. Derivados de aminoácidos: Aminas: Tiroxina y triyodotironina de la tiroides son derivados de tirosina, la melatonina de la glándula pineal es producida a partir de triptófano. Las hormonas tiroideas son liposolubles y atraviesan membranas por difusión. Aminas modificadas: Adrenalina o epinefrina y noradrenalina o norepinefrina (catecolaminas) de la médula adrenal. Las catecolaminas son solubles en medio acuoso, en sangre circulan libres o débilmente unidas a albúmina. No penetran en las células blanco. 3. Derivados de ácidos grasos: prostaglandinas, tromboxanos y leucotrienos, llamados genéricamente eicosanoides, se originan de ácidos grasos poliinsaturados. El ácido araquidónico es el precursor más importante. Sus acciones primarias son de tipo autocrino o paracrino. 4. Péptidos: Están formadas por menos de 100 aminoácidos. En esta categoría se incluyen los factores reguladores y las hormonas vasopresina y oxitocina del hipotálamo, corticotropina (ACTH) y hormona melanocito estimulante (MSH) de la adenohipófisis, glucagón del páncreas, gastrina, secretina, pancreozimina y otras hormonas del tracto gastrointestinal y calcitonina de la tiroides. 5. Proteínas: Formados por 100 o más aminoácidos. Hormona paratiroidea, insulina del páncreas, prolactina(PR), foliculoestimulante(FSH), luteinizante(LH), hormona de crecimiento(GH)y tirotrófica(TSH) de adenohipófisis son de naturaleza proteica. Las hormonas proteicas y peptídicas son sintetizadas en ribosomas asociados al retículo endoplasmático rugoso (RER). Inicialmente se produce una preprohormona de gran tamaño. Luego una peptidasa presente en la pared del RER provoca la escisión de una porción de la molécula transformándola en una molécula de menor tamaño llamada prohormona que se libera en la luz del RER en vesículas que se trasladan al Aparato de Golgi donde enzimas la vuelven a escindir y la transforman en Hormona madura, luego se almacenan en gránulos secretores en el citoplasma celular. Las hormonas son liberadas por exocitosis. Este proceso en algunos casos requiere como estímulo el aumento de Calcio intracelular y en otros la estimulación de un receptor de la membrana que eleva la concentración de AMPc. Son solubles en medio acuoso y en su mayoría, circulan libres en sangre. REGULACION HORMONAL Patrones de secrecion hormonal. Circadiano: permite sincronizar a los ritmos ambientales que posean un valor de periodo entre 20 y 28 horas, como son los ciclos de luz y de temperatura. El ciclo circadiano cambia según las condiciones diversas de vida que producen un cambio significativo tanto de día o de noche. Ultradiano: denota actividades biológicas que ocurren en ciclos fisiológicos de 20 horas o menos. Por ej. La prolactina. Semanal: ej. Estradiol, progesterona Estacional: ej. Melatonina, testosterona. Retroalimentación El mecanismo de control que utilizan la mayoría de las hormonas es por medio de retroalimentación o feed-back, el cual tiene la característica de reconocer sus propias señales. Existen dos tipos de retroalimentación hormonal: 1. Feedback positivo: es aquel en el cual la secreción de una sustancia estimula positivamente la secreción de otra, como ejemplo tenemos el Incremento de los estrógenos en la primera mitad del ciclo hormonal que produce aumento de la producción de la LH u hormona luteinizante para favorecer la ovulación. 2. Feedback negativo es cuando la elevación de la producción de una sustancia o la cantidad en el torrente sanguíneo se eleva produce la inhibición de esta sustancia, cuando existe cantidades suficientes en el torrente sanguíneo para cumplir con sus funciones biológicas, es capaz de informar que su efecto biológico ha sido o está por conseguirse y por lo tanto la cantidad de hormona que debe seguir produciéndose y liberándose debe disminuir. Este tipo de mecanismo de control de Feedback Negativo es probablemente el más utilizado por los sistemas hormonales. Este Feedback Negativo puede sub clasificarse en tres tipos: Feedback de Asa Larga: una glándula regula otra glándula que regula a una tercera glándula que regula a la primera glándula, por lo que en el eje están involucradas tres glándulas. En este intervienen glándula, hipófisis e hipotálamo. Feedback de asa corta: una glándula regula a otra glándula que regula a la primera glándula, por lo que en el eje están involucradas sólo dos glándulas. En este tipo solo intervienen hipófisis e hipotálamo Feedback de asa ultra corta: una glándula se regula a si misma. TIPOS DE ACCIONES PROMOVIDAS POR HORMONAS La acción de una hormona comienza con su unión a un receptor específico de la célula efectora, esto desencadena una cascada de reacciones que provocan una respuesta final. Las células que carecen de receptores para una hormona no responden a ella. Pese a la variedad de hormonas y a la variedad de respuestas que cada una de ellas suscita en el órgano efector, las acciones pueden agruparse en tres categorías: 1) transporte de membrana, 2) actividad de enzimas presentes en la célula y 3) síntesis de proteínas. 1. ACCIÓN SOBRE MECANISMOS DE TRANSPORTE DE MEMBRANA CELULARES: Algunas hormonas modifican el flujo de metabolitos o iones a través de membranas por su acción sobre sistemas de transporte o canales iónicos. 2. MODIFICACIÓN DE LA ACTIVIDAD ENZIMÁTICA: Esta acción es rápida y de carácter transitorio. Se ejerce principalmente a nivel de enzimas regulatorias cuya actividad es aumentada o disminuida 3. ACCIÓN SOBRE LA SÍNTESIS DE PROTEINAS: Muchas hormonas modulan la síntesis de enzimas y otras proteínas. Actúan predominantemente a nivel del ADN nuclear, regulando el proceso de transcripción génica. Esta acción requiere mas tiempo para manifestarse que la anterior y tiene efectos mas sostenidos. La misma hormona puede poner en marcha más de uno de los mecanismos señalados. Por ejemplo, la insulina favorece el transporte de determinados metabolitos a través de membranas, modifica la actividad de enzimas y también la síntesis de proteínas. Todos los mecanismos están estrechamente relacionados y dan lugar a interacciones. Por ejemplo, los efectos sobre sistemas de transporte de membrana pueden determinar el ingreso a la célula de sustancias con capacidad para modular la actividad de enzimas o la transcripción del núcleo. Asimismo un efecto directo sobre enzimas determina cambios en la disponibilidad de sustratos para el funcionamiento de vías metabólicas o afectan procesos de síntesis de proteínas o de transporte de membrana. Esta interrelación de los distintos mecanismos torna difícil, a veces, establecer con exactitud cual es la acción primaria asignable a la hormona. RECEPTORES El concepto de receptor es aplicable a las macromoléculas o asociaciones macromoleculares, que unen selectivamente hormonas, neurotransmisores, factores de crecimiento, citoquinas, y otras moléculas que inducen en ellos un cambio conformacional e inician las acciones determinadas del efecto final. La especificidad de las hormonas y su capacidad para identificar el blanco son posibles gracias a la presencia de Receptores en las células efectoras a los cuales la hormona se fija selectivamente en virtud de una estrecha adaptación conformacional y de complementariedad estructural. La hormona (H) y su receptor (R) forman un complejo (HR) que presenta las siguientes características: a) Adaptación inducida: la fijación de la hormona al receptor implica una adaptación estructural recíproca de ambas moléculas. b) Saturabilidad: El número de receptores existentes en una célula es limitado. c) Reversibilidad: La unión hormona –receptor es reversible El carácter y naturaleza de la respuesta dependen de la especialización funcional de la célula ‘’Blanco’’. A veces una misma hormona desencadena respuestas diferentes en células distintas. Por ejemplo, la adrenalina produce activación de la glucógeno lisis en músculo esquelético y estimula la lipólisis en adipositos. Se denominan Agonistas los compuestos de estructura semejante a la del agente fisiológico (hormona, neurotransmisor) con capacidad para unirse al receptor y provocar respuesta. Esta puede ser de igual, mayor, o menor intensidad que la inducida por el agente natural. Los Antagonistas se fijan al receptor, pero no producen respuesta. Se comportan como inhibidores competitivos. Localización de los receptores: Los receptores de hormonas pueden estar ubicados en el interior de la célula, ya sea en el citoplasma o en el núcleo, o en la membrana externa. Hormonas de carácter liposoluble, como tiroideas, los esteroides, metabolitos de vitamina D y ácidos retinoicos, atraviesan con facilidad las membranas y se unen a receptores intracelulares. Las de naturaleza proteica o peptídica o de moléculas pequeñas se fijan a receptores en la superficie de la célula blanco. Los eicosanoides, a pesar de su solubilidad en lípidos se unen a receptores de superficies celulares. La membrana no es un dispositivo rígido sino dotado de un alto grado de fluidez, gracias a la cual las proteínas asociadas a la membrana tienen libertad para desplazarse en todas direcciones del plano formado por la doble capa, por ello, se habla de Receptores móviles. Algunas hormonas fijadas a receptores de membrana plasmática son internadas en la célula por endocitosis Números de Receptores: El número de receptores de un tipo de terminado en la superficie de una célula puede variar entre 10.000 y 20.000. La cantidad de receptores intracelulares es generalmente mucho menor. No es necesario que la totalidad de los receptores de la célula esté unida a hormona para obtener una respuesta máxima. Comúnmente esto ocurre cuando alrededor del 20% de los receptores está ocupado por hormona. El resto corresponde a los llamados Receptores de reserva. La cantidad de receptores para un determinado ligando varía en distintos estados fisiológicos. Generalmente la concentración de hormona presente regula la cantidad de receptores específicos en las células blanco. Un aumento sostenido del nivel de hormona provoca disminución del número de receptores disponibles. En algunos casos de receptores de membrana, la disminución de receptores se realiza mediante un proceso de internación de receptores por endocitosis y posteriormente degradación en lisosomas. La disminución absoluta o relativa de la actividad de receptores puede obedecer a causas patológicas, ya sean alteraciones genéticas (mutaciones) que afectan la proteína del receptor o de algunos de los eslabones del sistema de transmisión de señales mas allá del receptor, o a procesos autoinmunes en los cuales se producen anticuerpos contra un receptor determinado. RECEPTORES INTRACELULARES: Las hormonas esteroides, tiroides, ácidos retinoicos y metabolitos activos de vitamina D3, al ser liposolubles, ingresan a través de las membranas de todas las células y son retenidas en aquellas que poseen en su interior receptores específicos. Estos receptores son estructuras proteicas que poseen varios dominios de interacción receptor-DNA, receptor-ligando, y receptor-receptor. Dominio DBD: La interacción receptor-DNA generalmente ocurre a través de un sitio central en la estructura del receptor identificado como dominio de interacción con el DNA o DBD (del inglés: DNA Binding Dominium). Dominio LBD: es el sitio o lugar de unión a la hormona Dominio NH2: es una región de transactivación que modula la efectividad con que puede unirse al ADN y, por tanto, potenciar la transcripción RECEPTORES ESTEROIDEOS Los receptores específicos de mineralocorticoides, glucocorticoides, estrógenos, andrógenos y progesterona se encuentran en el núcleo formando un complejo con proteínas que los mantienen en estado inactivo. Algunos de los receptores mencionados, especialmente, los de glucocorticoides, pueden hallarse también en el citoplasma. En ausencia de hormona esteroidea, los receptores están unidos en un complejo que contiene proteínas conocidas como proteínas de choque térmico o de calor (HSPs del inglés Heat Shock Proteins). Al llegar la hormona, se une con gran afinidad a su receptor específico y desplaza a las proteínas que lo mantiene inhibido. El receptor sufre un cambio conformacional, y se fija a sitios definidos del ADN llamados Elemento de respuesta a la hormona que activan o reprimen la transcripción de genes específicos y la formación de ARN mensajero. El dominio DBD posee dos dedos de Zinc capaces de interactuar con secuencias específicas del ADN. (Elemento de respuesta a la hormona) RECEPTORES DE MEMBRANA PLASMÀTICA: Los receptores de superficie en la membrana plasmática son transmisores de señales al interior de la célula. La llegada de una molécula de hormona, considerada el primer mensajero en el sistema de señales, produce cambios conformacionales en su receptor específico, los cuales son transmitidos a proteínas efectoras (enzimas o canales), y, en algunos casos se producen moléculas de pequeño tamaño (segundos mensajeros) que difunden rápidamente y hacen más efectiva la propagación de la señal en el interior de la célula. Hormonas diferentes, que actúan en células distintas y suscitan respuestas muy disímiles, suelen utilizar los mismos intermediarios para cumplir su acción. Por esta razón, el repertorio de sistemas transmisores de señales es más reducido que el de hormonas. RECEPTORES UNIDOS A CANALES IÓNICOS: Los neurotransmisores como Acetilcolina y Noradrenalina se combinan con receptores de la membrana pos sináptica, esto genera un cambio estructural de los receptores que generalmente consiste en la apertura o el cierre de un canal iónico (Na, K, Ca, etc.). Los movimientos de estos iones es lo que provoca los efectos en la célula pos sináptica. RECEPTORES ASOCIADOS A PROTEÍNAS G: Pertenecen a numerosa familia de receptores de superficie que comparten una estructura molecular similar; son una proteína de membrana integral con forma de serpentina que atraviesan la membrana siete veces y se unen a una proteína G, llamadas así por su propiedad de unirse a nucleótidos de guanina (GDP o GTP), también tienen actividad GTP-asa, es decir que tienen la capacidad de hidrolizar GTP Y formar GDP + un P libre. Juegan un papel esencial en sistemas de transmisión de señales. Sirven de nexo entre receptores de membrana y proteínas efectoras dentro de la célula. Las proteínas G son heterotriméricas, es decir, que están formadas por tres subunidades α, β y γ. Están adosadas a la cara interna o citosólica de la membrana, a la cual se mantiene anclada por la subunidad γ que se fija a la doble capa lipídica. Cuando un ligando se une al receptor se inicia una cadena de señales en la cual la proteína G representa el segundo eslabón. La subunidad α posee el sitio que fija con alta afinidad a nucleótidos de guanina (GDP o GTP). Mientras está unida a GDP se mantiene firmemente asociada al conjunto β-γ para integrar el heterotrímero, que es inactivo. La llegada de hormona al receptor de membrana promueve en este un cambio conformacional que permite su interacción con la proteína G inactiva. Se produce entonces liberación de GDP e ingreso de GTP que proviene del citosol a la subunidad α. El complejo α-GTP se disocia del dímero β-γ y adquiere actividad moduladora sobre la proteína efectora que le sigue en el sistema de señales. El mecanismo general de acción de receptores acoplados a proteínas G es el siguiente: a) La unión de hormona al receptor induce en este un cambio conformacional que le permite interactuar con una proteína G en la cara interna de la membrana b) La proteína G, unida a GDP en su estado de inactivo , reemplaza el GDP por GTP y se activa c) La proteína G activada estimula una enzima localizada en la membrana , que cataliza la producción de segundos mensajeros d) El segundo mensajero provoca cambios en determinadas proteínas celulares responsables de la respuesta final. RECEPTORES PROTEÍNA-TIROSINA-QUINASA: Los receptores acoplados a proteínas G requieren la mediación de éstas para modificar la actividad de enzimas integrantes del sistema de señales. En cambio, existen receptores con actividad catalítica en su propia molécula y otros asociados directamente a enzimas. RECEPTORES CON ACTVIDAD TIROSINA QUINASA INTRÍNSECA La insulina y numerosos factores de crecimiento se unen a receptores de este tipo en la membrana celular. En su mayoría están constituidos por una cadena polipeptídica cuyo extremo N-terminal, extracelular, posee el sitio de unión del ligando, la porción citosólica, correspondiente al segmento C-terminal, donde se encuentra el sitio activo de tirosina quinasa. .La fijación del ligando al dominio extracelular de estos receptores produce un cambio conformacional que induce dimerización de la tirosina quinasa. Se produce fosforilación cruzada de una cadena a otra en varios restos tirosina del dominio citosólico, se habla de autofosforilación del receptor. Como resultado de estas fosforilaciones aumenta aún más la actividad de la quinasa y se crean sitios a los cuales pueden unirse otras proteínas que actúan como eslabones en la cadena de transmisión de la señal. RECEPTORES ASOCIADOS A TIROSINA QUINASA EXTRÍNSECA: Existe otra familia de receptores sin actividad tirosina quinasa propia, pero con capacidad para asociarse a proteína-tirosina quinasas del citoplasma. Este grupo incluye los receptores de citoquinas y de algunas hormonas proteicas (ej.: hormona de crecimiento, prolactina). Son semejantes en estructura a los receptores proteínatirosina quinasa descriptos, aunque no presentan sitio catalítico. Cuando el ligando se fija al dominio extracelular se produce dimerización y la porción citosólica interacciona con tirosina quinasa. El resultado es prácticamente el mismo que el descripto para receptores con tirosina quinasa incluida en su molécula. SISTEMAS DE TRANSMISIÓN DE SEÑALES: “SEGUNDOS MENSAJEROS” La mayoría de las proteínas G activan y/o estimulan un canal iónico o una enzima para traducir el mensaje dentro del citoplasma. A estos canales y enzimas se los llama “segundos mensajeros”. Un segundo mensajero es una molécula o un ión que transporta información al interior del citoplasma en respuesta a una señal que se produce en la membrana (1º mensaje). MOLECULAS DE SEÑALIZACION INTRACELULAR Nucleótidos cíclicos o productos de hidrólisis lipídica sintetizados por ciclasas o fosfolipasas asociadas a la membrana. SISTEMA DEL AMP-3, 5 CÌCLICO: El AMP cíclico es una sustancia que se encuentra en todos los organismos vivientes y en casi todas las células de mamíferos. En algunas de esas células la exposición a determinadas hormonas produce un rápido aumento de la concentración del AMP-3,5- cíclico, se genera a partir de la hidrólisis de ATP en reacción catalizada por una enzima llamada adenilato ciclasa o adenilil ciclasa, que se localiza en la membrana plasmática. La adenilil ciclasa es una proteína integral de membrana formada por una cadena polipeptídica. El sistema funciona del modo siguiente: 1) El cambio conformacional producido en el receptor por la unión del ligando constituye la primera señal, que se transmite a moléculas de proteínas G. 2) La interacción con el complejo HR produce modificaciones en la proteína G, en la cual la subunidad α se desprende del GDP y fija GTP procedente del citosol. La unión de GTP disocia la subunidad α del dímero β-γ .El complejo α- GTP tiene capacidad para activar la adenilato ciclasa. 3) La adenilato ciclasa activada cataliza la formación de AMPc a partir de ATP y eleva la concentración de ese segundo mensajero en la célula. 4) La subunidad α posee actividad GTPasa, promueve la hidrólisis de GTP y queda unido a GDP, por lo cual vuelve a asociarse con el dímero β-γ para reconstruir la proteína G inactiva y deja de actuar sobre adenilato ciclasa. El AMPc difunde en la célula y estimula la proteína quinasa A. El mecanismo de activación de la proteína quinasa es el siguiente: La proteína quinasa A(dependiente de AMPc) en ausencia de AMPc se encuentra inactiva, formando un tetrámero constituido por dos subunidades llamadas catalíticas ( C) y dos monómeros reguladores ( R)Cuando aumenta el nivel de AMP cíclico en la célula, dos moléculas del nucleótido se fijan a sitios de unión específicos en cada una de las subunidades reguladoras, se produce un cambio conformacional que las obliga a desprenderse de la catalíticas. Las subunidades C libres tienen actividad enzimática. La unidad catalítica de proteína quinasa A transfiere fosfato de ATP a restos serina o treonina de proteínas que, al ser fosforiladas, adquieren nuevas propiedades. El AMPc que provoca respuestas muy distintas en diferentes células. Aunque la respuesta varía según el tejido considerado, en todos los casos la acción del AMPc se realiza a través de reacciones en cascadas iniciadas con la activación de la proteína quinasa A, que cataliza la acción de fosfato a diversas proteínas. La fosforilación de enzimas promovida por la proteína quinasa dependiente de AMPc produce, según los casos, estimulación o inhibición y constituye un importante mecanismo regulador del funcionamiento de vías metabólicas. También interviene como modulador de la actividad de sistemas transporte de membrana. A nivel del núcleo puede influir sobre la transcripción, en efecto, existen secuencias específicas en el ADN, llamadas elementos de respuesta dependientes de AMPc o CRE (del inglés ‘’cAMP response element’’). El elemento del nivel de AMPc en la célula estimula la proteína quinasa A y ésta fosforila una proteína, que entonces se une a secuencias y activa la transcripción de genes. Fosfodiesterasa: El AMP cíclico es un regulador muy potente y las células deben controlar su concentración. En la mayoría de los tejidos un importante factor de control es la fosfodiesterasa, enzima que cataliza la hidrólisis de la unión del fosfato al carbono3 en el AMPc y lo convierte en adenosina 5- monofosfato, inactivo. Metilxantinas como cafeína, teofilina, y aminofilina inhiben la fosfodiesterasa, impiden la degradación del AMPc y mantienen su acción. Catecolaminas que se unen a receptores adrenérgicos α y la insulina activan la fosfodiesterasa y producen reducción del nivel celular de AMPc. SISTEMA DEL GMP cíclico El GMP cíclico es un segundo mensajero importante. Aunque está distribuido por todo el organismo, el GMP cíclico tiene un papel crucial en el cerebro, el sistema cardiovascular y en los órganos sensoriales (por ejemplo, en la detección de luz por las células de la retina). La enzima que lo sintetiza es la guanilil ciclasa Su nombre es guanosín 3',5'-fosfato (cíclico) (abreviado habitualmente como GMP cíclico o cGMP) El GMP cíclico es químicamente muy similar al AMP cíclico. SISTEMA DEL FOSFATIDILINOSITOL BISFOSFATO: El fosfatidilinositol (PL) es un componente de membranas celulares que forma parte de la doble capa lipidia de la membrana plasmática, ubicado preferentemente en la hoja interna (en contacto con el citoplasma). El fosfatidinilinositol es fosforilado para formar fosfatidinilinositol- 4,5-bisfosfato (PIP2) Esta sustancia integra un sistema de transmisión de señales. La unión del ligando específico a un receptor unido a proteína G produce un cambio conformacional de la porción citosólica del receptor que estimula la fosfolipasa C. Esta enzima cataliza la hidrólisis de fosfatidinilisitol 4,5- bisfosfato incluido en la membrana para generar diacilglicerol e inositol- l, 4,5- trifosfato. Las dos moléculas actúan como segundos mensajeros. El inositol-l, 4,5 trifosfato (lP3) moviliza la liberación de Ca2+ almacenado en las cisternas del RE y las mitocondrias, lo cual determina un aumento brusco del nivel Ca2+ en el citosol, factor determinante de diversas respuestas celulares. El diacilglicerol se une y activa a una proteína llamada Protein cinasa que puede unirse de forma reversible a la cara interna de la membrana plasmática. Esta enzima fosforila proteínas vinculadas a procesos de multiplicación celular y factores de transcripción, regula receptores y canales iónicos. SISTEMA CALCIO-CALMODULINA: Este sistema opera con el aumento de Ca intracelular el cual puede entrar por diferentes estímulos, entre ellos la unión de ligandos a determinados receptores, desencadenan acciones que elevan la concentración de ion Ca2+ en el citosol, o por cambios en el potencial de membrana que abre los canales para este. El Ca2+ que ingresa en esas condiciones en el citoplasma puede proceder del exterior de la célula o de depósitos existentes en organelas como mitocondrias o retículo endoplasmático (RE). La elevación de los niveles de Ca2+ puede ser provocado por liberación de inositol-l, 4,5- trifosfato desde la membrana plasmática y en algunos casos, también por aumento de AMP y GMP cíclicos. El Ca2+ se convierte así en mensajero final de distintos sistemas de transmisión de señales. El Ca2+ en el citosol se une a proteínas receptoras específicas la más importante es la calmodulina. Cuando se une al Ca2+, la calmodulina sufre cambios conformacionales y adquiere capacidad para regular la actividad de numerosas proteínas blanco, incluidas diversas proteínas quinasas. Se han descripto varias proteína quinasas dependientes de Ca2+calmodulina que integran cascadas de fosforilación. Estas fosforilaciones modifican la actividad de enzimas, canales de iones y factores de transcripción. PRINCIPALES GLÁNDULAS ENDOCRINAS Y SUS HORMONAS MÁS IMPORTANTES. HIPÓFISIS – HIPOTÁLAMO La glándula pituitaria o hipófisis está compuesta por el lóbulo anterior (pars distalis o adenohipófisis), el lóbulo posterior (pars nervosa o neurohipófisis), el lóbulo intermedio (pars intermedia) y la pars tuberalis. La neurohipófisis está unida al hipotálamo por el tallo hipofisario, el cual contiene fibras nerviosas y vasos sanguíneos de un sistema porta. Estas estructuras establecen una importante conexión, no sólo anatómica sino también funcional entre hipotálamo e hipófisis. La secreción de la neurohipófisis está controlada por señales nerviosas que se originan en el hipotálamo y terminan en esta. Las Células neurosecretoras hipotalámicas están localizadas en el Núcleo paraventricular y el Núcleo supraóptico. Sus axones se prolongan por el tallo hipofisario hasta la neurohipófisis. La adenohipófisis produce hormonas tróficas o trofinas con capacidad para estimular el funcionamiento de otras glándulas de secreción interna. A su vez, la secreción de hormonas adenohipofisarias es controlada por factores reguladores de liberación y de inhibición producidos en el hipotálamo y llegan a la hipófisis por medio de vasos sanguíneos diminutos llamados “vasos porta hipotálamohipofisarios”. Sistema porta Hipotálamo-Hipofisario Se trata de un sistema de doble capilarización, donde a nivel de las células neurosecretoras hipotalámicas se encuentra la primera capilarización a la cual se vierten las hormonas del hipotálamo, que viajan hacia la adenohipófisis, donde se produce la segunda capilarización, que permite a dichas hormonas alcanzar las células glandulares estimulando o inhibiendo su secreción. Estos dos lechos capilares se unen permitiendo que la sangre fluya en una sola dirección (hipotálamo-hipófisis) HORMONAS HIPOTALÁMICAS NEUROHORMONAS: Son producidas en los núcleos supraóptico y paraventricular del hipotálamo y son transportadas por flujo axonal hasta la neurohipófisis donde son almacenadas y luego secretadas. Hormona antidiurética (ADH) o Vasopresina. La vasopresina regula el balance de agua en el cuerpo actuando sobre los riñones. Los estímulos que participan en su liberación se clacifican en: Osmóticos: aumento de la osmolaridad plasmática No osmóticos: severa hipovolemia e hipotensión (regulación hipovolémica), se necesita una disminución del 10 % de la vol. P arterial para que se libere ADH. Otro estímulo es la Angiotensina II. La regulación osmótica es controlada por osmoreceptores ubicados a nivel central (hipotálamo) y periférico (vena porta, el esófago y estómago que detectan la ingesta de agua). La regulación hipovolémica es controlada por baroreceptores ubicados a nivel periférico (cayado aórtico y carótidas). La ADH circula libre en sangre, su vida media es de unos 15 minutos. La acción principal de la hormona es controlar la reabsorción facultativa de agua en los túbulos distales de la nefrona. Aumenta la permeabilidad al agua de la superficie luminar de tubos colectores. También disminuye la filtración glomerular, lo que contribuye a reducir la diuresis. La ADH se une a receptores de membrana llamados V (V1, V2 y V3) acoplados a proteínas G presentes en el riñón, vasos sanguíneos, y adenohipófisis. Riñon: incrementa la permeabilidad al agua en las células de los túbulos contorneados distales y tubos colectores medulares provocando el traslado de canales de agua, (proteínas llamadas acuaporinas 2), desde vesículas en el interior de la célula hacia la membrana luminar. Induce activación de adenilato ciclasa, aumento en la concentración de AMPc y estimulación de proteína quinasa A, que inicia una cascada de fosforilaciones. En ausencia de vasopresina la membrana apical de las células tubulares es impermeable al agua. La acuaporina-2 está en vesículas intracelulares, pero no se expresa en la membrana apical del túbulo. La unión de la ADH con receptores V2 permite la migración de las acuaporinas 2 hacia la membrana apical de la célula tubular, esto incrementa la reabsorción de agua de la luz tubular (el agua se absorbe mediante ósmosis desde la luz tubular hacia el intersticio tras atravesar las células epiteliales tubulares), lo que produce aumento de la osmolalidad y disminución del volumen de la orina excretada. También estimula el bombeo de NA+ en el asa de Henle y disminuye velocidad de flujo sanguíneo en la medula renal. Sistema cardivascular: tiene una potente acción vasopresora en vasos periféricos. Este efecto es el resultado de la unión de la hormona a receptores V1 acoplados a proteínas G en el músculo liso vascular. Se activa fosfolipasa C que libera los segundos mensajeros inositoltrisfosfato y diacilglicerol. La respuesta final es la contracción del músculo liso. Elevación de la presión arterial a través de la constricción arteriolar durante las hemorragias masivas. Incrementa la motilidad gástrica y del colon. Hígado (receptores V1): Estimula la glucogenolisis, la liberación de factor VIII y de von Willebrand, aumenta la concentración de Ca+ y participa en el recambio de fosfatidilinositol. Cerebro, hipotálamo e hipófisis: Receptores V1 • • • • • Inhibe las descargas de los núcleos Supraóptico y Paraventricular. Memoria y aprendisaje. Regulación de la temperatura y presión sanguínea. Actúa en la amígdala como hormona del miedo. Participa en el reconocimiento social (emparejamiento y fidelidad en machos, territorialiad agresiva y defensa de crías) Receptores V3: • En la hipófisis estimula la secreción de ACTH. Oxitocina La oxitocina es también producida por el hipotálamo y almacenada y liberada por la neurohipófisis. La oxitocina circula libre en la sangre, es rápidamente degradada, principalmente en hígado y riñón. Su vida media es de 3 a 5 minutos. Estimula la contracción del útero, su efecto sobre el músculo liso uterino es condicionado por la presencia de estrógenos y progesterona. Los estrógenos acentúan el efecto contráctil mientras que la progesterona lo inhibe. Hacia el final del la preñez se produce una reducción notable de los niveles de progesterona y aumenta la sensibilidad a la oxitocina. La hormona no aumenta en sangre hasta que el trabajo de parto ha comenzado. En ese momento, la liberación de oxitocina contribuye decididamente a facilitarlo. Si bien se cree que normalmente la oxitocina no es el factor que inicia las contracciones. En la glándula mamaria, la oxitocina produce excreción de leche por contracción del músculo liso. La secreción de oxitocina es activada por la succión del pezón. La hormona no tiene activación sobre el proceso de formación de leche en la glándula lactante. FACTORES HIPOTALÁMICOS Aparte de las dos hormonas de acción directa mencionadas, el hipotálamo secreta diversas hormonas o factores que regulan la secreción de hormonas hipofisarias. Todos ellos son de naturaleza peptídica y poseen capacidad para modificar la síntesis y secreción hormonas de la adenohipófisis Hormonas estimuladoras Hormona liberadora de gonadotropinas (GnRH): actúa sobre la hipófisis, estimulando la producción y la liberación de la hormona luteinizante (LH) y la hormona foliculoestimulante (FSH). Hormona liberadora de tirotropina (TRH): Estimula la secreción de tirotropina (TSH) por parte de la adenohipófisis. Hormona liberadora de corticotropina (CRH o CRF): Se sintetiza en los núcleos paraventriculares, posee una vida larga (minutos). Estimula la liberación de adrenocorticotropina (ACTH) y β-endorfina por parte de la adenohipófisis. La hormona antidiurética y la angiotensina II potencian el efecto liberador de CRH. Hormona liberadora de somatotropina (STH) o factor liberador de hormona del crecimiento (GRF): estimula la liberación de la hormona del crecimiento hipofisaria (GH). Hormonas inhibidoras: Somatostatina u hormona inhibidora de la liberación de somatotropina (GIH): Como su nombre indica, inhibe la secreción de somatotropina y de otras hormonas como la insulina, el glucagón, el polipéptido pancreático y la TSH. La zona secretora se encuentra en la región periventricular del hipotálamo. Es un tetradecapéptido que se encuentra en el hipotálamo y en las células D de los islotes de Langerhans. Dopamina o Factor inhibidor de la liberación de prolactina (PIF): Actúa en forma constante inhibiendo la secreción de prolactina hipofisaria. HORMONAS DE LA ADENOHIPÒFISIS: Una de las características más salientes de la adenohipófisis es la elaboración de hormonas, llamadas tróficas o trofinas, que estimulan la síntesis y secreción de hormonas en otras glándulas endocrinas. La secreción de la mayoría de las hormonas tróficas está sujeta a control positivo por los factores liberadores del hipotálamo y a inhibición por retroalimentación. La concentración en sangre del producto hormonal de la glándula estimulada regula la secreción de la trofina correspondiente actuando a nivel de hipófisis o de hipotálamo. Todas las hormonas de adenohipófisis son de naturaleza polipeptídica. Tirotrofina, foliculoestimulante y luteinizante, son glicoproteínas. Hormona adrenocorticotrófica (ACTH): La adenohipófisis produce una trofina que estimula la corteza adrenal. La ACTH estimula la síntesis y liberación de corticoesteroides en la corteza adrenal. Promueve la activación de enzimas participantes en la síntesis de corticoides. Sus efectos se ejercen preferentemente sobre las células de la zona fascicular principales productoras de glucocorticoides. Si bien la acción principal recae sobre la síntesis y secreción de glucocorticoides, también hay aumento de otros corticoides, entre ellos aldosterona pero en muy poca cantidad. En la regulación de la secreción de esta hormona participan otros factores. La acción primaria de ACTH se ejerce a partir de su unión a receptores de membrana acoplados a proteínas G, activación de adenilato ciclasa y aumento de AMPcíclico. Hormona tiroestimulante (TSH): La tirotrofina activa la síntesis y liberación de hormonas T3 y T4 en la glándula tiroides. Esta acción es mediada por activación de adenilato ciclasa y aumento del nivel AMP cíclico en tiroides. Gonadotrofinas: Estas hormonas, producidas por las células gonadotropas del lóbulo anterior, actúan sobre la maduración y funcionamiento de ovarios y testículos. Se distinguen la hormona foliculoestimulante (FSH) y la luteinizante (LH). Están constituidas por dos unidades polipeptídicas diferente, las cadenas α y β. La subunidad α es idéntica para las dos hormonas y para tirotrofina de una misma especie, la cadena β es específica para cada una. Si bien la actividad depende de la cadena β, es indispensable la presencia de las dos subunidades para que la hormona demuestre acción biológica. FSH y LH, activan la adenilatociclasa en sus células diana. Acciones de FSH: Induce maduración y desarrollo de folículo de Graaf en el ovario. Por acción conjunta por LH estimula la producción de estrógenos. En testículo, FSH promueve el desarrollo de túbulos seminíferos y es uno de los factores involucrados en la iniciación de la espermatogénesis. Actúa sobre células de Sertoli para estimular la producción de estrógenos a partir de andrógenos y junto con testosterona, promueve la síntesis de proteína de unión a andrógenos que contribuye a mantener altos niveles de andrógenos en la vecindad de las células germinales. Acciones de LH Controla en la hembra el desarrollo del cuerpo luteo y promueve la secreción de estrógenos y progesterona. Sus blancos son el cuerpo lúteo en ovario y las células de Leydig en testículo. En el macho, LH estimula la producción y secreción de testosterona, que a su vez contribuye a mantener la espermatogénesis y el desarrollo de los órganos sexuales secundarios. PROLACTINA (PRL) Juntamente con LH, la prolactina promueve la formación del cuerpo lúteo y la producción de progesterona. Su función mejor caracterizada es la estimular el crecimiento lobuloalveolar en la glándula mamaria durante la preñez y la lactogénesis posparto. Si bien los estrógenos y la progesterona son necesarios para el desarrollo de los ductos y la proliferación alveolar, la prolactina es el factor principal en esas acciones. La prolactina también activa la función inmunitaria por estímulo de la proliferación de linfocitos. HORMONA DE CRECIMIENTO O SOMAFOTROFINA La hormona de crecimiento, generalmente indicada con la siglas GH (del inglés “growth hormone”), es sintetizada como prohormona en las células somatotrofas de hipófisis anterior. La secreción de GH está bajo control hipotalámico, mediado por la hormona liberadora de somatotrofina (GHRH) y la somatostatina, que respectivamente estimulan e inhiben la secreción de GH. En el plasma sanguíneo la mayor parte de la GH se transporta en unión con una proteína específica. La somatotrofina es una hormona multifuncional, promueve el crecimiento postnatal de tejidos esqueléticos y blandos por acciones directas e indirectas. Los efectos indirectos son mediados por los factores de crecimiento similares a insulina (IGF). La acción principal de la somatotrofina es estimular la proliferación y maduración de muchos tejidos, especialmente hueso, cartílago y músculo. Desarrolla funciones metabólicas muy generales: Proteínas y ácidos nucleicos: Estimula el anabolismo de proteínas. Incrementa el ingreso de aminoácidos en las células por activación de los sistemas de transporte, especialmente en músculo e hígado. Aumenta la actividad de ADN y ARN polimerasas. Lípidos: La GH disminuye la lipogénesis. Ejerce acción lipolítica, promueve movilización de ácidos grasos y aumento de ácidos grasos libres sangre. Carbohidratos: Disminuye la utilización de glucosa. En el músculo, la somatotrofina deprime el transporte de glucosa y la actividad glucolítica, acciones opuestas a las de insulina. En el hígado produce aumento de la gluconeogénesis a partir de aminoácidos, acción que secundariamente contribuye a aumentar la glucogenogénesis. La disminución de la utilización periférica de glucosa y la activación de la gluconeogénesis tienden a elevar los niveles de glucosa circulante. La GH se comporta como hiperglusemiante (diabetógena). GLÁNDULA TIROIDES La glándula tiroides contiene folículos formados por células epiteliales (células foliculares) dispuestas en círculos en cuyo interior se encuentra un material viscoso (coloide) con la glicoproteína tiroglobulina, que incluye en su estructura las hormonas sintetizadas en la glándula. Las hormonas tiroideas foliculares son tiroxina (3, 5,3,5 tetrayodotironina) o T4 y 3, 5,3- triyodotironina o T3. Ambas son aminoácidos yodados, derivados de la tirosina. Posee otro tipo de células llamadas parafoliculares o células C que se encuentran en el exterior de los folículos y son las encargadas de secretar la hormona calcitonina. Existen 4 elementos esenciales para sintetizar las hormonas tiroideas: el yodo, la tiroglobulina, tiroperoxidasa y peróxido de hidrógeno. El yodo es un constituyente esencial de la molécula de las hormonas tiroideas. Para sintetizarlas, la glándula utiliza el yodo provisto por los alimentos, principalmente en forma de yoduros inorgánicos. Este es transportado hasta la tiroides, y por medio de transporte activo, ingresa al interior de las células foliculares. El yoduro es oxidado (activado) en reacción catalizada por una enzima llamada tiroperoxidasa, que utiliza peróxido de hidrógeno como fuente de oxígeno. La enzima se encuentra fijada a al membrana apical de la célula folicular, próxima al lumen. La tiroglobulina es una glicoproteína que posee restos de tirosina, es sintetizada en las células tiroideas foliculares y luego es secretada hacia el lumen del folículo por exocitosis. El yodo activo es unido a tirosina reciclada en el citosol, si se une una molécula de yodo se forma Monoyodotirosina (MIT) y si se unen dos moléculas se forma diyodotirosina (DIT). Dos moléculas de diyodotirosina forman tetrayodotironina (T4) y una de monoyodotirosina mas una de diyodotirosina forman triyodotironina (T3). Cada molécula de tiroglobulina contiene unidas hasta 30 moléculas de T4 y algunas de T3. Luego de su síntesis las hormonas tiroideas permanecen en la luz acinar extracelular hasta su liberación. Para que las hormonas se liberen la tiroglobulina con T4 yT3 unidas deben ingresar al interior de la célula y separarse. Esta acción se realiza en los lisosomas en donde las enzimas escinden las moléculas. La T4 y la T3 libres atraviesan la membrana de la célula para alcanzar los capilares sanguíneos. El resto de tiroglobulina y yodo se reciclan quedando yodo por un lado y tirosina por otro que será utilizada para formar MIT y DIT. Transporte en plasma: La T3 y la T4 son transportadas en sangre en asociación con proteínas plasmáticas fundamentalmente son dos las proteínas que actúan como transportadores específicos de las hormonas tiroideas. Una es la globulina fijadora de tiroxina (TBG , ‘’thyroxine binding globulin’’), y la otra es la albúmina que tiene muy baja afinidad por T4 y T3. La TBG tiene la mayor afinidad, fija el 77% de T4 unida a proteína en el plasma. El 99,4% de T4 en plasma está unido y sólo 0,04% está libre. Para T3 con afinidad algo menor por las proteínas fijadoras , la proporción de hormona libre es del 0,4%. La forma libre es rápidamente disponible para ingresar en las células. La vida media T4 en el plasma es de unos 7 días mientras que la de T3 es de un día. Ingreso a los tejidos periféricos: Las hormonas tiroideas pueden atravesar la membrana plasmática de las células efectoras. En ellas la T4 pierde el yodo en posición 5’ o 5 por acción de 5’ o 5 monodesyodasa y se convierte en T3 o T3 r (T3 reversa o invertida, 3,3’,5’triyodotironina) y es más activa que T4. T3 r varía de un tejido a otro, aun en un mismo tejido cambia según su estado metabólico. Mecanismo de acción: Las hormonas tiroideas atraviesan la membrana plasmática de las células y llegan al núcleo donde se encuentran sus receptores específicos. Al unirse T3 se producen cambios conformacionales que habilitan al complejo HR para activar la transcripción de genes definidos. Los receptores de hormonas tiroideas pertenecen a la superfamilia de receptores de esteroides y presentan homología estructural con ellos. La afinidad del receptor es una diez veces mayor para T3 que para T4. Se han identificado receptores de hormonas tiroideas no sólo en el núcleo , sino también mitocondrias y en membrana plasmática. Las acciones directas sobre mitocondrias comprenden aumento del número y tamaño de las organelas e incremento del consumo de oxígeno y producción de calor (termogénesis). En la membrana estimulan el transporte de iones, glucosa y aminoácidos. Acciones Las acciones de las hormonas tiroideas son tan generales que prácticamente no hay célula en el organismo libre de su influencia. Dentro de esas acciones pueden mencionarse: a) Activación de la síntesis de ARN mensajero, ribosomal y de transferencia y como consecuencia de la síntesis de proteínas. Entre éstas se incluyen numerosas enzimas. b) Acción promotora del crecimiento en parte dependiente de los efectos mencionados c) Aumento de actividad Na+’, K’+-ATPasa pasa en casi todos los tejidos (una de las escasas excepciones es en el cerebro). Este efecto se debe al aumento del número ‘’bombas de sodio’’insertas en las membranas de las células. d) Incremento del consumo de oxígeno en tejidos y promoción de la utilización de glucosa, lípidos y aminoácidos e) Estimulación de la síntesis de colesterol y aumento de producción de receptores LDL, con ello se sustrae más colesterol del plasma. f) Participan en estimular la eritropoyesis junto con la eritropoyetina renal y glucocorticoides. En términos generales, las hormonas tiroideas tienen efecto anabólico. Incrementan la tasa metabólica basal, inducen la síntesis de óxidorreductasas mitocondriales. En el músculo aumentan el contenido de Na’+, K’+-ATPasa en la membrana y la actividad de ATPasa de miosina. Estimulan el ingreso de Ca2+ en retículo sarcoplásmico, lo que incrementa la cantidad de Ca2+ disponible. En el sistema nervioso las hormonas tiroideas son necesarias para el desarrollo fetal y neonatal del cerebro. Regulan la diferenciación neuronal, mielinogénesis, crecimiento neuronal y formación de sinapsis. El hipotiroidismo congénito resulta en daños cerebrales severos e irreversibles. En dosis elevadas, las hormonas tiroideas tienen acción catabólica, hay aumento de la proteólisis y el balance nitrogenado se torna negativo. Aumenta la degradación de carbohidratos y lípidos. Ejercen un efecto aparentemente desacoplante de las fosforilaciones con mayor consumo de oxígeno y producción de calor, disminuyen la formación de ATP .Se ha propuesto que la acción termo génica se debe al aumento de la actividad de Na’+, K’+-ATPasa en las membranas con el consiguiente incremento del gasto de energía en las células en reposo. Las hormonas tiroideas con frecuencia activan simultáneamente algunas vías en ambos sentidos, anabólicos y catabólicos. GLÁNDULAS ADRENALES: Las glándulas adrenales están constituídas por dos zonas claramente diferenciadas: a) La cortical o corteza, de origen mesodérmico, produce hormonas esteroides esenciales para la vida. b) la medular o médula, funcionalmente considerada parte del sistema nervioso autónomo, produce catecolaminas idénticas a las liberadas en otras formaciones del sistema adrenérgico. Corteza Adrenal: Según la disposición de los elementos celulares es posible distinguir en la corteza tres capas: a) externa o glomerular, b) media o fascicular, c) interna o reticular. Estas distintas zonas tienen especialización respecto al tipo de hormonas sintetizadas. De acuerdo con sus funciones generales, las hormonas de corteza adrenal se agrupan en tres categorías, con actividades fisiológicas diferenciadas: 1) Glucocorticoides: poseen efecto primario sobre el metabolismo de hidrato de carbono, lípidos y proteínas. Son producidos fundamentalmente en la zona fasciculada. 2) Mineralocorticoides: afectan primordialmente el transporte de electrolitos y distribución de agua en los tejidos. Son secretados por células de la zona glomerular. 3) Corticoides androgénicos: sus efectos principales se manifiestan sobre los caracteres sexuales secundarios. Son sintetizados en la zona reticular. Síntesis: El camino inicial obligado en la síntesis de esteroides es la producción de colesterol. La corteza adrenal es relativamente rica en colesterol, el cual es sintetizado en la propia glándula o es tomado de LDL del plasma por receptores LDL en la membrana plasmática. En las primeras etapas de la síntesis de esteroides, el colesterol es hidroxilado y luego se produce ruptura de la cadena lateral por acción de una enzima. Esta desmolasa es inducida por ACTH en las zonas fascicular y reticular y por angiotensina II en la zona glomerular. El compuesto formado es la pregnelonona , su producción es catalizada por un complejo multienzimático localizado en mitocondrias dependiente del Ca (P450). La pregnenolona sirve de compuesto intermedio en la síntesis de todas las hormonas esteroides. Las transformaciones siguientes , en su mayoría, son deshidrogenaciones e hidroxilaciones catalizadas por enzimas que requieren oxígeno molecular y NADPH como coenzima, comprenden oxigenasas de función mixta ligadas a citocromo P. Por este proceso la pregnelona se convierte en progesterona. A partir de la progesterona se sintetizan mineralo y glucocorticoides. Las enzimas que participan en estas vías biosintéticas se encuentran en mitocondrias y en el retículo endoplasmático. Transporte en plasma: Una vez sintetizados, los esteroides pasan con rapidez a la sangre. El cortisol es el corticoide más abundante en el plasma. La concentración de aldosterona es mucho más baja, alrededor de 0,02 μg por dL. Las hormonas corticoadrenales son transportadas , en parte, ligadas a proteínas plasmáticas. La transcortina (CBG del inglés ‘’corticosteroide binding globulin’’) y la albúmina sérica se unen a los corticoides y los vehiculizan en sangre. Cortisol y corticosterona se unen preferentemente a la transcortina(CBG),77% del cortisol normalmente presente en sangre es transportado por transcortina y 15% por albúmina, queda algo más del 7% libre en plasma. La aldosterona, en cambio, se une menos a la CBG, gran parte se encuentra libre. La hormona libre es la forma biológicamente activa y está en equilibrio con la ligada a proteínas. Inactivación y excreción: Los esteroides llegados a la circulación son rápidamente eliminados del organismo. Normalmente la vida media del cortisol es de alrededor de 70 minutos, a las 48 horas se ha excretado prácticamente todo. El hígado es el principal responsable de la inactivación de corticoesteroides. Son conjugados con ácido glucurónico y en menor proporción con sulfato. Los corticoesteroides conjugados se excretan con la bilis hacia el intestino donde son parcialmente reabsorbidos y devueltos al hígado por la circulación portal (ciclo enterohepàtico). La excreción principal tiene lugar por vía urinaria. Regulación de la síntesis y secreción: Retroalimentación La síntesis y secreción de esteroides adrerenales es controlada por adrenocorticotrofina (ACTH) de la adenohipófisis. Esta hormona trófica actúa preferentemente sobre la zona de la corteza. La secreción de ACTH , a su vez es regulada por el factor liberador de corticotrofina(CRH) producido en hipotálamo. El nivel de esteroides adrenales circulantes también controla, por retroalimentación, la secreción de ACTH. La estimulación de la adrenal por ACTH provoca rápida disminución del contenido de colesterol en la glándula. Este fenómeno es un índice de la activación de la síntesis de esteroides. La ACTH se une a los receptores de la membrana de células de la corteza adrerenal y produce activación deadenilato ciclasa. De este modo, su acción es mediada por AMP cíclico. La producción de aldosterona por las adrenales no es directamente estimulada por ACTH sino por angiotensina II hiponatremia e hipercalemia. Ritmo circadiano (excepto en el perro) • Sobreimpuesto a la secreción episódica • Cortisol aumenta a las 3-5 horas del sueño • Variabilidad individual: patrón de sueño, exposición luz-oscuridad, ingesta alimentaria • Alteración del ritmo: stress físico, psicológico (depresión, manía), enf SNC, S. Cushing, enf hepática, enf renal, ciproheptadina • Acciones metabólicas. Glucocorticoides: • Producen aumento de glucosa , ácidos grasos libres y aminoácidos en sangre circulante. En tejidos periféricos (adiposo, linfoide, muscular) deprimen las vías de utilización de glucosa, principalmente la glucólisis , mientras estimulan la degradación de proteínas (acción catabólica). En tejido adiposo activan la lipólisis. La depresión del metabolismo de la glucosa disminuye el glicerofosfato disponible y con ello la síntesis de triacilgliceroles. En hígado aumentan la síntesis de proteínas , especialmente de enzimas comprometidas en el metabolismo de aminoácidos y de las enzimas clave en la regulación de la gluconeogénesis Los cambios enzimáticos mencionados resultan en activación de la gluconeogénesis a partir de aminoácidos. La estimulación de la gluconeogénesis en hígado y la disminución del consumo de glucosa en tejidos periféricos favorecen la elevación del nivel de glucosa circulante (hiperglucemia). Hay también aumento del depósito de glucógeno en hígado. Acciones sobre inflamaciones e inmunidad: Los niveles bajos de glucocorticoides normalmente presentes en sangre tienen una acción tónica inhibitoria de la actividad de células inflamatorias y del sistema inmune. En concentraciones superiores a las fisiológicas, el cortisol es un potente antiinflamatorio y depresor de la respuesta inmunitaria. relacionados. El cortisol además estabiliza las membranas lisosomales, con lo cual disminuye la liberación de encimas que contribuyen al proceso inflamatorio. En la inflamación, los leucocitos abandonan el lecho vascular y acuden al sitio de la agresión. Como resultado de las acciones mencionadas, este proceso es inhibido por los glucocorticoides, que también deprimen la actividad fagocitaria de neutrófilos, el número de eosinófilos circulantes y la proliferación de fibroblastos. Altas dosis de cortisol inhiben los mecanismos de defensa contra las infecciones, especialmente la inmunidad celular (disminuye el número de linfocitos T circulantes). Aparentemente, la producción de anticuerpos por linfocitos B no es afectada. Efectos sobre la homeostasis del calcio: Los glucocorticoides disminuyen la absorción intestinal y la reabsorción renal de calcio, lo cual tiende a reducir los niveles de calcio en plasma y a estimular la secreción de hormona paratiroidea. Como resultado hay reabsorción de hueso (osteólisis). Disminuye la formación de hueso, se deprime la proliferación de fibroblastos y formación de colágeno. • • • • • • • Mineralocorticoides. Con excepción de los andrógenos, todos los corticoides activos aumentan la reabsorción de sodio en los túmulos renales y disminuyen su excreción en gl. sudoríparas, salivales y tracto gastrointestinal. El aumento de reabsorción de sodio determina secundariamente, incremento en la excreción de potasio. La aldosterona actúa en el nefrón distal (última porción del túbulo contorneado distal y del tubo colector cortical). El aumento de la volemia causado por la aldosterona estimula la liberación de péptido natriurético atrial, que promueve excreción renal de Na+ y agua.La aldosterona es el mineralocorticoide más potente en relación con la retención de sodio. Interviene en la regulación de la distribución de sodio y potasio en los espacios intra y extracelular. Como el movimiento de iones es acompañado por el desplazamiento de agua, los mineralocorticoides constituyen un importante factor en la regulación del volumen de los compartimientos hídricos del organismo. La aldosterona produce retención de Na+ y secreción de K+ y H+ estimulando la síntesis de una proteína que aumenta la permeabilidad a la entrada de Na en la superficie luminal celular desde el filtrado renal y la actividad de la Na+,K+-ATPasa. Los estímulos para la secreción de aldosterona son la hiponatremia, hipercalemia y la agiotensina II. Una concentración baja de Na y alta de potasio en sangre estimulan la secreción de aldosterona sin necesidad de activar el sistema Renina-angiotensina-aldosterona. Sistema renina-angiotensina- aldosterona: El riñón, por medio del sistema renina-angiotensina-aldosterona, es un importante órgano regulador de la secreción de aldosterona. La renina es una proteasa producida en las células granulares del aparato yuxtaglomerular presente en la arteriola aferente. La disminución de la presión arterial, del flujo sanguíneo renal, o de la concentración de Na’ en plasma, estimulan la secreción de renina. La renina actúa sobre angiotensinógeno, sintetizado en hígado y libera angiotensina I, biológicamente inactiva. En plasma existe una enzima convertidora de angiotensina (ECA), procedente de la membrana plasmática de células del endotelio vascular principalmente del pulmón y riñón que convierte la angiotensina I en angiotensina II. Esta produce constricción de la arteriola eferente del glomérulo y eleva la presión de filtración, tiene acción vasopresora general, activa la reabsorción de NaHCO3 en los túbulos contorneados proximales e induce la síntesis y secreción de aldosterona en corteza adrenal. Sus acciones tienden a mantener el volumen y la presión en el árbol arterial. Sistema Renina-Angiotensina-Aldosterona Na, PA, estímulo simpático Aparato yuxtaglomerular Renina Propranolol Angiotensinógeno iECA Angiotensina I ACE (Pulmón. Circulación) Saralasina Aldosterona Angioensina II Zona glomerular PA Médula Adrenal Las células cromafines de médula adrerenal producen las catecolaminas epinefrina o adrenalina y norepinefrina o noradrenalina, ambas derivadas del aminoácido tirosina. La noradrenalina es también neurotransmisor en neuronas pos ganglionares del sistema simpático. La dopamina ,metabolito Intermediario en la vía de síntesis de estas hormonas, es otra catecolamina que actúa como neurotransmisor. Biosíntesis: El paso inicial es la conversión de tirosina en dihidroxifenilalanina (DOPA), luego es convertida en dopamina en reacción catalizada por una descarboxilasa. La dopamina se almacena en vesículas (gránulos cromafines) en células de la médula adrenal y en neuronas del sistema simpático. Estas vesículas contienen dopamina β hidroxilasa, responsable de la conversión de dopamina en noradrenalina. La noradrenalina debe salir de la vesícula para ser transformada en adrenalina y reingresar como tal a los gránulos de secreción. La síntesis de catecolaminas es regulada por retroalimentación. Adrenalina y noradrenalina inhiben a la tirosina hidroxilasa. La gran mayoría de células cromafines en médula adrenal sintetiza adrenalina, sólo en el 10% del total de células la vía termina con la formación de noradrenalina. Los productos de secreción de la médula adrenal se almacenan en vesículas rodeadas por una membrana Secreción: La liberación del contenido de las vesículas es desencadenado por impulsos nerviosos que determinan el ingreso de Ca2+ en la célula. Las vesículas se desplazan hacia la membrana plasmática , se fusionan con ella, se abren al exterior y descargan su contenido(exocitosis). La mayor parte de las catecolaminas secretadas son metabolizadas en los tejidos, principalmente hígado. Las principales enzimas comprometidas en estas reacciones son monoaminooxidasa (MAO) y catecol-ortos-metiltransferasa (COMT). PANCREAS ENDOCRINO La función endocrina del páncreas está adscripta a los islotes de Langerhans. Estos islotes contienen diferentes tipos de células, cada uno de ellos responsable de la producción de una hormona determinada. Las células α son las encargadas de la síntesis de glucagón, las células β elaboran insulina, las de células δ secretan somatostatina y gastrina y las células F producen polipéptido pancreático. INSULINA: La insulina es una hormona de naturaleza proteínica que está formada por dos cadenas A y B unidas por puentes disulfuro. Síntesis: En el retículo endoplasmático (RE) rugoso de células β del páncreas se sintetiza preproinsulina, proteína precursora, esta se escinde y se forma proinsulina La disposición espacial de la proinsulina ubica las porciones de la molécula correspondientes a las cadenas A y B en la orientación adecuada para formar los puentes de disulfuro. Secreción: La proinsulina es englobada en vesículas y transportada al aparato de Golgi donde sucesivas hidrólisis catalizadas por peptidasas liberan insulina activa. La excreción del contenido de las vesículas hacia el espacio extracelular se realiza por exocitosis. El estímulo más eficaz para la síntesis y secreción de insulina es el aumento de la glucemia. La glucosa debe ser metabolizada en la célula β para estimular la secreción de insulina. La hexosa es fosforilada, ingresa en las vías glucolítica y de oxidación final para producir ATP. El ATP promueve el cierre de canales de k’ sensibles a adenilatos ,despolariza la membrana y determina la apertura de canales de Ca2+ accionados por voltaje. El ingreso de Ca2+ estimula el transporte intracelular de los gránulos y la exocitosis .Las vesículas de transporte son guiadas hacia la membrana plasmática por estructuras del citoesqueleto (microtúbulos) e impulsadas por proteínas motoras (actina y miosina). Los niveles elevados de los aminoácidos arginina y lisina y ácidos grasos libres estimulan la secreción. Además de estos factores, los alimentos, en especial, la glucosa, activan en intestino la secreción de hormonas gastrointestinales (gastrina ,colecistoquinina, secretina y enteroglucagón) que estimulan la liberación de insulina. El glucagón es otro importante activador de la secreción. El sistema nervioso parasimpático estimula la secreción, mientras que el simpático la inhibe. La somatostatina inhibe tanto la secreción de insulina como la de glucagón. La hormona es degradada por insulinasa en hígado, riñón y otros tejidos. Mecanismos de acción: La insulina actúa previa unión a los receptores específicos en la membrana plasmática de las células efectoras. Cuando la insulina se fija al sitio de unión del receptor produce un cambio conformacional que activa la tirosina quinasa. El receptor activado adquiere capacidad para autofosforilarse y catalizar la fosforilación de restos de tirosina de otras proteínas. La actividad de la tirosin quinasa del receptor inducida por la unión de insulina inicia una cascada de fosforilaciones. El complejo insulina receptor es internado por endocitosis. Frecuentemente después de la disociación del complejo HR, el receptor es devuelto a la membrana externa y la insulina degradada en lisosomas. Acciones metabólicas: Los principales tejidos efectores de la acción de insulina son: muscular, adiposo y hepático. Efectos sobre el transporte de metabolismo: En los tejidos muscular y adiposo, la hormona estimula el ingreso de la glucosa, aminoácidos, nucleótidos y fosfato en las células. En las células de los mamíferos existen transportadores de la glucosa llamados GLUT, son proteínas que permiten la difusión facilitada de dicha sustancia, es decir que transportan la glucosa desde el exterior al interior de las células. La mayoría de los transportadores GLUT están insertos en membranas de vesículas intracelulares. Existen muchos tipos de GLUT presentes en los diferentes tejidos, pero sólo los GLUT 4 son dependientes de la insulina, y se encuentran en el músculo estriado, tejido adiposo, e hígado, pero este último, posee también grandes cantidades de GLUT 2, GLUT 9 y GLUT 10, los cuales, no dependen de la insulina. LOS ÚNICOS TEJIDOS QUE DEPENDEN DE LA INSULINA PARA UTILIZAR LA GLUCOSA SON EL MUSCULAR ESTRIADO (ESQUELÉTICO Y CARDIACO), Y EL ADIPOSO, DEBIDO A QUE SOLO POSEEN GLUT 4. Localización de transportadores GLUT en los tejidos El aumento de glucosa estimula la liberación de insulina, la cual pone en marcha a través de sus receptores, sistemas de señales que promueven el rápido traslado de GLUT 4 desde el interior de la célula hacia la membrana plasmática y con ello aumenta marcadamente la captación de glucosa. Cuando la concentración extracelular de glucosa e insulina descienden, los transportadores GLUT 4 son internados por endocitosis. El ‘’reciclado’’ de transportadores controlado por insulina regula el ingreso de glucosa a los tejidos muscular y adiposo según las necesidades. Efectos sobre el metabolismo de carbohidratos: La insulina es la principal hormona hipoglucemiante. Esta acción se debe a su capacidad de estimular el ingreso de glucosa en los tejidos con transportadores sensibles a la hormona y de activar la utilización de glucosa en los tejidos. hígado. La insulina influye notablemente sobre las funciones glucorreguladoras del hígado. Aumenta la actividad de glucoquinasa y canaliza la glucosa hacia todas las vías de utilización. Se estimulan glucogenogénesis ,glucólisis , oxidación total de glucosa, vía de pentosa fosfato, conversión de glucosa en lípidos Músculo y tejido adiposo: La insulina estimula directamente el ingreso de glucosa en músculos esquelético y cardíaco y en adipositos. En músculo favorece la utilización de glucosa o su depósito como glucógeno. Efectos sobre metabolismo de lípidos: Estimula la síntesis de ácidos grasos y triacilgliceroles en hígado, tejido adiposo, glándula mamaria lactante y otros tejidos. La insulina activa la lipoproteína lipasa unida a membrana de capilares periféricos , lo cual aumenta la provisión de ácidos grasos a los tejidos (preferentemente adiposo) para la síntesis de triagliceroles, deprime la lipólisis y reduce el nivel de ácidos grasos libres circulantes. También reduce la cetogénesis. Efectos sobre metabolismo de proteínas: Estimula la captación de aminoácidos por las células y su incorporación a proteínas y activa los procesos de transcripción y traducción. Efectos sobre potasio: La insulina aumenta la actividad de Na’+, K’+-ATPasa e incrementa el potencial transmembrana. Cuando hay deficiencia de hormonas, el potasio escapa hacia el compartimiento extracelular y es eliminado por vía renal. GLUCAGÒN : El glucagón es producido en las células α de los islotes de Langerhans del páncreas. El glucagón circula libre en plasma y tiene una vida media muy breve(unos 6 minutos). El principal regulador de la secreción es el nivel de glucosa en sangre. El aumento de la glucemia inhibe la secreción de glucagón , mientras la disminución la activa. El incremento de aminoácidos en plasma y el sistema nervioso simpático tambièn estimulan la secreciòn. Mecanismo de acción: El glucagón se une a receptores específicos de membranas de hepatocitos y tejido adiposo acoplados a proteínas G que activan la adenilato ciclasa, aumentan la concentración de AMP cíclico e inician la cascad de fosforilaciones que modifican la actividad de determinadas enzimas Acciones del Glucagón: Es una hormona catabólica y tiene una importante función en la movilización de sustratos. Estimula la neoglucogenesis y la glucogenolisis, activando la producción hepática endógena de glucosa. Activa la lipólisis y el transporte de ácidos grasos hacia el hígado. Tiene un rol fundamental en la cetogénesis hepática, acelera el paso de ácidos grasos a la mitocondria y en condiciones de déficit insulínico, su transformación en cetoácidos. A nivel muscular, favorece la degradación de proteínas a aminoácidos, su salida hacia el hígado y su posterior transformación a glucosa (neoglucogenesis). BALANCE DEL Ca y P PARATIROIDES Paratohormona Como toda hormona peptídica se forma primero una prohormona que pasa al aparato de Golgi donde tiene lugar una hidrólisis. Se genera así la hormona paratiroidea activa, la cual pasa al citosol empaquetada en gránulos secretorios. A diferencia de otras glándulas, la paratiroides no almacena hormona, el depósito existente en las células es generalmente pequeño. Secreción: Tanto la síntesis como la secreción de la hormona son reguladas por la concentración de Ca2+ en sangre. El principal estímulo para la secreción de PTH es la disminución de la concentración de Ca2+ circulante. A su vez, aumentos exagerados de la calcemia inhiben la liberación de hormona en la glándula. Normalmente, la concentración de calcio en plasma se mantiene con gran constancia alrededor 10 mg/dL. En esas condiciones no existen variaciones en la liberación de PTH dese la glándula que la sintetiza y segrega a un ritmo basal constante. Cuando la calcemia disminuye por debajo de 9 mg/dL, la secreción de hormona aumenta rápidamente a medida que la calcemia desciende hasta alcanzar un máximo cuando se llega a 6 mg/dL. A partir de este nivel, la liberación de PTH no aumenta más, aunque la calcemia disminuya. Por otro lado, el incremento de la calcemia deprime la liberación de hormona desde la glándula. El efecto inhibitorio máximo se alcanza al llegar a 11mg/dL, pero nunca se llega a suprimir completamente la secreción, por más que se exceda ese valor. La capacidad de la paratiroides para detectar las fluctuaciones de la concentración de Ca2+ extracelular se debe a la existencia de un ‘’sensor’’ en la membrana plasmática de las células de la paratiroides, túbulos renales y células C de tiroides. Acciones La principal función de la PTH es contribuir junto con otros factores a mantener la concentración de calcio en el compartimiento extracelular. Para ello actúa a varios niveles. a) Tejido óseo b) Túbulos renales c) Metabolismo de vitamina D a) El mineral del hueso es movilizado para mantener la homeostasis del calcio. La PTH pone en juego dos procesos. Liberación rápida de calcio y reabsorción osteoclástica. Las células que poseen receptores para la PTH Los osteocitos producen rápida liberación de calcio desde el fluido óseo hacia las células y a través de uniones comunicantes o nexos, hacia la superficie de los osteoblastos (el conjunto de estas uniones, dadas por prolongaciones citoplasmáticas, se denomina “membrana osteocítica”) La PTH estimula el transporte activo de Ca2+ desde el fluido óseo al líquido extracelular. La PTH promueve la diferenciación de células precursoras en osteoclastos y activa la producción de citoquinas estimulantes de la reabsorción ósea. Este efecto es más lento (horas a días) que el de osteòlisis por osteocitos. El resultado final es remoción y destrucción del mineral y matriz del hueso, acciones que determinan pasaje de calcio hacia el LEC. b) La PTH estimula la reabsorción de Ca2+ en la rama ascendente gruesa del asa de Henle y en túbulos contorneados distales del nefrón. Disminuye la excreción de calcio por orina. La mayor parte de la reabsorción de Ca2+ se realiza en el túbulo proximal y no es regulada por PTH aunque la hormona controla sólo el 10% de calcio reabsorbido, tiene importantes efectos. La PTH aumenta la eliminación de fosfato, pues inhibe su reabsorción en la nefrona proximal y en menor proporción en el distal. La movilización del mineral del hueso aumenta el calcio y el fosfato circulantes. El incremento de la fosfaturia por la PTH tiende a prevenir la formación de fosfato de calcio que se depositaría en tejidos blandos reduciendo el efecto hipercalcemiante. La PTH disminuye la reabsorción renal de sodio, potasio, citrato y bicarbonato. c) Efecto sobre metabolismo de vitamina D: Promueve la absorción intestinal de calcio. No es un efecto primario de la hormona sino secundario a la formación de 1,25-(OH2)-D3 , metabolito activo de vitamina D. Este compuesto es el factor hormonal responsable del incremento en la absorción de calcio en intestino. Se activa en el riñón CALCITONINA: En los mamíferos es sintetizada y secretada por las células C (claras, de núcleo oval) de la tiroides. El principal estímulo para la secreción de calcitonina es el aumento de la concentración extracelular de calcio. También activan la secreción algunas hormonas gastrointestinales (gastrina, secretina y colecistoquinina). Tiene una vida media de 5 a 10 minutos y, es degradada en el riñón. Actúa a través de los receptores acoplados a proteína G , eleva el nivel deAMP cíclico en las células efectoras Acciones La calcitonina produce rápida disminución de las concentraciones sanguíneas de calcio y fosfato. Específicamente, afecta los niveles sanguíneos de calcio en cuatro formas: Inhibe la absorción intestinal de Ca +2 Inhibe la resorción ósea Inhibe la reabsorción de fosfato a nivel de los túbulos renales Aumenta la excreción de Ca+2 y Mg+ por los riñones. Vitamina D La vit. D se sintetiza en la piel como su precursor 7-deshidrocolesterol y con la luz solar se transforma en vitamina D la cual es inactiva y requiere una transformación que comienza en el hígado. Aquí la molécula sufre una primera hidroxilación. Luego en el riñón la paratohormona estimula una enzima llamada alfa-1-hidroxilasa que vuelve a hidroxilar la molécula y la convierte en su forma activa 1,25-vitamina D. Una vez sitetizada se tranporta en plasma unida a una proteína llamada transcalciferina. Acciones Sobre el hueso: Estimula la mineralización ósea. Sobre los osteoblastos actúa favoreciendo la síntesis de osteoclastina e incrementando la actividad de los receptores para factores de crecimiento. Induce la liberación de osteoclastos un factor estimulador producido por los osteoblastos. Estimulador de la reabsorción ósea. Sobre el Intestino: Estimula la absorción intestinal de calcio y fosfato. Acción mediada por una proteína ligadora de calcio, calbindina D Péptidos Natriuréticos Los PN son de tres tipos: 1) El tipo A es el ANP (A-type Natriuretic Peptide o Atrial Natriuretic Peptide), 2) El tipo B es el BNP (B-type Natriuretic Peptide o Brain Natriuretic Peptide ), que se origina en el miocardio, 3) El tipo C es el CNP (C-type o CNatriuretic Peptide); es producido por el endotelio, y presenta dos sub-tipos (de acuerdo al número de aminoácidos de cada uno), los subtipos de CNP también están presentes en el corazón, pero en cantidades muy bajas. Un cuarto PN es la urodilatina, pro ANP formado en el riñón, circula en escasos niveles en el plasma. En el año 1999 se descubrió la presencia de un quinto miembro, denominado Dendroaspis Natriuretic Peptide (DNP), originalmente aislado del veneno de la serpiente Mamba verde (Dendroaspis angusticeps), que se encuentra en el plasma y en las aurículas humanas, con efectos natriuréticos y vasodilatadores (en arterias coronarias). Se han descrito 3 nuevos PN presentes en la víbora Oxyuranos microlepidotus. Factor natriurético atrial A (ANP) Se sintetiza primariamente en aurículas, pero también en cerebro, lóbulo anterior de glándula pituitaria, pulmón y riñón Se almacena en los cardiomiocitos auriculares en forma de gránulos como prohormona o pro-ANP (formada por 126 aa) El estimulo para su liberación es el aumento de tensión de la pared auricular Mecanismo de acción Existen receptores específicos para los péptidos natriuréticos atriales, en varios tejidos efectores, renal, vascular, y adrenal. La hormona se une al receptor de membrana, activa la guanilato ciclasa en la porción citosólica del mismo receptor y aumenta el GMP cíclico que actúa como segundo mensajero del FNA. Otro efecto observado en algunas células es inhibición de adenilato ciclasa, con disminución de AMP cíclico. Acciones El factor natriurético atrial actúa a varios niveles: a) sobre sistema renina-angiotensina: Inhibe la secreción de renina. Esta acción puede secundariamente, deprimir la secreción de aldosterona. También existe en evidencia de efecto inhibitorio de la liberación de aldosterona por acción directa sobre adrenales. b) sobre riñón: Estimula la secreción de agua y sodio, aumenta el volumen de filtrado en los glomérulos y disminuye la reabsorción de sodio en los túbulos. c) sobre sistema vascular: Relaja la musculatura lisa especialmente en la arteriola aferente del riñón, disminuye la presión arterial y el gasto cardíaco. d) Sobre sistema nervioso: Se ha demostrado unión de la hormona a células del cerebro en sitios probablemente comprometidos con la regulación de los niveles de sodio y potasio, del volumen del líquido extracelular y de la presión arterial. El FNA inhibe la producción de vasopresina. Péptido Natriuretico Cerebral B (BNP): Se sintetiza en cardiomiocitos ventriculares aunque también en cerebro y amnios Se almacena escasamente, por lo que su sístesis y liberación son casi inmediatas al estímulo recibido El estimulo para su liberación es la distensión o el aumento de presión sobre la pared ventricular. Es secretado hacia la circulación en forma pulsátil a través de los senos coronarios en respuesta al estrés de pared ventricular. Tiene una vida media de 22 minutos. • • • • Angiotensina II, norepinefrina y endotelina-I Regulador hormonal ( Aldosterona y renina) Fibrosis miocardica y proliferación de músculo liso Acciones sobre el SNC Péptido natriuretico C (CNP) Se sintetiza predominantemente en las células del endotelio vascular (también en cerebro, riñón, corazón y pulmón) El estimulo para su liberación es la distensión mecánica que ejerce la sangre sobre el endotelio vascular Aunque no se conoce con total exactitud su función, parece tener efectos vasodilatadores y antiproliferativos sobre el músculo liso preferentemente a nivel local Urodilatina: Se sintetiza en las células renales y se excreta con la orina El estimulo para su liberación se desconoce (?) Su función principal parece ser la regulación de la reabsorción de agua y sodio a nivel de los túbulos colectores (?) EN ESTUDIO GLANDULA PINEAL Se encuentra cerca del hipotálamo formada por pinealicitos que son células neuroepiteliales. Melatonina Es una hormona sintetizada en glándula pineal de vertebrados, es una indolamina derivada de triptófano. La melatonina es liberada desde la pineal a la circulación durante el período de oscuridad del ciclo diario. La secreción es suprimida en individuos expuestos a la luz intensa. El ritmo circadiano de síntesis y secreción es regulado por vía neural desde el núcleo supraquiasmático del hipotálamo. En los mamíferos, este núcleo es el ‘’marcapaso’’ de los ciclos circadianos, entre ellos los de temperatura corporal, sueño, secreción de cortisol. Es posible que la glándula pineal a través de la melatonina module la sensibilidad del sistema circadiano a la luz ambiental y contribuya a sincronizar los ‘’relojes biológicos’’. Existen receptores específicos de melatonina en varias áreas de cerebro de mamíferos, notablemente en núcleo supraquiasmático. Algunos de esos receptores están acoplados a proteína G. Hay tipos que Inhiben a la adenilato ciclasa y reducen los niveles de AMPc, y otros ponen en marcha el sistema de fosfatidilinocitolbisfosfato. Las acciones sobre las funciones sexuales han sido observadas sólo en especies con reproducción estacional. En ovinos, por ejemplo, la prolongación de los períodos diarios de oscuridad, con niveles elevados de melatonina, es la señal para la actividad reproductiva. Independientemente de su acción hormonal, se ha demostrado que la molécula de melatonina tiene gran capacidad como agente antioxidante in vivo.